Кислые соли соляной кислоты: гидрохлорид, формула
Все, кто когда-либо изучал химию (начиная со школы и заканчивая аспирантурой), хоть раз сталкивался с таким понятием, как «гидрохлорид». Формула такого вещества тоже хоть раз, но встречалась. Редко кто не только не знает, что это за вещество, но и не помнит, что встречал такое понятие когда-то на занятиях по химии. Что же такое «гидрохлорид»? Химическая формула и свойства вещества будут рассмотрены в этой статье.
Соляная кислота
Необходимо разобраться, что такое соляная кислота, прежде чем узнать, что такое кислая соль соляной кислоты (гидрохлорид). Формула представлена ниже.
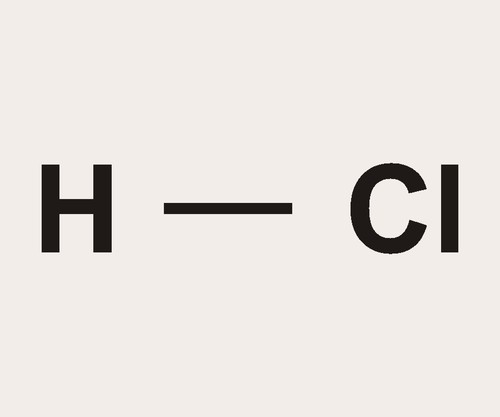
У этой кислоты существует несколько названий: хлороводородная (кислоты, состоящие из атома водорода и атома другого элемента, называются водородными: сероводородная, фтороводородная и т. д.), хлористый водород, «солянка» (это, скорее, жаргонное название), хлористоводородная. Соли хлористого водорода носят название «хлорид», а кислые соли — «гидрохлорид».
Формула хлоридов достаточно проста: [элемент] — Cl. Нужно учитывать степень элемента. Например, у алюминия она равна +3, хлорид алюминия AlCl3. Итак, с кислотой и ее солями все понятно. Теперь необходимо поговорить о гидрохлоридах.
Кислые соли соляной кислоты
Нужно уточнить, что гидрохлориды — это не совсем соли хлороводородной кислоты. В этом случае катион водорода образует комплексное соединение с молекулой основания. Название «гидрохлориды» распространены в органической химии, в неорганической принято называть «хлориды». Ярким примером служит хлорид аммония — никому не приходит в голову назвать его «аммиака гидрохлорид».
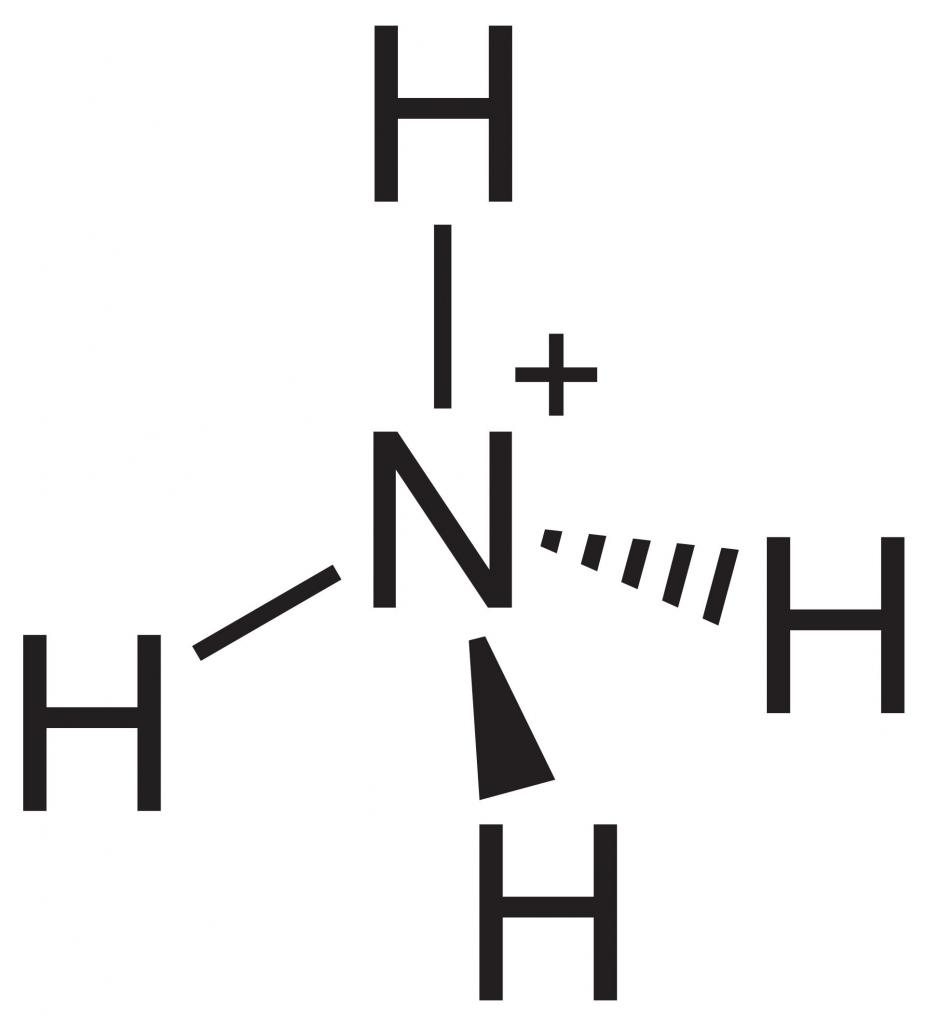
Формула (речь идет о гидрохлоридах) имеет общий вид: [основание] * HCl. Большинство кислых солей соляной кислоты являются бесцветными кристаллами. Если такое соединение имеет окраску, то это значит, что основание, с котором образован комплекс, придал кристаллам определенный цвет. Гидрохлориды весьма широко используются в фармацевтическом производстве.
Применение гидрохлоридов
Множество лекарств изготавливается именно на основе кислых солей хлороводородной кислоты. В качестве примеров можно привести такие вещества гидрохлорида, как полигексаметиленгуанидин, фенилпропаноламин, глюкозамин. Однако это далеко не полный список. Препараты на основе этих веществ используются для лечения позвоночника и суставов, для уничтожения микробов, для борьбы с воспалительными процессами (в верхних дыхательных путях, включая хронические заболевания). Это далеко не весь спектр областей применения лекарственных средств, а лишь малая их доля.
Витамин В6
Ни для кого не секрет, что витамин В6 является одним из наиболее важных витаминов, необходимых человеку для нормальной жизнедеятельности. Его нехватка вызывает головную боль, утомляемость, различные кожные заболевания, нарушения работы сосудов и т. д.
Одной из форм витамина В6 является пиридоксин (три наиболее распространенных формы — пиридоксин, пиридоксаль, пиридоксамин). В лекарственных препаратах его можно встретить под названием пиридоксина гидрохлорид. Формула самого пиридоксина вещества приведена ниже.
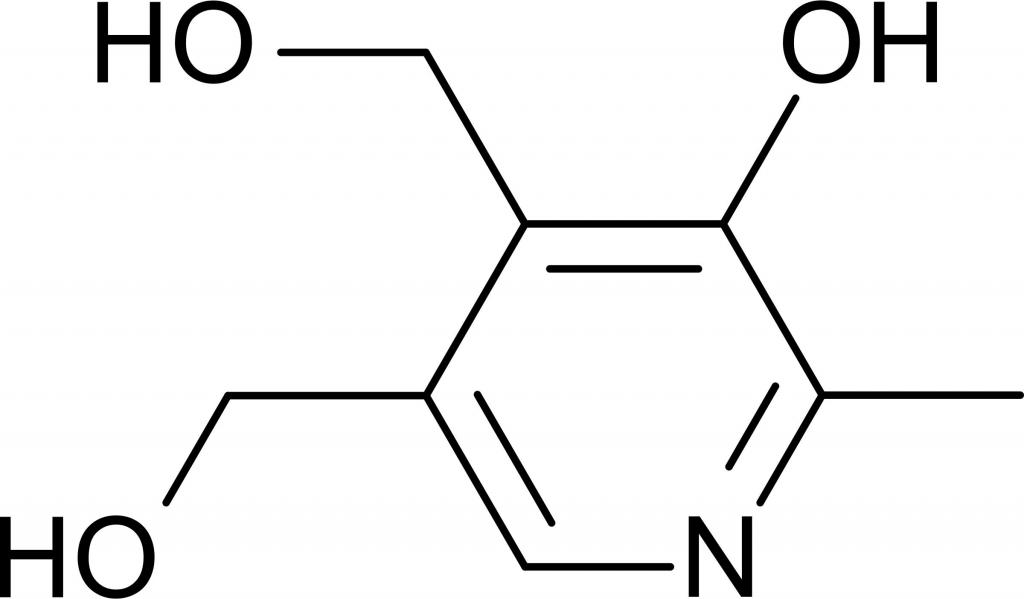
Витамин В6 используется также в качестве антидота при отравлениях гидразином.
Заключение
Итак, существуют не только неорганические соли хлороводородной кислоты, но и органические, которые являются комплексными соединениям. Наиболее распространено применение гидрохлоридов в фармакологии: великое множество препаратов изготавливаются на их основе или с содержанием этих веществ. Однако применение этих лекарственных средств требует особой внимательности, не допускающей превышения дозировки, назначенной специалистом. И ни в коем случае нельзя принимать препараты одновременно с алкоголем.
Гипохлорит натрия — вся польза Лабарраковой воды
СОДЕРЖАНИЕ СТАТЬИ
Для чего нужен раствор гипохлорита натрия
Гипохлорит натрия – технический химикат для очистки зараженной воды, оборудования, стоков, кроме того, его используют для отбелки разных материалов, для окисления в фармацевтической отрасли при изготовлении витаминов. Давайте рассмотрим более полный список:
- Гипохлорит натрия для очистки воды – один из самых безопасных и дешевых методов получения очищенной воды для нужд коммунального хозяйства.
- Обеззараживание сточных вод гипохлоритом натрия дает возможность контролировать эпидемиологическую ситуацию.
- Детоксикация отходов и сточных масс улучшает экологию и повышает безопасность ряда производств.
- Вещество применяется врачами для антисептирования ран, а также для мытья полов, туалетов, мебели, некоторых видов оборудования и инструмента позволило поднять гигиену на новый уровень.
- Помогает как специальный препарат в химиотерапии раковых опухолей.
- Белизна используется в быту и производстве как отбеливатель тканей, целлюлозы, древесины и других материалов.
- Применяется как компонент в промышленном и лабораторном химическом синтезе, в частности, синтезе гидразина.
- Альгицидная обработка: гипохлорит натрия бассейн или канал сделает чистым от водорослей и инфекции.
- Используется при получении синтетического пищевого крахмала.
ИНТЕРЕСНО! В регионе побережья Карибского моря и прилегающих стран произошла вспышка холеры (конец XX века), которую удалось ликвидировать с помощью ГПХН. Кроме того, применение этого дезинфектанта помогло остановить такие заболевания, как брюшной тиф и дизентерию.
Итак, мы видим, что сфера применения препарата весьма и весьма широка. Если говорить в целом, то львиная доля всего произведенного на планете ГПХН расходуется на отбеливание (67%) и дезинфекцию (33%).
Химические характеристики гипохлорита натрия
Гипохлорит натрия ГОСТ определяет, как продукт хлорирования газом раствора едкого гидрокарбоната натрия. Несмотря на наличие массы других способов его получения, за эталон взят именно этот. В результате реакции получается химическое соединение с формулой NaOCl.
Это вещество называют натриевой солью хлорноватистой кислоты. Кристаллы крайне нестабильны и быстро разлагаются. Относительно стабильная форма получается путем образования пентагидрата.
ИНТЕРЕСНО! Соединение изначально именовали в честь изобретателя – Лабарраковой водой. Именно водой, так как гипохлорит натрия жидкий является более предпочтительным для хранения и перевозки, а также использования. В сухом виде ромбовидные кристаллы быстро разлагаются с выделением хлора и кислорода, на их месте остается чистая вода.
Гипохлорит натрия — ГОСТ 11086 76 – желто-зеленая жидкость с возможной взвесью частиц. Отличается отчетливым запахом хлора, при вдыхании вызывает жжение в носоглотке и глазах. Не горит, не взрывается, однако после взаимодействия с некоторыми органическими соединениями может стать причиной возгорания.
Разновидности гипохлорит натрия
Гипохлорит натрия — ГОСТ 11086 — жидкий раствор соли натрия хлорноватистой кислоты в воде. Соответственно, существуют разновидности этого вещества в зависимости от концентрации, кислотности, количества хлора и ряда других показателей.
Важно! Сегодня множество производств заняты изготовлением гипохлорита натрия. Однако далеко не все из них руководствуются государственным стандартом, некоторые обходятся техническими условиями. Само собой, лучше выбирать вещество, которое сделано в соответствие с Государственным стандартом.
Чтобы читателю было проще увидеть разницу между марками ГПХН, мы свели их основные отличия в таблицу:
Таблица видов ГПХН
 Гипохлорит натрия
Гипохлорит натрияНаиболее качественным и чистым можно считать гипохлорит натрия МАРКА А. Именно здесь отмечается самое высокое содержание хлора, самая малая концентрация оснований и железа, соответственно, это дает более высокие результаты в отбелке тканей и дезинфекции. Гипохлорит натрия 25 кг в канистрах производит компания GOODHIM в соответствие со стандартом для марки А (возможна покупка гипохлорита натрия оптом).
Производство гипохлорита натрия
Мировые показатели объемов производства препарата приближаются к нескольким миллионам тонн. Потребности человечества в антисептике постоянно растут вместе с ростом населения, потребления искусственно подготовленной воды и общим развитием цивилизации на планете.
В промышленности используют такие методы получения:
- Основной процесс. Это химический путь получения ГПХН, который не отличается от реакции, открытой Антуаном Лабарраком в 1820 году и заключается в обработке едкого натра обычным хлором.
- Низкосолевой процесс. Здесь также происходит обработка гидроксида натрия хлором, только она протекает за две стадии, что позволяет получать концентрированные до 40% растворы, которые отличаются чистотой.
- Электролиз. Этот способ представляет собой знакомое всем разложение раствора с помощью тока. В качестве исходного вещества используют морскую воду или раствор поваренной соли.
Наиболее эффективным способом получения товарного ГПХН является низкосолевой процесс. В России так производит гипохлорит натрия фирма GOODHIM.
Воздействие на человека и природу
Интересно, что бактерицидное и, вообще, биоцидное действие ГПХН связано с выделением в процессе разложения таких частиц, как синглетный кислород. Это весьма напоминает борьбу некоторых наших клеток, например, гепатоцидов, с инородными микроорганизмами путем синтеза хлорноватистой кислоты.
Под влиянием антисептика погибают не только лишь микробы, но дрожжевые грибы, энтерококки, а также многие опасные бактерии. При этом некоторые простейшие, такие как лямблии и протисты, демонстрируют устойчивость к данному агенту.
Для человека ГПХН может нести опасность при проникновении в глаза, на участки незащищенной кожи и при вдыхании. Вдыхание вызывает жжение в глотке, резь в области глаз, кашель и эффект удушения. Поражение глаз способно привести к химическому ожогу с потерей зрения. Длительный контакт с кожей вызывает раздражение, при повышении концентрации – изъязвление и даже некроз.
Прием препарата в пищу ведет к гастропатии, раздражению внутренних поверхностей кишечника и пищевода, иногда – к ацидозу печени и перфорации ЖКТ.
Средство длительное время подвергалось всестороннему исследованию ученых разных стран мира, ведь его эффективность в разы превышала показатели риска и отвергнуть столь действенный дезинфектант было бы безрассудно! В исследованиях была убедительно показана безопасность дезинфектанта при применении по назначению и согласно инструкции. Также было установлено, что соединение не вызывает тенденции к образованию рака, мутации или неправильной беременности.
Заключение
Гипохлорит натрия – один из наиболее распространенных, эффективных и безопасных дезинфектантов и отбеливателей из всех известных человечеству. Вещество отличается доступностью для покупки, низкой ценой и солидным опытом использования. Польза Лабарраковой воды была убедительно показана в борьбе с эпидемиями, для обеззараживания воды, в отбелке целлюлозы и тканей.
- Болезни
- Инфекционные и паразитарные болезни
- Новообразования
- Болезни крови и кроветворных органов
- Болезни эндокринной системы
- Психические расстройства
- Болезни нервной системы
- Болезни глаза
- Болезни уха
- Болезни системы кровообращения
- Болезни органов дыхания
- Болезни органов пищеварения
- Болезни кожи
- Болезни костно-мышечной системы
- Болезни мочеполовой системы
- Беременность и роды
- Болезни плода и новорожденного
- Врожденные аномалии (пороки развития)
- Травмы и отравления
- Симптомы
- Системы кровообращения и дыхания
- Система пищеварения и брюшная полость
- Кожа и подкожная клетчатка
- Нервная и костно-мышечная системы
- Мочевая система
- Восприятие и поведение
- Речь и голос
- Общие симптомы и признаки
- Отклонения от нормы
- Диеты
- Снижение веса
- Лечебные
- Быстрые
- Для красоты и здоровья
- Разгрузочные дни
- От профессионалов
- Монодиеты
- Звездные
- На кашах
- Овощные
- Детокс-диеты
- Фруктовые
- Модные
- Для мужчин
- Набор веса
- Вегетарианство
- Национальные
- Лекарства
- Антибиотики
- Антисептики
- Биологически активные добавки
- Витамины
- Гинекологические
- Гормональные
- Дерматологические
- Диабетические
- Для глаз
- Для крови
- Для нервной системы
- Для печени
- Для повышения потенции
- Для полости рта
- Для похудения
- Для суставов
- Для ушей
- Желудочно-кишечные
- Кардиологические
- Контрацептивы
- Мочегонные
- Обезболивающие
- От аллергии
- От кашля
- От насморка
- Повышение иммунитета
- Противовирусные
- Противогрибковые
- Противомикробные
- Противоопухолевые
- Противопаразитарные
- Противопростудные
- Сердечно-сосудистые
- Урологические
- Другие лекарства
- Врачи
- Клиники
- Справочник
- Аллергология
- Анализы и диагностика
- Беременность
- Витамины
- Вредные привычки
- Геронтология (Старение)
- Дерматология
- Дети
- Женское здоровье
- Инфекция
- Контрацепция
- Косметология
- Народная медицина
- Обзоры заболеваний
- Обзоры лекарств
- Ортопедия и травматология
- Питание
- Пластическая хирургия
- Процедуры и операции
- Психология
- Роды и послеродовый период
- Сексология
- Стоматология
- Травы и продукты
- Трихология
- Другие статьи
- Словарь терминов
- [А] Абазия .. Ацидоз
- [Б] Базофилы .. Богатая тромбоцитами плазма
- [В] Вазопрессин .. Выкидыш
- [Г] Галлюциногены .. Грязи лечебные
- [Д] Деацетилазы гистонов .. Дофамин
- [Ж] Железы .. Жиры
- [И] Иммунитет .. Искусственная кома
- [К] Каверна .. Кумарин
- [Л] Лапароскоп .. Лучевая терапия
- [М] Макрофаги .. Мутация
- [Н] Наркоз .. Нистагм
- [О] Онкоген .. Отек
- [П] Паллиативная помощь .. Пульс
- [Р] Реабилитация .. Родинка (невус)
- [С] Секретин .. Сыворотка крови
- [Т] Таламус .. Тучные клетки
- [У] Урсоловая кислота
- [Ф] Фагоциты .. Фитотерапия
- [Х] Химиоте
натрий гидрохлорид — с русского на латинский
См. также в других словарях:
ЛИНКОМИЦИНА ГИДРОХЛОРИД — ( Lyncomycini hydrochloridum ). Линкомицин антибиотик, продуцируемый Streptomyces lincolniensis или другими родственными актиномицетами. Синонимы: Нелорен, Albiotic, Cillimycin, Lincocin, Lincolnensin, Liocin, Mycivin, Neloren и др. Выпускается в … Словарь медицинских препаратов
ФУЗИДИН-НАТРИЙ — ( Fusidinum natrium ). Натриевая соль фузидиевой кислоты антибиотического вещества, образуемого при биосинтезе грибом Fusidium coccineum. Синонимы: Фузидат натрия, Fucidine, Fusidin, Ramycin, Sodium fusidicum. Белый с желтоватым оттенком… … Словарь медицинских препаратов
Аппаратура, реактивы и растворы — 6.2. Аппаратура, реактивы и растворы Весы по ГОСТ 29329 или ГОСТ 24104. Фотоколориметр ФЭК 56М или спектрофотометр СФ 4, или другие аналогичные приборы. Цилиндры стеклянные вместимостью 250 см3 из прозрачного бесцветного стекла (внутренний… … Словарь-справочник терминов нормативно-технической документации
Реактивы и растворы — 5.2 Реактивы и растворы Натрий углекислый по ГОСТ 83. Кремния двуокись по ГОСТ 9428. Кислота азотная по ГОСТ 4461, разбавленная 1:4. Аммоний углекислый по ГОСТ 3770. Метиловый оранжевый индикатор, водный раствор с массовой концентрацией 1 г/дм3.… … Словарь-справочник терминов нормативно-технической документации
71.040.30 — Хімічні реактиви ГОСТ 8.134 98 ГСИ. Шкала рН водных растворов. Взамен ГОСТ 8.134 74 ГОСТ 8.315 97 ГСИ. Стандартные образцы состава и свойств веществ и материалов. Основные положения. Взамен ГОСТ 8.315 91 ГОСТ 61 75 Кислота уксусная. Технические… … Покажчик національних стандартів
Аппаратура, материалы — 7.3 . Аппаратура, материалы 7.3.1. Для проведения испытания применяют: весы технические по ГОСТ 24104; шкаф сушильный по ОСТ 16.0.801.397; штангенциркуль по ГОСТ 166; стальные линейки по ГОСТ 427; эксикатор по ГОСТ 25336; хлористый кальций… … Словарь-справочник терминов нормативно-технической документации
Аппаратура, материалы и реактивы — 2.2. Аппаратура, материалы и реактивы Посуда мерная лабораторная стеклянная по ГОСТ 1770, ГОСТ 29169 и ГОСТ 29251, вместимостью: колбы 100 и 1000 см3; пипетки без делений 5, 10, 25 см3; бюретка с краном 25, 50 см3; микробюретка 5 см3. Колбы… … Словарь-справочник терминов нормативно-технической документации
АСТМА БРОНХИАЛЬНАЯ — мед. Бронхиальная астма (БА) хроническое воспалительное заболевание дыхательных путей, сопровождающееся гиперреактивностью бронхов. Основное клиническое проявление периодически возникающие приступы затруднённого дыхания или удушья, вызываемые… … Справочник по болезням
Аппаратура — 4.2. Аппаратура Весы по ГОСТ 29329 или ГОСТ 24104. Шкаф сушильный. Сита с сеткой № 1,25 по ГОСТ 6613 и с круглыми отверстиями диаметрами 5 и 2,5 мм. Лупа минералогическая по ГОСТ 25706. Игла стальная. Источник … Словарь-справочник терминов нормативно-технической документации
Аппаратура и реактивы — 7.2. Аппаратура и реактивы Весы по ГОСТ 29329 или ГОСТ 24104. Набор сит с сетками № 1,25; 063; 0315 и 016 по ГОСТ 6613 и с круглыми отверстиями диаметрами 5 и 2,5 мм. Шкаф сушильный. Микроскоп бинокулярный с увеличением от 10 до 50×,… … Словарь-справочник терминов нормативно-технической документации
определение — 2.7 определение: Процесс выполнения серии операций, регламентированных в документе на метод испытаний, в результате выполнения которых получают единичное значение. Источник … Словарь-справочник терминов нормативно-технической документации
Формула и структура: Химическая формула гипохлорита натрия — NaClO, а его молярная масса — 74,44 г / моль.
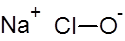
Это ионное соединение, состоящее из катиона металлического натрия (Na + ), связанного с анионом гипохлорита (ClO — ).
Приготовление: Он готовится промышленным способом по методу Хукера, в котором разбавленный гидроксид натрия реагирует с газообразным хлором с образованием NaClO, а также хлорида натрия и воды.
2 NaOH + Cl 2 → NaClO + NaCl + H 2 O
Физические свойства: в чистом виде оно существует в виде нестабильного светло-зеленого твердого вещества с плотностью 1,11 г / мл, температурой плавления 18 ° C и температурой кипения 101 ° C. Он чаще встречается в виде водного бледно-зеленоватого или желтого раствора. Водные растворы NaClO доступны в нескольких различных концентрациях или концентрации (от 1% до 25%), в зависимости от конечного использования.
Химические свойства: Гипохлорит натрия является хорошим окислителем.Он реагирует с протонными кислотами, такими как HCl, с образованием солей, выделяя при этом токсичный газообразный хлор. Он также реагирует с некоторыми кислотами с образованием хлорноватистой кислоты (HClO). В воде он разлагается на ионы натрия и хлорида, а также на мощный окислитель, гидроксильный радикал (OH . ). NaClO также разлагается на хлорид натрия и кислород.
Применение: его основное применение — отбеливающее и дезинфицирующее средство как для бытовых, так и для промышленных целей. Он также используется на водоочистных сооружениях, в бассейнах, в некоторых медицинских и стоматологических учреждениях, в пищевой промышленности в качестве дезинфицирующего средства, в домах в качестве дезодорирующего и моющего средства и в моющих средствах для стирки в качестве пятновыводителя и отбеливателя.
Воздействие на здоровье / опасности для здоровья: Гипохлорит натрия является токсичным и коррозийным соединением в более высоких концентрациях. При проглатывании может быть очень токсичным. Он также реагирует с некоторыми кислотами и аммиаком с образованием токсичных газов, таких как хлор, что может привести к сильному раздражению глаз и проблемам с дыханием. Сильные растворы отбеливателя также могут вызвать ожоги кожи.
Формула и структура: Химическая формула хлорида натрия — NaCl, а его молярная масса — 58,44 г / моль. Это ионное соединение, состоящее из катиона натрия (Na + ) и хлорид-аниона (Cl — ). Твердый NaCl имеет кристаллическую структуру, в которой каждый ион Na + окружен шестью хлорид-ионами в октаэдрической геометрии.
Возникновение: Хлорид натрия присутствует в морских и океанских водах, придавая им соленость.Приблизительно 1-5% морской воды сделано из хлорида натрия. Это также найдено как минерал галит или каменная соль.
Приготовление: Соль получают в больших масштабах путем испарения морской воды или соленой воды (рассола) из соленых озер и соляных скважин. Поскольку морская вода содержит несколько других солей (кальция, магния и других элементов), процесс испарения проводится осторожно, так что различные соли осаждаются в разное время в зависимости от их растворимости. Другой важный метод добычи — добыча запасов каменной соли.
Физические свойства: Хлорид натрия представляет собой белое кристаллическое твердое вещество с плотностью 2,16 г / мл и температурой плавления 801 ° C. Он также доступен в виде водных растворов различной концентрации, называемых солевыми растворами.
Химические свойства: Хлорид натрия легко растворяется в воде и других полярных растворителях. Это стабильное тело. Он разлагается только при высоких температурах с образованием токсичных паров соляной кислоты (HCl) и оксида динатрия (Na 2 O).
Использование: Хлорид натрия наиболее известен как поваренная соль и широко используется в пищевой промышленности для ароматизации и консервации.Он также используется в производстве многих важных химических веществ, включая гидроксид натрия, карбонат натрия, пищевую соду, соляную кислоту и т. Д. Он также применяется в нефтеперерабатывающих заводах, текстильной промышленности, целлюлозно-бумажной промышленности, огнезащитных составах, резиновой промышленности и в дорожных сооружениях. Другим важным применением является удаление льда с дорог и тротуаров в холодных и заснеженных регионах. Солевые растворы также используются во многих медицинских целях.
Воздействие на здоровье / опасности для здоровья: При низких концентрациях хлорид натрия не токсичен и неопасен, а также является важным источником электролита для организма.Высокое потребление соли в течение длительного времени может вызвать дисбаланс электролитов в организме. Проглатывание высоких концентраций может вызвать рвоту, тошноту, диарею и обезвоживание. Он также может раздражать глаза и вызывать повреждение глаз при высоких концентрациях.
.Формула и структура: Химическая формула гидроксида натрия — NaOH, и его молярная масса составляет 40,01 г / моль. Это щелочная соль натрия, и ее структура показана ниже:
Это ионное соединение, состоящее из катиона натрия (Na + ) и гидроксида (OH — ) аниона.
Приготовление: гидроксид натрия промышленно производится с использованием электролитического процесса хлоралкалия, при котором электролиз водного раствора хлорида натрия дает газообразный хлор и гидроксид натрия.NaOH получают в виде 50% -ного раствора в воде, а затем сушат, чтобы получить твердые чешуйки или пеллеты гидроксида натрия.
2 NaCl + 2 H 2 O → 2 NaOH + Cl 2 + H 2
Физические свойства: Это белое кристаллическое твердое вещество без запаха с плотностью 2,13 г / мл и температурой плавления 318 ° C. Он широко доступен в виде гранул, хлопьев, гранул, а также в виде водных растворов различных концентраций.
Химические свойства: Гидроксид натрия растворим в полярных растворителях, таких как вода, этанол и метанол, и нерастворим в органических растворителях.Растворение твердого NaOH в воде является сильно экзотермической реакцией, и в результате Раствор NaOH представляет собой бесцветную, без запаха и важную основу, используемую в лаборатории. Как сильное основание, гидроксид натрия легко реагирует с кислотами, такими как HCl, с образованием соответствующих солей, как показано ниже:
NaOH + HCl → NaCl + H 2 O
Гидроксид натрия очень гигроскопичен (поглощает воду из воздуха), а также поглощает углекислый газ из воздуха.
Использование: Гидроксид натрия является одним из наиболее широко используемых основ в промышленности.Его основное использование в бумажной промышленности, нефтяной промышленности, текстильной промышленности, в производстве мыла и моющих средств, в процессе производства алюминия в Байере, в промышленной очистке и для регулирования pH. Он также используется в пищевой промышленности для многих применений.
Воздействие на здоровье / опасности для здоровья: Это сильная и очень едкая щелочь, которая легко разлагает живые ткани. Попадание на кожу растворов NaOH может привести к серьезным химическим ожогам, а попадание в глаза может вызвать постоянную слепоту.Твердый NaOH реагирует с водой и кислотами в очень экзотермической реакции и может вызвать ожоги в результате разбрызгивания.
О компании
Год основания2010
Правовой статус фирмы FirmSole (физическое лицо)
Характер бизнесаПроизводитель
Количество сотрудников от 26 до 50 человек
Годовой оборотR.10 — 25 Crore
IndiaMART Участник с январь 2015
GST24ANAPD8968R1ZB
CHEM IMPEX — это развивающегося производителя / оптового продавца / дистрибьютора / трейдера в мире химикатов в Vapi, задуманного в 2010 году. За короткий период мы выросли с точки зрения разнообразия продуктов, количества продуктов с большим ростом числа клиентов. Chem Impex проник на большой рынок Южного Гуджарата, в частности Вапи, Даман, Сильвасса, Навсари, Валсад, Саригам, Сурат и Анклешвар.
Почему мы?
Chem Impex стремится предоставлять своим клиентам продукцию высшего качества и внедрила строгую систему качества для обеспечения этого. Мы уделяем большое внимание качественным параметрам, предлагаемым нашим уважаемым клиентом, и работаем над тем, чтобы обеспечить высокое качество нашей продукции.
Следовательно, мы призываем наших клиентов предоставлять нам как можно больше отзывов, и на протяжении многих лет мы формализовали процесс анализа этого ценного вклада для поиска решений.Мы способствуем постоянным улучшениям во всех сферах деятельности посредством четко определенных целей, измеримых показателей и системы управления, ориентированной на процессы.
Вот некоторые из ключевых факторов, которые помогли нам преуспеть на этом конкурентном рынке:
Качество
Наша ориентация на качество очевидна в нашем ассортименте и характеристиках, поскольку мы поставляем химикаты от известных производителей и импортеров. Мы назначили команду анализа контроля качества, которая предпримет строгие меры контроля качества, обеспечивающие высочайшее качество продукции.Все наши продукты стоят на грани любого качества, чтобы они могли легко противостоять национальной и международной конкуренции. Наши продукты постоянно тестируются и проверяются на предмет их свойств.
Стремление к безопасности окружающей среды
Мы стремимся к безопасности наших операций. наше обязательство распространяется на надлежащее функционирование бизнеса наших клиентов, для этого мы обеспечиваем безопасное и эффективное удовлетворение ваших потребностей.
Направленность бизнеса
На протяжении многих лет мы зарекомендовали себя в отрасли благодаря нашим высококачественным продуктам, надежным услугам и способности принимать новые вызовы и возможности.Наша постоянная цель — поддерживать качество, эффективность и конкурентоспособность нашей продукции на рынке, на котором мы работаем.
,