Гидроксид алюминия
Гидроксид алюминия — химическое вещество, которое представляет собой соединение оксида алюминия с водой. Может пребывать в жидком и твердом состояниях. Жидкий гидроксид является желеподобным прозрачным веществом, которое очень плохо растворяется в воде. Твердый гидроксид представляет собой кристаллическое вещество белого цвета, которое обладает пассивными химическими свойствами и не реагирует практически ни с одним другим элементом или соединением.
Получение гидроксида алюминия
Получение гидроксида алюминия происходит благодаря химической реакции обмена. Для этого используют водный раствор аммиака и какую-либо соль алюминия, чаще всего хлорид алюминий. Таким образом получают жидкое вещество. Если необходим твердый гидроксид, через растворенную щелочь тетрагидроксодиакваалюмината натрия пропускают диоксид углерода. Многих любителей экспериментов волнует вопрос, как получить гидроксид алюминия в домашних условиях? Для этого достаточно приобрести в специализированном магазине необходимые реагенты и химическую посуду.
Для получения твердого вещества понадобится еще и специально оборудование, так что лучше остановиться на жидком варианте. При проведении реакции необходимо использовать хорошо проветриваемое помещение, так как одним из побочных продуктов может быть газ или вещество с резким запахом, который может негативно сказаться на самочувствии и здоровье человека. Работать стоит в специальных защитных перчатках, так как большинство кислот при попадании на кожу вызывают химические ожоги. Не лишним будет позаботиться и о защите для глаз в виде специальных очков. Приступая к любому делу, в первую очередь необходимо думать об обеспечении безопасности!
Свежесинтезированный гидроксид алюминия реагирует с большинством активных кислот и щелочей. Именно поэтому для его получения используют аммиачную воду, чтобы сохранить образованное вещество в чистом виде. При использовании для получения кислоты или щелочи необходимо максимально точно рассчитать пропорцию элементов, иначе при избытке полученный гидроксид алюминия взаимодействует с остатками непоглощенной основы и полностью растворяется в ней. Это происходит из-за высокого уровня химической активности алюминия и его соединений.
Это происходит из-за высокого уровня химической активности алюминия и его соединений.
В основном, гидроксид алюминия получают из бокситовой руды с высоким содержанием оксида металла. Процедура позволяет быстро и относительно дешево отделить полезные элементы от пустой породы. Реакции гидроксида алюминия с кислотами приводят к восстановлению солей и образованию воды, а с щелочами — к получению комплексных гидрооксоалюминиевых солей. Твердый гидроксид методом сплавки соединяют с твердыми щелочами с образованием метаалюминатов.
Основные свойства вещества
Физические свойства гидроксида алюминия: плотность — 2,423 грамм на сантиметр кубический, уровень растворяемости в воде — низкий, цвет — белый либо прозрачный. Вещество может существовать в четырех полиморфных вариантах. Под воздействием низких температур образуется альфа-гидроксид, называемый байеритом. Под воздействие нагревания можно получить гамма-гидроксид или гиббсит. Оба вещества имеют кристаллическую молекулярную решетку с водородными межмолекулярными типами связи. Также встречаются еще две модификации — бета-гидроксид или нордстандрит и триклинный гибсит. Первая получается путем прокаливания байерита или гиббсита.Второй отличается от остальных видов триклинным, а не монообразным строением кристаллической решетки.
Также встречаются еще две модификации — бета-гидроксид или нордстандрит и триклинный гибсит. Первая получается путем прокаливания байерита или гиббсита.Второй отличается от остальных видов триклинным, а не монообразным строением кристаллической решетки.
Химические свойства гидроксида алюминия: молярная масса — 78 моль, в жидком состоянии хорошо растворяется в активных кислотах и щелочах, при нагревании разлагается, обладает амфотерными признаками. В промышленности в подавляющем большинстве случаев используется именно жидкий гидроксид, так как благодаря высокому уровню химической активности, он легко поддается обработки и не требует использования катализаторов или специальных условий протекания реакции.
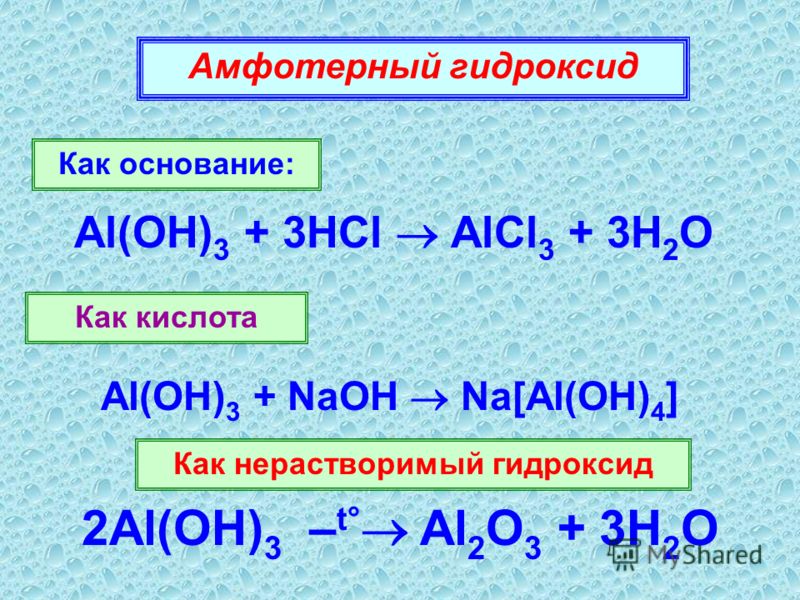
Амфотерность гидроксида алюминия проявляется в двойственности его природы. Это означает, что в различных условиях он может проявлять кислотные либо щелочные свойства. Когда гидроксид принимает участие в реакции как щелочь, образуется соль, в которой алюминий является положительно заряженным катионом.
Гидроксид алюминия входит в состав вакцин в качестве вещества, усиливающего иммунную реакцию организма на раздражитель. Нерастворимость осадка гидроксида алюминия в воде позволяет использовать вещество в водоочистных целях. Химическое соединение является очень сильным адсорбентом, который позволяет извлекать из состава воды большое количество вредных элементов.
Применение в промышленности
Применение гидроксида в промышленности связано с получением чистого алюминия. Технологический процесс начинается с обработки руды, содержащей оксид алюминия, который по завершению процесса переходит в гидроксид.
Процедура не требует специальных условий, так как вещество хорошо разлагается при нагревании до температуры свыше 180 градусов по Цельсию. Этот этап позволяет выделить оксид алюминия. Это соединение является базовым или вспомогательным материалом для изготовления большого количества промышленных и бытовых изделий. При необходимости получения чистого алюминия используют процесс электролиза с добавлением в раствор криолита натрия. Катализатор забирает из оксида кислород, и чистый алюминий оседает на катоде.
Гидроксид алюминия: получение и свойства
Гидроксид алюминия
Способы получения
1. Гидроксид алюминия можно получить действием раствора аммиака на соли алюминия.
Например, хлорид алюминия реагирует с водным раствором аммиака с образованием гидроксида алюминия и хлорида аммония:
AlCl3 + 3NH3 + 3H2O = Al(OH)3 + 3NH4Cl
2. Пропусканием углекислого газа, сернистого газа или сероводорода через раствор тетрагидроксоалюмината натрия:
Пропусканием углекислого газа, сернистого газа или сероводорода через раствор тетрагидроксоалюмината натрия:
Na[Al(OH)4] + СО2 = Al(OH)3 + NaНCO3
Чтобы понять, как протекает эта реакция, можно использовать несложный прием: мысленно разбить сложное вещество Na[Al(OH)4] на составные части: NaOH и Al(OH)3. Далее мы определяем, как реагирует углекислый газ с каждым из этих веществ, и записываем продукты их взаимодействия. Т.к. Al(OH)3 не реагирует с СО2, то мы записываем справа Al(OH)3 без изменения.
3. Гидроксид алюминия можно получить действием недостатка щелочи на избыток соли алюминия.
Например, хлорид алюминия реагирует с недостатком гидроксида калия с образованием гидроксида алюминия и хлорида калия:
AlCl3 + 3KOH(недост) = Al(OH)3↓+ 3KCl
4. Также гидроксид алюминия образуется при взаимодействии растворимых солей алюминия с растворимыми карбонатами, сульфитами и сульфидами. Сульфиды, карбонаты и сульфиты алюминия необратимо гидролизуются в водном растворе.
Также гидроксид алюминия образуется при взаимодействии растворимых солей алюминия с растворимыми карбонатами, сульфитами и сульфидами. Сульфиды, карбонаты и сульфиты алюминия необратимо гидролизуются в водном растворе.
Например: бромид алюминия реагирует с карбонатом натрия. При этом выпадает осадок гидроксида алюминия, выделяется углекислый газ и образуется бромид натрия:
2AlBr3 + 3Na2CO3 + 3H2O = 2Al(OH)3↓ + CO2↑ + 6NaBr
Хлорид алюминия реагирует с сульфидом натрия с образованием гидроксида алюминия, сероводорода и хлорида натрия:
2AlCl3 + 3Na2S + 6H2O = 2Al(OH)3 + 3H2S↑ + 6NaCl
Химические свойства
1. Гидроксид алюминия реагирует с растворимыми кислотами. При этом образуются средние или кислые соли, в зависимости от соотношения реагентов и типа соли.
При этом образуются средние или кислые соли, в зависимости от соотношения реагентов и типа соли.
Например, гидроксид алюминия взаимодействует с азотной кислотой с образованием нитрата алюминия:
Al(OH)3 + 3HNO3 → Al(NO3)3 + 3H2O
Al(OH)3 + 3HCl → AlCl3 + 3H2O
2Al(OH)3 + 3H2SO4 → Al2(SO4)3 + 6H2O
Al(OH)3 + 3HBr → AlBr3 + 3H2O
2. Гидроксид алюминия взаимодействует с кислотными оксидами сильных кислот.
Например, гидроксид алюминия взаимодействует с оксидом серы (VI) с образованием сульфата алюминия:
2Al(OH)3 + 3SO3 → Al2(SO4)3 + 3H2O
3. Гидроксид алюминия взаимодействует с растворимыми основаниями (щелочами). При этом в расплаве образуются соли—алюминаты, а в растворе – комплексные соли. При этом гидроксид алюминия проявляет кислотные свойства.
Гидроксид алюминия взаимодействует с растворимыми основаниями (щелочами). При этом в расплаве образуются соли—алюминаты, а в растворе – комплексные соли. При этом гидроксид алюминия проявляет кислотные свойства.
Например, гидроксид алюминия взаимодействует с гидроксидом калия в расплаве с образованием алюмината калия и воды:
2KOH + Al(OH)3 → 2KAlO2 + 2H2O
Гидроксид алюминия растворяется в избытке щелочи с образованием тетрагидроксоалюмината:
Al(OH)3 + KOH → K[Al(OH)4]
4. Гидроксид алюминия разлагается при нагревании:
2Al(OH)3 → Al2O3 + 3H2O
Видеоопыт взаимодействия гидроксида алюминия с соляной кислотой и щелочами (амфотерные свойства гидроксида алюминия) можно посмотреть здесь.
Понравилось это:
Нравится Загрузка…
Гидроксид алюминия
Гидроксид алюминия- Главная >
- Продукты >
- Каучук и химия для РТИ >
- Химия для РТИ >
- Гидроксид алюминия
Руководитель направления
Гимадиева Анна
- +7 (495) 225–44–40 (доб. 1610)
- [email protected]
Менеджер по работе с клиентами
Косолапова Светлана
- +7 (495) 225-44-40 (доб.

- [email protected]
Описание
Антипирены на основе гидроксидов алюминия (Portaflame SG) наиболее широко применяются для снижения горючести различных систем: кабельной изоляции, РТИ изделий специального применения (конвейерные ленты в шахтах и туннелях) искусственных ковровых покрытий (особенно высокие требования для общественных зданий), широкого спектра строительных материалов, в том числе отделочных, гидроизоляционных.
Все возрастающие требования к экологичности и безопасности готовых систем и продуктов ограничивают применение других, иногда даже более активных антипиренов на основе сурьмы, фосфора и галогенов.
Кроме того гидроксид алюминия удобен в обращении, сам по себе являются нетоксичным и безопасным продуктам, относительно дешевым.
Антигорючие свойства готовых композиций, содержащих гидроксид алюминия, обусловлены образованием воды в момент разложения гидроксидов металлов под действием высоких температур.
Температуры разложения гидроксида алюминия составляют диапазон 190–230 °С. Это определяет применение данного антипирена в производстве конструкционных пластиков: полиолефинов, АБС и т.д. Значительное влияние на температуру разложения оказывает дисперсность порошков. Чем больше удельная поверхность наполнителя (меньше размер частиц), тем более эффективны его антигорючие и дымоподавляющие свойства. Эффективность антипиренов напрямую зависит от количества гидроксида алюминия в системе. Большие концентрации (выше 50%) наполнителя приводят к значительному загущению системы, к снижению физико-механических показателей. Компания Sibelco имеет в своем портфеле специальные марки гидроксидов алюминия (Portaflame LV, low viscosity) с определенным распределением частиц порошка по размеру. Оптимальная упаковка частиц разного диаметра позволяет уменьшить влияние больших количеств порошка на вязкость систем.
Характеристики
Листать влево
Основные марки гидроксида алюминия Portaflame SG
| Марка |
D50, мкм Лазерная дифракция |
Удельная площадь поверхности, М2/г |
Цветовые характеристики, (D65;10º) L* |
Кажущаяся плотность, г/см3 |
Влажность, % |
|---|---|---|---|---|---|
| SG10LSA | 3,3 | 5,0 | 98,5 | 0,6 | 0,4 |
| SG25 | 7,3 | 4,1 | 97,5 | 0,6 | 0,2 |
| SG40 | 11,5 | 2,7 | 97,0 | 0,7 | 0,2 |
| SG63 | 23,0 | 0,7 | 96,5 | 1,0 | 0,2 |
| SG100 | 28,0 | 0,65 | 95,0 | 1,2 | 0,2 |
| SG200 | 100 | – | 94,0 | 1,3 | – |
Упаковка:
— Бумажный мешок, 25 кг
— Паллета, 1200 кг
Используется в совместной рецептуре
Руководитель направления
Гимадиева Анна
- +7 (495) 225–44–40 (доб.
 1610)
1610) - [email protected]
Менеджер по работе с клиентами
Косолапова Светлана
- +7 (495) 225-44-40 (доб. 1614)
- [email protected]
Наверх
Разновидности Гидрооксидов Алюминия в Природе
Гидроксид алюминия
Гидроксид алюминия в природе встречается в двух возможных формах: тригидроксид Al (OH)3 и моногидроксид ALOOH. Каждый из представленных видов характеризуется наличием кристаллических разновидностей.
Тригидроксид алюминия отличается тремя полиморфными кристаллическими разновидностями:
- гидраргиллит;
- байерит;
- нордстрандит.
Моногидрит алюминия имеет две основных разновидности:
- бёмит;
- диаспор.
Гидраргиллит
Гидраргиллит представляет собой основу гидраргиллитовых бокситов и латеритов. Последние ‒ это продукты, которые образовались в результате выветривания известняка. В чистом виде гидраргиллит добывают на Урале в продуктах изменения нефелина или в пустотах тальковых сланцев.
Последние ‒ это продукты, которые образовались в результате выветривания известняка. В чистом виде гидраргиллит добывают на Урале в продуктах изменения нефелина или в пустотах тальковых сланцев.
Искусственным способом получить данный элемент можно во время производства глинозема. В таком случае осуществляется разложение алюминатных растворов, когда температура составляет выше +40 градусов.
Кристаллы гидраргиллита, полученные за счет применения метода Байера, характеризуются формой пластинок и призм. Кристаллы, полученные путем карбонизации алюминатных растворов, имеют форму прямоугольных пластин или клиновидную форму удлиненного типа.
Характер агрегирования кристаллов, полученных после декомпозиции алюминатных растворов ‒ листовато-пластинчатый. В таком гидроксиде всевозможные добавки равномерно расположены по всей поверхности материала.
Характер
агрегирования кристаллов, которые были получены при карбонизации растворов ‒
радиально-лучистый. В этом гидроксиде кристаллы расположены в центральной части
и направлены в разные стороны. Новые кристаллообразные элементы будут
сфокусированы уже по радиальным направлениям.
Новые кристаллообразные элементы будут
сфокусированы уже по радиальным направлениям.
Кристаллы гидраргиллита могут быть разных цветовых оттенков:
- белый;
- светло-розовый;
- светло-зеленый;
- светло-бурый.
При этом все кристаллы имеют стеклянный блеск.
В зарубежной технической литературе гидраргиллит достаточно часто встречается под названием гиббсит.
Химический состав гидраргиллита: Al2O3*3H2O = 2Al (OH)3.
Одним из первых, кто предложил модель кристаллической структуры гидраргиллита, был Паулинг.
Структура гидраргиллита состоит из нескольких слоев, между которыми находится лист ионов алюминия.
Байерит
Байерит ‒ это искусственно созданный минерал. Его добывают из кислых растворов солей алюминия, когда отмечают повышенный pH.
Такой материал выделяется в результате:
- Карбонизации
алюминатных растворов, в составе которых содержится порядка 200 г/л оксида
алюминия в условиях комнатной температуры.

- Самостоятельного разложения данных растворов при комнатной температуре.
- Старения коллоидного гидроксида алюминия.
В природе байерит содержится в известняках, где минерал представлен в виде волокон. Такие известняки были найдены в Израиле. В Украине минерал отыскали в коре выветривания амфиболитов.
По своим размерам кристаллы данного минерала достаточно мелкие. Они характеризуются клиноподобной формой, а также встречаются варианты в форме иглы. В результате создаются агрегаты, которые прозвали соматоидами.
По химическому составу байерит абсолютно идентичный с гидраргиллитом: Al (OH)
3.Что касается конкретной структуры байерита, на сегодняшний день не существует единого мнения. Некоторые ученые считали, что этот минерал по своей структуре напоминает гидраргиллит и также характеризуется тремя слоями. Однако нашлись ученые, которые утверждали: байерит подразумевает под собой спирально-дислокационный рост гидраргиллита.
Однако
на сегодня многие придерживаются мнения, что байерит все же имеет много общего
со структурой гидраргиллита. Отличие заключается лишь в расположении слоев
октаэдров.
Отличие заключается лишь в расположении слоев
октаэдров.
Нордстрандит
Изначально этот минерал был получен искусственным путем, но немного позже было выяснено, что норстрандит встречается также и в природе.
Искусственным путем минерал впервые получил Нордстранд, когда происходил процесс обработки металлического алюминия или геля гидроксида алюминия с применением растворов диаминового этилена на основе воды. В чистом виде представленный минерал также добывали в процессе старения хелатообразующих агентов в условиях, при которых мог бы получиться байерит, если бы не были использованы эти агенты.
В
природе минерал встречается достаточно редко. Впервые его отыскали на острове
Гуам в порах красного миоценового известняка в участке, где он контактировал с
базальтом, что уже успел обветриться. На другом острове (Борнео) нордстрандит
обнаружили в карстовых полостях известняков, где отмечают огромное количество
красноземных почв. В Венгрии минерал отыскали в присутствии байерита и
гидраргиллита: здесь нордстрандит был представлен фракциями размером 1-5 мкм.
Отличить представленный минерал достаточно просто, он имеет вид кристаллов ‒ бесцветных или белого цвета, которые отличаются разнообразными формами. По сравнению с кристаллами гидраргиллита, эти кристаллы имеют более крупные размеры и волнистую структуру. Еще одно отличие нордстрандита от гидраргиллита заключается в отсутствии кристаллической решетки ионов щелочных металлов. От байерита такой минерал отличается следующим: при использовании щелочей или 2%-ного раствора алюмината калия он все равно не превращается в гидраргиллит.
Во время открытия такой разновидности тригидроксида алюминия Нордстранд прозвал ее байеритом-II или рандомитом. Свое название нордстрандит получил уже после проведения Международного симпозиума по глинозему, который проходил в Мюнстере.
Бёмит
Бёмит
‒ минерал, который впервые открыл немецкий минералог И. Бём. Он отыскал такой
минерал в бокситах, а потому и назвал его бокситом. Немного позже Лаппаран
отыскал данный минерал в бокситах Франции, а также в бокситовых глинах в
Шотландии. На Урале бёмит можно встретить в темно-красных и зеленовато-серых
бокситах, представленных в виде миниатюрных кристаллов.
На Урале бёмит можно встретить в темно-красных и зеленовато-серых
бокситах, представленных в виде миниатюрных кристаллов.
Бёмит также можно получить и искусственным путем, если приготовить раствор азотнокислого алюминия, что будет дополнительно подкисленным азотной кислотой. Представленный раствор необходимо подогреть до температуры 320-360 градусов с учетом давления, что варьируется от 200 до 300 ат.
Бёмит ‒ это моногидроксид алюминия, а его химический состав выглядит следующим образом: Al2O3*H2O = 2AlOOH.
Удельный вес минера составляет 3-3,2 г/см3, а показатели твердости ‒ 3,01-4,00.
Бёмит не имеет ярко-выраженного цветового оттенка, а в бокситах отличается светло-желтым оттенком. Чаще всего его можно встретить в мелкодисперсном виде, он находится в скрытокристаллической или слабокристаллической форме.
Структура бёмита
О
кристаллической структуре минерала впервые рассказали Рейхерт и Йостом. Она
подразумевает наличие двойных слоев «гофрированного» типа кислородных октаэдров. По центу находятся ионы алюминия.
По центу находятся ионы алюминия.
Также, в структуре минера находятся атомы кислорода сразу нескольких видов:
- Атомы, которые расположены посередине слоев. Они разделяются четырьмя октаэдрами.
- Наружные атомы, что разделяются только двумя октаэдрами.
Каждый из наружных атомов кислорода соединен посредством надежной водородной связи с несколькими аналогичными атомами, которые находятся в соседнем слое. Двойные слои были созданы таким образом, что на каждую элементарную ячейку рассчитано по два слоя. В результате в бёмите около 50% от общего количества атомов кислорода не принимают участия в водородной связи.
По сравнению с гидраргиллитом, в котором каждый ион находится в окружении шести гидроксильных групп, в бёмите ионы Al3+ расположены в окружении четырех кислородных ионов, а также двух гидроксилов.
Помимо известного
бёмита отмечают еще одну менее популярную метастабильную моногидроксидную форму
‒ псевдобёмит. Он является изоморфной формой бёмита и имеет достаточно много
отличительных свойств.
Псевдобёмит подразумевает собой соединение состава Al2O3*x H2O, где 2<x>1. В составе псевдобёмита содержится на 30-100% больше воды, чем необходимо согласно формуле AlOOH. Такое большое количество воды связано с прочными водородными связями, которые имеются между слоями решетки. Поэтому псевдобёмит невозможно рассматривать в качестве коллоидного слабокристаллизованного бёмита.
Диаспор
Диаспор ‒ это составной элемент диаспоровых, а также диаспор-бёмитовых бокситов. В чистом виде такой минерал отыскали в наждачных копях США и Греции, на Урале, в Узбекистане. Получить диаспор можно искусственным путем, если на протяжении долгого времени выдерживать бёмит в условиях температурного режима от +280 градусов.
Кристаллы
отличаются пластинчатой формой. Иногда можно встретить игольчатые и чешуйчатые,
а также призматическую форму. Такие различные формы объясняются всевозможными
температурными показателями и особенностями среды, где находится диаспор. Ведь
именно от этих показателей напрямую зависит скорость процесса кристаллизации.
Ведь
именно от этих показателей напрямую зависит скорость процесса кристаллизации.
Что касается цветовых оттенков, диаспор может быть представлен в белом, розовом, светло-фиолетовом, желтовато-буром, коричневом и зеленовато-сером оттенках.
Диаспор имеет аналогичный бёмиту состав: Al2O3*H2O = 2AlOOH. Удельный вес варьируется от 3,2 до 3,5 г/см3, а показатели твердости составляют ‒ от 6,5 до 7,25.
Самая простая ячейка состоит из четырех формульных единиц AlOOH. Точно также, как и бёмит, диаспор кристаллизуется в орторомбической или же орто-дипирамидальной системе.
Кристаллическую структуру такого элемента предложили Дефландром и Такане.
В основе находятся слои, что состоят из кислородных атомов. Ионы алюминия находятся в октаэдрическом положении и расположены между слоями. Таким образом, удалось получить целые ленты октаэдров.
Характерная
особенность диаспора заключается в отсутствии воды. Из каждой пары кислородных
атомов один атом кислорода достаточно прочно связан с атомом водорода, поэтому
отмечают следующую формулу диаспор: AlO*(OH).
Таким образом, все вышеперечисленные разновидности гидроксидов алюминия считаются слоистыми типами минералов, которые были собраны на основе октаэдрических алюмогидроксилксилородных слоев. Все минералы, кроме бёмита, расположены в гексагональном или же псевдогексагональном порядке. Между ними сохраняется надежная водородная связь.
По возрастанию и стабильности все три вида тригидроксида алюминия расположены в следующем порядке: нордстрандит → байерит → гидраргиллит.
Гидроксид алюминия в природе расположен в следующем порядке: диаспор → бёмит → гидраргиллит.
Превращения и равновесные состояния в системе Al
2O3 ‒ H2OРазновидности три- и моно- гидроксидов алюминия могут превращаться друг в друга, если были соблюдены определенные для этого условия. Было отмечено, что чаще всего подобные превращения наблюдаются внутри отдельно взятого ряда элементов, чем из одного ряда в другой.
Исходя из этого, Габер классифицировал гидроксид алюминия, выделяя две основных группы:
- γ-ряд, куда относится бёмит и гидраргиллит;
- α-ряд,
куда относится корунд и диаспор.

Процесс превращения осуществляется при нагревании до температуры от +500 градусов и больше.
В природе образование гидроксидов алюминия происходит в такой последовательности: аморфный гель Al3+ → псевдобёмит → байерит → гидраргиллит.
Если речь идет о нейтральной и кислой среде обитания, тогда псевдобёмит может превратиться в бёмит, а в условиях щелочной среды ‒ в байерит.
В
результате активного влияния атмосферного давления гидроксиды алюминия могут с
легкостью превращаться один в другой, а после ‒ в оксид алюминия. Последнее
превращение происходит в процессе тонкого измельчения, что часто сопровождается
последующей дегидратацией, а также разрушением структурного и морфологического
типа. После тонкого измельчения на поверхности гидроксидов можно увидеть
активные молекулы, что характеризуются большим количеством свободной энергии.
Именно этот аспект становится значимым при частичной аморфизации поверхности и
дальнейшем превращении байерита, гидраргиллита и бёмита в амфорный продукт, а
уже потом в определенную форму Al2O3.
Границы термической устойчивости гидроксидов алюминия и Al2O3 заметно отличаются между собой. К примеру, Вейц и Лаубенгауэр детально изучили особенности структуры в условиях температурных показателей, что варьируются от 100 до 500 градусов.
Таким образом, были получены следующие данные:
- Байерит достаточно устойчив в равновесных условиях при наличии воды, температура которой не выше 155 градусов.
- Гидраргиллит характеризуется отличной устойчивостью в аналогичных условиях, что и байерит. Если температура воды повышается, он может превратиться в бёмит.
- Бёмит демонстрирует свою устойчивость при температурах от 155 до 280 градусов.
- Стабильность диаспора наблюдается в условиях температурных показателей от 280 до 450 градусов. Если температура увеличивается, он превращается в корунд.
- Форма γ отличается стабильностью при температуре от 100 до 500 градусов.
- Форма
α Al2O3 стабильна, если температурные показатели выше 450 градусов.

Термическое разложение гидроксид алюминия
Многие исследователи спорят о том, как именно происходит такой сложный процесс разложения гидроксидов алюминия. Большинство придерживаются мнения, что разложение осуществляется в два этапа:
- До температуры 340 градусов отмечают наличие двух молекул кристаллизационной воды. Таким образом, гидраргиллит превращается в бёмит.
- Когда температурные показатели увеличиваются до 600 градусов, отмечают выделение последней молекулы воды и бёмит переходит в следующую форму ‒ безводный глинозем. Если подогреть такой глинозем до температуры 900 градусов, он становится полноценным корундом.
Многочисленные
исследования подтвердили, что в первую очередь происходит выделение порядка 0,5
молей кристаллизационной воды, когда температурные показатели варьируются от
167 до 270 градусов. После этого выделяется еще 1,5 моля воды, когда отмечают
температуру от 240 до 420 градусов. Последняя молекула воды выделятся, когда
температура увеличивается до 420-580 градусов.
При увеличении температурных показателей прокаливания гидраргиллита его структура становится упорядоченной. Однако отмечают существенные изменения в физическом и структурном плане. Поэтому исследования доказали кардинальные изменения в таких характеристиках, как:
- удельный вес;
- пористость структуры;
- гидрофильность;
- насыпной вес;
- удельная поверхность;
- дисперсионный состав;
- оптические свойства.
Термическое разложение гидраргиллитов
В случае сильного обезвоживания гидраргиллита под воздействием воздушных масс внутри кристаллов образовывается повышенное давление водяных паров. Их воздействие на материал можно сравнить с действием насыщенного водяного пара в гидротермальных условиях. В таком случае происходит образование бёмита.
При
малейшем понижении давления водяных паров процесс создания бёмита постепенно
замедляется. Это приводит к тому, что гидраргиллит в обезвоженном виде при
температурных показателях от 300 до 400 градусов превращается в Al2O3.
Термическое разложение байерита осуществляется подобно процессу изменения гидраргиллита: через бёмит и через промежуточные стадии Al2O3 в корунд.
Что касается термограммы нордстрандита, она имеет много общего с показателями природного гидраргиллита. Однако отмечают одно существенное отличие: наличие большей интенсивности эндотермического эффекта при температурных показателях от 500 до 600 градусов. Это объясняется дегидратацией созданного бёмита.
Термические превращения, которые были проведены Русселем и Кохраном, исключают θ-модификацию Al2O3. От размеров частиц бёмита зависит дальнейшая реакционноспособность и направление реакции термического процесса разложения. Переход бёмита к корунду является достаточно сложным процессом, так по своей структуре это два совершенно разных элемента.
Диаспор при нагревании до температуры от 450 градусов и больше превращается в корунд. Ведь такие элементы характеризуются похожими структурами.
По материалам книги «Глинозем и пути содержания в нем примесей», А. А. Ханамирова, издательство АН Армянской ССР, Ереван, 1983 г.
6)Оксид и гидроксид алюминия. Получение и свойства
Оксид алюминия – Al2O3. Физические свойства: оксид алюминия – белый аморфный порошок или очень твердые белые кристаллы.
Получение: оксид алюминия получают методом восстановления алюминием металлов из их оксидов: хрома, молибдена, вольфрама, ванадия и др. – металлотермия, открытый Бекетовым:
Cr2O3 + Al = Al2O3 + 2Cr
Химические свойства:
Оксид алюминия проявляет амфотерные свойства
1. взаимодействие с кислотами
А12О3 +6HCl = 2AlCl3 + 3h3O
2. взаимодействие со щелочами
А12О3 + 2NaOH – 2NaAlO2 + h3O
Al2O3 + 2NaOH + 5h3O = 2Na[Al(OH)4(h3O)]
3.
при накаливании смеси оксида
соответствующего металла с порошком
алюминия происходит бурная реакция,
ведущая к выделению из взятого оксида
свободного металла. Метод восстановления
при помощи Al
(алюмотермия) часто применяют для
получения ряда элементов (Cr,
Мп, V,
W
и др.) в свободном состоянии
Метод восстановления
при помощи Al
(алюмотермия) часто применяют для
получения ряда элементов (Cr,
Мп, V,
W
и др.) в свободном состоянии
2А1 + WO3 = А12Оз + W
4. взаимодействие с солями, имеющими сильнощелочную среду, вследствие гидролиза
Al2O3 + Na2CO3 = 2 NaAlO2 + CO2
Гидроксид алюминия – А1(ОН)3. Физические свойства: гидроксид алюминия – белы, аморфный (гелеобразный) или кристаллический. Почти не растворим в воде;
Получение:
1) из солей алюминия под действием раствора щелочей: AlСl3 + 3NaOH = Al(ОН)3 + 3Н2О;
2) разложением нитрида алюминия водой: AlN + 3Н2О = Аl(ОН)3 + NН3?;
3) пропусканием СО2 через раствор гидроксокомплекса: [Аl(ОН)4]-+ СО2 = Аl(ОН)3 + НСО3-;
4) действием на соли Аl гидратом аммиака; при комнатной температуре образуется Аl(ОН)3.
Химические свойства:
1. взаимодействие с кислотами
Al(OH)3 +3HCl = 2AlCl3 + 3h3O
2. при взаимодействии с сильными щелочами образуются соответствующие алюминаты:
NaOH + А1(ОН)з = Na[A1(OH)4]
3. термическое разложение
термическое разложение
2Al(OH)3 = Al2О3 + 3h3O
Гидроксид алюминия не реагирует с гидратом аммиака, хлоридомаммония, диоксидами углерода и серы, сероводородом.
Al2O3 – твердое вещество белого цвета, тугоплавкое. Не реагирует с водой и не растворяется.
Типичный амфотерный оксид, поэтому реагирует с кислотами и щелочами.
Al2O3 + 6 HCl = 2 AlCl3 + 3 H2O
При сплавлении образуется метаалюминат натрия:
Al2O3 (тв)+ 2 NaOH (тв) t→ 2 NaAlO2 + H2O,
В растворе щёлочи образуется тетрагидроксоалюминат натрия:
Al2O3 + 2 NaOH + 3 H2O = 2Na[Al(OH)4]
Алюминаты неустойчивы и даже при слабом подкислении разрушаются:
Na[Al(OH)4] + CO2 = Al(OH)3 + NaHCO3
Al(OH)3 –
белое вещество, нерастворимое в
воде, амфотерный
гидроксид.
Получают косвенно реакцией обмена между солью алюминия и щелочью:
AlCl3 + NaOH (по каплям)= Al(OH)3 ↓ + 3 NaCl
Взаимодействует с кислотами и щелочами.
Al(OH)3 + 3 HCl = AlCl3 + 3 H2O
В растворе: Al(OH)3 + NaOH(избыток) = Na[Al(OH)4]
или Al(OH)3 + 3 NaOH = Na3[Al(OH)6]
В расплавах: Al(OH)3 + NaOH = NaAlO2 + 2H2O
Очень часто амфотерные гидроксиды элементов в степени окисления +III существуют также в мета-форме, например:
AlO(OH) — метагидроксид алюминия
FeO(OH) — метагидроксид железа (орто-форма «Fe(OH)3» не существует).
Амфотерные гидроксиды практически нерастворимы в воде, наиболее удобный способ их получения — осаждение из водного раствора с помощью слабого основания — гидрата аммиака:
Al(NO3)3 + 3(Nh4 · h3O) = Al(OH)3↓ + 3Nh5NO3 (20 °C)
Al(NO3)3 + 3(Nh4 · h3O) = AlO(OH)↓ + 3Nh5NO3 + h3O (80 °C)
В случае использования избытка щелочей в обменной реакции подобного типа гидроксид алюминия осаждаться не будет, поскольку алюминий в силу своей амфотерности переходит в анион:
Al(OH)3(т) + OH− = [Al(OH)4]−
Пример молекулярного уравнения реакции этого типа:
Al(NO3)3 + 4NaOH(избыток) = Na[Al(OH)4] + 3NaNO3
Образующаяся
соль относится к числу комплексных
соединений (комплексных солей): они
включают комплексный анион [Al(OH)4]−. Названия этой соли таково:
Названия этой соли таково:
Na[Al(OH)4] — тетрагидроксоалюминат натрия
Растворение амфотерных гидроксидов в щелочных растворах рассматривается как процесс образования гидроксосолей (гидроксокомплексов). Экспериментально доказано существование гидроксомплексов [Аl(ОН)4(Н2О)2]—, [Аl(ОН)6]3-, [Аl(ОН)5(Н2O)]2-; из них первый — наиболее прочный. Координационное число алюминия в этом комплексе равно 6, т.е. алюминий является шестикоординированным.
Комплексным
(координационным) соединением
(комплексом) называется
такое соединение, в узлах кристаллической
решетки которого находятся комплексные
ионы, обладающие высокой симметрией,
устойчивые как в твердом состоянии, так
и в растворах.
В центре комплексного
иона находится металл (обычно d-металл,
реже р-металл), который
называется комплексообразователь.
Вокруг него очень симметрично
располагаются лиганды,
за счет чего электронная плотность
распределяется равномерно и комплекс
становится устойчивым. Лигандами могут
быть анионы кислот или нейтральные
молекулы (Н2О,
СО, NH3),
которые имеют неподеленную пару
электронов. Она принимает участие в
донорно-акцепторном взаимодействии с
вакантной орбиталью комплексообразователя.
Лигандами могут
быть анионы кислот или нейтральные
молекулы (Н2О,
СО, NH3),
которые имеют неподеленную пару
электронов. Она принимает участие в
донорно-акцепторном взаимодействии с
вакантной орбиталью комплексообразователя.
Гидроксид алюминия, характеристика, свойства и получение, химические реакции
Гидроксид алюминия, характеристика, свойства и получение, химические реакции.
Гидроксид алюминия – неорганическое вещество, имеет химическую формулу Al(OH)3.
Краткая характеристика гидроксида алюминия
Модификации гидроксида алюминия
Физические свойства гидроксида алюминия
Получение гидроксида алюминия
Химические свойства гидроксида алюминия
Химические реакции гидроксида алюминия
Применение и использование гидроксида алюминия
Краткая характеристика гидроксида алюминия:
Гидроксид алюминия – неорганическое вещество белого цвета.
Химическая формула гидроксида алюминия Al(OH)3.
Плохо растворяется в воде.
Обладает способностью адсорбировать различные вещества.
Модификации гидроксида алюминия:
Известны 4 кристаллические модификации гидроксида алюминия: гиббсит, байерит, дойлеит и нордстрандит.
Гиббсит обозначается γ-формой гидроксида алюминия, а байерит – α-формой гидроксида алюминия.
Гиббсит является наиболее химически стабильной формой гидроксида алюминия.
Физические свойства гидроксида алюминия:
| Наименование параметра: | Значение: |
| Химическая формула | Al(OH)3 |
| Синонимы и названия иностранном языке для гидроксида алюминия α-формы | aluminum hydroxide α-form (англ.) байерит (рус.) |
| Синонимы и названия иностранном языке для гидроксида алюминия γ-формы | aluminium hydroxide (англ.) aluminum hydroxide (англ.) гиббсит (рус.) |
| Синонимы и названия иностранном языке для гидроксида алюминия γ’-формы | hydrargillite (англ. ) )гидраргиллит (рус.) |
| Тип вещества | неорганическое |
| Внешний вид гидроксида алюминия α-формы | белые гексагональные кристаллы |
| Внешний вид гидроксида алюминия γ-формы | белые моноклинные кристаллы |
| Цвет | белый |
| Вкус | —* |
| Запах | без запаха |
| Агрегатное состояние (при 20 °C и атмосферном давлении 1 атм.) | твердое вещество |
| Плотность гидроксида алюминия γ-формы (состояние вещества – твердое вещество, при 20 °C), кг/м3 | 2420 |
| Плотность гидроксида алюминия γ-формы (состояние вещества – твердое вещество, при 20 °C), г/см3 | 2,42 |
| Температура разложения гидроксида алюминия, °C | 150-200 °C, > 575 °C |
| Молярная масса, г/моль | 78,004 |
* Примечание:
— нет данных.
Получение гидроксида алюминия:
Гидроксид алюминия получают в результате следующих химических реакций:
- 1.
 в результате взаимодействия хлорида алюминия и гидроксида натрия:
в результате взаимодействия хлорида алюминия и гидроксида натрия:
AlCl3 + 3NaOH → Al(OH)3 + 3NaCl.
При этом гидроксид алюминия выпадает в виде белого студенистого осадка.
Гидроксид алюминия получают также при взаимодействии солей алюминия с водными растворами щёлочи, избегая их избытка.
- 2. в результате взаимодействия хлорида алюминия, карбоната натрия и воды:
2AlCl3 + 3Na2CO3 + 3H2O → 2Al(OH)3 + 3CO2 + 6NaCl.
При этом гидроксид алюминия выпадает в виде белого студенистого осадка.
Гидроксид алюминия получают также при взаимодействии водорастворимых солей алюминия с карбонатами щелочных металлов.
Химические свойства гидроксида алюминия. Химические реакции гидроксида алюминия:
Гидроксид алюминия обладает амфотерными свойствами, т. е. обладает как основными, так и кислотными свойствами.
Химические свойства гидроксида алюминия аналогичны свойствам гидроксидов других амфотерных металлов. Поэтому для него характерны следующие химические реакции:
1. реакция гидроксида алюминия с гидроксидом натрия:
Al(OH)3 + NaOH → NaAlO2 + 2H2O (t ≈ 1000 °C),
Al(OH)3 + 3NaOH → Na3[Al(OH)6],
Al(OH)3 + NaOH → Na[Al(OH)4].
В результате реакции образуются в первом случае – алюминат натрия и вода, во втором – гексагидроксоалюминат натрия, в третьем – тетрагидроксоалюминат натрия. В третьем случае в качестве исходного вещества гидроксид натрия используется в виде концентрированного раствора.
2. реакция гидроксида алюминия с гидроксидом калия:
Al(OH)3 + KOH → KAlO2 + 2H2O (t ≈ 1000 °C),
Al(OH)3 + KOH → K[Al(OH)4].
В результате реакции образуются в первом случае – алюминат калия и вода, во втором – тетрагидроксоалюминат калия. Во втором случае в качестве исходного вещества гидроксид калия используется в виде концентрированного раствора.
Во втором случае в качестве исходного вещества гидроксид калия используется в виде концентрированного раствора.
3. реакция гидроксида алюминия с азотной кислотой:
Al(OH)3 + 3HNO3 → Al(NO3)3 + 3H2O.
В результате реакции образуются нитрат алюминия и вода.
Аналогично проходят реакции гидроксида алюминия и с другими кислотами.
4. реакция гидроксида алюминия с фтороводородом:
Al(OH)3 + 3HF → AlF3 + 3H2O,
6HF + Al(OH)3 → H3[AlF6] + 3H2O.
В результате реакции образуются в первом случае – фторид алюминия и вода, во втором – гексафтороалюминат водорода и вода. При этом фтороводород в первом случае в качестве исходного вещества используется в виде раствора.
5. реакция гидроксида алюминия с бромоводородом:
Al(OH)3 + 3HBr → AlBr3 + 3H2O.
В результате реакции образуются бромид алюминия и вода.
6. реакция гидроксида алюминия с йодоводородом:
Al(OH)3 + 3HI → AlI3 + 3H2O.
В результате реакции образуются йодид алюминия и вода.
7. реакция термического разложения гидроксида алюминия:
Al(OH)3 → AlO(OH) + H2O (t = 150-200 °C),
2Al(OH)3 → Al2O3 + 3H2O (t > 575 °C).
В результате реакции образуются в первом случае – метагидроксид алюминия и вода, во втором – оксид алюминия и вода.
8. реакция гидроксида алюминия и карбоната натрия:
2Al(OH)3 + Na2CO3 → 2NaAlO2 + CO2 + 3H2O.
В результате реакции образуются алюминат натрия, оксид углерода (IV) и вода.
10. реакция гидроксида алюминия и гидроксида кальция:
Ca(OH)2 + 2Al(OH)3 → Ca[Al(OH)4]2.
В результате реакции образуется тетрагидроксоалюмината кальция.
Применение и использование гидроксида алюминия:
Гидроксид алюминия используется при очистке воды (как адсорбирующее вещество), в медицине, в качестве наполнителя в зубной пасте (как абразивное вещество), пластиках и пластмассах (как антипирен).
Примечание: © Фото //www.pexels.com, //pixabay.com
гидроксид алюминия реагирует кислота 1 2 3 4 5 вода
уравнение реакций соединения реакции масса взаимодействие гидроксида
Коэффициент востребованности 11 057
Гидроксид алюминия: информация о лекарствах MedlinePlus
произносится как (a loo’ mi num) (hye drox’ ide)
Чтобы использовать функции обмена на этой странице, включите JavaScript.
Гидроксид алюминия используется для облегчения боли при изжоге, кислом желудке и пептической язве, а также для ускорения заживления пептической язвы.
Гидроксид алюминия выпускается в виде капсул, таблеток, пероральной жидкости и суспензии. Доза и частота использования зависят от состояния, которое лечат. Перед введением суспензию необходимо хорошо взболтать. Внимательно следуйте указаниям на упаковке или этикетке с рецептом и попросите своего врача или фармацевта объяснить любую часть, которую вы не понимаете.
Гидроксид алюминия также иногда используется для уменьшения количества фосфатов в крови у пациентов с заболеваниями почек. Поговорите со своим врачом о возможных рисках использования этого препарата для вашего состояния.
Прежде чем принимать гидроксид алюминия,
- сообщите своему врачу и фармацевту, если у вас аллергия на гидроксид алюминия или какие-либо другие лекарства.
- сообщите своему врачу и фармацевту, какие лекарства, отпускаемые по рецепту и без рецепта, вы принимаете, особенно аллопуринол (лопурин, зилоприм), алпразолам (ксанакс), хлордиазепоксид (либриум, митран и другие), хлорохин (арален), циметидин (тагамет), клоназепам (клонопин), клоразепат, дексаметазон (декадрон и др.
 ), диазепам (валиум, валрелиз и зетран), дифлунисал (долобид), дигоксин (ланоксин), этамбутол (миамбутол), фамотидин (пепцид), галазепам (паксипам), гидрокортизон ( Кортон, Гидрокортон), изониазид (Ланиазид, Нидразид), левотироксин (Левотроид, Левоксил, Синтроид и др.), Лоразепам (Ативан), метилпреднизолон (Медрол), оксазепам (Серакс), пеницилламин (Купримин, Депен), преднизолон (Дельтазон, Оразон), препараты, содержащие железо, тетрациклин (Сумицин, Тетракап и др.), тиклопидин (Тиклид), витамины.
), диазепам (валиум, валрелиз и зетран), дифлунисал (долобид), дигоксин (ланоксин), этамбутол (миамбутол), фамотидин (пепцид), галазепам (паксипам), гидрокортизон ( Кортон, Гидрокортон), изониазид (Ланиазид, Нидразид), левотироксин (Левотроид, Левоксил, Синтроид и др.), Лоразепам (Ативан), метилпреднизолон (Медрол), оксазепам (Серакс), пеницилламин (Купримин, Депен), преднизолон (Дельтазон, Оразон), препараты, содержащие железо, тетрациклин (Сумицин, Тетракап и др.), тиклопидин (Тиклид), витамины. - имейте в виду, что гидроксид алюминия может мешать действию других лекарств, делая их менее эффективными. Принимайте другие лекарства за 1 час до или через 2 часа после приема гидроксида алюминия.
- Сообщите своему врачу, если у вас есть или когда-либо были гипертония, болезни сердца или почек или желудочно-кишечные кровотечения.
- сообщите своему врачу, если вы беременны, планируете забеременеть или кормите грудью. Если вы забеременели при приеме гидроксида алюминия, позвоните своему врачу.

Примите пропущенную дозу, как только вспомните. Однако, если почти пришло время для следующей дозы, пропустите пропущенную дозу и продолжайте свой обычный график дозирования. Не принимайте двойную дозу, чтобы компенсировать пропущенную.
Гидроксид алюминия может вызывать побочные эффекты. Сообщите своему врачу, если эти симптомы являются серьезными или не проходят:
- запор
- потеря аппетита
Если вы испытываете какие-либо из следующих симптомов, немедленно обратитесь к врачу:
- спутанность сознания
- необычная усталость или дискомфорт
- мышечная слабость
Если вы испытываете серьезные побочные эффекты, вы или ваш врач можете отправить отчет в онлайн-программу MedWatch для сообщений о нежелательных явлениях Управления по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) (http ://www.fda.gov/Safety/MedWatch) или по телефону (1-800-332-1088).
Храните это лекарство в контейнере, в котором оно было получено, плотно закрытым и в недоступном для детей месте. Храните его при комнатной температуре и вдали от избыточного тепла и влаги (не в ванной).
Храните его при комнатной температуре и вдали от избыточного тепла и влаги (не в ванной).
Важно хранить все лекарства вне поля зрения и в недоступном для детей месте, так как многие контейнеры (например, контейнеры для еженедельных таблеток и контейнеры для глазных капель, кремов, пластырей и ингаляторов) не защищены от детей, и маленькие дети могут легко их открыть . Чтобы защитить маленьких детей от отравления, всегда запирайте защитные колпачки и немедленно кладите лекарство в безопасное место — то, которое находится наверху и далеко, вне поля их зрения и досягаемости. http://www.upandaway.org
Ненужные лекарства следует утилизировать особым образом, чтобы домашние животные, дети и другие люди не могли их употребить. Однако не следует смывать это лекарство в унитаз. Вместо этого лучший способ избавиться от ваших лекарств — это воспользоваться программой возврата лекарств. Поговорите со своим фармацевтом или обратитесь в местный отдел мусора/переработки, чтобы узнать о программах возврата в вашем районе. Посетите веб-сайт FDA по безопасной утилизации лекарств (http://goo.gl/c4Rm4p) для получения дополнительной информации, если у вас нет доступа к программе возврата.
Посетите веб-сайт FDA по безопасной утилизации лекарств (http://goo.gl/c4Rm4p) для получения дополнительной информации, если у вас нет доступа к программе возврата.
- Alderagel ®
- ALU-CAP ®
- ALU-TAB ®
- AMPHOJEL ®
Просмотр лекарств и лекарственных средств
Гидроксид алюминия и гидроксид магния: информация о лекарствах MedlinePlus
произносится как (a loo’ mi num) (hye drox’ ide) (mag nee’ zhum) (hye drox’ ide)
Чтобы использовать функции обмена на этой странице, включите JavaScript.
Гидроксид алюминия, Гидроксид магния — это антациды, используемые вместе для облегчения изжоги, кислотного несварения желудка и расстройства желудка. Их можно использовать для лечения этих симптомов у пациентов с язвенной болезнью, гастритом, эзофагитом, грыжей пищеводного отверстия диафрагмы или повышенным содержанием кислоты в желудке (повышенная кислотность желудка). Они соединяются с желудочной кислотой и нейтрализуют ее. Гидроксид алюминия, гидроксид магния доступны без рецепта.
Их можно использовать для лечения этих симптомов у пациентов с язвенной болезнью, гастритом, эзофагитом, грыжей пищеводного отверстия диафрагмы или повышенным содержанием кислоты в желудке (повышенная кислотность желудка). Они соединяются с желудочной кислотой и нейтрализуют ее. Гидроксид алюминия, гидроксид магния доступны без рецепта.
Это лекарство иногда назначают для других целей; попросите вашего врача или фармацевта для получения дополнительной информации.
Это лекарство выпускается в виде жевательных таблеток и жидкости для приема внутрь. Тщательно разжевывайте таблетки; не глотайте их целиком. Выпейте полный стакан воды после приема таблеток. Хорошо встряхните жидкость для приема внутрь перед каждым использованием, чтобы равномерно смешать лекарство. Жидкость можно смешивать с водой или молоком.
Внимательно следуйте указаниям на этикетке на упаковке или на этикетке с рецептом и попросите своего врача или фармацевта объяснить любую часть, которую вы не понимаете. Принимайте антациды гидроксида алюминия, гидроксида магния точно в соответствии с указаниями. Не принимайте больше или меньше и не принимайте чаще, чем предписано врачом. Не принимайте антациды более 1–2 недель, если это не предписано врачом.
Принимайте антациды гидроксида алюминия, гидроксида магния точно в соответствии с указаниями. Не принимайте больше или меньше и не принимайте чаще, чем предписано врачом. Не принимайте антациды более 1–2 недель, если это не предписано врачом.
Прежде чем принимать антациды на основе гидроксида алюминия, антациды на основе гидроксида магния,
- , сообщите своему врачу и фармацевту, если у вас аллергия на антациды на основе гидроксида алюминия, антациды на основе гидроксида магния или какие-либо другие препараты.
- сообщите своему врачу и фармацевту, какие рецептурные и безрецептурные лекарства вы принимаете, особенно аспирин, хиноксацин (Cinobac), ципрофлоксацин (Cipro), дигоксин (ланоксин), диазепам (валиум), эноксацин (Penetrex), сульфат железа (железо), флуконазол (Дифлюкан), индометацин, изониазид (INH), итраконазол (Споранокс), кетоконазол (Низорал), левофлоксацин (Левакин), ломефлоксацин (Максакин), налидиксовая кислота (НегГрам), норфлоксацин (Нороксин), офлоксацин (Флоксин), спарфлоксацин ( Загам), тетрациклин (Ахромицин, Сумицин) и витамины.
 Если ваш врач рекомендует вам принимать антациды во время приема этих лекарств, не принимайте их в течение 2 часов после приема антацида.
Если ваш врач рекомендует вам принимать антациды во время приема этих лекарств, не принимайте их в течение 2 часов после приема антацида. - Сообщите своему врачу, если у вас есть или когда-либо было заболевание почек.
- сообщите своему врачу, если вы беременны, планируете забеременеть или кормите грудью. Если вы забеременели при приеме антацидов гидроксида алюминия, гидроксида магния, позвоните своему врачу.
Если вы принимаете это лекарство от язвы, тщательно соблюдайте диету, назначенную врачом.
Если вы принимаете запланированные дозы гидроксида алюминия, гидроксида магния, примите пропущенную дозу, как только вспомните об этом. Однако, если почти пришло время для следующей дозы, пропустите пропущенную дозу и продолжайте свой обычный график дозирования. Не принимайте двойную дозу, чтобы компенсировать пропущенную.
Побочные эффекты от гидроксида алюминия и гидроксида магния встречаются редко. Чтобы избежать мелового вкуса, принимайте с водой или молоком.
 Сообщите своему врачу, если какой-либо из этих симптомов является серьезным или не проходит:
Сообщите своему врачу, если какой-либо из этих симптомов является серьезным или не проходит:- диарея
- запор
- потеря аппетита
- необычная усталость
- мышечная слабость
Храните это лекарство в контейнере, в котором он пришел, плотно закрытым и в недоступном для детей месте. Храните его при комнатной температуре и вдали от избыточного тепла и влаги (не в ванной).
Ненужные лекарства следует утилизировать особым образом, чтобы домашние животные, дети и другие люди не могли их употребить. Однако не следует смывать это лекарство в унитаз. Вместо этого лучший способ избавиться от ваших лекарств — это воспользоваться программой возврата лекарств. Поговорите со своим фармацевтом или обратитесь в местный отдел мусора/переработки, чтобы узнать о программах возврата в вашем районе. Посетите веб-сайт FDA по безопасной утилизации лекарств (http://goo.gl/c4Rm4p) для получения дополнительной информации, если у вас нет доступа к программе возврата.
Важно хранить все лекарства вне поля зрения и в недоступном для детей месте, так как многие контейнеры (например, контейнеры для еженедельных таблеток и контейнеры для глазных капель, кремов, пластырей и ингаляторов) не защищены от детей, и маленькие дети могут легко их открыть . Чтобы защитить маленьких детей от отравления, всегда запирайте защитные колпачки и немедленно кладите лекарство в безопасное место — то, которое находится наверху и далеко, вне поля их зрения и досягаемости. http://www.upandaway.org
- Аламаг ®
- Alumina and Magnesia ®
- Antacid (aluminum-magnesium) ®
- Antacid M ®
- Antacid Suspension ®
- Gen-Alox ®
- Kudrox ®
- M.A.H. ®
- Маалокс HRF ®
- Маалокс Т.С. ®
- Магагель ®
- Магналокс ®
- Мальдроксал ®
- Миланта ® Ultimate
- Ri-Mox ®
- Rulox ®
 05.2019
05.2019Просмотр лекарств и медикаментов
EWG Skin Deep® | Что такое ГИДРОКСИД АЛЮМИНИЯ
Знай свою окружающую среду. Защитите свое здоровье.
Данные: Fair
Гидроксид алюминия
ИСТОЧНИК ИЗОБРАЖЕНИЯ: PubChem
ПОИСК ПРОДУКТОВ
- НАЙТИ ПРОДУКТЫ С ЭТИМ ИНГРЕДИЕНТОМ
Другие проблемы
Токсичность нерепродуктивной системы органов (умеренная)
СИНОНИМЫ
ГИДРОКСИД АЛЮМИНИЯ, ГИДРОКСИД АЛЮМИНИЯ, ГИДРАТНЫЙ, ГЛИНОЗЕМ, ТРИГИДРАТ, СУЛЬФАТ АЛЮМИНИЯ ГИДРОКСИД, ГИДРОКСИД АЛЮМИНИЯ, СУЛЬФАТ ГИДРОКСИД АЛЮМИНИЯ (AL(OH)(SO4)), ТРИГИДРАТ ОКСИДА АЛЮМИНИЯ, ОКСИД АЛЮМИНИЯ, ГИДРАТ, ТРИГИДРОКСИД АЛЮМИНИЯ, ГИДРОКСИД АЛЮМИНИЯ 270, ГИДРОКСИД АЛЮМИНИЯ70, ОКСИД АЛЮМИНИЯ, ГИДРАТИРОВАННЫЙ ГЛИНОЗ АЛЮМИНИЙ, ПИГМЕНТ БЕЛЫЙ 24, ТРИГИДРАТ АЛЮМИНИЯ, ТРИГИДРОКСИЛЬ АЛЮМИНИЯ и ТРИГИДРОКСЯЛЮМИНИЙ
Гидроксид алюминия, также известный как гидратированный оксид алюминия, представляет собой форму алюминия, используемую в качестве красителя.
Общие проблемы
Посмотрите, как этот продукт оценивается по общим проблемам.
Рак
Аллергия и иммунотоксичность
Токсичность для развития и репродуктивной функции
Ограничения на использование
Проблемы с ингредиентами
- Проблемы
- ИСТОЧНИКИ ДАННЫХ
| foundation | 683 products |
| concealer | 351 products |
| lipstick | 299 products |
| daily use with SPF | 131 products |
| CC cream | 108 products |
| карандаш для бровей | 92 товаров |
| блеск для губ | 87 товаров |
| лак для ногтей | 77 products |
| BB cream | 75 products |
| blush | 75 products |
| eye shadow | 66 products |
| eye liner | 58 products |
| recreational sunscreen | 47 товаров |
| бронзер/хайлайтер | 28 товаров |
| основа под макияж | 22 товара |
| lip liner | 18 products |
| lip balm | 14 products |
| glitter | 12 products |
| facial powder | 12 products |
| facial moisturizer/treatment | 12 products |
| средство для увеличения губ | 12 товаров |
| против старения | 10 товаров |
| маска | 10 товаров | around-eye cream | 8 products |
| setting powder/spray | 7 products |
| pore strips | 7 products |
| lip balm with SPF | 6 products |
| serums & эссенции | 5 товаров |
| зубная паста | 5 товаров |
| 4 товара | |
| увлажняющий крем | 90 296 90 297 20297 |
| mascara | 3 products |
| baby sunscreen | 3 products |
| bar soap | 2 products |
| conditioner | 2 products |
| skin fading/lightener | 2 products |
| воски для депиляции | 2 продукта |
| средства для снятия макияжа | 2 продукта |
| тоники/вяжущие средства | 1 products |
| damaged skin treatment | 1 products |
| facial cleanser | 1 products |
| body powder | 1 products |
| exfoliant/scrub | 1 products |
| отбеливание зубов | 1 товаров |
| клей для ногтей | 1 товаров |
| КОНЦЕРН | НОМЕР |
|---|---|
| , классифицированные, как ожидалось, будет токсичным или вредным | Список внутренних веществ Канады |
| Список средней группы | . org Информация о токсичности org Информация о токсичности |
| КОНЦЕРН | ССЫЛКА |
|---|---|
| Нет подозрений на то, что он является экологическим токсином | Внутренний список веществ Канады по охране окружающей среды |
| КОНЦЕРН | НОМЕР |
|---|---|
| Нет подозрений на биоаккумуляцию | Внутренний список веществ Канады по охране окружающей среды |
| КОНЦЕРН | НОМЕР |
|---|---|
| Обозначен как безопасный для общего или специального ограниченного использования в пищевых продуктах | FDA Все, что добавляется в продукты питания |

 2008. Категоризация отечественного списка веществ. Экологический реестр Канадского закона об охране окружающей среды (CEPA).
2008. Категоризация отечественного списка веществ. Экологический реестр Канадского закона об охране окружающей среды (CEPA).
 Сообщите каждому из ваших медицинских работников обо всех ваших заболеваниях, аллергиях и всех лекарствах, которые вы принимаете.
Сообщите каждому из ваших медицинских работников обо всех ваших заболеваниях, аллергиях и всех лекарствах, которые вы принимаете.


 («Multum»), но никаких гарантий на этот счет не дается. Содержащаяся здесь информация о препарате может меняться с течением времени. Информация Multum была собрана для использования практикующими врачами и потребителями в Соединенных Штатах, и поэтому Multum не гарантирует, что использование за пределами Соединенных Штатов допустимо, если специально не указано иное. Информация о лекарствах Multum не поддерживает лекарства, не диагностирует пациентов и не рекомендует лечение. Информация о лекарствах Multum — это информационный ресурс, предназначенный для помощи лицензированным практикующим врачам в уходе за своими пациентами и/или для обслуживания потребителей, пользующихся этой услугой, в качестве дополнения, а не замены опыта, навыков, знаний и суждений практикующих врачей. Отсутствие предупреждения для данного препарата или комбинации препаратов никоим образом не должно толковаться как указание на то, что препарат или комбинация препаратов являются безопасными, эффективными или подходящими для данного пациента.
(«Multum»), но никаких гарантий на этот счет не дается. Содержащаяся здесь информация о препарате может меняться с течением времени. Информация Multum была собрана для использования практикующими врачами и потребителями в Соединенных Штатах, и поэтому Multum не гарантирует, что использование за пределами Соединенных Штатов допустимо, если специально не указано иное. Информация о лекарствах Multum не поддерживает лекарства, не диагностирует пациентов и не рекомендует лечение. Информация о лекарствах Multum — это информационный ресурс, предназначенный для помощи лицензированным практикующим врачам в уходе за своими пациентами и/или для обслуживания потребителей, пользующихся этой услугой, в качестве дополнения, а не замены опыта, навыков, знаний и суждений практикующих врачей. Отсутствие предупреждения для данного препарата или комбинации препаратов никоим образом не должно толковаться как указание на то, что препарат или комбинация препаратов являются безопасными, эффективными или подходящими для данного пациента. Multum не несет никакой ответственности за какой-либо аспект медицинского обслуживания, осуществляемого с помощью информации, предоставляемой Multum. Информация, содержащаяся здесь, не предназначена для охвата всех возможных способов применения, указаний, мер предосторожности, предупреждений, взаимодействий с лекарственными средствами, аллергических реакций или побочных эффектов. Если у вас есть вопросы о лекарствах, которые вы принимаете, проконсультируйтесь с врачом, медсестрой или фармацевтом.
Multum не несет никакой ответственности за какой-либо аспект медицинского обслуживания, осуществляемого с помощью информации, предоставляемой Multum. Информация, содержащаяся здесь, не предназначена для охвата всех возможных способов применения, указаний, мер предосторожности, предупреждений, взаимодействий с лекарственными средствами, аллергических реакций или побочных эффектов. Если у вас есть вопросы о лекарствах, которые вы принимаете, проконсультируйтесь с врачом, медсестрой или фармацевтом.
 Вы должны проверить, безопасно ли давать этот препарат вместе со всеми другими препаратами и проблемами со здоровьем вашего ребенка. Не начинайте, не останавливайте и не изменяйте дозу любого препарата, который принимает ваш ребенок, без консультации с врачом.
Вы должны проверить, безопасно ли давать этот препарат вместе со всеми другими препаратами и проблемами со здоровьем вашего ребенка. Не начинайте, не останавливайте и не изменяйте дозу любого препарата, который принимает ваш ребенок, без консультации с врачом. Поговорите с доктором.
Поговорите с доктором.


 Будьте готовы рассказать или показать, что было снято, сколько и когда это произошло.
Будьте готовы рассказать или показать, что было снято, сколько и когда это произошло. Эта информация не подтверждает какие-либо методы лечения или лекарства как безопасные, эффективные или одобренные для лечения конкретного пациента. UpToDate, Inc. и ее аффилированные лица отказываются от каких-либо гарантий или ответственности в отношении этой информации или ее использования. Использование этой информации регулируется Условиями использования, доступными по адресу https://www.wolterskluwer.com/en/know/clinical-efficientness-terms.
Эта информация не подтверждает какие-либо методы лечения или лекарства как безопасные, эффективные или одобренные для лечения конкретного пациента. UpToDate, Inc. и ее аффилированные лица отказываются от каких-либо гарантий или ответственности в отношении этой информации или ее использования. Использование этой информации регулируется Условиями использования, доступными по адресу https://www.wolterskluwer.com/en/know/clinical-efficientness-terms. Гидроксид алюминия также используется для снижения уровня фосфатов у людей с определенными заболеваниями почек.
Гидроксид алюминия также используется для снижения уровня фосфатов у людей с определенными заболеваниями почек.

 Избегайте приема других лекарств в течение 2 часов до или 2 часов после приема гидроксида алюминия.
Избегайте приема других лекарств в течение 2 часов до или 2 часов после приема гидроксида алюминия.