Масляная кислота — важное для здоровья органическое соединение
Масляная кислота — органическое соединение, относящееся к классу жирных карбоновых кислот. Название «масляная кислота» — исторически сложившееся, тривиальное. Химики же называют ее бутановой или этилуксусной кислотой. Общая химическая формула — C4H8O2 или С3Н7СООН. Последний вариант отражает структурный состав, содержащий одну карбоксильную группу —COOH.
Кислота встречается в естественном виде в природе, входит в состав нефти; она есть в коровьем масле, в поте человека и выделениях животных; является продуктом жизнедеятельности некоторых анаэробных микроорганизмов, в том числе обитающих в кишечнике человека.
Получают кислоту химическим или ферментативным синтезом. В первом случае — методом окисления масляного альдегида или бутанола. Во втором — брожением отходов растительного сырья, содержащего крахмал.
Свойства
Летучая маслянистая прозрачная жидкость без цвета, с несильным, но неприятным запахом прогорклого масла. Хорошо смешивается с водой в любых соотношениях, растворяется в спиртах, эфирах и органических растворителях. Образует азеотропную смесь с водой.
Хорошо смешивается с водой в любых соотношениях, растворяется в спиртах, эфирах и органических растворителях. Образует азеотропную смесь с водой.
Относится к одноосновным низкомолекулярным низшим карбоновым кислотам. Образует соли и сложные эфиры. Обладает всеми свойствами карбоновых кислот, вступает в реакции с активными металлами, оснóвными оксидами, щелочами. Взаимодействует со спиртами с образованием сложных эфиров с плодовыми запахами.
Концентрированная масляная кислота вызывает раздражение кожи и глаз. Она токсична для водных организмов.
Значение масляной кислоты для человека
Масляная кислота и ее соли играют огромную роль в физиологических процессах нашего организма. В процессе ферментативных реакций кислота и ее соли создают в кишечнике кислую среду, благоприятную для развития полезных бактерий и подавляющую развитие патогенных, таких как возбудитель сальмонеллы и кишечная палочка E.Coli. Кроме этого, масляная кислота способствует регуляции водно-электролитного баланса в кишечнике, регулирует его моторику.
Этилуксусная кислота регулирует кишечный гомеостаз (способность организма поддерживать свою жизнедеятельность на оптимальном уровне) и защитные свойства слизистой. Обладает противовоспалительным и противораковым действием, улучшает аппетит, способствует эффективному снабжению энергией клеток эпителия, защищает от развития окислительного стресса (процесса повреждения клетки в результате окисления).
Недостаток бутановой кислоты в организме, как правило, приводит к развитию различных воспалительных и онкологических заболеваний толстого кишечника.
По содержанию масляной кислоты в крови и других физиологических жидкостях медики могут судить о наличии/отсутствии заболеваний желудочно-кишечного тракта.
Применение
• Натриевые и кальциевые соли масляной кислоты используются в животноводстве, птицеводстве и рыбоводстве как кормовые добавки. Эти добавки усиливают иммунитет, способствуют лучшей усвояемости пищи, подавляют деятельность многих вредных кишечных бактерий, уменьшают необходимость применения антибиотиков.
• Сырье для синтеза ацетилбутиратов целлюлозы, применяющихся в производстве погодоустойчивых покрытий — в химпроме. Для изготовления лакокрасочных материалов, пластификаторов для лаков, эмульгаторов.
• В фармацевтике — для производства лекарственных препаратов, диагностических систем.
• Для лечения некоторых заболеваний желудочно-кишечного тракта — в медицине.
• В пищепроме на основе эфиров масляной кислоты изготавливают пищевые ароматизаторы с плодовыми запахами, например, с запахом яблока, груши, земляники, ананаса. Эти ароматизаторы используются при производстве варенья, некоторых сортов рома.
• Для синтеза душистых веществ в косметической промышленности.
• В кожевенном производстве кислота применяется для декальцинации кож.
• В аналитической химии — для разделения щелочно-земельных и редкоземельных элементов.
Классификация, строение, изомерия карбоновых кислот
Карбоновые кислоты – это вещества, в молекулах которых содержится одна или несколько карбоксильных групп СООН. |
Общая формула предельных одноосновных карбоновых кислот: СnH2nO2
Строение, изомерия и гомологический ряд карбоновых кислот
Химические свойства карбоновых кислот
Способы получения карбоновых кислот
По числу карбоксильных групп:
- одноосновные карбоновые кислоты — содержат одну карбоксильную группу -СООН. Общая формула CnH2n+1COOH или CnH2nO2.
| Например, уксусная кислота |
- многоосновные карбоновые кислоты — содержат две и более карбоксильные группы СООН. Например, общая формула двухосновных карбоновых кислот
| Например, щавелевая кислота |
Классификация по строению углеводородного радикала
- Предельные карбоновые кислоты – карбоксильная группа СООН соединена с предельным радикалом.
 Например, этановая кислота СН3–СООН.
Например, этановая кислота СН3–СООН. - Непредельные карбоновые кислоты – карбоксильная группа СООН соединена с непредельным радикалом. Например, акриловая кислота: СН2=СН–СООН.
- Ароматические кислоты — карбоксильная группа СООН соединена с непредельным радикалом. Например, бензойная кислота: С6Н5СООН.
- Циклические кислоты — карбоксильная группа СООН соединена с углеводородным циклом. Например, циклопропанкарбоновая кислота: С3Н5СООН.
Карбоксильная группа сочетает в себе две функциональные группы – карбонил и гидроксил, взаимно влияющие друг на друга.
| Электроотрицательность кислорода (ЭО = 3,5) больше электроотрицательности водорода (ЭО = 2,1) и углерода (ЭО = 2,4). |
Электронная плотность смещена к более электроотрицательному атому кислорода.
Атом углерода карбоксильной группы находится в состоянии sp2-гибридизации, образует три σ-связи и одну π-связь.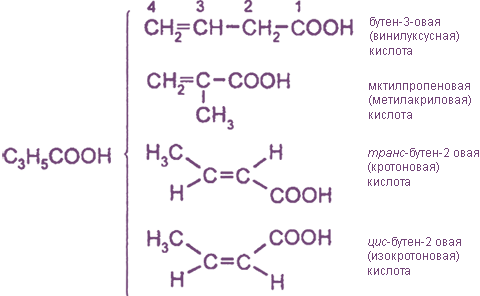
В жидком состоянии и в растворах молекулы карбоновых кислот образуют межмолекулярные водородные связи. Водородные связи вызывают притяжение и ассоциацию молекул карбоновых кислот.
Молекулы карбоновых кислот с помощью водородных связей соединены в димеры.
Это приводит к увеличению растворимости в воде и высоким температурам кипения низших карбоновых кислот.
С увеличением молекулярной массы растворимость кислот в воде уменьшается.
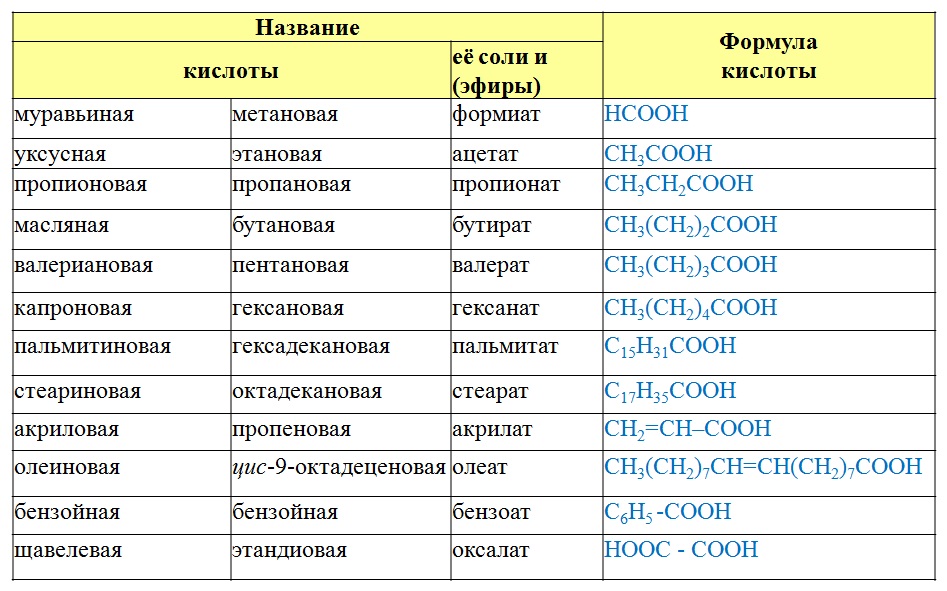
Предельные одноосновные карбоновые кислоты.
| Тривиальное название | Систематическое название | Название соли и эфира | Формула кислоты |
| Муравьиная | Метановая | Формиат (метаноат) | HCOOH |
| Уксусная | Этановая | Ацетат (этаноат) | CH3COOH |
| Пропионовая | Пропановая | Пропионат (пропаноат) | CH3CH2COOH |
| Масляная | Бутановая | Бутират (бутаноат) | CH 3(CH2)2COOH |
| Валериановая | Пентановая | Пентаноат | CH3(CH2)3COOH |
| Капроновая | Гексановая | Гексаноат | CH3(CH2)4COOH |
| Пальмитиновая | Гексадекановая | Пальмитат | С15Н31СООН |
| Стеариновая | Октадекановая | Стеарат | С17Н35СООН |
Таблица. Непредельные одноосновные карбоновые кислоты.
Непредельные одноосновные карбоновые кислоты.
| Тривиальное название | Систематическое название | Название соли и эфира | Формула кислоты |
| Акриловая | Акрилат | CH2=CH–COOH | |
| Метакриловая | 2-Метилпропеновая | Метакрилат | CH2=C(СH3)–COOH |
| Кротоновая | транс-2-Бутеновая | Кротонат | СН3 -CH=CH–COOH |
| Олеиновая | 9- цис-Октадеценовая | Олеат | СН3(СН2)7СН=СН(СН2)7СООН
|
| Линолевая | 9,12-цис-Октадекадиеновая | Линолеат | СН3(СН2)4(СН=СНСН2)2(СН2)6СООН |
| Линоленовая | 9,12,15-цис-Октадекатриеновая | Линоленоат | СН3СН2(СН=СНСН2)3(СН2)6СООН |
Таблица.
| Тривиальное название | Систематическое название | Название соли и эфира | Формула кислоты |
| Щавелевая | Этандиовая | Оксалат | НООС – COOH |
| Малоновая | Пропандиовая | Малонат | НООС-СН2-СООН |
| Янтарная | Бутандиовая | Сукцинат | НООС-(СН2)2-СООН |
| Глутаровая | Пентандиовая | Глутарат | НООС-(СН2)3-СООН |
| Адипиновая | Гександиовая | Адипинат | НООС-(СН2)4-СООН |
| Малеиновая | цис-Бутендиовая | Малеинат | цис-НООССН=СНСООН |
| Фумаровая | транс-Бутендиовая | Фумарат | транс-НООССН=СНСООН |
Таблица. Ароматические карбоновые кислоты.
Ароматические карбоновые кислоты.
| Тривиальное название | Систематическое название | Название соли и эфира | Формула кислоты |
| Бензойная | Фенилкарбоновая | Бензоат | |
| Фталевая | Бензол-1,2-дикарбоновая кислота | Фталат | |
| Изофталевая | Бензол-1,3-дикарбоновая кислота | Изофталат | |
| Терефталевая | Бензол-1,4-дикарбоновая кислота | Терефталат |
Для предельных карбоновых кислот характерна структурная изомерия – изомерия углеродного скелета и межклассовая изомерия.
Структурные изомеры – это соединения с одинаковым составом, которые отличаются порядком связывания атомов в молекуле, т. е. строением молекул.
е. строением молекул.
Изомеры углеродного скелета характерна для карбоновых кислот, которые содержат не менее четырех атомов углерода.
| Например. Формуле С4Н8О2 соответствуют бутановая и 2-метилпропановая кислота |
| Бутановая (масляная) кислота | Изомасляная (2-метилпропановая) кислота |
Межклассовые изомеры — это вещества разных классов с различным строением, но одинаковым составом. Карбоновые кислоты изомерны сложным эфирам. Общая формула и спиртов, и простых эфиров —
| Например. Межклассовые изомеры с общей формулой С2Н4О2: уксусная кислота СН3–CОOH и метилформиат H–COOCH3 |
| Уксусная кислота | Метиловый эфир муравьиной кислоты |
| СН3–CОOH | HCOOCH3 |
Общую формулу СnH2nO2 могут также иметь многие другие полифункциональные соединения, например: альдегидоспирты, непредельные диолы, циклические простые диэфиры и т. п.
п.
Понравилось это:
Нравится Загрузка…
Глава 4 — Карбоновые кислоты, сложные эфиры — CHE 120 — Введение в органическую химию — Учебник
Цели обучения
- Назовите карбоновые кислоты общепринятыми названиями.
- Назовите карбоновые кислоты по номенклатуре IUPAC.
Карбоновые кислоты широко распространены в природе, часто в сочетании со спиртами или другими функциональными группами, такими как жиры, масла и воски. Они входят в состав многих продуктов питания, лекарств и предметов домашнего обихода. Неудивительно, что многие из них наиболее известны под общими именами, основанными на латинских и греческих словах, описывающих их источник. То, что вы узнаете из этой главы о химии карбоновых кислот, поможет вам понять биохимию (глава 6 «Углеводы» — глава 11 «Метаболические пути и производство энергии»).
Простейшая карбоновая кислота, муравьиная кислота (HCOOH), была впервые получена перегонкой муравьев (лат. formica , что означает «муравей»). Укусы некоторых муравьев выделяют муравьиную кислоту, а укусы ос и пчел содержат муравьиную кислоту (а также другие ядовитые материалы).
Укусы некоторых муравьев выделяют муравьиную кислоту, а укусы ос и пчел содержат муравьиную кислоту (а также другие ядовитые материалы).
Следующим более высоким гомологом является уксусная кислота, которая производится путем ферментации сидра и меда в присутствии кислорода. В результате ферментации получается уксус, раствор, содержащий 4–10% уксусной кислоты, а также ряд других соединений, которые придают ему вкус. Уксусная кислота, вероятно, является наиболее известной слабой кислотой, используемой в учебных и промышленных химических лабораториях.
Примечание
Чистая уксусная кислота затвердевает при 16,6°C, что лишь немного ниже нормальной комнатной температуры. В плохо отапливаемых лабораториях конца 19 — начала 20 веков на севере Северной Америки и Европы уксусная кислота часто «замерзала» на полке хранения. По этой причине чистая уксусная кислота (иногда называемая концентрированной уксусной кислотой) стала известна как ледяная уксусная кислота , и это название сохранилось до наших дней.
Третий гомолог, пропионовая кислота (CH 3 CH 2 COOH), редко встречается в быту. Четвертый гомолог, масляная кислота (СН 3 СН 2 СН 2 СООН), является одним из самых дурно пахнущих веществ, которые только можно себе представить. Он содержится в прогорклом масле и является одним из компонентов неприятного запаха тела. Распознавая очень небольшие количества этого и других химических веществ, ищейки могут выслеживать беглецов. Модели первых четырех карбоновых кислот показаны на рис. 4.1 «Шарикостержневые модели карбоновых кислот».
Рис. 4.1 Шарико-стержневые модели карбоновых кислот
Карбоновые кислоты имеют атом углерода, дважды связанный с атомом кислорода, а также присоединенный к группе ОН. Здесь показаны четыре кислоты: муравьиная кислота (а), уксусная кислота (б), пропионовая кислота (в) и масляная кислота (г).
Кислота с карбоксильной группой, присоединенной непосредственно к бензольному кольцу, называется бензойной кислотой (C 6 H 5 COOH).
В общих названиях карбоновых кислот используются греческие буквы (α, β, γ, δ и т. д.), а не числа для обозначения положения замещающих групп в кислотах. Эти буквы относятся к положению атома углерода по отношению к атому углерода карбоксильной группы.
В номенклатурной системе Международного союза теоретической и прикладной химии (IUPAC) исходным углеводородом является тот, который соответствует самой длинной непрерывной цепи (LCC), содержащей карбоксильную группу. Окончание — e исходного алкана заменяется суффиксом — oic и словом кислота . Например, карбоновая кислота, полученная из пентана, представляет собой пентановую кислоту (СН 3 СН 2 СН 2 СН 2 СООН). Как и в случае с альдегидами, сначала считается карбоксильный атом углерода; цифры используются для обозначения любых замещенных атомов углерода в исходной цепи.
Примечание
Греческие буквы используются с общими именами; номера используются с именами IUPAC.
Пример 1
Дайте общее название и название IUPAC для каждого соединения.
- ClCH 2 CH 2 CH 2 COOH
Раствор
LCC содержит четыре атома углерода; поэтому соединение называют замещенной масляной (или бутановой) кислотой.
Атом хлора присоединен к γ-углероду в общей системе или C4 в системе IUPAC. Соединение представляет собой γ-хлормасляную кислоту или 2-бромбутановую кислоту.
- LCC содержит четыре атома углерода; поэтому соединение называют замещенной масляной (или бутановой) кислотой.
Атом брома (Br) находится при α-углероде в обычной системе или C2 в системе IUPAC. Соединение представляет собой α-броммасляную кислоту или 4-хлорбутановую кислоту.
Упражнение для развития навыков
Дайте название IUPAC для каждого соединения.
ClCH 2 CH 2 CH 2 CH 2 COOH
(CH 3 ) 2 CHCH 2 CHBrCOOH
Пример 2
Напишите сокращенную структурную формулу β-хлорпропионовой кислоты.
Раствор
Пропионовая кислота имеет три атома углерода: C–C–COOH. Присоединить атом хлора (Cl) к материнской цепи по бета-атому углерода, второй от карбоксильной группы: Cl–C–C–COOH. Затем добавьте столько атомов водорода, чтобы дать каждому атому углерода четыре связи: ClCH 2 СН 2 СООН.
Упражнение по развитию навыков
Напишите сокращенную структурную формулу 4-бром-5-метилгексановой кислоты.
Упражнения по обзору концепции
Как называется IUPAC карбоновой кислоты с прямой цепью с шестью атомами углерода?
Альдегид с прямой цепью с пятью атомами углерода имеет общее название валеральдегид. Каково общее название соответствующей карбоновой кислоты с прямой цепью?
Ответы
гексановая кислота
валериановая кислота
Ключевые выводы
- Простые карбоновые кислоты наиболее известны под общими названиями, основанными на латинских и греческих словах, описывающих их источник (например, муравьиная кислота, латинское formica , что означает «муравей»).

- Греческие буквы, а не цифры, обозначают положение замещенных кислот в общепринятом соглашении об именах.
- Названия IUPAC получены из LCC исходного углеводорода с — е окончание исходного алкана заменено суффиксом — ойк и словом кислота .
Упражнения
1. Нарисуйте структуру каждого соединения.
а. гептановая кислота
b. 3-метилбутановая кислота
c. 2,3-дибромбензойная кислота
d. β-гидроксимасляная кислота
2. Изобразите структуру каждого соединения.
а. o -кислота нитробензойная
b. p -хлорбензойная кислота
в. 3-хлорпентановая кислота
d. α-хлорпропионовая кислота
3. Назовите каждое соединение либо по ИЮПАК, либо по общепринятому названию, либо по тому и другому.
а. (СН 3 ) 2 СНСН 2 СООН
б. (CH 3 ) 3 CCH(CH 3 )CH 2 COOH
c. CH 2 OHCH 2 CH 2 COOH
CH 2 OHCH 2 CH 2 COOH
4. Назовите каждое соединение его названием IUPAC.
а. СН 3 (СН 2 ) 8 СООН
б. (CH 3 ) 2 CHCCl 2 CH 2 CH 2 COOH
c. CH 3 CHOHCH(CH 2 CH 3 )CHICOOH
Ответы
1.
a. СН 3 СН 2 СН 2 СН 2 СН 2 СН 2 СООН
b.
в.
д.
3.
а. 3-метилбутановая кислота; β-метилмасляная кислота
б. 3,4,4-триметилпентановая кислота
c. 4-гидроксибутановая кислота; γ- оксимасляная кислота
Напишите структурную формулу пропановой кислоты
OSWAL PUBLICATION-DIKSHA QUESTIONS-CARBON COMOUNDS (КОРОТКИЙ ОТВЕТ)
17 видеоРЕКЛАМА
Ab Padhai karo bina ads ke
0 киси ад ки рукаават ке!Входит в систему, если уже куплен
Обновлен: 27-06-2022
লিখিত
Раствор
Пропаноевая кислота: CH4-SCHOOH
সংশ্লিষ্ট
निमпусти
সংশ্লিষ্ট ভিডিও
निमчей निम 3 40011
. (i) प्रोपेन-2-आल (i) 2-हाइड्राक्सी प्रोपेनोइक अम्ल।
(i) प्रोपेन-2-आल (i) 2-हाइड्राक्सी प्रोपेनोइक अम्ल।
94981241
03:43
2 — हाइड्रोक्सी -प्रोपेनोइक अम्ल संरचना सूत्र बनाओ?
121333361
04:49
अमीनो अमраться
234032888
01:33
.
306991306
01:13
350665892
01:16
Напишите структурную формулу линии связи для 2-(4-изобутилфенил)пропановой кислоты. Напишите структурную формулу бензойной кислоты.
642898074
02:01
निम्न यौगिकों के आण्विक सूत्र सं सं выполнительный 643156387
05:09
निम्न यौगिकों के संरचनात्मक सूत्र लिखें
प्रोपेनॉइक अम्ल (C2H5COOH)
643530660
01:34
Нарисуйте конструкцию.0011
Напишите название IUPAC и формулу пропановой кислоты.
644565849
01:19
फॉ выполнительный
644979120
01:11
Напишите структурную формулу бензойной кислоты.
644985184
Text Solution
प्रोपेनॉइक अम्ल
645451112
01:17
Напишите строение и формулу кислоты Каро.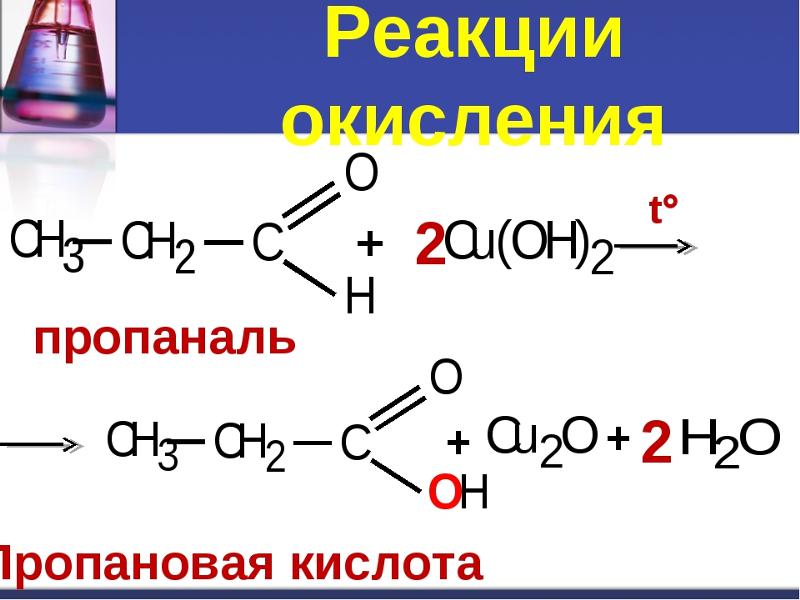
645643251
01:09
РЕКЛАМА
OSWAL ПУБЛИКАЦИЯ-ДИКША ВОПРОСЫ-СОЕДИНЕНИЯ УГЛЕРОДА (КОРОТКИЙ ОТВЕТ)
Что такое денатурированный спирт? Почему этанол денатурируют? Укажите любое два использования …
03:28
Напишите структурную формулу пропанола
01:59
Напишите структурную формулу пропановой кислоты
01:42
Напишите структуру. формула хлорпропана
01:09
Напишите химическое уравнение реакции, протекающей при эт…
02:38
Назовите функциональную группу органических соединений, которые могут гидрироваться…
01 :23
Перечислите в табличной форме три физических и два химических свойства на…
04:11
Различают насыщенные и ненасыщенные углеводороды.
03:19
Соединение с молекулярной формулой C2H6O. Может использоваться в качестве топлива.

