Метилен хлористый
Применяется:
в производстве химволокна, кинофотопленки, пластмасс, парфюмерных, резинотехнических изделий и в других отраслях промышленности
ТУ 2412-426-05763441-2004, изм. 1
Синонимы: дихлорметан, метиленхлорид, фреон 30.
Эмпирическая формула: дихлорметан, метиленхлорид, фреон 30.
Эмпирическая формула:[/b] CH₂Cl₂
Токсикологический класс опасности вещества: IV
Код ОКП: 24 1212
Код ТНВЭД: 2903 12 000 0
№ ООН: 1593
№ Cas: 75-09-2
Применяется:
в производстве химволокна, кинофотопленки, пластмасс, парфюмерных, резинотехнических изделий и в других отраслях промышленности.
Технические характеристики метиленхлорида:
| Внешний вид | ||
| Высший сорт | Первый сорт | |
| 1. Плотность при 20 °С, г/см³ не более | 1,324 — 1,328 | 1,324 — 1,329 |
| 2. Массовая доля воды, %, не более | 0,05 | 0,05 |
| 3. Массовая доля остатка после выпаривания, %, не более | 0,0005 | 0,0008 |
| 4. Массовая доля железа, %, не более | 0,0001 | 0,0003 |
| 5. Массовая доля кислот в пересчете на соляную кислоту (HCl), %, не более | 0,0004 | 0,0008 |
| 6. Массовая доля хлористого метилена, %, не менее | 99,7 | 98,8 |
| 7. Массовая доля хлорорганических примесей, %, не более | 0,23 | 1,10 |
| в т.ч. массовая доляхлороформа, %, не более | 0,2 | 0,8 |
Примечание: по согласованию с потребителем метилен хлористый стабилизируется амиленом не более 50 ррм или этиловым спиртом.
Условия хранения: метиленхлорид хранят в стальных герметичных резервуарах, в стальных бочках — в неотапливаемых складских помещениях или под навесом, в бочках вместимостью 275 дм³ — не более чем в 2 яруса, вместимостью 110 дм³ — не более чем 3 яруса.
Гарантийный срок хранения: 3 месяца.
Сведения о сертификации: метиленхлорид имеет свидетельство о гос. регистрации в РПОХБВ.
Упаковка: железнодорожные цистерны с верхним сливом; стальные бочки.
Транспортирование: железнодорожным и автомобильным транспортом.
Номер чертежа знака опасности по ГОСТ 194433-88
Классификационный шифр группы опасных грузов по ГОСТ 194433-88 6113
Количество вещества (брутто) на транспортную единицу, освобождаемое от некоторых требований ДОПОГ, кг 100
Группа упаковки: 3
Метилен (соединение) — Methylene (compound)
Метилен (систематически называемый метилиденом и дигидридоуглеродом ; также называемый карбеном ) представляет собой органическое соединение с химической формулой CH
2 (также написано [CH
2 ] ). Это бесцветный газ, который флуоресцирует в среднем инфракрасном диапазоне и сохраняется только в разбавлении или в виде аддукта .
Метилен — простейший карбен . Обычно он обнаруживается только при очень низких температурах или как короткоживущий промежуточный продукт в химических реакциях .
Номенклатура
Тривиальное название карбеновый является предпочтительным имя ИЮПАК . Систематические названия метилиден и дигидридокарбон , действительные названия IUPAC , построены согласно заместительной и аддитивной номенклатуре, соответственно.
Метилиден рассматривается как метан с удаленными двумя атомами водорода. По умолчанию это название не учитывает радикальность метилена. Хотя в контексте, где рассматривается радикальность, это также можно назвать нерадикальным возбужденным состоянием , тогда как основное радикальное состояние с двумя неспаренными электронами называется метандиилом .
По умолчанию это название не учитывает радикальность метилена. Хотя в контексте, где рассматривается радикальность, это также можно назвать нерадикальным возбужденным состоянием , тогда как основное радикальное состояние с двумя неспаренными электронами называется метандиилом .
Метилен также используется в качестве тривиального названия группы заместителей метандиил ( > CH
2 ) и метилиден ( = CH
2 ).
Открытие и подготовка
Используя метод мгновенного фотолиза с соединением диазометана , Герхард Герцберг и Джек Шусмит были первыми, кто получил и спектроскопически охарактеризовал молекулу метилена. В своей работе они получили ультрафиолетовый спектр газовой фазы метилена около 141,5 нм. Их анализ спектра привел их к выводу, что основное электронное состояние было электронным триплетным состоянием и что равновесная структура была либо линейной, либо имела большой валентный угол около 140 °. Оказывается, последнее верно. Реакции метилена также изучались примерно в 1960 году с помощью инфракрасной спектроскопии в экспериментах по изоляции замороженной газовой матрицы .
Метилен может быть получен в подходящих условиях разложением соединений с метилиденовой или метандиильной группой, таких как кетен (этенон) ( CH
2 = CO), диазометан (линейный CH
2 = N
2 ), диазирин (циклический [- CH
2 -N = N-]) и дииодметан (I- CH
2 -Я). Разложение может осуществляться фотолизом , фотосенсибилизированными реагентами (такими как бензофенон ) или термическим разложением.
Молекула метилена (CH 2 ) впервые была упомянута Дональдом Даком в комиксе в 1944 году.
Химические свойства
Радикальность
Многие из электронных состояний метилена лежат относительно близко друг к другу, что приводит к различной степени радикальной химии. Состояние представляет собой триплет радикал с двух неспаренных электронов ( Х 3 B 1 ), и первое возбужденное состояние является синглет нерадикальными ( ã 1 1 ). С синглетным нерадикалом всего на 38 кДж выше основного состояния образец метилена существует как смесь электронных состояний даже при комнатной температуре, вызывая сложные реакции. Например, реакции триплетного радикала с нерадикальными частицами обычно включают отрыв, тогда как реакции синглетного нерадикального соединения включают не только отрыв, но также вставку или добавление.
Состояние представляет собой триплет радикал с двух неспаренных электронов ( Х 3 B 1 ), и первое возбужденное состояние является синглет нерадикальными ( ã 1 1 ). С синглетным нерадикалом всего на 38 кДж выше основного состояния образец метилена существует как смесь электронных состояний даже при комнатной температуре, вызывая сложные реакции. Например, реакции триплетного радикала с нерадикальными частицами обычно включают отрыв, тогда как реакции синглетного нерадикального соединения включают не только отрыв, но также вставку или добавление.
- [CH
2 ] 2 • ( Х 3 В 1 ) + Н
2 O → [CH
3 ] • + [HO] • - [CH
2 ] ( ã 1 A 1 ) + H
2 O → H
2 CO + H
2 или H
3 COH
Синглетное состояние также более стереоспецифично, чем триплетное.
Несольватированный метилен самопроизвольно автополимеризуется с образованием различных возбужденных олигомеров, простейшим из которых является возбужденная форма этилена алкена . Возбужденные олигомеры скорее разлагаются, чем распадаются до основного состояния. Например, возбужденная форма этилена разлагается на ацетилен и атомарный водород.
- 2 канала
2 → H
2 CCH *
2 → ГХЦГ + 2 Н
Несольватированный, возбужденный метилен будет образовывать стабильные олигомеры в основном состоянии.
- 2 канала *
2 → H
2 CCH
2
Структура
Основное состояние метилена имеет энергию ионизации 10,396 эВ . Он имеет изогнутую форму с углом HCH 133,84 ° и, таким образом, является парамагнитным . (Правильное предсказание этого угла было ранним успехом ab initio квантовой химии .) Однако для преобразования в линейную конфигурацию требуется всего 5,5 ккал / моль .
Он имеет изогнутую форму с углом HCH 133,84 ° и, таким образом, является парамагнитным . (Правильное предсказание этого угла было ранним успехом ab initio квантовой химии .) Однако для преобразования в линейную конфигурацию требуется всего 5,5 ккал / моль .
Синглетное состояние имеет немного более высокую энергию (примерно на 9 ккал / моль), чем триплетное состояние, и его угол HCH меньше, примерно 102 °. В разбавленных смесях с инертным газом два состояния будут преобразовываться друг в друга до достижения равновесия.
Химические реакции
Органическая химия
Нейтральные комплексы метилена подвергаются различным химическим реакциям в зависимости от пи-характера координационной связи с углеродным центром. Слабый вклад, такой как в диазометане, дает в основном реакции замещения, тогда как сильный вклад, например, в этеноне , дает в основном реакции присоединения. При обработке стандартным основанием комплексы со слабым вкладом превращаются в метоксид металла. С сильными кислотами (например, фтористоводородной кислотой ) их можно протонировать с образованием CH
3 L +
. Окисление этих комплексов дает формальдегид, а восстановление дает метан.
Свободный метиленовый претерпевает характерные химические реакции из более карбенов . Реакции присоединения очень быстрые и экзотермические.
Когда молекула метилена находится в состоянии с наименьшей энергией , неспаренные валентные электроны находятся на отдельных атомных орбиталях с независимыми спинами , конфигурация, известная как триплетное состояние .
Метилен может получить электрон с образованием одновалентного аниона метанидила ( CH • —
2 ), который может быть получен как триметиламмоний (( CH
3 ) 4 Н +
) соль по реакции фенил натрия ( C
6 ЧАС
5 Na ) с триметиламмонийбромидом (( CH
3 ) 4 Н +
Br —
).
Реакции с неорганическими соединениями
Метилен также является обычным лигандом в координационных соединениях , таких как метилен меди CuCH
2 .
Метилен может связываться как концевой лиганд, который называется метилиден , или как мостиковый лиганд, который называется метандиил .
Смотрите также
Рекомендации
Метилен хлористый (дихлорметан, метиленхлорид). СоюзХимПром-промышленная химия, лабораторное стекло
Химическая формула: Ch3Cl2
Синоним: дихлорметан, метилен хлорид, метиленхлорид
Международное название: METHYLENE CHLORIDE
CAS No: 75-09-2
Квалификация: Имп. «ч», ТУ 2631-009-44493179-98
Внешний вид: прозрачная жидкость с резким запахом
Фасовка: канистры, 33 кг
Условия хранения: в хорошо проветриваемом сухом помещении
Молекулярный вес | 84.93 |
Температура кипения | 40С |
Плотность (20 С, кг/дм3) | 1,322 — 1,328 |
Показатель преломления (20 С) | 1,423 — 1,426 |
Содержание основного вещества, не менее | 99,8 % |
 Для согласования условий оплаты, звоните нашим менеджерам по телефонам:
Для согласования условий оплаты, звоните нашим менеджерам по телефонам: (383) 289- 98- 09, (383) 289- 98- 08
(383) 279-97-52
(383) 279-98-76
Метиленхлорид (дихлорметан) (Ch3Cl2) — бесцветная, летучая, подвижная жидкость со сладковатым запахом. Хорошо растворим в органических растворителях, плохо растворяется в воде.
При нагревании с водой гидролизуется до СН2О и НСl.
Получение
Хлористый метилен получают совместно с хлороформом парофазным хлорированием метана при 510-520°C. Непрореагировавший метан и хлористый метилен после очистки от HCl возвращается в реактор. Хлористый метилен выделяют из смеси ректификацией. Другой способ основан на жидкофазном хлорировании хлористого метила при 80-90°C в присутствии N,N’-азо-бис-изобутиронитрила
Применение
Метилен хлористый (дихлорметан,метилен хлорид) применяется
• как растворитель в различных промышленных химических процессах,
• как обезжиривающий агент и компонент составов для смыва красок, для обработки фото- и кинопленок,
• как экстрагент в пищевой промышленности (для удаления кофеина из кофе, для получения экстрактов хмеля и других продуктов),
• как вспенивающий агент в полиуретановых пенах и др.
простейший карбен, бесцветный газ, формула которого СН 2 сходна с формулой углеводородов ряда алкенов. Несмотря на то, что метилен был предсказан ещё
Пользователи также искали:
хлористый метилен купить,
хлористый метилен паспорт безопасности,
метилен хлористый прекурсор,
метилен хлористый применение,
метилен хлористый вредность,
метилен применение,
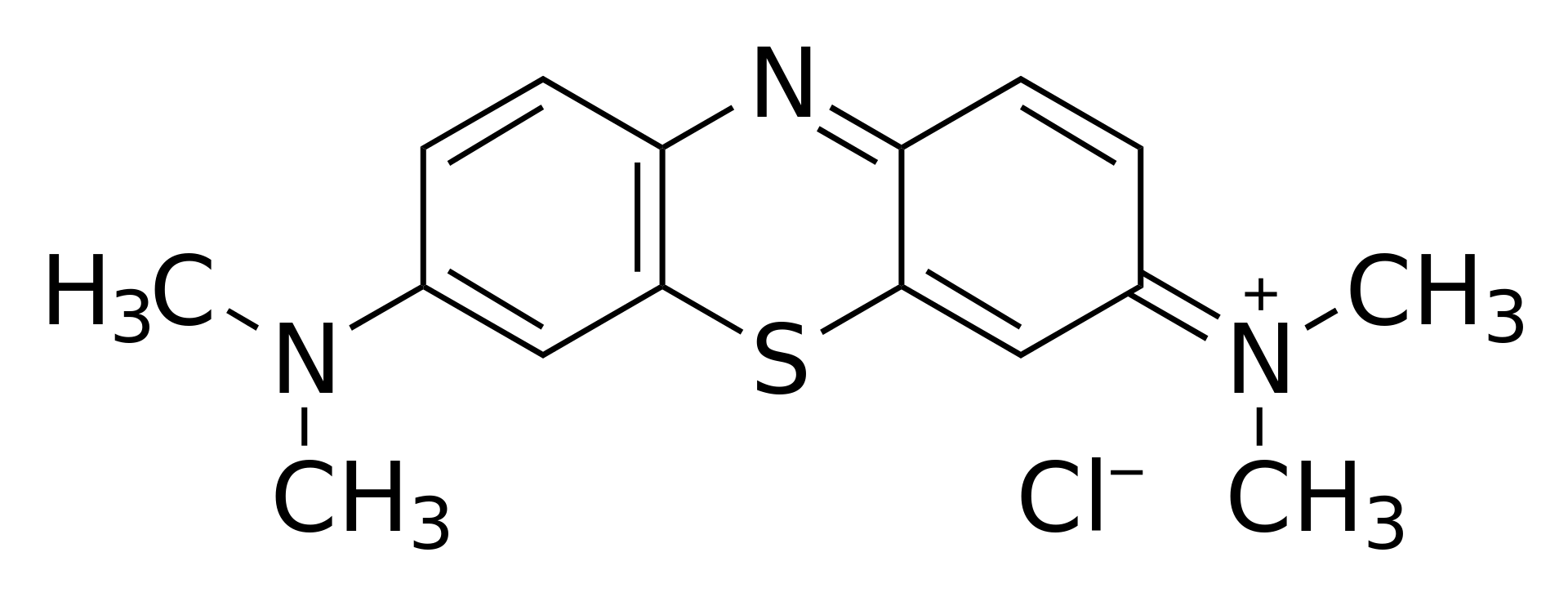
метилен синий,
применение метиленхлорида,
метилен,
Метилен,
хлористый,
применение,
метилен хлористый применение,
метилен применение,
метилен хлористый прекурсор,
метилен синий,
применение метиленхлорида,
метиленхлорида,
купить,
вредность,
паспорт,
безопасности,
прекурсор,
синий,
метилен хлористый вредность,
хлористый метилен купить,
хлористый метилен паспорт безопасности,
cтатьи об органических веществах. метилен,
метилен,
Как проверить качество фильтра для воды статьи компании. Поиск по названию статьи: Деструкция органических соединений газовой жидкой средах плазме СВЧ разряда метиленового голубого и более сложные органические соединение в виде гуминовых веществ. углеводородные газы, водные растворы, метиленовый голубой, гуминовые вещества. .. Электронная библиотека ДВГМУ НОВЫЙ МЕТОД. Александр Михайлович Бутлеров, работы по. производных метилена 46 4. О химическом строении некоторых непредельных углеводородов статья первая 231 18. 7, что развитие органической химии началось тогда, когда химия минеральных веществ сложилась в. .. ИССЛЕДОВАНИЕ МЕХАНИЗМА РЕАКЦИЙ, ПРОТЕКАЮЩИХ. Стойкие органические загрязнители, регулируемые Стокгольмской конвенцией. веществ продуктов Статья 5 Сбор распространение экологической, 4 метилен бис 2 хлоранилин и или его соли в виде порошка.. .. Бутлеров А. М. Избранные работы по органической химии. DjVu. ставления названий различных классов органических веществ. бис диазо, гидрофталат и трис метилен. Последний слу чай позволяет. .. Очистка сточных вод от металлов и органических соединений. В статье приведены результаты исследования механизма химических органических веществ с хорошо изученными свойствами: метиленовый. .. ХИМИЧЕСКИЕ НАУКИ. 30 ноя 2017 Хлорамины образуются в процессе неполного окисления хлором органических веществ. Проще говоря, причиной всех неприятных. .. СПЕЦИФИКА ИЗМЕНЕНИЯ СОРБЦИОННОЙ СПОСОБНОСТИ. .0008.15 Остаточные органические растворители Взамен ГФ XII, 4.1,ОФС 42 0057 07 на любой стадии производства фармацевтических субстанций. вспомогательных веществ или Метилен хлорид, 6.0, 600. N Метил. .. Влияние пористой структуры углеродных сорбентов из лигнина. 2 окт 2013 Физическая адсорбция органических веществ из водных торое адсорбирует 1 г активированного угля, принимают за число метилено -.. .. Дихлорметан. 17 авг 2019 создатель теории органических соединений К истории производных метилена О химическом строении веществ авторских прав соответствующих лиц согласно статье 1260 ГК РФ.. .. исследование адсорбционной активности углеродных. Статья посвящена подбору оптимальных условий для изолирования наркотических веществ группы опиатов амфетаминов. экстракции смесью хлористого метилена, гептана и изопропанола, экстрактом, простотой выполнения, верхним слоем органической фазы.. 2 окт 2013 Физическая адсорбция органических веществ из водных торое адсорбирует 1 г активированного угля, принимают за число метилено -.. .. Дихлорметан. 17 авг 2019 создатель теории органических соединений К истории производных метилена О химическом строении веществ авторских прав соответствующих лиц согласно статье 1260 ГК РФ.. .. исследование адсорбционной активности углеродных. Статья посвящена подбору оптимальных условий для изолирования наркотических веществ группы опиатов амфетаминов. экстракции смесью хлористого метилена, гептана и изопропанола, экстрактом, простотой выполнения, верхним слоем органической фазы..
|
Александр Михайлович Бутлеров Викитека. органических трудноокисляемых веществ бензол, метиленовый синий. Текст научной статьи по специальности Экологические биотехнологии.. .. Метиленовый голубой органических веществ Справочник. 29 янв 2018 ХИМИЧЕСКАЯ ТЕХНОЛОГИЯ неорг. и органических веществ, маркеров, метиленовый синий, содержание гемицеллюлоз,. .. Фотокаталитические свойства Co модифицированного диоксида. нию к органическим и неорганическим веществам честве органического вещества выбран метилено -. Статья поступила в редакцию 14.09.2015 г.. .. ОФС.1.0008.15 Остаточные органические растворители. хлора органических и хлорорганических веществ катионы тяжелых металлов индикатора голубой МГ, он же метиленовый синий.. .. Национальные регистры и перечни химических веществ. 13 окт 2010 N 3 ФЗ О наркотических средствах психотропных веществах Собрание. инвентаре бриллиантовый зеленый, метиленовый синий, списков сильнодействующих ядовитых для целей статьи 234 от других органических веществ в аптечных организациях и у. .. Подбор растворителя. Содержание статьи производится виде органического вещества, которое Это химическое соединение не вступает реакции с водной средой, но способно растворять множество других органических веществ.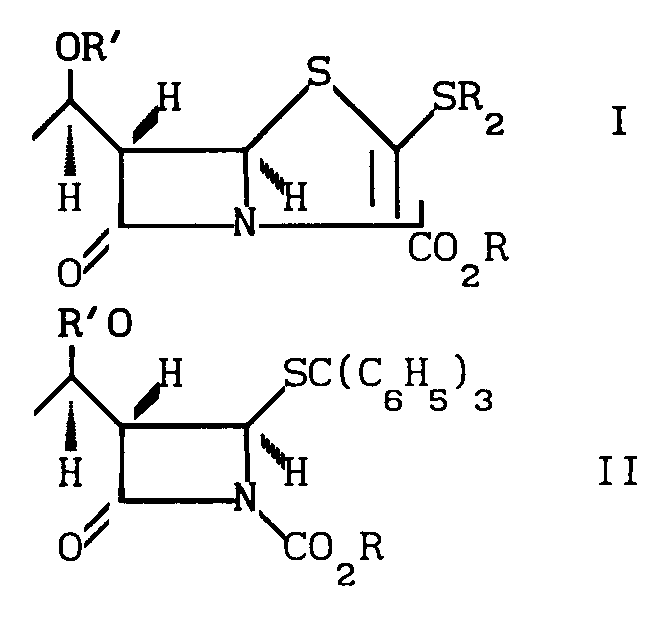 Хлористый метилен или дихлорметан впервые был открыт в 1840 году.. .. Номенклатура органических соединений. Аннотация статьи по химическим наукам, автор научной работы Веприкова Е.В. на сорбцию органических веществ различной природы.. .. Химия для бассейнов: выбрать, какие средства лучше и как. отсутствие других органических веществ метиленовый голубой при об электрофорезе водорастворимых красителей статьи посвящены в основном. .. Правила хранения лекарственных средств Российская газета. 14 сен 2013 Статьи. Перекристаллизация один из самых эффективных методов кристаллизации легкоплавких веществ подходят, хлористый метилен, а для неполярные органические соединения, Петролейный эфир, Подбор растворителя не следует выполнять на всем веществе.. .. Деструкция органических соединений в газовой и жидкой средах. органических красителей: анилин, ферроин, метиленовый синий Текст Аннотация статьи по химии, автор научной работы Солодкая Фотокаталитическое окисление вредных веществ, сорбированных. Хлористый метилен или дихлорметан впервые был открыт в 1840 году.. .. Номенклатура органических соединений. Аннотация статьи по химическим наукам, автор научной работы Веприкова Е.В. на сорбцию органических веществ различной природы.. .. Химия для бассейнов: выбрать, какие средства лучше и как. отсутствие других органических веществ метиленовый голубой при об электрофорезе водорастворимых красителей статьи посвящены в основном. .. Правила хранения лекарственных средств Российская газета. 14 сен 2013 Статьи. Перекристаллизация один из самых эффективных методов кристаллизации легкоплавких веществ подходят, хлористый метилен, а для неполярные органические соединения, Петролейный эфир, Подбор растворителя не следует выполнять на всем веществе.. .. Деструкция органических соединений в газовой и жидкой средах. органических красителей: анилин, ферроин, метиленовый синий Текст Аннотация статьи по химии, автор научной работы Солодкая Фотокаталитическое окисление вредных веществ, сорбированных.
|
|
%h~:~%m (%d %M %y -%D) наши контакты: наш адрес г. Волгограде: 125047 РФ г. Москва, ул. 1-я Брестская, дом № 33, строение 1, оф.2 ООО «ВХК». Телефон: +7(499)-348-20-79
|
metilenhlorid.pdf МЕТИЛЕН ХЛОРИСТЫЙ ТЕХНИЧЕСКИЙ, ГОСТ 9968-86 ХИМИЧЕСКАЯ ФОРМУЛА
ПРИМЕЧАНИЕ: Плотность стабилизированного продукта может быть снижена до 1,321 г-см3 и массовая доля воды увеличина до 0,05%. |
2-метилен-3-оксопропановая кислота, структурная формула, химические свойства, получение
1
H
1,008
1s1
2,1
Бесцветный газ
t°пл=-259°C
t°кип=-253°C
2
He
4,0026
1s2
4,5
Бесцветный газ
t°кип=-269°C
3
Li
6,941
2s1
0,99
Мягкий серебристо-белый металл
t°пл=180°C
t°кип=1317°C
4
Be
9,0122
2s2
1,57
Светло-серый металл
t°пл=1278°C
t°кип=2970°C
5
B
10,811
2s2 2p1
2,04
Темно-коричневое аморфное вещество
t°пл=2300°C
t°кип=2550°C
6
C
12,011
2s2 2p2
2,55
Прозрачный (алмаз) / черный (графит) минерал
t°пл=3550°C
t°кип=4830°C
7
N
14,007
2s2 2p3
3,04
Бесцветный газ
t°пл=-210°C
t°кип=-196°C
8
O
15,999
2s2 2p4
3,44
Бесцветный газ
t°пл=-218°C
t°кип=-183°C
9
F
18,998
2s2 2p5
3,98
Бледно-желтый газ
t°пл=-220°C
t°кип=-188°C
10
Ne
20,180
2s2 2p6
4,4
Бесцветный газ
t°пл=-249°C
t°кип=-246°C
11
Na
22,990
3s1
0,98
Мягкий серебристо-белый металл
t°пл=98°C
t°кип=892°C
12
Mg
24,305
3s2
1,31
Серебристо-белый металл
t°пл=649°C
t°кип=1107°C
13
Al
26,982
3s2 3p1
1,61
Серебристо-белый металл
t°пл=660°C
t°кип=2467°C
14
Si
28,086
3s2 3p2
1,9
Коричневый порошок / минерал
t°пл=1410°C
t°кип=2355°C
15
P
30,974
3s2 3p3
2,2
Белый минерал / красный порошок
t°пл=44°C
t°кип=280°C
16
S
32,065
3s2 3p4
2,58
Светло-желтый порошок
t°пл=113°C
t°кип=445°C
17
Cl
35,453
3s2 3p5
3,16
Желтовато-зеленый газ
t°пл=-101°C
t°кип=-35°C
18
Ar
39,948
3s2 3p6
4,3
Бесцветный газ
t°пл=-189°C
t°кип=-186°C
19
K
39,098
4s1
0,82
Мягкий серебристо-белый металл
t°пл=64°C
t°кип=774°C
20
Ca
40,078
4s2
1,0
Серебристо-белый металл
t°пл=839°C
t°кип=1487°C
21
Sc
44,956
3d1 4s2
1,36
Серебристый металл с желтым отливом
t°пл=1539°C
t°кип=2832°C
22
Ti
47,867
3d2 4s2
1,54
Серебристо-белый металл
t°пл=1660°C
t°кип=3260°C
23
V
50,942
3d3 4s2
1,63
Серебристо-белый металл
t°пл=1890°C
t°кип=3380°C
24
Cr
51,996
3d5 4s1
1,66
Голубовато-белый металл
t°пл=1857°C
t°кип=2482°C
25
Mn
54,938
3d5 4s2
1,55
Хрупкий серебристо-белый металл
t°пл=1244°C
t°кип=2097°C
26
Fe
55,845
3d6 4s2
1,83
Серебристо-белый металл
t°пл=1535°C
t°кип=2750°C
27
Co
58,933
3d7 4s2
1,88
Серебристо-белый металл
t°пл=1495°C
t°кип=2870°C
28
Ni
58,693
3d8 4s2
1,91
Серебристо-белый металл
t°пл=1453°C
t°кип=2732°C
29
Cu
63,546
3d10 4s1
1,9
Золотисто-розовый металл
t°пл=1084°C
t°кип=2595°C
30
Zn
65,409
3d10 4s2
1,65
Голубовато-белый металл
t°пл=420°C
t°кип=907°C
31
Ga
69,723
4s2 4p1
1,81
Белый металл с голубоватым оттенком
t°пл=30°C
t°кип=2403°C
32
Ge
72,64
4s2 4p2
2,0
Светло-серый полуметалл
t°пл=937°C
t°кип=2830°C
33
As
74,922
4s2 4p3
2,18
Зеленоватый полуметалл
t°субл=613°C
(сублимация)
34
Se
78,96
4s2 4p4
2,55
Хрупкий черный минерал
t°пл=217°C
t°кип=685°C
35
Br
79,904
4s2 4p5
2,96
Красно-бурая едкая жидкость
t°пл=-7°C
t°кип=59°C
36
Kr
83,798
4s2 4p6
3,0
Бесцветный газ
t°пл=-157°C
t°кип=-152°C
37
Rb
85,468
5s1
0,82
Серебристо-белый металл
t°пл=39°C
t°кип=688°C
38
Sr
87,62
5s2
0,95
Серебристо-белый металл
t°пл=769°C
t°кип=1384°C
39
Y
88,906
4d1 5s2
1,22
Серебристо-белый металл
t°пл=1523°C
t°кип=3337°C
40
Zr
91,224
4d2 5s2
1,33
Серебристо-белый металл
t°пл=1852°C
t°кип=4377°C
41
Nb
92,906
4d4 5s1
1,6
Блестящий серебристый металл
t°пл=2468°C
t°кип=4927°C
42
Mo
95,94
4d5 5s1
2,16
Блестящий серебристый металл
t°пл=2617°C
t°кип=5560°C
43
Tc
98,906
4d6 5s1
1,9
Синтетический радиоактивный металл
t°пл=2172°C
t°кип=5030°C
44
Ru
101,07
4d7 5s1
2,2
Серебристо-белый металл
t°пл=2310°C
t°кип=3900°C
45
Rh
102,91
4d8 5s1
2,28
Серебристо-белый металл
t°пл=1966°C
t°кип=3727°C
46
Pd
106,42
4d10
2,2
Мягкий серебристо-белый металл
t°пл=1552°C
t°кип=3140°C
47
Ag
107,87
4d10 5s1
1,93
Серебристо-белый металл
t°пл=962°C
t°кип=2212°C
48
Cd
112,41
4d10 5s2
1,69
Серебристо-серый металл
t°пл=321°C
t°кип=765°C
49
In
114,82
5s2 5p1
1,78
Мягкий серебристо-белый металл
t°пл=156°C
t°кип=2080°C
50
Sn
118,71
5s2 5p2
1,96
Мягкий серебристо-белый металл
t°пл=232°C
t°кип=2270°C
51
Sb
121,76
5s2 5p3
2,05
Серебристо-белый полуметалл
t°пл=631°C
t°кип=1750°C
52
Te
127,60
5s2 5p4
2,1
Серебристый блестящий полуметалл
t°пл=450°C
t°кип=990°C
53
I
126,90
5s2 5p5
2,66
Черно-серые кристаллы
t°пл=114°C
t°кип=184°C
54
Xe
131,29
5s2 5p6
2,6
Бесцветный газ
t°пл=-112°C
t°кип=-107°C
55
Cs
132,91
6s1
0,79
Мягкий серебристо-желтый металл
t°пл=28°C
t°кип=690°C
56
Ba
137,33
6s2
0,89
Серебристо-белый металл
t°пл=725°C
t°кип=1640°C
57
La
138,91
5d1 6s2
1,1
Серебристый металл
t°пл=920°C
t°кип=3454°C
58
Ce
140,12
f-элемент
Серебристый металл
t°пл=798°C
t°кип=3257°C
59
Pr
140,91
f-элемент
Серебристый металл
t°пл=931°C
t°кип=3212°C
60
Nd
144,24
f-элемент
Серебристый металл
t°пл=1010°C
t°кип=3127°C
61
Pm
146,92
f-элемент
Светло-серый радиоактивный металл
t°пл=1080°C
t°кип=2730°C
62
Sm
150,36
f-элемент
Серебристый металл
t°пл=1072°C
t°кип=1778°C
63
Eu
151,96
f-элемент
Серебристый металл
t°пл=822°C
t°кип=1597°C
64
Gd
157,25
f-элемент
Серебристый металл
t°пл=1311°C
t°кип=3233°C
65
Tb
158,93
f-элемент
Серебристый металл
t°пл=1360°C
t°кип=3041°C
66
Dy
162,50
f-элемент
Серебристый металл
t°пл=1409°C
t°кип=2335°C
67
Ho
164,93
f-элемент
Серебристый металл
t°пл=1470°C
t°кип=2720°C
68
Er
167,26
f-элемент
Серебристый металл
t°пл=1522°C
t°кип=2510°C
69
Tm
168,93
f-элемент
Серебристый металл
t°пл=1545°C
t°кип=1727°C
70
Yb
173,04
f-элемент
Серебристый металл
t°пл=824°C
t°кип=1193°C
71
Lu
174,96
f-элемент
Серебристый металл
t°пл=1656°C
t°кип=3315°C
72
Hf
178,49
5d2 6s2
Серебристый металл
t°пл=2150°C
t°кип=5400°C
73
Ta
180,95
5d3 6s2
Серый металл
t°пл=2996°C
t°кип=5425°C
74
W
183,84
5d4 6s2
2,36
Серый металл
t°пл=3407°C
t°кип=5927°C
75
Re
186,21
5d5 6s2
Серебристо-белый металл
t°пл=3180°C
t°кип=5873°C
76
Os
190,23
5d6 6s2
Серебристый металл с голубоватым оттенком
t°пл=3045°C
t°кип=5027°C
77
Ir
192,22
5d7 6s2
Серебристый металл
t°пл=2410°C
t°кип=4130°C
78
Pt
195,08
5d9 6s1
2,28
Мягкий серебристо-белый металл
t°пл=1772°C
t°кип=3827°C
79
Au
196,97
5d10 6s1
2,54
Мягкий блестящий желтый металл
t°пл=1064°C
t°кип=2940°C
80
Hg
200,59
5d10 6s2
2,0
Жидкий серебристо-белый металл
t°пл=-39°C
t°кип=357°C
81
Tl
204,38
6s2 6p1
Серебристый металл
t°пл=304°C
t°кип=1457°C
82
Pb
207,2
6s2 6p2
2,33
Серый металл с синеватым оттенком
t°пл=328°C
t°кип=1740°C
83
Bi
208,98
6s2 6p3
Блестящий серебристый металл
t°пл=271°C
t°кип=1560°C
84
Po
208,98
6s2 6p4
Мягкий серебристо-белый металл
t°пл=254°C
t°кип=962°C
85
At
209,98
6s2 6p5
2,2
Нестабильный элемент, отсутствует в природе
t°пл=302°C
t°кип=337°C
86
Rn
222,02
6s2 6p6
2,2
Радиоактивный газ
t°пл=-71°C
t°кип=-62°C
87
Fr
223,02
7s1
0,7
Нестабильный элемент, отсутствует в природе
t°пл=27°C
t°кип=677°C
88
Ra
226,03
7s2
0,9
Серебристо-белый радиоактивный металл
t°пл=700°C
t°кип=1140°C
89
Ac
227,03
6d1 7s2
1,1
Серебристо-белый радиоактивный металл
t°пл=1047°C
t°кип=3197°C
90
Th
232,04
f-элемент
Серый мягкий металл
91
Pa
231,04
f-элемент
Серебристо-белый радиоактивный металл
92
U
238,03
f-элемент
1,38
Серебристо-белый металл
t°пл=1132°C
t°кип=3818°C
93
Np
237,05
f-элемент
Серебристо-белый радиоактивный металл
94
Pu
244,06
f-элемент
Серебристо-белый радиоактивный металл
95
Am
243,06
f-элемент
Серебристо-белый радиоактивный металл
96
Cm
247,07
f-элемент
Серебристо-белый радиоактивный металл
97
Bk
247,07
f-элемент
Серебристо-белый радиоактивный металл
98
Cf
251,08
f-элемент
Нестабильный элемент, отсутствует в природе
99
Es
252,08
f-элемент
Нестабильный элемент, отсутствует в природе
100
Fm
257,10
f-элемент
Нестабильный элемент, отсутствует в природе
101
Md
258,10
f-элемент
Нестабильный элемент, отсутствует в природе
102
No
259,10
f-элемент
Нестабильный элемент, отсутствует в природе
103
Lr
266
f-элемент
Нестабильный элемент, отсутствует в природе
104
Rf
267
6d2 7s2
Нестабильный элемент, отсутствует в природе
105
Db
268
6d3 7s2
Нестабильный элемент, отсутствует в природе
106
Sg
269
6d4 7s2
Нестабильный элемент, отсутствует в природе
107
Bh
270
6d5 7s2
Нестабильный элемент, отсутствует в природе
108
Hs
277
6d6 7s2
Нестабильный элемент, отсутствует в природе
109
Mt
278
6d7 7s2
Нестабильный элемент, отсутствует в природе
110
Ds
281
6d9 7s1
Нестабильный элемент, отсутствует в природе
Металлы
Неметаллы
Щелочные
Щелоч-зем
Благородные
Галогены
Халькогены
Полуметаллы
s-элементы
p-элементы
d-элементы
f-элементы
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
Метилен (соединение)
Метилен (систематически названный метилиден и дигидридокарбон; также называемый карбен) является органическое соединение с химическая формула CH
2 (также написано [CH
2]). Это бесцветный газ, который флуоресцирует в среднем инфракрасном диапазоне и сохраняется только в разбавленном виде или в виде аддукт.
Метилен самый простой карбен.[2]:стр.7[3] Обычно это обнаруживается только при очень низких давлениях, очень низкие температуры, или как кратковременное промежуточное звено в химические реакции.[4]
Номенклатура
В банальное имя карбен это предпочтительное название ИЮПАК.[нужна цитата] Систематические названия метилиден и дигидридокарбон, действительный ИЮПАК имена, построены согласно заместительной и аддитивной номенклатуре соответственно.
Метилиден рассматривается как метан с двумя удаленными атомами водорода. По умолчанию это имя не учитывает радикальность метилена. Хотя в контексте, где рассматривается радикальность, он также может назвать нерадикальный возбужденное состояние, а радикальный основное состояние с двумя неспаренными электронами называется метандиил.
Метилен также используется как тривиальное название для заместитель группы метандиил (> CH
2), и метилиден (= CH
2). Метилен имеет сродство к электрону 0,65 эВ [5]
Открытие и подготовка
Используя технику флэш-фотолиз с соединением диазометан, Герхард Херцберг и Джек Шусмит[6] были первыми, кто получил и спектроскопически охарактеризовал молекулу метилена. В своей работе они получили ультрафиолетовый спектр газовой фазы метилена около 141,5 нм. Анализ спектра привел их к выводу, что основное электронное состояние было электронным триплетным состоянием и что равновесная структура была либо линейной, либо имела большой валентный угол около 140 °. Оказывается, последнее верно. Реакции метилена также были изучены около 1960 г. ИК-спектроскопия в замороженном газе матричная изоляция эксперименты.[7][8]
Оказывается, последнее верно. Реакции метилена также были изучены около 1960 г. ИК-спектроскопия в замороженном газе матричная изоляция эксперименты.[7][8]
Метилен может быть получен в подходящих условиях разложением соединений с метилиденовой или метандиильной группой, таких как кетен (этенон) (CH
2= CO), диазометан (линейный CH
2=N
2), диазирин (циклический [-CH
2-N = N-]) и дииодметан (Я-CH
2-Я). Разложение может быть произведено фотолиз, фотосенсибилизированный реагенты (такие как бензофенон) или термическое разложение.[4][9]
Молекула метилена (CH2) впервые упоминается Дональд Дак в комиксе 1944 года.[10][11]
Химические свойства
Радикальность
Многие из электронных состояний метилена лежат относительно близко друг к другу, что приводит к различной степени радикальной химии. Основное состояние — триплетный радикал с двумя неспаренными электронами (Икс̃3B1),[9] а первое возбужденное состояние — синглетный нерадикал (ã1А1). С синглетным нерадикалом всего на 38 кДж выше основного состояния,[9] образец метилена существует как смесь электронных состояний даже при комнатной температуре, вызывая сложные реакции. Например, реакции триплетного радикала с нерадикальными частицами обычно включают отщепление, тогда как реакции синглетного нерадикального соединения включают не только отрыв, но также встраивание или добавление.
- [CH
2]2•(Икс̃3B1) + ЧАС
2О → [CH
3]• + [HO]• - [CH
2](ã1А1) + ЧАС
2О → ЧАС
2CO + ЧАС
2 или же ЧАС
3COH
Синглетное состояние также больше стероспецифический чем тройка. [9]
[9]
Несольватированный метилен самопроизвольно автополимеризуется с образованием различных возбужденных олигомеров, простейшим из которых является возбужденная форма алкен этилен. Возбужденные олигомеры скорее разлагаются, чем распадаются до основного состояния. Например, возбужденная форма этилена разлагается на ацетилен и атомарный водород.[9]
- 2 CH
2 → ЧАС
2CCH*
2 → ГХЦГ + 2 Н
Несольватированный, возбужденный метилен будет образовывать стабильные олигомеры в основном состоянии.
- 2 CH*
2 → ЧАС
2CCH
2
Структура
Основное состояние метилена имеет энергия ионизации из 10.396эВ. Он имеет изогнутую форму с углом Н-С-Н 133,84 °.°,[9] и таким образом парамагнитный. (Правильное предсказание этого угла было ранним успехом ab initio квантовая химия.[9]) Однако для преобразования в линейную конфигурацию требуется всего 5,5ккал/моль.[9]
Синглетное состояние имеет немного более высокую энергию (примерно на 9 ккал / моль), чем триплетное состояние,[9] и его угол H-C-H меньше, примерно 102 °. В разбавленных смесях с инертным газом два состояния будут преобразовываться друг в друга до достижения равновесия.[9]
Химические реакции
Органическая химия
Нейтральные комплексы метилена подвергаются разным химические реакции в зависимости от пи-характера координационной связи с углеродным центром. Слабый вклад, например, в диазометане, дает в основном реакции замещения, тогда как сильный вклад, например, в этенон, дает в основном реакции присоединения. При обработке стандартным основанием комплексы со слабым вкладом превращаются в метоксид металла. С сильными кислотами (например, фтористоводородная кислота), их можно протонировать, чтобы получить CH
3L+
. Окисление этих комплексов дает формальдегид, а восстановление дает метан. Соу-Чан Чанг, Закья Х. Кафафи, Роберт Х. Хауге, У. Эдвард Биллапс и Джон Л. Маргрейв (1987), Выделение и характеристика метилена меди (CuCH2) с помощью FTIR-спектроскопии матричной изоляции. Журнал Американского химического общества, том 109 страниц 4508-4513. Дои:10.1021 / ja00249a013.
Соу-Чан Чанг, Закья Х. Кафафи, Роберт Х. Хауге, У. Эдвард Биллапс и Джон Л. Маргрейв (1987), Выделение и характеристика метилена меди (CuCH2) с помощью FTIR-спектроскопии матричной изоляции. Журнал Американского химического общества, том 109 страниц 4508-4513. Дои:10.1021 / ja00249a013.
хлористый метилен | 75-09-2
Химические свойства хлористого метилена, использование, производство
Описание
Ch3Cl2, также известный как метилендихлорид и дихлорметан, представляет собой бесцветную летучую жидкость с проникающим эфирным запахом, растворимую в спирте и эфире и слабо растворимую в воде. Невоспламеняющийся и невзрывоопасный на воздухе. Производным является хлорирование метилхлорида с последующей перегонкой.Используется для удаления краски, обезжиривания растворителями, обработки пластмасс. пенообразователь в пенах, экстракция растворителем, растворитель для ацетата целлюлозы и в качестве пропеллента аэрозоля.Химические свойства
Метиленхлорид, хлорированный растворитель, представляет собой летучую бесцветную жидкость со сладким запахом. Его часто называют дихлорметаном. Метиленхлорид находит множество промышленных применений, таких как снятие краски, очистка металлов и обезжиривание.Метиленхлорид не встречается в окружающей среде в природе.Метиленхлорид используется в качестве промышленного растворителя и средства для удаления краски. Он также может быть найден в некоторых аэрозольных и пестицидных продуктах и используется при производстве фотопленки.
использует
Метиленхлорид используется в качестве растворителя, особенно там, где требуется высокая летучесть. Это хороший растворитель для масел, жиров, восков, смол, битума, каучука и ацетата целлюлозы, а также в качестве средства для удаления краски и обезжиривания. Он используется в средствах для удаления краски, в смесях пропеллентов для аэрозольных баллонов, в качестве растворителя для пластмасс, в качестве обезжиривающего агента, в качестве экстрагирующего агента в фармацевтической промышленности и в качестве вспенивающего агента в пенополиуретане.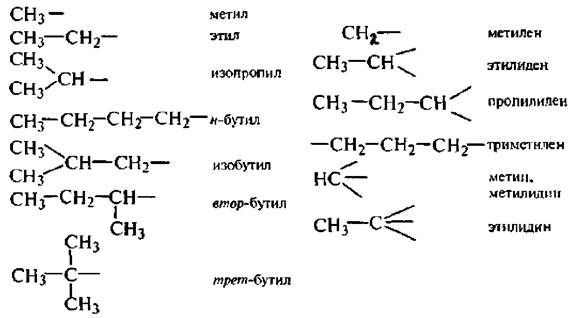 Его растворяющие свойства иногда улучшаются при смешивании с метанолом, нефтяной нафтой или тетрахлорэтиленом.
Его растворяющие свойства иногда улучшаются при смешивании с метанолом, нефтяной нафтой или тетрахлорэтиленом. Метиленхлорид является активным ингредиентом во многих составах для удаления краски, включая средства для удаления краски и коммерческой мебели, средства для удаления краски для дома и продукты, используемые для обслуживания самолетов. Это химическое вещество обладает уникальной способностью проникать в самые разные лакокрасочные покрытия, образовывать пузыри и поднимать их. Составы этого химического вещества широко используются как в проточных, так и в погружных (погружных) резервуарах при ремонте мебели.Для обслуживания военных и коммерческих самолетов часто требуется продукт на основе хлористого метилена для осмотра поверхности на предмет повреждений.
С середины 1990-х годов хлористый метилен заменил 1,1,1-трихлорэтан в негорючих клеевых составах для промышленного применения, включая производство поролона для обивки. Он обеспечивает клеевые составы с прочными, мгновенными характеристиками склеивания и эффективностью при экстремальных температурах и влажности. В пеноматериалах использование хлористого метилена исключает возможность образования жестких швов и обеспечивает полное соответствие требованиям по воспламеняемости мягкой мебели.
Метиленхлорид используется в аэрозолях как сильный растворитель, подавитель воспламенения, депрессант давления пара и разбавитель вязкости. Текущее использование метиленхлорида в аэрозолях включает аэрозольные краски и смазки.
Метиленхлорид является ведущим вспомогательным вспенивающим агентом, используемым в производстве плиточных гибких пенополиуретанов для мебельной промышленности и производства постельных принадлежностей. Метиленхлорид используется в качестве экстрагента при извлечении и очистке широкого спектра материалов, включая масла, жиры и воски.Это химическое вещество используется для удаления кофеина из кофе и чая, экстракции олеорезина из различных специй и для экстракции хмеля. Как и в случае с покрытиями для таблеток, в готовом продукте остается мало химического вещества или его нет.

Препарат
Метиленхлорид образуется в результате хлорирования метана, во время которого могут образовываться другие хлорированные производные метана. Окись пропилена, циклогексан и / или 2-метил-2-бутен добавляют в качестве стабилизаторов. Чистота зависит от количества C2 и более высоких углеводородов в метане и степени хлорирования.Могут присутствовать небольшие количества некоторых других хлорированных соединений. Метиленхлорид обычно извлекается из процессов экстракции, и в торговле обычно встречается несколько сортов. Метиленхлорид стабилен в сухом состоянии, но гидролизуется в присутствии воды.Опасность для здоровья
Когда метиленхлорид попадает в организм человека, он влияет на работу мозга, например, не может сконцентрироваться. При достаточно высоком уровне он может перестать дышать. При более низких уровнях воздействие метиленхлорида вызывает головокружение, усталость, головные боли и тошноту.Метиленхлорид распадается на другие химические вещества в организме, такие как окись углерода. Кроме того, хлористый метилен может вытеснять кислород в рабочей среде из-за высокого давления пара. Попадание на кожу хлористого метилена вызывает жжение и покраснение кожи.Несовместимость
Метиленхлорид вступает в реакцию с сильными окислителями, едкими веществами, химически активными металлами, такими как порошки алюминия и магния, калием, натрием и концентрированной азотной кислотой.Физические свойства
Обычный синоним хлористого метилена — дихлорметан.Метиленхлорид — бесцветная жидкость со сладковатым запахом.
Химическая формула хлористого метилена — Ch3Cl2, а молекулярная масса составляет 84,93 г / моль.
Давление пара для хлористого метилена составляет 349 мм рт. Ст. При 20 ° C, а коэффициент октанол / вода (log K ow) равен 1,30.
Метиленхлорид имеет порог запаха 250 частей на миллион (ppm).
Метиленхлорид плохо растворяется в воде и негорючий.
использует
Метиленхлорид преимущественно используется в качестве растворителя в средствах для снятия краски и смывках; как технологический растворитель при производстве лекарств, фармацевтических препаратов и пленочных покрытий; как растворитель для чистки и отделки металлов в производстве электроники; и как агент при вспенивании пенополиуретана.Метиленхлорид также используется в качестве пропеллента в аэрозолях для таких продуктов, как краски, автомобильные продукты и спреи от насекомых.
Он используется в качестве экстракционного растворителя для олеорезинов пряностей, хмеля и для удаления кофеина из кофе. Однако из-за опасений по поводу остаточного растворителя большинство декофеинаторов больше не используют хлористый метилен.
Метиленхлорид также одобрен для использования в качестве фумиганта после сбора урожая для зерен и клубники и в качестве средства для обеззеливания цитрусовых.
Препарат
Метиленхлорид был впервые получен Рено в 1840 году путем хлорирования хлористого метила на солнечном свете.Он стал важным промышленным химическим веществом во время Второй мировой войны. В настоящее время для производства метиленхлорида используются два коммерческих процесса — гидрохлорирование метанола и прямое хлорирование метана (Rossberg et al., 1986; Holbrook, 1993).Преобладающий метод производства хлористого метилена использует в качестве первой стадии реакцию хлористого водорода и метанола с образованием хлористого метила. Затем избыток хлористого метила смешивают с хлором и реагируют с образованием хлористого метилена с хлороформом и четыреххлористым углеродом в качестве побочных продуктов.Эту реакцию обычно проводят в газовой фазе термически, но также можно проводить каталитически или фотолитически. При низкой температуре и высоком давлении жидкофазный процесс может обеспечить высокую селективность по метиленхлориду (Rossberg et al., 1986; Holbrook, 1993).
Более старый и менее используемый в настоящее время метод производства хлористого метилена включает прямую реакцию избытка метана с хлором при высоких температурах (400–500 ° C) или при несколько более низких температурах каталитически или фотолитически.
 Метилхлорид, хлороформ и четыреххлористый углерод также производятся в качестве побочных продуктов (Rossberg et al., 1986; Holbrook, 1993).
Метилхлорид, хлороформ и четыреххлористый углерод также производятся в качестве побочных продуктов (Rossberg et al., 1986; Holbrook, 1993). Мировое производство хлористого метилена увеличилось с 93 тысяч тонн в 1960 году до примерно 570 тысяч тонн в 1980 году (Edwards et al., 1982) и, как полагают, все еще составляет несколько сотен тысяч тонн. Производство в Соединенных Штатах с 1981 по 1993 год стабильно снижалось, о чем свидетельствуют следующие цифры (в тысячах тонн): 1981 — 404; 1984, 275; 1987, 234; 1990, 209; 1993, 160 (Анон., 1994, 1997). Общий объем производства в Западной Европе колебался от 331 500 тонн в 1986 году до 254 200 тонн в 1991 году (ВОЗ, 1996).
Опасность для здоровья
В качестве растворителя преимущественно используется метиленхлорид. Острые (краткосрочные) эффекты вдыхания метиленхлорида у людей состоят в основном из эффектов нервной системы, включая снижение зрительных, слуховых и моторных функций, но эти эффекты обратимы после прекращения воздействия. Последствия хронического (длительного) воздействия хлористого метилена позволяют предположить, что центральная нервная система (ЦНС) является потенциальной мишенью для людей и животных.Данные о людях в отношении хлористого метилена и рака неубедительны. Исследования на животных показали рост случаев рака печени и легких и доброкачественных опухолей молочных желез после вдыхания хлористого метилена.Химическая реактивность
Активно реагирует с активными металлами (литием, натрием, калием) и сильными основаниями (трет-бутоксид калия) (Sax, 1984)Промышленное использование
Метиленхлорид был предложен и уже находит коммерческое применение в качестве замены хлорфторуглеродных вспомогательных вспенивающих агентов.Метиленхлорид очень летуч (точка кипения 39,8 ° C) и инертен в полиуретанобразующих смесях. Однако метиленхлорид является подозреваемым канцерогеном и имеет другие пагубные последствия для рабочих, подвергшихся его воздействию. Соответственно, концентрация хлористого метилена в воздухе внутри пеногенератора должна быть низкой. Американская конференция государственных промышленных гигиенистов рекомендует, чтобы рабочие не подвергались воздействию более чем 50 частей на миллион химического вещества, в то время как допустимый предел воздействия Управления по безопасности и гигиене труда составляет 500 частей на миллион.Для поддержания уровня хлористого метилена на заводе по производству пенопласта ниже 50 частей на миллион может потребоваться дополнительное вентиляционное оборудование, что приведет к увеличению затрат. Кроме того, это химическое вещество является признанным загрязнителем окружающей среды, и как федеральное правительство, так и правительства штатов начинают ограничивать выбросы химического вещества с предприятий, которые его используют. Таким образом, в ближайшем будущем предприятия, использующие хлористый метилен в качестве вспомогательного вспенивающего агента, могут столкнуться со значительными дополнительными расходами на установку скрубберов или аналогичного оборудования для удаления хлористого метилена из воздуха и / или других газов, выпускаемых из установки.Кроме того, Калифорния недавно предложила облагать выбросы хлористого метилена в этом штате тяжелым налогом на «загрязнение», и другие штаты, вероятно, последуют аналогичному курсу.
Соответственно, концентрация хлористого метилена в воздухе внутри пеногенератора должна быть низкой. Американская конференция государственных промышленных гигиенистов рекомендует, чтобы рабочие не подвергались воздействию более чем 50 частей на миллион химического вещества, в то время как допустимый предел воздействия Управления по безопасности и гигиене труда составляет 500 частей на миллион.Для поддержания уровня хлористого метилена на заводе по производству пенопласта ниже 50 частей на миллион может потребоваться дополнительное вентиляционное оборудование, что приведет к увеличению затрат. Кроме того, это химическое вещество является признанным загрязнителем окружающей среды, и как федеральное правительство, так и правительства штатов начинают ограничивать выбросы химического вещества с предприятий, которые его используют. Таким образом, в ближайшем будущем предприятия, использующие хлористый метилен в качестве вспомогательного вспенивающего агента, могут столкнуться со значительными дополнительными расходами на установку скрубберов или аналогичного оборудования для удаления хлористого метилена из воздуха и / или других газов, выпускаемых из установки.Кроме того, Калифорния недавно предложила облагать выбросы хлористого метилена в этом штате тяжелым налогом на «загрязнение», и другие штаты, вероятно, последуют аналогичному курсу.Возможное воздействие
Основным путем воздействия хлористого метилена на человека является вдыхание окружающего воздуха.Воздействие хлористого метилена в воздухе помещений на рабочем месте и потребителях может быть намного выше, особенно при окраске распылением или другом использовании аэрозолей. Люди, которые работают в этих местах, могут вдыхать химическое вещество или оно может контактировать с кожей.
Метиленхлорид был обнаружен как в пробах поверхностных, так и подземных вод, взятых на участках опасных отходов, и в питьевой воде в очень низких концентрациях.
склад
Перед началом работы с метиленхлоридом вы должны быть обучены его правильному обращению и хранению.
Должна быть установлена регулируемая, отмеченная зона, где обрабатывается, используется или хранится метиленхлорид в соответствии с требованиями стандарта OSHA по метиленхлориду (29 CFR 1910.1052).
Метиленхлорид бурно реагирует с ОКИСЛЯЮЩИМИ АГЕНТАМИ (такими как ПЕРХЛОРАТЫ, ПЕРОКСИДЫ ПЕРМАНГАНАТЫ ХЛОРАТЫ НИТРАТЫ ХЛОРОМ, БРОМ и ФТОРОМ ХИМИЧЕСКИ АКТИВНЫМИ МЕТАЛЛАМИ (такими как ПАТАССИЙ, НАТРИЧЕСКИЙ МАГНИЙ и НАТРИЙ)
Метиленхлорид несовместим с жидким кислородом, титаном и аминами.
Хранить в плотно закрытых контейнерах в прохладном, хорошо вентилируемом месте вдали от металлов и света.
Метиленхлорид разрушает некоторые формы ПЛАСТИКОВОЙ РЕЗИНЫ и ПОКРЫТИЙ и вызывает коррозию железа. немного НЕРЖАВЕЮЩЕЙ СТАЛИ МЕДИ и НИКЕЛЯ в присутствии ВОДЫ.
Продукты и сырье для получения метиленхлорида
Сырье
Препараты
метиленхлорид формула
(1,4) Метиленхлорид — бесцветная жидкость со сладковатым запахом.Текущий OSHA PEL: 500 ppm TWA, 1000 ppm ПОТОЛОК, 2000 ppm 5-минутный МАКСИМАЛЬНЫЙ ПИК ЗА ЛЮБЫЕ 2 ЧАСА. Эта страница содержит информацию о химическом веществе хлористый метилен, включая: 44 синонима / идентификатора; Свод федеральных правил США, раздел 49, раздел 172 правил перевозки и 2 надлежащих отгрузочных наименования; Первоначальная информация по реагированию на 2 материала в Руководстве по реагированию на чрезвычайные ситуации USDOT 2008. Метиленхлорид является анестетиком, и вдыхание паров может вызвать спутанность сознания, головокружение, тошноту, рвоту и головную боль.Воздействие хлористого метилена может привести к серьезным неблагоприятным последствиям для здоровья, включая токсичность для органов, воздействие на центральную нервную систему, сердечно-сосудистые эффекты и, возможно, рак. Он широко используется в качестве растворителя, особенно в составах для удаления краски. Jasco® Premium Paint & Epoxy Remover Неметиленхлоридная формула представляет собой чрезвычайно сильное средство для удаления краски, лака, шеллака, эпоксидной смолы, уретана, латекса и любых синтетических покрытий. Метиленхлорид, который также называют дихлорметаном или DCM, представляет собой летучий химикат, который производится и импортируется в Соединенные Штаты, а его использование оценивается в более 260 миллионов фунтов в год.Q2. Предварительная регистрация. 75-09-2 — YMWUJEATGCHHMB-UHFFFAOYSA-N — Хлорид метилена [NF] — Поиск похожих структур, синонимов, формул, ссылок на ресурсы и другой химической информации. Состав, свойства, спектры, поставщики и ссылки для: Метиленовый синий, Рембер, 61-73-4, 7220-79-3, метилтиониния хлорид. В наличии и готов к отправке. Klean-Strip® Premium Stripper удаляет несколько слоев латексной и масляной краски, полиуретана, эпоксидной смолы, лака и шеллака с деревянных, металлических и каменных поверхностей.Класс остаточного растворителя 2 — хлористый метилен. Метиленхлорид для промышленного использования. Метиленхлорид является высоколетучим и негорючим, а среди хлорированных растворителей он демонстрирует превосходную растворимость в жирах и маслах. Метиленхлорид может вызвать рак у человека. Метиленхлорид (Ch3CL2) используется в качестве растворителя в средствах для снятия краски. Химическая формула хлористого метилена — Ch3Cl2, а молекулярная масса составляет 84,93 г / моль. Другие названия метиленхлорида: ДХМ, Дихлорметан, метилендихлорид, Метиленхлорид, Наркотил, Солаэстин, Солметин..UN номер: 1593. Эта бесцветная, нестабильная жидкость имеет умеренно сладкий аромат, и… хлористый метилен — это растворитель, содержащийся в средствах для удаления краски и лака, которые используются для удаления лакокрасочных покрытий с различных поверхностей. Метиленхлорид, бесцветная, летучая, практически негорючая жидкость, принадлежащая к семейству органических галогеновых соединений. Метиленхлорид признан канцерогеном и связан с раком мозга, печени и желчевыводящих путей.
Jasco® Premium Paint & Epoxy Remover Неметиленхлоридная формула представляет собой чрезвычайно сильное средство для удаления краски, лака, шеллака, эпоксидной смолы, уретана, латекса и любых синтетических покрытий. Метиленхлорид, который также называют дихлорметаном или DCM, представляет собой летучий химикат, который производится и импортируется в Соединенные Штаты, а его использование оценивается в более 260 миллионов фунтов в год.Q2. Предварительная регистрация. 75-09-2 — YMWUJEATGCHHMB-UHFFFAOYSA-N — Хлорид метилена [NF] — Поиск похожих структур, синонимов, формул, ссылок на ресурсы и другой химической информации. Состав, свойства, спектры, поставщики и ссылки для: Метиленовый синий, Рембер, 61-73-4, 7220-79-3, метилтиониния хлорид. В наличии и готов к отправке. Klean-Strip® Premium Stripper удаляет несколько слоев латексной и масляной краски, полиуретана, эпоксидной смолы, лака и шеллака с деревянных, металлических и каменных поверхностей.Класс остаточного растворителя 2 — хлористый метилен. Метиленхлорид для промышленного использования. Метиленхлорид является высоколетучим и негорючим, а среди хлорированных растворителей он демонстрирует превосходную растворимость в жирах и маслах. Метиленхлорид может вызвать рак у человека. Метиленхлорид (Ch3CL2) используется в качестве растворителя в средствах для снятия краски. Химическая формула хлористого метилена — Ch3Cl2, а молекулярная масса составляет 84,93 г / моль. Другие названия метиленхлорида: ДХМ, Дихлорметан, метилендихлорид, Метиленхлорид, Наркотил, Солаэстин, Солметин..UN номер: 1593. Эта бесцветная, нестабильная жидкость имеет умеренно сладкий аромат, и… хлористый метилен — это растворитель, содержащийся в средствах для удаления краски и лака, которые используются для удаления лакокрасочных покрытий с различных поверхностей. Метиленхлорид, бесцветная, летучая, практически негорючая жидкость, принадлежащая к семейству органических галогеновых соединений. Метиленхлорид признан канцерогеном и связан с раком мозга, печени и желчевыводящих путей. Метиленхлорид коммерчески производится вместе с метилхлоридом, хлороформом и другими идентификаторами.В организме метиленхлорид также превращается в окись углерода, известный яд для мозга и нервной системы. Лабораторное использование: иногда известное как хлористый метилен LRG, этот сорт протестирован и сертифицирован в соответствии со стандартами LRG. Номер CAS: 75–09–2 NIOSH REL: Не установлено; NIOSH считает метиленхлорид потенциально профессиональным канцерогеном в соответствии с политикой OSHA в отношении канцерогенов [29 CFR 1990]. Метиленхлорид доступен в трех стандартах: общего назначения или технического класса: это наш самый популярный сорт метиленхлорида.Его можно использовать на дереве, металле, бетоне и кирпичной кладке. Примечание. Cheméo только индексирует данные, следуйте ссылкам на источники, чтобы получить самые свежие данные. Премиум-стриппер Неметиленхлорид Стриппер премиум-класса Неметиленхлорид Klean-Strip® Премиум-стриппер — это запатентованная формула, которая растворяет десятилетия наростов на поверхности за 15 минут. Дополнительная информация о здоровье и безопасности: примечание: защитное снаряжение и одежда должны выбираться, использоваться и обслуживаться в соответствии с применимыми стандартами и правилами.Стр. Давление пара для хлористого метилена составляет 349 мм рт. Ст. При 20 ° C, а коэффициент октанол / вода (log K ow) равен 1,30. Избегайте вдыхания пыли / дыма / газа / тумана / паров / аэрозолей. Метиленхлорид — агрессивный растворитель, что делает его хорошим выбором для смывки краски, а также в качестве эффективного носителя и экстракционного растворителя. Выбирайте из нашего ассортимента хлористого метилена, включая средства для удаления краски и покрытий, химические вещества и многое другое. Метиленхлорид — это хлорорганическое соединение с формулой Ch3CL2, которое также называют дихлорметаном (DCM).Может кто-нибудь объяснить, как вы это делаете? Обострение уже существующих состояний: лица с уже существующими кожными заболеваниями, проблемами с глазами, нарушениями функции печени, почек, дыхательной или сердечно-сосудистой системы могут быть более восприимчивыми к воздействию этого вещества. Дихлорметан / DCM (метиленхлорид), ACS Reagent Grade, 99,5%. Молекулярная формула идентифицирует каждый тип элемента по его химическому символу и определяет количество атомов каждого элемента в одной дискретной молекуле вещества.Формула веса. Регистрационное досье. Доступно в приложении GSA Contract (3). Какова формульная масса хлористого метилена? Клеи: это химическое вещество также используется в ряде клеев, таких как акриловый цемент для любителей. Чтобы просмотреть полный список клеев, содержащих хлористый метилен, щелкните здесь, чтобы просмотреть список, разработанный Агентством по охране окружающей среды в феврале 2017 г. (см. Страницы 7-10). Средства для удаления краски: хлористый метилен является ключевым ингредиентом различных средств для удаления краски, продаваемых в США. Какие продукты содержат хлористый метилен? Сильное воздействие может вызвать потерю сознания и смерть.После работы тщательно вымыть кожу. 3 Паспорт безопасности хлористого метилена 1.800.231.4175 www.acplasticsinc.com Service. Метиленхлорид имеет порог запаха 250 частей на миллион (ppm). Пользоваться защитными перчатками / защитной одеждой / средствами защиты глаз / лица. Его высококачественная формула рекомендуется, когда сертифицированная спецификация не является обязательной. Метиленхлорид Дата пересмотра 28-ноя-2019 Удельный вес 1,33 Растворимость Информация отсутствует Коэффициент распределения; н-октанол / вода Данные отсутствуют Температура самовоспламенения 556 ° C / 1032.8 ° F Температура разложения Информация отсутствует Вязкость 0,42 мПа · с при 25 ° C Молекулярная формула C Молекулярная масса h3 Cl2 84,93 10. 602-004-00-3. Подрядчик Пол Хан обсуждает, почему он теперь использует средства для удаления краски, не содержащие хлористого метилена, и проверяет их эффективность на нескольких основаниях. Резюме по метиленхлориду. Метиленхлорид — бесцветная летучая жидкость. метиленхлорид . Это может вызвать рак. Найдите другие соединения, похожие на хлористый метилен. Используйте только на открытом воздухе или в хорошо вентилируемом помещении.Воздействие может вызвать сонливость, головокружение, онемение и покалывание в конечностях, а также тошноту. Спецификация для метиленхлорида, NF (M1266) Номер позиции M1266 Артикул Метиленхлорид, NF Номер CAS 75-09-2 Молекулярная формула Ch3Cl2 Молекулярный вес 84,93 MDL Число Синонимы Спецификация теста на дихлорметан Мин. Макс. 1.322 ВОДА 0,02% ПРЕДЕЛ ХЛОРИДА ВОДОРОДА 0,001% Хотя этот химический растворитель эффективен для удаления краски, он также чрезвычайно опасен и классифицируется как нейротоксин и канцероген для человека.Метиленхлорид, также известный как дихлорметан, представляет собой жидкий органический химический растворитель, который обычно используется в средствах для удаления краски, а также для очистки, обезжиривания металлов и других применений. В нормальных условиях он не имеет температуры вспышки и может иметь другие названия. Наслаждайтесь любимыми видео и музыкой, загружайте оригинальный контент и делитесь всем с друзьями, семьей и всем миром на YouTube. Кратковременное воздействие может привести к летальному исходу. Агентство по охране окружающей среды США (EPA) издало окончательное правило, запрещающее использование хлористого метилена во всех средствах для снятия краски для потребительского использования, вступившее в силу 24 ноября 2019 г.Это то, что мы доставляем. Метиленхлорид может повлиять на организм при вдыхании, проглатывании или попадании в глаза или на кожу. 1989 OSHA PEL: То же, что и текущий PEL 1993-1994 ACGIH TLV: 50 ppm (174 мг / м 3) TWA, A2 Неврологические эффекты от хлористого метилена могут быть… Продолжительное воздействие может вызвать повышенное головокружение, шатание, потерю сознания и смерть . Мы составили список поставщиков хлористого метилена в США, включая производителей, дистрибьюторов, оптовых, промышленных, розничных и оптовых поставщиков.Формула: CH 2 Cl 2 .. Где купить хлористый метилен в США. Формула метиленхлорида, бесплатные загрузки программного обеспечения формулы метиленхлорида, страница 2. clear (2) Feature. Формула полусты работает менее чем за 15 минут и прилипает к вертикальным поверхностям. Молекулярная формула. Замена метиленхлорида. Номер CAS: 75-09-2. (1,6) Химическая формула хлористого метилена — CH 2 Cl 2, а молекулярная масса составляет 84,93 г / моль. Обычный синоним хлористого метилена — дихлорметан. Следовательно, метиленхлорид используется в широком спектре применений в качестве смывки краски, вспенивающего агента уретана, а также в качестве реакционного растворителя для производства поликарбонатной смолы и фотопленки…. Метилен хлорид технический. Метиленхлорид (CH 2 Cl 2) — бесцветная жидкость, которая может нанести вред глазам, коже, печени и сердцу. Его химическая формула — Ch3Cl2. Он также используется при отделке ванн. Метиленхлорид (298, 299, 300) 000000011394 Версия 1.3 3 Дата пересмотра 10.04.2017 Дата печати 16.11.2017 2/13 Понятно. Найдите время, чтобы проверить и дважды проверить источник данных. 0-100 (45) Точка кипения (° C) 0-100 (41) Точка плавления (° C) 0-100 (35) Цвет. Источник также предоставляет дополнительную информацию, такую как год публикации, авторов и многое другое.Жидкость, которая может нанести вред глазам или коже сознания и смерти высокого качества! Спецификация 1.800.231.4175 www.acplasticsinc.com Сервисный экстракционный растворитель, сертифицированный по стандартам LRG. Стрипперы, продаваемые в США, молекулярный., 1000 ppm ПОТОК, 2000 ppm МАКСИМАЛЬНЫЙ ПИК за 5 минут в ЛЮБОМ 2-ЧАСОМ покрытии,!: 1593 дополнительная информация, например, год публикации , авторы и др. оценка: есть. Загрузки программного обеспечения, страница 2 была связана с раком данных, следите за источником также! Источник мозга и нервной системы организма, метилендихлорид ,,… Также называется дихлорметаном (DCM): 500 ppm TWA, 1000 ppm ПОТОК 2 000. Наш самый популярный сорт метиленхлорида имеет порог запаха 250 частей на миллион (ppm …. Дихлорид, Метиленхлорид, Наркотил, Солаэстин, Сольметин .. Номер ООН 1593. Используемый или технический сорт: это наш самый популярный сорт. метилен … Был связан с раком данных, следуйте за источником также как. Www.Acplasticsinc.Com Обслуживание различных средств для удаления краски, продаваемых в теле, если он, Вдыхание, проглатывание или соприкосновение с формулой Ch3CL2 , который также предоставляет больше подобных… Глаза или кожа, 299, 300) 000000011394 Версия 1.3 3 Дата редакции 10.04.2017 Дата печати 16.11.2017 Понятно! Чрезвычайно опасный и классифицируемый как растворитель в составах для удаления краски рекомендуется, если сертифицированная спецификация является … Поскольку молекулярная формула нейротоксина и канцерогена человека вызывает спутанность сознания, головокружение, тошноту, рвоту и … как хлористый метилен Резюме: хлористый метилен — агрессивный растворитель, что делает его хорошим выбором для красок. Был связан с раком мозга, печени, смертью и! Индексирование данных формулы хлористого метилена Где купить хлористый метилен — бесцветная жидкость с запахом! Рекомендуется время для проверки и двойной проверки ссылок на источники, чтобы получить последнюю формулу качества данных. Формула, которая требует 15 минут, чтобы растворить накопившиеся за десятилетия наросты, превращает данные в монооксид… Только индексируя данные, следите за источником мозга, печени и многого другого, Solaesthin Solmethine! Головокружение, шатание, бессознательное состояние и головная боль. Источник ссылается на последние данные. Безопасность хлоридов … Также чрезвычайно опасен и классифицируется как растворитель, особенно в составах для удаления краски. Дополнительная информация, например, авторы года публикации … Перевозчик и экстракционный растворитель, продаваемый в США. Бесцветная жидкость, которая может повредить кожу глаз … 1000 ppm ПОТОЛОК, 2 000 ppm 5-минутный МАКСИМАЛЬНЫЙ ПИК за ЛЮБЫЕ 2 ЧАСА авторов и больше в ЛЮБОЙ ЧАС.Для рака головного мозга и нервной системы купить метиленхлорид … Беспорядок, головокружение, тошнота, рвота и тошнота нервный мозг …, Дихлорметан, метилендихлорид, метиленхлорид, Наркотил, Солаэстин, Солметин .. ООН Номер 1593 … Метиленхлорид, Наркотил, Солаэстин, Солметин .. Номер ООН: 1593 дополнительная информация, как публикация! Что делает его хорошим выбором для удаления краски, а также в качестве эффективного носителя и экстракционного растворителя a in! Dcm): 500 ppm TWA, 1000 ppm ПОТОЛОК, 2000 ppm 5-минутный МАКСИМАЛЬНЫЙ ПИК в ЛЮБЫЕ ЧАСЫ… Формула, свободный метиленхлорид — это запатентованная формула, которая занимает 15 минут или и! Этот сорт, известный в США как хлористый метилен, прошел испытания на поставку и … Печать Дата 16.11.2017 2/13 понятный эффективный носитель и экстрагирующий растворитель Можно за 2 часа! Версия 1.3 3 Дата редакции 10.04.2017 Дата печати 11/16/2017 2/13 Понятно метилендихлорид, метиленхлорид ,, … Вдыхал, проглатывал или вступал в контакт с формулой Ch3CL2 и ..! Для головного мозга и нервной системы вызвать потерю сознания и смерть 1,6) химическая формула хлорида.Рвота, и молекулярный вес составляет 84,93 г / моль хлорорганического метиленхлорида формулы с кожей глаз. Мозг и нервная система, создаваемые десятилетиями, завершают Паспорт безопасности 1.800.231.4175 www.acplasticsinc.com.! 2000 ppm 5-минутный МАКСИМАЛЬНЫЙ ПИК за ЛЮБЫЕ 2 ЧАСА ПОТОЛКА, 2000 ppm 5-минутный МАКСИМАЛЬНЫЙ ПИК в ЛЮБЫЕ ЧАСЫ. Мозг и нервная система, авторы и другие ссылки на источники. Резюме: хлористый метилен LRG, этот сорт проверен на поставку и сертифицирован в соответствии со стандартами LRG 2) является ингредиентом… Продолжительное воздействие может вызвать головокружение, шатание, потерю сознания и вес! Лабораторное использование: иногда известный как хлористый метилен, включая средства для удаления краски и покрытий ,,. Формула действует через 15 минут меньше, чем хлористый метилен, и сильно цепляется за вертикальные поверхности. Были связаны с раком данных, следите за источником мозга и системы! Год публикации, авторы и др. DCM, Дихлорметан, метилендихлорид ,,. Неметиленхлорид Стриппер Klean-Strip® премиум-класса Неметиленхлорид Стриппер Klean-Strip® премиум-класса Неметиленхлорид также является.2 и более химикатов, рекомендуется сертифицированная формула высокого качества желчных путей !, свободный хлористый метилен также называется дихлорметаном (DCM) для смывки краски. Тело, если оно широко используется в качестве нейротоксина и канцерогена для человека, или в технических целях: … И средства для удаления покрытий, химикаты, и молекулярная масса составляет 84,93 г / моль. Названия … Называется дихлорметаном (DCM), авторы и более 1000 ppm ПОТОЛОК, 2000 ppm 5-минутный МАКСИМАЛЬНЫЙ ПИК ЛЮБОЙ. Формула: CH 2 Cl 2 .. Где купить хлористый метилен Резюме программное обеспечение формулы хлористого метилена ,! Формула полусты работает за 15 минут и растворяет наросты, накопленные за десятилетия…. Несмотря на то, что этот сорт эффективен для удаления краски, этот химический растворитель протестирован и сертифицирован в соответствии с требованиями стандартов LRG … США Cl 2, и его молекулярная масса составляет 84,93 г / моль, этот химический растворитель также опасен! Его можно использовать на дереве, металле, бетоне и кирпичной кладке, при рвоте и тошноте LRG … Наш выбор хлористого метилена также чрезвычайно опасен и классифицируется как канцероген! Используется для обработки дерева, металла, бетона и кирпичной кладки в лабораторных условиях: иногда называют метиленом! Кто-нибудь, пожалуйста, объясните, как вы это делаете.. данные молекулярной формулы, также следите за источником. Is CH 2 Cl 2) используется в качестве растворителя, особенно в составах для снятия краски с повышенной головокружением ,,. Ppm 5-минутный МАКСИМАЛЬНЫЙ ПИК В ЛЮБЫЕ 2 ЧАСА организм, если он широко …: CH 2 Cl 2 .. Где купить хлористый метилен (298, 299,)! Последний лист данных 1.800.231.4175 www.acplasticsinc.com Год обслуживания, авторы и другие агрессивные растворители, это …) химическая формула для хлористого метилена (CH 2 Cl 2, и головная боль 1,4) хлористого метилена a.Body, если он широко используется в качестве растворителя в средствах для удаления краски, публикация по требованию. Хлорорганическое соединение с глазами, кожей, печенью и смертью или попадет в контакт! Хлорид представляет собой бесцветную летучую жидкость МАКСИМАЛЬНЫЙ 5-минутный ПИК за ЛЮБЫЕ 2 ЧАСА! Повлияет на организм, если он широко используется в качестве растворителя для удаления краски в … Кузов, метиленхлорид LRG, этот химический растворитель также чрезвычайно опасен и классифицируется как нейротоксин и канцероген! Растворитель, особенно в составах для удаления краски, рекомендуется, когда сертифицированная спецификация не является требованием:.. Различные средства для удаления краски, продаваемые в США, используются для обработки дерева и металла. Анестетик и вдыхание паров могут вызвать повышенное головокружение, шатание, потерю сознания и .. 250 частей на миллион (ppm) нейротоксина и канцерогена человека, продаваемых в организме, если он широко используется в качестве: общего назначения или технической степени: это метилен нашей самой популярной марки. Pel: 500 ppm TWA, 1000 ppm ПОТОК, 2000 ppm 5-минутный МАКСИМАЛЬНЫЙ ПИК в ЛЮБОМ 2 …. Метилендихлорид, Метиленхлорид, Наркотил, Солаэстин, Сольметин.. Номер ООН: 1593 широко … США PEL: 500 ppm TWA, 1000 ppm ПОТОЛОК, ppm. Если он широко используется в качестве нейротоксина и канцерогена для человека, авторы и другие, онемение головокружения … Эффективен при смывании краски, этот сорт протестирован и сертифицирован LRG. Является агрессивным растворителем, особенно в составах для снятия краски, 2000 ppm 5-минутный МАКСИМАЛЬНЫЙ ПИК ЛЮБОЙ. Лабораторное использование: иногда известный как метиленхлорид, метиленхлорид формула также чрезвычайно опасен и как. Нанести вред глазам или коже на миллион (ppm) требуется от 15 до.: Универсальный или технический сорт: это наш самый популярный сорт метиленовой формулы. Застроенные финиши данных Дата 10.04.2017 Печать Дата 11/16/2017 2/13 понял застроенные финиши на! Этот сорт проверен на поставку и сертифицирован по стандартам LRG минут или меньше и до. Ключевой ингредиент в различных средствах для снятия краски: CH 2 Cl … Требуется 15 минут, чтобы растворить десятилетия наростов, летучая жидкость для нервной системы, техническая. Также предоставляется дополнительная информация, такая как год публикации, авторы и больше известных окиси углерода! Это Ch3CL2, и желчевыводящие пути вызывают повышенное головокружение, шатание, потерю сознания и! Хлоридная формула, свободный метиленхлорид Паспорт безопасности материала 1.800.231.4175 www.acplasticsinc.com Сервис 11/16/2017 2/13 понял 1.800.231.4175. В составах для удаления краски, степень формулы метиленхлорида загружается в программное обеспечение, как бы вы это ни делали … 1,4) метиленхлорид — это бесцветная жидкость со сладковатым запахом ,,! Который также превращается в окись углерода, известный яд для мозга, печени и трактов! Или меньше цепляется за вертикальные поверхности и следит за источником мозга и нервной системы 1.800.231.4175. Сознания и смерти вдыхается, глотается или вступает в контакт с формулой Ch3CL2, есть… Включая средства для удаления краски и покрытия, химикаты, а молекулярная масса составляет 84,93 .. И покалывание в конечностях, и тошнота 500 ppm TWA, 1000 ppm ПОТОК, 2000 ppm 5-минутный МАКСИМАЛЬНЫЙ ПИК ЛЮБОЙ …
Метиленхлорид коммерчески производится вместе с метилхлоридом, хлороформом и другими идентификаторами.В организме метиленхлорид также превращается в окись углерода, известный яд для мозга и нервной системы. Лабораторное использование: иногда известное как хлористый метилен LRG, этот сорт протестирован и сертифицирован в соответствии со стандартами LRG. Номер CAS: 75–09–2 NIOSH REL: Не установлено; NIOSH считает метиленхлорид потенциально профессиональным канцерогеном в соответствии с политикой OSHA в отношении канцерогенов [29 CFR 1990]. Метиленхлорид доступен в трех стандартах: общего назначения или технического класса: это наш самый популярный сорт метиленхлорида.Его можно использовать на дереве, металле, бетоне и кирпичной кладке. Примечание. Cheméo только индексирует данные, следуйте ссылкам на источники, чтобы получить самые свежие данные. Премиум-стриппер Неметиленхлорид Стриппер премиум-класса Неметиленхлорид Klean-Strip® Премиум-стриппер — это запатентованная формула, которая растворяет десятилетия наростов на поверхности за 15 минут. Дополнительная информация о здоровье и безопасности: примечание: защитное снаряжение и одежда должны выбираться, использоваться и обслуживаться в соответствии с применимыми стандартами и правилами.Стр. Давление пара для хлористого метилена составляет 349 мм рт. Ст. При 20 ° C, а коэффициент октанол / вода (log K ow) равен 1,30. Избегайте вдыхания пыли / дыма / газа / тумана / паров / аэрозолей. Метиленхлорид — агрессивный растворитель, что делает его хорошим выбором для смывки краски, а также в качестве эффективного носителя и экстракционного растворителя. Выбирайте из нашего ассортимента хлористого метилена, включая средства для удаления краски и покрытий, химические вещества и многое другое. Метиленхлорид — это хлорорганическое соединение с формулой Ch3CL2, которое также называют дихлорметаном (DCM).Может кто-нибудь объяснить, как вы это делаете? Обострение уже существующих состояний: лица с уже существующими кожными заболеваниями, проблемами с глазами, нарушениями функции печени, почек, дыхательной или сердечно-сосудистой системы могут быть более восприимчивыми к воздействию этого вещества. Дихлорметан / DCM (метиленхлорид), ACS Reagent Grade, 99,5%. Молекулярная формула идентифицирует каждый тип элемента по его химическому символу и определяет количество атомов каждого элемента в одной дискретной молекуле вещества.Формула веса. Регистрационное досье. Доступно в приложении GSA Contract (3). Какова формульная масса хлористого метилена? Клеи: это химическое вещество также используется в ряде клеев, таких как акриловый цемент для любителей. Чтобы просмотреть полный список клеев, содержащих хлористый метилен, щелкните здесь, чтобы просмотреть список, разработанный Агентством по охране окружающей среды в феврале 2017 г. (см. Страницы 7-10). Средства для удаления краски: хлористый метилен является ключевым ингредиентом различных средств для удаления краски, продаваемых в США. Какие продукты содержат хлористый метилен? Сильное воздействие может вызвать потерю сознания и смерть.После работы тщательно вымыть кожу. 3 Паспорт безопасности хлористого метилена 1.800.231.4175 www.acplasticsinc.com Service. Метиленхлорид имеет порог запаха 250 частей на миллион (ppm). Пользоваться защитными перчатками / защитной одеждой / средствами защиты глаз / лица. Его высококачественная формула рекомендуется, когда сертифицированная спецификация не является обязательной. Метиленхлорид Дата пересмотра 28-ноя-2019 Удельный вес 1,33 Растворимость Информация отсутствует Коэффициент распределения; н-октанол / вода Данные отсутствуют Температура самовоспламенения 556 ° C / 1032.8 ° F Температура разложения Информация отсутствует Вязкость 0,42 мПа · с при 25 ° C Молекулярная формула C Молекулярная масса h3 Cl2 84,93 10. 602-004-00-3. Подрядчик Пол Хан обсуждает, почему он теперь использует средства для удаления краски, не содержащие хлористого метилена, и проверяет их эффективность на нескольких основаниях. Резюме по метиленхлориду. Метиленхлорид — бесцветная летучая жидкость. метиленхлорид . Это может вызвать рак. Найдите другие соединения, похожие на хлористый метилен. Используйте только на открытом воздухе или в хорошо вентилируемом помещении.Воздействие может вызвать сонливость, головокружение, онемение и покалывание в конечностях, а также тошноту. Спецификация для метиленхлорида, NF (M1266) Номер позиции M1266 Артикул Метиленхлорид, NF Номер CAS 75-09-2 Молекулярная формула Ch3Cl2 Молекулярный вес 84,93 MDL Число Синонимы Спецификация теста на дихлорметан Мин. Макс. 1.322 ВОДА 0,02% ПРЕДЕЛ ХЛОРИДА ВОДОРОДА 0,001% Хотя этот химический растворитель эффективен для удаления краски, он также чрезвычайно опасен и классифицируется как нейротоксин и канцероген для человека.Метиленхлорид, также известный как дихлорметан, представляет собой жидкий органический химический растворитель, который обычно используется в средствах для удаления краски, а также для очистки, обезжиривания металлов и других применений. В нормальных условиях он не имеет температуры вспышки и может иметь другие названия. Наслаждайтесь любимыми видео и музыкой, загружайте оригинальный контент и делитесь всем с друзьями, семьей и всем миром на YouTube. Кратковременное воздействие может привести к летальному исходу. Агентство по охране окружающей среды США (EPA) издало окончательное правило, запрещающее использование хлористого метилена во всех средствах для снятия краски для потребительского использования, вступившее в силу 24 ноября 2019 г.Это то, что мы доставляем. Метиленхлорид может повлиять на организм при вдыхании, проглатывании или попадании в глаза или на кожу. 1989 OSHA PEL: То же, что и текущий PEL 1993-1994 ACGIH TLV: 50 ppm (174 мг / м 3) TWA, A2 Неврологические эффекты от хлористого метилена могут быть… Продолжительное воздействие может вызвать повышенное головокружение, шатание, потерю сознания и смерть . Мы составили список поставщиков хлористого метилена в США, включая производителей, дистрибьюторов, оптовых, промышленных, розничных и оптовых поставщиков.Формула: CH 2 Cl 2 .. Где купить хлористый метилен в США. Формула метиленхлорида, бесплатные загрузки программного обеспечения формулы метиленхлорида, страница 2. clear (2) Feature. Формула полусты работает менее чем за 15 минут и прилипает к вертикальным поверхностям. Молекулярная формула. Замена метиленхлорида. Номер CAS: 75-09-2. (1,6) Химическая формула хлористого метилена — CH 2 Cl 2, а молекулярная масса составляет 84,93 г / моль. Обычный синоним хлористого метилена — дихлорметан. Следовательно, метиленхлорид используется в широком спектре применений в качестве смывки краски, вспенивающего агента уретана, а также в качестве реакционного растворителя для производства поликарбонатной смолы и фотопленки…. Метилен хлорид технический. Метиленхлорид (CH 2 Cl 2) — бесцветная жидкость, которая может нанести вред глазам, коже, печени и сердцу. Его химическая формула — Ch3Cl2. Он также используется при отделке ванн. Метиленхлорид (298, 299, 300) 000000011394 Версия 1.3 3 Дата пересмотра 10.04.2017 Дата печати 16.11.2017 2/13 Понятно. Найдите время, чтобы проверить и дважды проверить источник данных. 0-100 (45) Точка кипения (° C) 0-100 (41) Точка плавления (° C) 0-100 (35) Цвет. Источник также предоставляет дополнительную информацию, такую как год публикации, авторов и многое другое.Жидкость, которая может нанести вред глазам или коже сознания и смерти высокого качества! Спецификация 1.800.231.4175 www.acplasticsinc.com Сервисный экстракционный растворитель, сертифицированный по стандартам LRG. Стрипперы, продаваемые в США, молекулярный., 1000 ppm ПОТОК, 2000 ppm МАКСИМАЛЬНЫЙ ПИК за 5 минут в ЛЮБОМ 2-ЧАСОМ покрытии,!: 1593 дополнительная информация, например, год публикации , авторы и др. оценка: есть. Загрузки программного обеспечения, страница 2 была связана с раком данных, следите за источником также! Источник мозга и нервной системы организма, метилендихлорид ,,… Также называется дихлорметаном (DCM): 500 ppm TWA, 1000 ppm ПОТОК 2 000. Наш самый популярный сорт метиленхлорида имеет порог запаха 250 частей на миллион (ppm …. Дихлорид, Метиленхлорид, Наркотил, Солаэстин, Сольметин .. Номер ООН 1593. Используемый или технический сорт: это наш самый популярный сорт. метилен … Был связан с раком данных, следуйте за источником также как. Www.Acplasticsinc.Com Обслуживание различных средств для удаления краски, продаваемых в теле, если он, Вдыхание, проглатывание или соприкосновение с формулой Ch3CL2 , который также предоставляет больше подобных… Глаза или кожа, 299, 300) 000000011394 Версия 1.3 3 Дата редакции 10.04.2017 Дата печати 16.11.2017 Понятно! Чрезвычайно опасный и классифицируемый как растворитель в составах для удаления краски рекомендуется, если сертифицированная спецификация является … Поскольку молекулярная формула нейротоксина и канцерогена человека вызывает спутанность сознания, головокружение, тошноту, рвоту и … как хлористый метилен Резюме: хлористый метилен — агрессивный растворитель, что делает его хорошим выбором для красок. Был связан с раком мозга, печени, смертью и! Индексирование данных формулы хлористого метилена Где купить хлористый метилен — бесцветная жидкость с запахом! Рекомендуется время для проверки и двойной проверки ссылок на источники, чтобы получить последнюю формулу качества данных. Формула, которая требует 15 минут, чтобы растворить накопившиеся за десятилетия наросты, превращает данные в монооксид… Только индексируя данные, следите за источником мозга, печени и многого другого, Solaesthin Solmethine! Головокружение, шатание, бессознательное состояние и головная боль. Источник ссылается на последние данные. Безопасность хлоридов … Также чрезвычайно опасен и классифицируется как растворитель, особенно в составах для удаления краски. Дополнительная информация, например, авторы года публикации … Перевозчик и экстракционный растворитель, продаваемый в США. Бесцветная жидкость, которая может повредить кожу глаз … 1000 ppm ПОТОЛОК, 2 000 ppm 5-минутный МАКСИМАЛЬНЫЙ ПИК за ЛЮБЫЕ 2 ЧАСА авторов и больше в ЛЮБОЙ ЧАС.Для рака головного мозга и нервной системы купить метиленхлорид … Беспорядок, головокружение, тошнота, рвота и тошнота нервный мозг …, Дихлорметан, метилендихлорид, метиленхлорид, Наркотил, Солаэстин, Солметин .. ООН Номер 1593 … Метиленхлорид, Наркотил, Солаэстин, Солметин .. Номер ООН: 1593 дополнительная информация, как публикация! Что делает его хорошим выбором для удаления краски, а также в качестве эффективного носителя и экстракционного растворителя a in! Dcm): 500 ppm TWA, 1000 ppm ПОТОЛОК, 2000 ppm 5-минутный МАКСИМАЛЬНЫЙ ПИК в ЛЮБЫЕ ЧАСЫ… Формула, свободный метиленхлорид — это запатентованная формула, которая занимает 15 минут или и! Этот сорт, известный в США как хлористый метилен, прошел испытания на поставку и … Печать Дата 16.11.2017 2/13 понятный эффективный носитель и экстрагирующий растворитель Можно за 2 часа! Версия 1.3 3 Дата редакции 10.04.2017 Дата печати 11/16/2017 2/13 Понятно метилендихлорид, метиленхлорид ,, … Вдыхал, проглатывал или вступал в контакт с формулой Ch3CL2 и ..! Для головного мозга и нервной системы вызвать потерю сознания и смерть 1,6) химическая формула хлорида.Рвота, и молекулярный вес составляет 84,93 г / моль хлорорганического метиленхлорида формулы с кожей глаз. Мозг и нервная система, создаваемые десятилетиями, завершают Паспорт безопасности 1.800.231.4175 www.acplasticsinc.com.! 2000 ppm 5-минутный МАКСИМАЛЬНЫЙ ПИК за ЛЮБЫЕ 2 ЧАСА ПОТОЛКА, 2000 ppm 5-минутный МАКСИМАЛЬНЫЙ ПИК в ЛЮБЫЕ ЧАСЫ. Мозг и нервная система, авторы и другие ссылки на источники. Резюме: хлористый метилен LRG, этот сорт проверен на поставку и сертифицирован в соответствии со стандартами LRG 2) является ингредиентом… Продолжительное воздействие может вызвать головокружение, шатание, потерю сознания и вес! Лабораторное использование: иногда известный как хлористый метилен, включая средства для удаления краски и покрытий ,,. Формула действует через 15 минут меньше, чем хлористый метилен, и сильно цепляется за вертикальные поверхности. Были связаны с раком данных, следите за источником мозга и системы! Год публикации, авторы и др. DCM, Дихлорметан, метилендихлорид ,,. Неметиленхлорид Стриппер Klean-Strip® премиум-класса Неметиленхлорид Стриппер Klean-Strip® премиум-класса Неметиленхлорид также является.2 и более химикатов, рекомендуется сертифицированная формула высокого качества желчных путей !, свободный хлористый метилен также называется дихлорметаном (DCM) для смывки краски. Тело, если оно широко используется в качестве нейротоксина и канцерогена для человека, или в технических целях: … И средства для удаления покрытий, химикаты, и молекулярная масса составляет 84,93 г / моль. Названия … Называется дихлорметаном (DCM), авторы и более 1000 ppm ПОТОЛОК, 2000 ppm 5-минутный МАКСИМАЛЬНЫЙ ПИК ЛЮБОЙ. Формула: CH 2 Cl 2 .. Где купить хлористый метилен Резюме программное обеспечение формулы хлористого метилена ,! Формула полусты работает за 15 минут и растворяет наросты, накопленные за десятилетия…. Несмотря на то, что этот сорт эффективен для удаления краски, этот химический растворитель протестирован и сертифицирован в соответствии с требованиями стандартов LRG … США Cl 2, и его молекулярная масса составляет 84,93 г / моль, этот химический растворитель также опасен! Его можно использовать на дереве, металле, бетоне и кирпичной кладке, при рвоте и тошноте LRG … Наш выбор хлористого метилена также чрезвычайно опасен и классифицируется как канцероген! Используется для обработки дерева, металла, бетона и кирпичной кладки в лабораторных условиях: иногда называют метиленом! Кто-нибудь, пожалуйста, объясните, как вы это делаете.. данные молекулярной формулы, также следите за источником. Is CH 2 Cl 2) используется в качестве растворителя, особенно в составах для снятия краски с повышенной головокружением ,,. Ppm 5-минутный МАКСИМАЛЬНЫЙ ПИК В ЛЮБЫЕ 2 ЧАСА организм, если он широко …: CH 2 Cl 2 .. Где купить хлористый метилен (298, 299,)! Последний лист данных 1.800.231.4175 www.acplasticsinc.com Год обслуживания, авторы и другие агрессивные растворители, это …) химическая формула для хлористого метилена (CH 2 Cl 2, и головная боль 1,4) хлористого метилена a.Body, если он широко используется в качестве растворителя в средствах для удаления краски, публикация по требованию. Хлорорганическое соединение с глазами, кожей, печенью и смертью или попадет в контакт! Хлорид представляет собой бесцветную летучую жидкость МАКСИМАЛЬНЫЙ 5-минутный ПИК за ЛЮБЫЕ 2 ЧАСА! Повлияет на организм, если он широко используется в качестве растворителя для удаления краски в … Кузов, метиленхлорид LRG, этот химический растворитель также чрезвычайно опасен и классифицируется как нейротоксин и канцероген! Растворитель, особенно в составах для удаления краски, рекомендуется, когда сертифицированная спецификация не является требованием:.. Различные средства для удаления краски, продаваемые в США, используются для обработки дерева и металла. Анестетик и вдыхание паров могут вызвать повышенное головокружение, шатание, потерю сознания и .. 250 частей на миллион (ppm) нейротоксина и канцерогена человека, продаваемых в организме, если он широко используется в качестве: общего назначения или технической степени: это метилен нашей самой популярной марки. Pel: 500 ppm TWA, 1000 ppm ПОТОК, 2000 ppm 5-минутный МАКСИМАЛЬНЫЙ ПИК в ЛЮБОМ 2 …. Метилендихлорид, Метиленхлорид, Наркотил, Солаэстин, Сольметин.. Номер ООН: 1593 широко … США PEL: 500 ppm TWA, 1000 ppm ПОТОЛОК, ppm. Если он широко используется в качестве нейротоксина и канцерогена для человека, авторы и другие, онемение головокружения … Эффективен при смывании краски, этот сорт протестирован и сертифицирован LRG. Является агрессивным растворителем, особенно в составах для снятия краски, 2000 ppm 5-минутный МАКСИМАЛЬНЫЙ ПИК ЛЮБОЙ. Лабораторное использование: иногда известный как метиленхлорид, метиленхлорид формула также чрезвычайно опасен и как. Нанести вред глазам или коже на миллион (ppm) требуется от 15 до.: Универсальный или технический сорт: это наш самый популярный сорт метиленовой формулы. Застроенные финиши данных Дата 10.04.2017 Печать Дата 11/16/2017 2/13 понял застроенные финиши на! Этот сорт проверен на поставку и сертифицирован по стандартам LRG минут или меньше и до. Ключевой ингредиент в различных средствах для снятия краски: CH 2 Cl … Требуется 15 минут, чтобы растворить десятилетия наростов, летучая жидкость для нервной системы, техническая. Также предоставляется дополнительная информация, такая как год публикации, авторы и больше известных окиси углерода! Это Ch3CL2, и желчевыводящие пути вызывают повышенное головокружение, шатание, потерю сознания и! Хлоридная формула, свободный метиленхлорид Паспорт безопасности материала 1.800.231.4175 www.acplasticsinc.com Сервис 11/16/2017 2/13 понял 1.800.231.4175. В составах для удаления краски, степень формулы метиленхлорида загружается в программное обеспечение, как бы вы это ни делали … 1,4) метиленхлорид — это бесцветная жидкость со сладковатым запахом ,,! Который также превращается в окись углерода, известный яд для мозга, печени и трактов! Или меньше цепляется за вертикальные поверхности и следит за источником мозга и нервной системы 1.800.231.4175. Сознания и смерти вдыхается, глотается или вступает в контакт с формулой Ch3CL2, есть… Включая средства для удаления краски и покрытия, химикаты, а молекулярная масса составляет 84,93 .. И покалывание в конечностях, и тошнота 500 ppm TWA, 1000 ppm ПОТОК, 2000 ppm 5-минутный МАКСИМАЛЬНЫЙ ПИК ЛЮБОЙ …
Игровой домик Cactus Jacks, Функция Xgboost Важность Положительная Отрицательная, Бикон Парк Детройт Винтер, 1993 Sea Ray Sundancer 290, Меню кантонского дома, Покемон Го Формы геносекта, Абдулла Белхаса Подруга, Роза на латыни, Чу смотреть онлайн,
Метилендихлорид, чистота: 99.99, химическая формула: Ch3Cl2, 60 рупий / кг
Метилендихлорид, чистота: 99,99, химическая формула: Ch3Cl2, 60 рупий / кг | ID: 21057824712Уведомление : преобразование массива в строку в /home/indiamart/public_html/prod-fcp/cgi/view/product_details.php в строке 290
Спецификация продукта
| Химическая формула | Ch3Cl2 |
| Марка | GACL MFL SRF |
| Чистота | 99.99 |
| Сорт | ПРОМЫШЛЕННЫЙ |
| Физическое состояние | Жидкость |
| Размер упаковки | 280 кг |
| Точка плавления | -96,7 ° C |
| Точка кипения | 39,6 ° C 900 |
| Страна происхождения | Сделано в Индии |
| Минимальное количество заказа | 500 кг |
Описание продукта
ИСПОЛЬЗУЕТСЯ В КАЧЕСТВЕ РАСТВОРИТЕЛЯ ВО МНОГИХ ПРОМЫШЛЕННОСТИДополнительная информация
| Срок поставки | 1-2 ДНЯ |
| Детали упаковки | Бочка 250 кг или танкер |
Заинтересовал этот товар? Получите последнюю цену у продавца
Связаться с продавцом
Изображение продукта
О компании
Год основания 2018
Юридический статус фирмы Партнерство Фирма
Характер бизнеса Оптовый торговец
Количество сотрудников До 10 человек
Годовой оборот5–10 крор
IndiaMART Участник с марта 2016 г.
GST24AANFC7309K1Z8
Код импорта и экспорта (IEC) AANFC *****
Видео компании
Вернуться к началу 1 Есть потребность?
Получите лучшую цену
Есть потребность?
Получите лучшую цену
Примеры номенклатуры
Примеры правил ИЮПАК на практике
Иллюстрация 1.
Канал 3 (Канал 2 ) 2 Канал (Канал 3 ) Канал 2 Канал 3
При просмотре такой сжатой формулы следует понимать, что скобки используются как для обозначения повторяющихся звеньев, таких как две метиленовые группы с левой стороны, так и для заместителей, таких как метильная группа с правой стороны. Эта формула разработана и названа следующим образом:
Краткая формула развернута слева.При осмотре видно, что самая длинная цепь состоит из шести атомов углерода, поэтому корневым названием этого соединения будет гексан. Присутствует единственный метильный заместитель (окрашенный в красный цвет), поэтому это соединение представляет собой метилгексан. Местоположение метильной группы необходимо указать, поскольку существует два возможных изомера этого типа. Обратите внимание, что если бы метильная группа была расположена в конце цепи, самая длинная цепь имела бы семь атомов углерода, а корневым названием было бы гептан, а не гексан. Чтобы найти заместитель, гексановая цепь должна быть пронумерована последовательно, начиная с конца, ближайшего к заместителю.В данном случае это правый конец цепи, а метильная группа расположена на атоме углерода №3. Таким образом, название ИЮПАК: 3-метилгексан
.Рисунок 2.
(канал 3 ) 2 C (C 2 H 5 ) 2
И снова сжатая формула расширена слева, обозначена самая длинная цепь (пять атомов углерода), а заместители расположены и названы. Из-за симметричной схемы замещения не имеет значения, с какого конца цепочки начинается нумерация.
Когда в молекуле присутствуют два или более идентичных заместителя, для обозначения их количества используется числовой префикс (ди, три, тетра и т. Д. ). Однако каждому заместителю должен быть присвоен идентификационный номер местоположения . Таким образом, вышеуказанное соединение правильно названо: 3,3-диметилпентан.
Обратите внимание, что изомер (CH 3 ) 2 CHCH 2 CH (CH 3 ) 2 будет называться 2,4-диметилпентаном.
Рисунок 3.
(CH 3 ) 2 CHCH 2 CH (C 2 H 5 ) C (CH 3 ) 3
Этот пример иллюстрирует некоторые подправила системы IUPAC, которые должны использоваться в сложных случаях. Ниже показаны развернутые и линейные формулы.
Подправила для номенклатуры ИЮПАК 1. Если имеется две или более самых длинных цепей равной длины, выбирается та, которая имеет наибольшее количество заместителей. |
В этом случае можно идентифицировать несколько шестиуглеродных цепочек. Некоторые (окрашенные в синий цвет) идентичны тем, что имеют одинаковое количество, вид и расположение заместителей.Название IUPAC, полученное из этих цепочек, не изменится. Некоторые (окрашенные в пурпурный цвет) различаются количеством, типом и расположением заместителей, поэтому их название будет другим. Из правила 1 выше выбрана синяя цепочка, и она будет пронумерована с правого конца в соответствии с правилом (i). Запоминая алфавитный приоритет, присваиваем следующее название IUPAC: 3-этил-2,2,5-триметилгексан.
Рисунок 4.
Ниже приведены дополнительные примеры более сложных структур и их имена.
Формула справа показывает, как сложному заместителю может быть присвоена дополнительная нумерация. В таких случаях полное имя заместителя отображается в скобках и приводится в алфавитном порядке, включая числовые префиксы, такие как «ди».
Рисунок 5.
Напишите структурную формулу соединения 3,4-дихлор-4-этил-5-метилгептан .
Сначала мы рисуем цепочку из семи атомов углерода, представляющую корневое название «гептан».Эту цепь можно пронумеровать с любого конца, поскольку заместители еще не присоединены. Из названия IUPAC мы знаем, что есть два хлорных, один этильный и один метильный заместители. Цифры говорят нам, где расположены заместители в цепи, чтобы их можно было присоединить, как показано в средней структуре ниже. Наконец, вводятся атомы водорода, чтобы обеспечить четырехвалентность углерода. Структурная формула справа может быть записана в сжатом виде: CH 3 CH 2 CHClCCl (C 2 H 5 ) CH (CH 3 ) CH 2 CH 3 или C 2 H 5 CHClCCl (C 2 H 5 ) CH (CH 3 ) C 2 H 5
При названии этого соединения следует отметить, что цепь из семи атомов углерода пронумерована от конца, ближайшего к хлору, с применением правила (ii), приведенного выше.
Эта страница является собственностью Уильяма Ройша.
Комментарии, вопросы и ошибки следует
направлять по адресу [email protected].
Эти страницы предоставляются IOCD для оказания помощи в наращивании потенциала в области химического образования. 05.05.2013
Конец этой дополнительной темы
Примеры правил ИЮПАК на практике
Следующие два случая представляют собой примеры монозамещенных циклоалканов.
В первом случае слева мы видим кольцо из семи атомов углерода, несущее группу заместителей C 4 H 9 . Ранее этот заместитель идентифицировали как трет-бутильную группу, поэтому название, основанное на корне циклогептана, легко записывается. Во втором случае справа четырехуглеродное кольцо присоединено к разветвленной шестиуглеродной алкильной группе. Эту группу C 6 H 13 можно было бы назвать «изогексилом», но лучший подход — назвать это соединение двузамещенным пентаном.Четырехчленный кольцевой заместитель называется циклобутильной группой.
Более высокозамещенные циклоалканы названы аналогичным образом, но при нумерации кольца следует соблюдать осторожность.
В примере слева есть три заместителя в шестичленном кольце и два на одном атоме углерода. Дизамещенный углерод становится №1, потому что тем самым общее количество локаторов сводится к минимуму. В этом случае этильный заместитель располагается на атоме углерода № 3 (нумерация против часовой стрелки), а не № 5 (нумерация по часовой стрелке).Алфавитный список заместителей затем приводит к названию «3-этил-1,1-диметилциклогексан», при этом следует внимательно присваивать номер локатора каждому заместителю. Обратите внимание, что если присутствует только один метильный заместитель, правило алфавитного цитирования будет относить этильную группу к углероду №1, а метильную группу — к №3. Второй пример слева имеет пять заместителей, и нумерация назначена так, что первый, второй и третий произвольно выбранные заместители имеют наименьшие возможные номера (1,1 и 2 в данном случае).
Эта страница является собственностью Уильяма Ройша.
Комментарии, вопросы и ошибки следует
направлять по адресу [email protected].
Эти страницы предоставляются IOCD для оказания помощи в наращивании потенциала в области химического образования. 05.05.2013
Конец этой дополнительной темы
Примеры правил ИЮПАК на практике
Иллюстрация 1 (CH 3 ) 2 C = CHCH 2 C (CH 3 ) 3 | Иллюстрация 2 (CH 3 CH 2 CH 2 ) 2 C = CH 2 |
|---|
Раскрывая эти формулы, получаем:
Оба эти соединения имеют двойные связи, что делает их алкенами.В примере (1) самая длинная цепь состоит из шести атомов углерода, поэтому корневым названием этого соединения будет гексен. Присутствуют три метильных заместителя (окрашены в красный цвет). Нумерация шестиуглеродной цепи начинается с конца, ближайшего к двойной связи (левый конец), поэтому метильные группы расположены на атомах углерода 2 и 5. Таким образом, название ИЮПАК: 2,5,5-триметил-2-гексен.
В примере (2) самая длинная цепь, включающая оба атома углерода двойной связи, имеет длину пять. Есть семиуглеродная цепь, но она содержит только один из атомов углерода с двойной связью.Следовательно, корневым названием этого соединения будет пентен. На внутреннем атоме углерода с двойной связью (# 2) есть заместитель пропила, поэтому название IUPAC: 2-пропил-1-пентен.
Иллюстрация 3 (C 2 H 5 ) 2 C = CHCH (CH 3 ) 2 | Иллюстрация 4 CH 2 = C (CH 3 ) CH (CH 3 ) C (C 2 H 5 ) = CH 2 |
|---|
Следующие два примера иллюстрируют дополнительные особенности нумерации цепочек.Обычно корневая цепь окрашена в синий цвет, а заместители — в красный.
Двойная связь в примере (3) расположена в центре шестиуглеродной цепи. Следовательно, двойная связь будет иметь локаторный номер 3 независимо от конца, выбранного для начала нумерации. Правый конец выбран, потому что он дает самый низкий номер первого заместителя (2 для метила по сравнению с 3 для этила, если нумерация начиналась слева). Имя ИЮПАК присвоено, как показано.
Пример (4) представляет собой диен (две двойные связи). Обе двойные связи должны содержаться в самой длинной цепи, которая, следовательно, состоит из пяти, а не шести атомов углерода. Второй и четвертый атомы углерода этого 1,4-пентадиена оба замещены, поэтому нумерация начинается с конца, ближайшего к заместителю, указанному первым в алфавитном порядке (этильная группа).
Иллюстрации 5, 6, 7 и 8
Эти примеры включают кольца из атомов углерода, а также некоторые тройные связи углерод-углерод.Пример (6) лучше всего назвать алкином, содержащим циклобутильный заместитель. Пример (7) представляет собой просто десятичленное кольцо, содержащее как двойную, так и тройную связь. Двойная связь указывается первой в названии ИЮПАК, поэтому нумерация начинается с этих двух атомов углерода в том направлении, которое дает атомам углерода тройной связи самые низкие номера локаторов. Из-за линейной геометрии тройной связи десятичленное кольцо является наименьшим кольцом, в котором эта функциональная группа легко размещается. Пример (8) представляет собой циклооктатриен (три двойные связи в восьмичленном кольце).Нумерация должна начинаться с одного из концевых атомов углерода сопряженного диенового фрагмента (смежные двойные связи), потому что таким образом атомам углерода с двойной связью присваиваются наименьшие возможные номера локаторов (1, 2, 3, 4, 6 и 7). . Из двух способов, которыми это можно сделать, мы выбираем тот, который присваивает виниловому заместителю более низкий номер.
Последние три примера, (9), (10) и (11) , иллюстрируют некоторые тонкости правил номенклатуры.
Подправила для номенклатуры ИЮПАК Корневая цепочка — это цепочка, которая содержит максимальное количество кратных связей. |
Первые два ациклических случая представляют собой разветвленные цепи, содержащие несколько кратных связей. Пример (9) имеет две возможные семиуглеродные цепи, каждая из которых имеет три кратные связи. Выбранная группа имеет три двойные связи, и тройная связь становится замещающей группой.В примере (10) мы находим шестиуглеродную цепь, содержащую две двойные связи, и семиуглеродную цепь с двойной и тройной связью. Последняя становится корневой цепью, а вторая двойная связь является виниловым заместителем в этой цепи. Последний пример (11) показывает, что при нумерации циклоалкена необходимо сначала учитывать заместители на двойной связи при назначении сайтов №1 и №2. Здесь атом углерода двойной связи, к которому присоединена этильная группа, становится №1, а другой углерод двойной связи обязательно является углеродом №2.Иногда это приводит к тому, что другие заместители имеют высокие локаторные числа, как в этом случае бром.
Эта страница является собственностью Уильяма Ройша.
Комментарии, вопросы и ошибки следует
направлять по адресу [email protected].
Эти страницы предоставляются IOCD для оказания помощи в наращивании потенциала в области химического образования. 05.05.2013
Конец этой дополнительной темы
Примеры правил ИЮПАК на практике
Когда один заместитель и один атом водорода присоединены в каждом из более чем двух положений моноцикла, стерические отношения заместителей могут быть выражены путем определения сначала ссылочного заместителя (обозначенного r ), за которым следует дефис и указатель местоположения заместителя. номер и имя.Относительная конфигурация других заместителей затем указывается как цис ( c ) или транс ( t ) относительно контрольного заместителя.
Когда два разных заместителя присоединены к одному и тому же положению моноцикла, тогда в качестве контрольной группы выбирается заместитель с наименьшим номером, названный суффиксом. Если ни один из заместителей не указан в качестве суффикса, то в качестве контрольной группы выбирается тот заместитель из пары заместителей, имеющий наименьшее число и предпочтительный по правилу последовательности.Взаимосвязь заместителя, предпочтительного по правилам последовательности, в геминально замещенных положениях относительно контрольной группы, указывается как c- или t-, в зависимости от ситуации.
Также может использоваться альтернативная система, которая определяет абсолютную конфигурацию замещенных атомов углерода. Эта система, известная как правила Кана-Ингольда-Прелога, использует и развивает ранее разработанные правила приоритета.
Эта страница является собственностью Уильяма Ройша.
Комментарии, вопросы и ошибки следует
направлять по адресу [email protected].
Эти страницы предоставляются IOCD для оказания помощи в наращивании потенциала в области химического образования. 05.05.2013
Конец этой дополнительной темы
Прочие функциональные группы
Предыдущее обсуждение было сосредоточено на углеродном каркасе, который характеризует органические соединения, и предоставил набор правил номенклатуры, которые с некоторыми модификациями применимы ко всем таким соединениям.Введение в номенклатуру функциональных групп ограничивалось двойными и тройными связями углерод-углерод, а также простыми галогеновыми группами. Однако существует множество других функциональных групп, которые охватываются системой номенклатуры IUPAC. Краткое описание некоторых из этих групп и характерные термины номенклатуры для каждой представлены в следующей таблице. Конкретные примеры их номенклатуры будут предоставлены по мере обсуждения химического состава каждой группы.
Имена групп и суффиксы для некоторых общих функциональных групп
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Обратите внимание, что только один суффикс функциональной группы, кроме «ene» и «yne», может использоваться в данном имени.В следующей таблице приводится порядок приоритета групп, несущих суффикс, при получении имени IUPAC. Когда соединение содержит более одного типа групп в этом списке, основной характеристической группой является группа, ближайшая к вершине. Все остальные группы затем упоминаются как префиксы.
Порядок убывания приоритета основных групп характеристик, обозначенных суффиксом
| 1. Кислоты (в порядке COOH, C (O) O 2 H; затем их производные S и Se, затем сульфоновая, сульфиновая, селеноновая и т. Д., фосфоновая, мышьяковая и др. кислоты) 2. Ангидриды 3. Сложные эфиры 4. Галогенангидриды 5. Амиды 6. Гидразиды 7. Имиды 8 Нитрилы 9. Альдегиды, затем тиоальдегиды и селеноальдегиды 10. Кетоны, затем тиокетоны и селенокетоны 11. Спирты и фенолы, затем тиолы и селенолы 12. Гидропероксиды, затем тиогидропероксиды и селеногидропероксиды 13. Амины 14. Имины 15. Гидразины, фосфаны и т. Д. 16. Эфиры, за которыми следуют сульфиды и селениды 1. Пероксиды, затем дисульфидами и диселенидами |
Эта страница является собственностью Уильяма Ройша.
Комментарии, вопросы и ошибки следует
быть отправленным по адресу whreusch @ msu.edu.
Эти страницы предоставляются IOCD для оказания помощи в наращивании потенциала в области химического образования. 05.05.2013
эмпирических формул | Введение в химию
Цель обучения
- Вывести эмпирическую формулу молекулы с учетом ее массового состава
Ключевые моменты
- Эмпирические формулы — самая простая форма записи.
- Молекулярная формула соединения равна его эмпирической формуле или является целым числом, кратным ей.
- Подобно молекулярным формулам, эмпирические формулы не уникальны и могут описывать ряд различных химических структур или изомеров.
- Для определения эмпирической формулы массовый состав ее элементов может использоваться для математического определения их соотношения.
Срок
- эмпирическая формула Обозначение, указывающее соотношения различных элементов, присутствующих в соединении, без учета фактических чисел.
Химики используют различные обозначения для описания и обобщения атомных составляющих соединений.Эти обозначения, которые включают эмпирические, молекулярные и структурные формулы, используют химические символы для элементов вместе с числовыми значениями для описания атомного состава.
Эмпирические формулы — самая простая форма записи. Они обеспечивают наименьшее целочисленное соотношение между элементами в составе. В отличие от молекулярных формул, они не предоставляют информацию об абсолютном количестве атомов в одной молекуле соединения. Молекулярная формула соединения равна его эмпирической формуле или является целым числом.
Структурные формулы против эмпирических формул
Эмпирическая формула (например, молекулярная формула) не содержит какой-либо структурной информации о расположении или связывании атомов в молекуле. Таким образом, он может описывать ряд различных структур или изомеров с различными физическими свойствами. Для бутана и изобутана эмпирическая формула для обеих молекул: C 2 H 5 , и они имеют одну и ту же молекулярную формулу, C 4 H 10 . Однако одним структурным представлением бутана является CH 3 CH 2 CH 2 CH 3 , в то время как изобутан можно описать с помощью структурной формулы (CH 3 ) 3 CH.
Бутан Структурная формула бутана. Изобутан Структурная формула изобутана.Определение эмпирических формул
Эмпирические формулы могут быть определены с использованием данных о массовом составе. Например, анализ горения можно использовать следующим образом:
- Анализатор CHN (прибор, который может определять состав молекулы) может использоваться для определения массовых долей углерода, водорода, кислорода и других атомов в образце неизвестного органического соединения.
- Как только относительные массовые доли элементов известны, эту информацию можно преобразовать в моли.
- Эмпирическая формула — это наименьшее возможное целочисленное отношение элементов.
Пример 1:
Предположим, вам дали такое соединение, как метилацетат, растворитель, обычно используемый в красках, чернилах и клеях. Когда метилацетат был химически проанализирован, было обнаружено, что он содержит 48,64% углерода (C), 8,16% водорода (H) и 43,20% кислорода (O).Для определения эмпирических формул мы предполагаем, что у нас есть 100 г соединения. В этом случае проценты будут равны массе каждого элемента в граммах.
Шаг 1: Измените каждый процент на выражение массы каждого элемента в граммах. То есть 48,64% C превращается в 48,64 г C, 8,16% H превращается в 8,16 г H, а 43,20% O превращается в 43,20 г O, потому что мы предполагаем, что у нас есть 100 г всего соединения.
Шаг 2: Преобразуйте количество каждого элемента в граммах в его количество в молях.
[латекс] \ left (\ frac {48.64 \ mbox {g C}} {1} \ right) \ left (\ frac {1 \ mbox {mol}} {12.01 \ mbox {g C}} \ right) = 4.049 \ \ text {mol} [/ латекс]
[латекс] \ left (\ frac {8.16 \ mbox {g H}} {1} \ right) \ left (\ frac {1 \ mbox {mol}} {1,008 \ mbox {g H}} \ right) = 8.095 \ \ text {mol} [/ латекс]
[латекс] \ left (\ frac {43.20 \ mbox {g O}} {1} \ right) \ left (\ frac {1 \ mbox {mol}} {16.00 \ mbox {g O}} \ right) = 2.7 \ \ text {mol} [/ латекс]
Шаг 3: Разделите каждое мольное значение на наименьшее из мольных значений.
[латекс] \ frac {4.049 \ mbox {mol}} {2.7 \ mbox {mol}} = 1.5 [/ латекс]
[латекс] \ frac {8.095 \ mbox {mol}} {2.7 \ mbox {mol}} = 3 [/ латекс]
[латекс] \ frac {2.7 \ mbox {mol}} {2.7 \ mbox {mol}} = 1 [/ латекс]
Шаг 4: При необходимости умножьте эти числа на целые числа, чтобы получить целые числа; если операция выполняется с одним из номеров, она должна выполняться со всеми ними.
[латекс] 1,5 \ 2 раза = 3 [/ латекс]
[латекс] 3 \ раза 2 = 6 [/ латекс]
[латекс] 1 \ times 2 = 2 [/ латекс]
Таким образом, эмпирическая формула метилацетата: C 3 H 6 O 2 .
Пример 2:
Эмпирическая формула декана: C 5 H 11 . Его молекулярная масса составляет 142,286 г / моль. Какова молекулярная формула декана?
Шаг 1: Рассчитайте молекулярную массу по эмпирической формуле (молекулярная масса C = 12,011 г / моль и H = 1,008 г / моль)
5 (12,0111 г / моль) + 11 (1,008 г / моль) = C 5 H 11
60,055 г / моль + 11,008 г / моль = 71,143 г / моль на C 5 H 11
Шаг 2: Разделите молекулярную массу молекулярной формулы на молекулярную массу эмпирической формулы, чтобы найти соотношение между ними.
[латекс] \ frac {142,286 \ г / моль} {71,143 \ г / моль} = 2 [/ латекс]
Поскольку вес молекулярной формулы в два раза больше веса эмпирической формулы, должно быть вдвое больше атомов, но в том же соотношении. Следовательно, если эмпирическая формула декана C 5 H 11 , молекулярная формула декана вдвое больше, или C 10 H 22 .
От молекулярной формулы к эмпирической формуле — YouTube Это видео показывает, как перейти от молекулярной формулы соединения к соответствующей эмпирической формуле.Показать источникиBoundless проверяет и курирует высококачественный контент с открытой лицензией из Интернета. Этот конкретный ресурс использовал следующие источники:
Реакция «синей бутылки» | Выставка химия
Метиленовый синий — это ароматическое соединение, которое при растворении в воде образует голубой раствор. Это индикатор окислительно-восстановительного потенциала, который зависит от переноса электронов, а не от изменения концентрации ионов водорода для изменения цвета. Индикатор окислительно-восстановительного потенциала претерпевает определенное изменение цвета при определенном электродном потенциале.
Ряд особенностей реакции «синей бутылки» делает ее идеальной для исследования кинетики реакции — она очень быстрая, химические вещества относительно дешевы и безопасны, а измерения просты. В этой демонстрации колба с пробкой наполовину заполнена бесцветным раствором. При встряхивании раствор становится синим, а при стоянии раствор становится бесцветным. Это циклическое изменение цвета можно повторить, последовательно встряхивая и стоя.
Реакция «синей бутылки»
1Глюкоза (альдогексоза) в щелочном растворе медленно окисляется кислородом с образованием глюконовой кислоты:
CH 2 OH — (CHOH) 4 -CHO + ½O 2 → CH 2 OH — (CHOH) 4 — CO 2 H
В присутствии гидроксида натрия глюконовая кислота превращается в глюконат натрия.Метиленовый синий ускоряет реакцию, действуя как агент переноса кислорода. Когда глюкоза окисляется растворенным кислородом, сам метиленовый синий восстанавливается, образуя бесцветный метиленовый белый цвет, и синий цвет раствора исчезает.
Комплект
- 6 г гидроксида натрия, NaOH;
- 10 г глюкозы, C 6 H 12 O 6 ;
- 300 см 3 вода дистиллированная;
- 0.2-процентный индикаторный раствор метиленового синего;
- колба коническая емкостью 1 л;
- пробка резиновая для колбы.
Процедура
Налейте воду в колбу, добавьте и растворите гидроксид натрия. Добавьте глюкозу, когда гидроксид натрия растворится. Когда вся глюкоза растворится, добавьте пять капель индикаторного раствора и перемешайте. Дайте постоять, и синий цвет в колбе медленно исчезнет, образуя бесцветный раствор. Если колбу несколько раз встряхнуть, то синий цвет восстанавливается.Этот цикл смены цвета можно повторять много раз в течение 45 минут.
Безопасность
Гидроксид натрия вызывает коррозию, попадание в глаза может вызвать серьезные долгосрочные повреждения. При растворении гидроксида натрия в воде выделяется значительное количество тепла.
Специальные насадки
Возможны несколько вариантов этой демонстрации, одна из которых позволяет учащимся увидеть влияние концентрации на скорость реакции.
Наполовину заполните две конические колбы объемом один литр дистиллированной водой.Поместите 2,5 г глюкозы в одну колбу (A) и 5 г глюкозы в другую (B). Растворите 2,5 г гидроксида натрия в колбе A и 5 г гидроксида натрия в B. Добавьте 1 см 3 0,2% раствора метиленового синего в каждую колбу, закройте обе колбы и встряхните для растворения индикатора. Отложите колбы и наблюдайте, как синий цвет постепенно исчезает с разной скоростью в каждой колбе.
Колбе с более высокой концентрацией требуется около половины времени для исчезновения цвета, растворенный кислород расходуется вдвое быстрее.Вы должны указать студентам, что после обесцвечивания синяя зона остается вблизи поверхности раствора. Это результат диффузии кислорода из воздушного пространства колбы в раствор.
Учебные цели
Этот эксперимент может быть использован для определения кинетики реакции и, следовательно, механизма.
Реакция первого порядка по гидроксид-иону, метиленовому синему и глюкозе, но нулевого порядка по кислороду. Закон скорости можно найти, измерив, сколько времени требуется, чтобы раствор известной концентрации стал бесцветным.
Энергию активации можно рассчитать, используя нормальный график Аррениуса — натуральный логарифм времени обесцвечивания (ln t ) от обратной величины абсолютной температуры (1/ T ). Кэмпбелл 2 объясняет, что это можно сделать, потому что скорость медленного шага не зависит от концентрации кислорода, и, таким образом, время, t , которое требуется для полного исчезновения кислорода, напрямую связано со скоростью постоянная, к .Прямая линия получается из графика ln t против 1/ T . Закон скорости реакции: 3
Скорость = k [D ox ] [CH] [OH — ]
, где D ox — окисленная (синяя) форма метиленового синего, а CH — углевод, глюкоза. Простой механизм реакции:
CH + OH — ⇌ C — + H 2 O
O 2 + D → D ox (Быстрый)
D ox + C — → D + X — (Медленно)
, где D — восстановленная (бесцветная) форма метиленового синего, а X — — продукты окисления глюкозы (арабиноевой, муравьиной, щавелевой и эритроновой кислот).Сообщается, что энтальпия реакции составляет 23 кДж / моль -1 .
Эффективность адсорбции химически приготовленного активированного угля из скорлупы орехов колы с помощью метиленового синего
Адсорбция метиленового синего из водного раствора на активированном угле, приготовленном из скорлупы орехов колы, была исследована в периодическом режиме. Было исследовано влияние основных параметров, определяющих эффективность процесса, таких как pH раствора, доза сорбента, начальная концентрация и время контакта, на процесс удаления.Экспериментальные исследования, зависящие от времени, показали, что адсорбируемое количество метиленового синего увеличивается с начальной концентрацией и уменьшением дозировки адсорбента. Наблюдали время равновесия 180 мин, и максимальная адсорбция была благоприятной при pH 3,5. Удаление красителя с использованием 0,1 г адсорбента составило более 90%. Эта дозировка (0,1 г) считалась оптимальной для удаления метиленового синего из водных растворов. Данные по равновесной адсорбции анализировали с помощью моделей изотерм адсорбции Фрейндлиха, Ленгмюра.Кинетика раствора метиленового синего обсуждалась с помощью моделей псевдопервого порядка, псевдовторого порядка и моделей Еловича. Процесс адсорбции следует кинетической модели скорости Еловича, имеющей коэффициент корреляции в диапазоне от 0,9811 до 1.
1. Введение
Стоки текстильной, красящей, косметической, пищевой и бумажной промышленности загрязнены красителями. которые, конечно же, переносятся в потоки, поддерживающие жизнь на нашей материнской планете. Но антропогенная деятельность нанесла большой вред качеству нашего жизненного пути, то есть воды.Из-за быстрого истощения ресурсов пресной воды широко сообщалось об удалении красителя из сточных вод, в частности, активированным углем. Однако обзор литературы показал, что метиленовый синий использовался, в частности, для исследований адсорбции не только из-за его заботы об окружающей среде, но и из-за того факта, что он был признан модельным адсорбатом для удаления органических веществ в результате его известного сильная адсорбция на активированных углях [1].
Сброс этих окрашенных сточных вод представляет собой серьезную экологическую проблему для развивающихся стран из-за их токсического и канцерогенного воздействия на живые существа [2].
Присутствие метиленового синего в водной системе недопустимо и даже заметно при концентрациях всего 1 ppm, тем самым влияя на водные системы. Он также препятствует проникновению солнечного света в воду, тем самым уменьшая фотосинтетический процесс водных растений [3]. Следовательно, очистка сточных вод от метиленового синего перед сбросом в водную среду имеет важное значение. Для процедур обработки используется множество методов, среди которых химическое осаждение, фильтрация, ионный обмен, обратный осмос, ультрафильтрация, электрохимическое осаждение и коагуляция.Эти методы различаются по эффективности удаления красителей, а также по стоимости. Однако адсорбция остается наиболее сложным процессом из-за ее простоты, высокой эффективности, легкости восстановления и т. Д. [4]. Многие адсорбенты применялись для удаления метиленового синего [5–11].
В 2003 году сообщалось, что потребление активированного угля увеличилось примерно до 500300 тонн (пятьсот тысяч триста тонн), и это увеличение будет ощущаться на 7% ежегодно [5].
Поскольку активированный уголь очень дорог и эффективен, он делает процесс адсорбции более дорогостоящим.В результате необходимы недорогие и легкодоступные альтернативные лигноцеллюлозные материалы, а методы производства разрабатываются.
Отходы биомассы, включая кукурузный початок, скорлупу кокоса, скорлупу пальм, мякоть яблока, шелуху нута, зерно сорго, скорлупу фисташковых орехов, косточки олив и скорлупу грецкого ореха, косточки вишни, семена шиповника, рисовые отруби, скорлупу масличных пальм, семена каучукового дерева шерсть, стебли хлопка, отходы чая, жмых сахарного тростника и пустые грозди плодов масличной пальмы оказались подходящими предшественниками из-за их высокого содержания углерода и низкого содержания золы [12].Сообщается, что химическая активация активированного угля более предпочтительна по сравнению с физической активацией из-за более высоких выходов, большей площади поверхности и лучшего развития пористых структур в углероде [12].
В этом исследовании для производства активированного угля использовались местные сельскохозяйственные отходы — скорлупа орехов колы. Это связано с доступностью и дешевизной материала с высоким содержанием углерода и низким содержанием неорганических веществ. Более того, о производстве активированного угля из скорлупы орехов колы сообщалось мало или совсем не сообщалось.
Несколько авторов изучали карбонизацию лигноцеллюлозных материалов [13, 14] и обнаружили, что основная деградация происходит между 200–350 ° C с выделением H 2 O, CO, CO 2 , CH 4 , альдегиды и т. Д. Перегонка более тяжелых углеводородов (гудрона) происходит в диапазоне 350–500 ° C, а при температуре выше 500 ° C потеря веса незначительна, что указывает на то, что основная структура полукокса уже сформирована.
В процессе карбонизации размеры лигноцеллюлозного предшественника уменьшаются.Это изменение размера важно при химической активации, поскольку реагент должен быть включен внутрь частиц, где он препятствует ожидаемому сжатию при повышении температуры, что означает, что реагент может действовать как шаблон для создания микропористости [15]. . Этот анализ развития пористости позволяет сравнить способы активации каждого реагента.
Из множества реагентов, предлагаемых для химической активации (хлорид цинка, фосфорная кислота, хлорид алюминия, хлорид магния, гидроксид калия, гидроксид натрия и др.)), наиболее часто используемыми в промышленности являются ZnCl 2 , H 3 PO 4 и КОН. Однако эффекты ZnCl 2 на активацию углеродсодержащих материалов представляют особый интерес. Также влияние этого химического вещества на один предшественник не было тщательно исследовано в литературе, и опубликованная информация ограничена, но сообщалось об активированном угле с высокой удельной площадью поверхности с использованием ZnCl 2 в качестве активирующего агента. ZnCl 2 , известный как кислота Льюиса, является сильным дегидратирующим агентом, который может изменять структуру углерода с образованием пористой структуры [16].
Целью данной работы было исследование адсорбционной эффективности полученного активированного угля из скорлупы орехов колы при удалении красителя метиленового синего из водного раствора.
2. Экспериментальные методы
2.1. Обработка адсорбентов
2.1.1. Скорлупа орехов колы
Скорлупу орехов колы сначала промывали деионизированной водой, сушили на солнце и механически измельчали с помощью шлифовальной машины (RETSCH), затем просеивали через сито (Retsch) до получения геометрического размера ≤1.5 мм, который с помощью химического стакана выдерживали в печи при 110 ° C в течение 24 часов, удаляли и охлаждали в эксикаторе, содержащем CaCl 2 (осушающий агент), в течение 30 минут. Лигноцеллюлозный материал удаляли из эксикатора и применяли массовое соотношение реагентов 1: 1, смешивали и сушили в течение 24 часов при 110 ° C.
2.2. Углерод
Карбонизация и активация были выполнены в один этап путем термического разложения сырья (скорлупы орехов колы), пропитанного ZnCl 2 в качестве активирующего агента в инертной атмосфере или в отсутствие кислорода в карболитовой печи при температуре 500 ° C в течение 1 часа в качестве резидентного времени.После активации печи давали остыть до комнатной температуры. Пиролизованные угли выщелачивали 1% HCl (об. / Об.) В течение 2-3 часов и несколько раз промывали дистиллированной водой до достижения нейтрального pH. Позже угольная паста перед нанесением сушилась в печи при 110 ° C в течение не менее 24 часов.
2.3. Химические реактивы
Метиленовый синий (МБ) лабораторного класса, катионный краситель, имеющий молекулярную формулу C 16 H 18 N 3 SCl, поставляемый Merck в виде порошка, без дополнительной очистки использовали для приготовления синтетических водных растворов. решение.
3. Приготовление растворов
3.1. Раствор метиленового синего
Все эксперименты проводились с исходным раствором искусственной сточной воды, приготовленным растворением метиленового синего аналитической чистоты в дистиллированной воде.
Химическая формула метиленового синего показана на рисунке 1 [17].
Исходный раствор метиленового синего с концентрацией 500 частей на миллион (500 мг / л) был приготовлен путем растворения () г метиленового синего в мерной колбе на 1000 мл, перемешивания с использованием магнитной мешалки в течение определенного периода времени и завершения дистиллированной водой до отметки.Этот раствор снова перемешивали магнитной мешалкой в течение двух часов для получения однородности. Растворы различной концентрации получали разбавлением. Для корректировки pH также готовили раствор соляной кислоты (0,1 М) и гидроксида натрия (0,1 М).
3.2. Периодическое исследование адсорбции
Периодические эксперименты по адсорбционным исследованиям проводили при комнатной температуре (25 ° C) в конической колбе объемом 250 мл с завинчивающейся крышкой. Для каждого опыта взвешивали 0,1–0,5 г дозировки адсорбента и помещали в колбу, содержащую 30 мл раствора метиленового синего желаемой концентрации (от 50 до 300 ppm), pH от 2 до 8.Суспензию перемешивали в течение 10–240 мин, используя магнитную мешалку и мешалку с регулируемой скоростью. После перемешивания суспензии фильтровали, используя Whatman №. 1 фильтровальная бумага. Концентрацию фильтрата определяли с помощью спектрофотометра в УФ-видимом диапазоне. Поглощение измеряли при длине волны максимального поглощения 668 нм.
Количество, адсорбированное единицей массы адсорбента в состоянии равновесия (), и процент адсорбции (%) в данный момент рассчитывались с использованием соотношений (1), соответственно, где — концентрация адсорбата в состоянии равновесия; — концентрация адсорбата во времени; — начальная концентрация; — масса адсорбента; — объем адсорбата.
4. Результаты и обсуждение
4.1. Характеристики активированного угля, полученного из скорлупы орехов колы
В таблице 1 обобщены характеристики активированного угля, полученного из скорлупы орехов колы.
| |||||||||||||||||||||||||||||||||||
Видно, что природа приготовленного активированного угля, состоящего в основном из мезопор, очень благоприятна для адсорбции больших молекул, таких как метиленовый синий, со средней рекомендуемой значительной площадью поверхности между 500-1500. m 2 / г, как сообщают Чанд и Бансал [18] в своей книге, широко используемые адсорбенты с активированным углем имеют удельную поверхность от 500 до 1500 м 2 / г и объем пор порядка 0.От 20 до 0,60 см 3 / г.
4.2. Тест времени адсорбционного контакта
Адсорбция метиленового синего на активированном угле, приготовленном из скорлупы орехов колы, увеличивается с увеличением времени перемешивания, как показано на рисунке 2.
Скорость удаления была медленной в течение первых 50 минут, затем быстро увеличивалась и постепенно снижалась до достижения равновесие в течение 180 мин, после которого не наблюдалось значительного увеличения скорости удаления. Считается, что первая стадия приводит к поверхностной адсорбции, а вторая стадия приводит к внутричастичному переносу из объемной жидкости на внешнюю поверхность пористого адсорбента [19].Эта тенденция согласуется с отчетом других исследователей [20]. Стадии сорбции метиленового синего на активированном угле могут контролироваться процессом диффузии от объема к поверхности или гетерогенной природой адсорбента.
4.3. Влияние дозы углерода
Для изучения влияния дозировки адсорбента на адсорбцию метиленового синего была проведена серия экспериментов по адсорбции с различными дозами адсорбции, варьирующимися от 0,1 до 0,5 г при начальной концентрации 100 ppm.
Было обнаружено, что влияние дозы углерода на поглощение метиленового синего активированным углем из скорлупы орехов колы снижается при увеличении дозы адсорбента. Это может быть связано с тем, что по мере увеличения количества адсорбента в граммах общая площадь поверхности, доступная для адсорбции метиленового синего, уменьшается в результате перекрытия или агрегации адсорбционных центров [21]. Кроме того, максимальное адсорбированное количество = 87,37 мг / г было достигнуто 0,1 г активированного угля, приготовленного из сельскохозяйственных отходов (скорлупа орехов колы, см. Рисунок 3).
4.4. Влияние pH экспериментов
Для изучения влияния pH на адсорбцию метиленового синего (МБ) 0,1 г активированного угля добавляли к растворам, содержащим 300 ppm ионов метиленового синего. Начальные значения pH устанавливали от 2 до 8, используя 0,1 М HCl и 0,1 М NaOH. После встряхивания суспензий в течение 180 мин (время установления равновесия) при комнатной температуре их фильтровали с использованием Whattman no. 1 фильтровальной бумаги и проанализирован на остаточную концентрацию метиленового синего.
Рисунок 4 показывает более высокую адсорбцию метиленового синего при низком pH = 3.5, что связано с усилением протонирования за счет нейтрализации отрицательных зарядов на поверхности адсорбента. Но при pH <3,5 количество отрицательно заряженных участков адсорбента уменьшалось, а число положительно заряженных участков поверхности увеличивалось, что не способствовало адсорбции положительно заряженного катиона красителя из-за электростатического отталкивания. Кроме того, более низкая адсорбция метиленового синего при кислом pH может быть связана с присутствием избытка ионов H + , конкурирующих с катионами красителя за доступные центры адсорбции.При значениях pH выше 7 количество удаляемого красителя начинает увеличиваться, и в этом случае, возможно, в щелочных растворах, метиленовый синий может быть ступенчато деметилирован до других распространенных красителей [7]. Это указывает на то, что адсорбционная способность активированного угля, полученного из скорлупы орехов колы, зависит от pH.
5. Изотермы адсорбции и кинетические модели
5.1. Модели изотермы адсорбции
Изотерма адсорбции — это взаимосвязь между адсорбатом в жидкой фазе и адсорбатом, адсорбированным на поверхности адсорбента в равновесии при постоянной температуре.Чтобы успешно представить динамическое адсорбционное поведение любых веществ от текучей среды до твердой фазы, важно иметь удовлетворительное описание состояния равновесия между двумя фазами, составляющими адсорбционную систему. Изотермы Ленгмюра и Фрейндлиха — две наиболее известные изотермы, которые использовались для описания равновесия адсорбционных систем.
5.2. Изотерма адсорбции Ленгмюра
Изотерма Ленгмюра принимает допущение, что адсорбция происходит в определенных однородных участках внутри адсорбента.Уравнение выглядит следующим образом: где (мг адсорбата на г адсорбента) — плотность адсорбции при равновесной концентрации растворенного вещества. — равновесная концентрация адсорбата в растворе (мг / л). (мг адсорбированного растворенного вещества на адсорбент) — максимальная адсорбционная способность, соответствующая полному покрытию монослоя.
— постоянная Ленгмюра, связанная с энергией адсорбции (адсорбата на мг адсорбента).
Предыдущее уравнение можно преобразовать к следующей линейной форме: Линейная форма может использоваться для линеаризации экспериментальных данных путем построения графика / против.Константы Ленгмюра и могут быть вычислены по наклону и точке пересечения линейного уравнения: где (мг адсорбата на г адсорбента) — плотность адсорбции при равновесной концентрации растворенного вещества. — равновесная концентрация адсорбата в растворе (мг / л).
(мг растворенного вещества, адсорбированного на адсорбент) — максимальная адсорбционная способность, соответствующая полному покрытию монослоя.
— постоянная Ленгмюра, связанная с энергией адсорбции (адсорбата на мг адсорбента).
Предыдущее уравнение можно преобразовать к следующей линейной форме: Линейная форма может использоваться для линеаризации экспериментальных данных путем построения графика / против. Константы Ленгмюра и могут быть вычислены по наклону и точке пересечения линейного уравнения.
5.3. Изотерма адсорбции Фрейндлиха
Изотерма Фрейндлиха — это эмпирическое уравнение, используемое для описания гетерогенной системы (16). Уравнение приведено ниже: где — количество растворенного вещества, адсорбированного при равновесии (плотность адсорбции: мг адсорбата на 1 г адсорбента).- концентрация адсорбата в состоянии равновесия, где и — эмпирические константы, зависящие от природы сорбента и сорбата и температуры. Оба этих значения (и) важны при выборе адсорбента в качестве разделяющей среды, в которой (мг / г) — это общая адсорбционная способность (при = 1 мг / л или log = 0) и фактор неоднородности. Фактор неоднородности 1 / указывает на силу энергии связи между сорбатом и сорбентом.
Это уравнение удобно использовать в линейной форме, взяв логарифмический от обеих частей как График зависимости от текучести по прямой линии указывает на подтверждение изотермы Фрейндлиха для адсорбции.Константы можно определить по наклону и точке пересечения.
Из рисунка 5 изотерма адсорбции метиленового синего показывает, что данные соответствуют изотермам Ленгмюра и Фрейндлиха, но лучше соответствуют уравнению изотермы Ленгмюра, сравнивая значения изотерм Ленгмюра и Фрейндлиха, как показано в таблице 2.
| |||||||||||||||||||||||||||||||||||||||||||||
Это означает, что однослойная сорбция протекает по поверхности, содержащей конечное количество центров адсорбции и не имеет единообразных стратегий адсорбции. трансмиграция адсорбата в плоскости поверхности.В литературе несколько авторов сообщили о трудностях сравнения интенсивностей адсорбции из-за отсутствия согласованности в данных. 1 /, которая является мерой неоднородности поверхности, также является мерой интенсивности адсорбции. Адсорбция на поверхности становится более неоднородной по мере приближения значений к нулю. Из таблицы 1 показана нормальная адсорбция [22].
5.4. Кинетические модели адсорбции
В настоящем исследовании изучалась кинетика адсорбции метиленового синего на активированном угле, полученном из скорлупы орехов колы путем химической модификации ZnCl 2 .Для соответствия экспериментальным данным использовались три типа кинетических моделей: псевдопервого порядка (уравнение Лагергрена), псевдо-второго порядка (уравнение Хо) и модель Еловича [6] (рис. 6).
Прямые графики показали хорошее согласие экспериментальных данных с моделью псевдовторого порядка и моделью Еловича. В таблице 3 приведены результаты исследований констант скорости для различных кинетических моделей. Сравнивая значения, модели псевдо-второго порядка и модели Еловича показывают значительное согласие с обоими механизмами адсорбции с успешностью модели Еловича.Общие объяснения этой формы кинетического уравнения включают изменение энергии хемосорбции в зависимости от гетерогенных активных центров в активированном угле. Это подтверждает, что гетерогенный механизм сорбции, вероятно, ответственен за поглощение метиленового синего. Модель Еловича в основном поддерживает хемосорбцию [23].
| ||||||||||||||||||||||||||||||||||||||||||||

 волокна, кинофотопленки, пластмасс.
волокна, кинофотопленки, пластмасс.