Формиат натрия / НПО ЭТЦ
Описание:
Формиат натрия (натрий муравьинокислый / HCO2Na) — химическое соединение с формулой HCOONa, побочный продукт производства пентаэритрита. Используется как восстановитель в органическом синтезе. Формиат натрия технический представляет собой формиат натрия с незначительной примесью пентаэритрита и его производных. Формиат натрия технический используется в качестве противоморозной и пластифицирующей добавки в производстве строительных конструкций, в кожевенной промышленности как агент в преддубильных операциях, как сырьё в производстве муравьиной кислоты.
Физико-химические свойства
Кристаллический порошок белого или серого цвета без посторонних примесей, видимых невооружённым глазом. Допускается зеленоватый оттенок. Массовая доля формиата натрия, %, не менее 92 Массовая доля воды, %, не более 3.0 Массовая доля сахаристых веществ в пересчёте на глюкозу к массе сухих веществ, %, не более 1.
Основные свойства
Хорошо растворим в воде, слабо растворим в спиртах, не растворим в эфирах. Взрывобезопасен и не горюч, однако в местах хранения и работы с формиатом натрия следует запрещать курение и применение открытого огня.
Требования безопасности
По степени воздействия на организм относится к веществам класса опасности 3. Опасность для человека: формиат натрия вызывает раздражение верхних дыхательных путей и слизистых оболочек. Индивидуальные средства защиты: при работе с формиатом натрия следует применять индивидуальные средства защиты — халат, респиратор, резиновые перчатки. В аварийных ситуациях необходимо использовать противогаз марки А или М.
Формиат натрия технический взрывобезопасен и не горюч, однако в местах хранения и работы с ним следует запрещать курение и применение открытого огня.
Применение
Как противоморозная добавка формиат натрия применяется при возведении монолитных бетонных и железобетонных конструкций, монолитных частей сборно-монолитных конструкций и замоноличивания стыков сборных конструкций, а также при изготовлении сборных бетонных и железобетонных изделий на полигонах при установившейся среднесуточной температуре наружного воздуха ниже 5 градусов.
Бетон с данной добавкой запрещается применять в предварительно напряжённых конструкциях, армированных сталью классов AT-IY, AT-YI, A-IY и А-У, в бетонных и железобетонных конструкциях, предназначенных для эксплуатации в водных и газовых средах при относительной влажности воздуха более 60 % при наличии в заполнителе включений реакционноспособного кремнеза, в железобетонных конструкциях для электрифицированного транспорта и промышленных предприятий, применяющих постоянный электрический ток.
Формиат натрия вводится в бетонную смесь в количестве: — 2% от массы цемента в пересчете на сухой формиат натрия при расчетной температуре твердения до −5 °C; — 3% от массы цемента в пересчете на сухой формиат натрия при расчетной температуре твердения до −10 °C; — 4% от массы цемента при пересчете на сухой формиат натрия при расчетной температуре твердения до −15 °C.
При приготовлении бетона (раствора) добавку необходимо растворить в тёплой воде. Полученный раствор добавляется вместе с водой затворения. Полученный раствор следует дозировать в бетоносмеситель через дозатор химических добавок или через дозатор воды, при этом следует снизить расход воды затворения на 7-13%
Полученный раствор следует дозировать в бетоносмеситель через дозатор химических добавок или через дозатор воды, при этом следует снизить расход воды затворения на 7-13%
Технические Характеристики:
Физико-химические показатели
| Сорт | Внешний вид |
Массовая доля формиата натрия, %, н/м |
Массовая доля формиата натрия, %, н/б |
||
| марка А марка Б марка С |
Кр слежив. порошок бел/сер цв. без постор. п. Доп-ся зел. от. |
95 92 90 |
1 3 6 |
||
| № партии |
Кол-во | Дата изготовл. 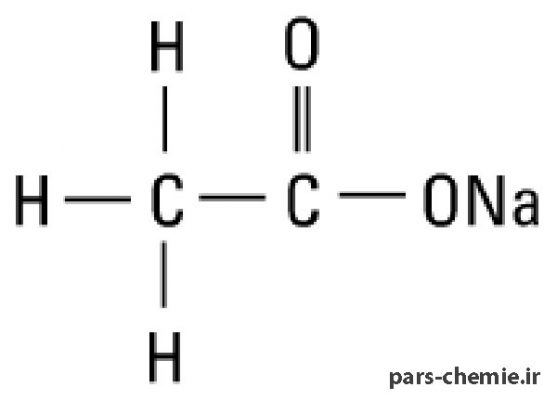 |
Результат | Результат | Резуль- тат |
| 471-11 | 109 | 31.08.11 | СООТ | 90 | 4 |
| 494-11 | 171 | 12.09.11 | СООТ | 90 | 4 |
| 507-11 | 680 | 18.09.11 | СООТ | 93 | 3 |
| 508-11 | 720 | 19.09.11 | СООТ | 92 | 4 |
| 509-11 | 720 | 19.09.11 | СООТ | 90 | 4 |
Заключение: Качество продукции соответствует ТУ 2432-011-00203803-98 с изм. 1,2
Для марки Б — 17 Т
Для марки С — 43 Т
Возможно Вас Заинтересует:
- Гипохлорит кальция 45%
- Кислота сульфаминовая
- Сода каустическая ТР (Натр едкий) Китай
- Кальций хлористый БСК
- Сода кальцинированная марка Б
- Полиэлектролит ВПК — 402
- Молочная кислота 80% (Lactic Acid)
- Кислота соляная ХЧ
- Сода пищевая (Бикарбонат натрия)
- Гипохлорит натрия
- Натр едкий ЧДА
- Тринатрийфосфат ГОСТ 201-76
- Сода каустическая ТР (Натр едкий) Иран
- Сода каустическая ТР (Натр едкий) АО "БСК"
- Лаурилсульфат натрия
- Поливинилхлорид суспензионный
- Триполифосфат натрия
Натрий муравьиновокислый позволяет проводить бетонирование при минусовых температурах
Натрий муравьинокислый — органическое соединение, натриевая соль муравьиной кислоты. Его называют также формиатом натрия, добавкой Е237. Формула — НСООNa. Производства формиата натрия как основного продукта не существует. Реактив получают в качестве побочного продукта при синтезе пентаэритрита.
Его называют также формиатом натрия, добавкой Е237. Формула — НСООNa. Производства формиата натрия как основного продукта не существует. Реактив получают в качестве побочного продукта при синтезе пентаэритрита.
Встречается в природе в естественном виде — в соках некоторых растений, в организме животных.
Свойства
Порошкообразное кристаллическое вещество белого цвета. Возможен сероватый или зеленоватый оттенок. Водорастворим, гигроскопичен. Плохо растворяется в спиртах, совсем не растворяется в эфирах. Не горит, не ядовит. С точки зрения химии — восстановитель. Реагирует с кислотами и сильными окислителями.
| Перчатки химзащитные КЩС-2 (L) | Натрий муравьиновокислый (формиат) |
Меры предосторожности
Относится к 3-му классу опасности для человеческого организма. Пыль, пары, аэрозоли реактива вызывают раздражение верхних органов дыхания, слизистых глаз, открытой кожи.
Пожаро- и взрывобезопасен, но рядом с ним нельзя курить, использовать устройства с открытым пламенем. На рабочем месте сотрудникам следует использовать средства защиты: халат с длинными рукавами, респиратор, защитные очки и перчатки.
Хранят муравьинокислый натрий на сухих складах, в герметичных контейнерах или полиэтиленовых мешках, защищающих реактив от влаги воздуха.
Применение
- В строительной индустрии — добавка в морозостойкие бетоны, использующиеся для возведения различных конструкций и зданий. Улучшает пластичность бетонных растворов, ускоряет их затвердевание, увеличивает срок эксплуатации сооружения. Особенно востребован при заливке бетона при минусовых температурах воздуха, вплоть до -30 °С. Применение добавки экономически выгоднее использования тепло- или электрообогрева сооружения. К тому же, упрощается технологический процесс.
- В химпроме — сырье для получения муравьиной и щавелевой кислоты, гидросульфита натрия; восстановитель в органических синтезах; добавка в моющие средства; добавка в сильные неорганические кислоты для увеличения их рН.

- Добавка в противогололедные смеси, помогает снизить температуру замерзания раствора. Формиат натрия замедляет процесс коррозии металлических деталей машин и оборудования, уменьшает вредное воздействие смеси на окружающую среду.
- В кожевенном деле используется при подготовке кож к дублению — нейтрализует кислотность кож, оказывает дубильное воздействие, повышает итоговое качество кож.
- В тестильпроме — реактив для травления перед окрашиванием тканей.
- Используется при печатании обоев.
- В фармацевтике входит в состав дезинтоксикационного препарата «Медихронал» (снижает содержание в крови токсичных метаболитов этилового спирта).
- Консервант в косметических продуктах.
- В сельском хозяйстве — добавка в корма для животных, улучшает усвояемость корма.
- В гальванике — для регенерации фосфатного электролита родирования; для приготовления электролита для химического никелирования.
- На предприятиях нефтепереработки.
- В качестве пищевой добавки Е237 в настоящее время запрещен в РФ, ЕС, США и многих других странах.
 Еще недавно применялся как консервант в безалкогольных напитках, как заменитель соли в диетических продуктах, маринадах.
Еще недавно применялся как консервант в безалкогольных напитках, как заменитель соли в диетических продуктах, маринадах.
Муравьиная кислота — Sciencemadness Wiki
Муравьиная кислота или метановая кислота — органическое соединение с химической формулой HCOOH и простейшая карбоновая кислота.
Содержание
- 1 Свойства
- 1.1 Химическая
- 1.2 Физический
- 2 Наличие
- 3 Подготовка
- 4 проекта
- 5 Обращение
- 5.1 Безопасность
- 5.2 Хранение
- 5.3 Утилизация
- 6 Каталожные номера
- 6.1 Соответствующие темы Sciencemadness
Свойства
Химический
Муравьиная кислота легко дегидратируется концентрированной серной кислотой до монооксида углерода и часто используется в лаборатории как удобный и хранимый источник газа.
- HCOOH + H 2 SO 4 → CO + H 2 O + H 2 SO 4
Как и другие карбоновые кислоты, муравьиная кислота легко этерифицируется первичными спиртами, часто образуя приятно пахнущие соединения, такие как метилформиат. Поскольку это сильная кислота, этерификации муравьиной кислотой обычно не требуют кислотного катализатора.
Поскольку это сильная кислота, этерификации муравьиной кислотой обычно не требуют кислотного катализатора.
В органической химии муравьиная кислота используется для введения формильной группы.
Физический
Муравьиная кислота представляет собой прозрачную жидкость с сильно раздражающим резким запахом, вызывающую болезненные ощущения при укусах многих муравьев. Его точка кипения почти такая же, как у воды (100,8 ° C), хотя он образует азеотроп 22,4% муравьиной кислоты с водой, которая вместо этого кипит при 107,3 ° C.
Поскольку муравьиная кислота медленно разлагается при кипячении, перегонку следует проводить при низкой температуре и почти в вакууме (25 °C при 40 мм рт. ст.). [1]
Доступность
Хотя муравьиная кислота обычно не встречается в качестве потребительского товара, ее можно купить в Интернете по относительно низкой цене, как правило, в смеси с 5-10% воды. Хороший поставщик — Дуда Дизель.
Муравьиную кислоту также можно приобрести в пчеловодческих магазинах в концентрации 60-85%. Используется для лечения варроаза.
Используется для лечения варроаза.
Подготовка
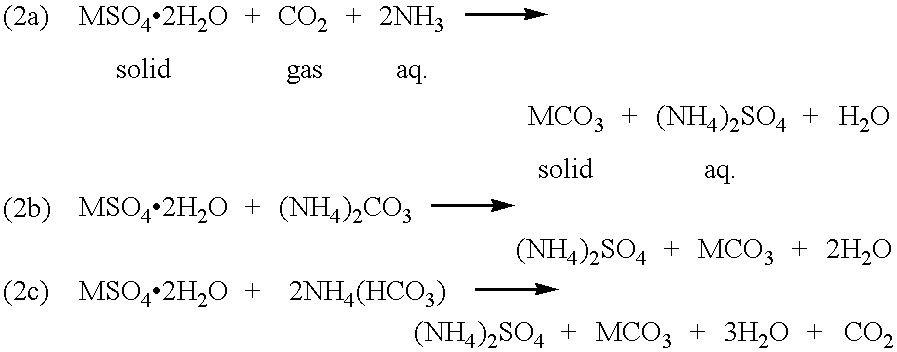
Водная муравьиная кислота может быть перегнана из смеси безводного глицерина и щавелевой кислоты с образованием двуокиси углерода в качестве побочного продукта. Его также можно получить путем подкисления формиата натрия разбавленной серной или фосфорной кислотой с получением муравьиной кислоты в растворе, который затем можно перегнать. Использование концентрированной серной кислоты или чрезмерное нагревание приведет к образованию угарного газа и потенциально может создать очень опасную ситуацию.
Проекты
- Получение сложных эфиров формиата
- Получение монооксида углерода для реакций
- Синтез муравьиного ангидрида (стабильный только в виде раствора в диэтиловом эфире)
Обращение
Безопасность
Концентрированные растворы муравьиной кислоты вызывают коррозию кожи человека, а также носа, рта и глаз, а также медленно разлагаются с образованием воды и углерода монооксид, который может вызвать взрыв из-за повышения давления в герметичном контейнере. Добавление обезвоживающего агента также приведет к образованию большого количества угарного газа, смертельного газа, который невозможно обнаружить с помощью органов чувств человека. Муравьиная кислота по своей природе не очень токсична при попадании внутрь, хотя длительное воздействие ее любыми способами может вызвать хронические телесные последствия. Особенно важно, чтобы муравьиная кислота не попадала в глаза, так как она легко повреждает зрительный нерв и может вызвать необратимую слепоту.
Добавление обезвоживающего агента также приведет к образованию большого количества угарного газа, смертельного газа, который невозможно обнаружить с помощью органов чувств человека. Муравьиная кислота по своей природе не очень токсична при попадании внутрь, хотя длительное воздействие ее любыми способами может вызвать хронические телесные последствия. Особенно важно, чтобы муравьиная кислота не попадала в глаза, так как она легко повреждает зрительный нерв и может вызвать необратимую слепоту.
Хранение
Муравьиную кислоту следует хранить в закрытых бутылях вдали от источников тепла. Держите его подальше от жилых помещений, так как со временем он медленно выделяет угарный газ.
Утилизация
Муравьиная кислота должна быть нейтрализована перед утилизацией. Это можно сделать, разбавив кислоту, а затем медленно добавляя ее в водный раствор основания. как карбонат натрия или бикарбонат натрия.
Ссылки
- ↑ Очистка лабораторных химикатов (пятое издание), Уилфред Л.
 Ф. Армарего и Кристина Ли Лин Чай, 2003 г.
Ф. Армарего и Кристина Ли Лин Чай, 2003 г.
Соответствующие темы Sciencemadness
- Создание муравьиной кислоты
- Муравьиная кислота
- Обращение с муравьиной кислотой? Сила по сравнению с другими кислотами?
- Муравьиная кислота, производство/закупка
- Муравьиная кислота Доступно средство для удаления накипи с муравьиной кислотой
- .
- Топливный элемент с муравьиной кислотой
- Муравьиная кислота от Esy Off Bam
- Сушка муравьиной кислоты молекулярными ситами – риск угарного газа?
Глицерин — Sciencemadness Wiki
Глицерин , альтернативно пишется глицерин или глицерин , представляет собой простой сахарный спирт, иногда используемый в качестве растворителя. Это полиол, состоящий из молекулы пропана с одним водородом на каждом из атомов углерода, замещенным гидроксильной группой.
Глицерин иногда используется в качестве лабораторного растворителя, хотя это затруднено из-за его высокой вязкости. Он также используется в производстве известного взрывчатого нитроглицерина.
Он также используется в производстве известного взрывчатого нитроглицерина.
Содержание
- 1 Свойства
- 1.1 Химическая
- 1.2 Физический
- 2 Наличие
- 3 Подготовка
- 4 проекта
- 5 Обращение
- 5.1 Безопасность
- 5.2 Хранение
- 5.3 Утилизация
- 6 Каталожные номера
- 6.1 Соответствующие темы Sciencemadness
Свойства
Химический
Глицерин имеет несколько нишевых применений в бытовой химии. Смесь глицерина и щавелевой кислоты можно перегнать для получения муравьиной кислоты. Эта реакция протекает в несколько стадий при температуре выше 100°С.
При нагревании глицерина до 280 °C он разлагается на акролеин:
- (CH 2 OH) 2 CHOH → CH 2 =CHCHO + 2 H 2 O
Возможно, наиболее известно, что он может быть азотирован с использованием ледяной азотной кислоты и азотной кислоты. нитроглицерин, чувствительная жидкая взрывчатка, используемая для изготовления динамита.
нитроглицерин, чувствительная жидкая взрывчатка, используемая для изготовления динамита.
Может также использоваться в качестве инертного растворителя для получения растительных экстрактов или проведения органических реакций.
Физический
Глицерин представляет собой бесцветную, вязкую жидкость без запаха при комнатной температуре с мягким сладким вкусом, похожим на искусственные подсластители. Он растворим в воде, но имеет ограниченную растворимость в большинстве органических растворителей, таких как ацетон, хлороформ и диэтиловый эфир. Он гигроскопичен.
Доступность
Глицерин можно найти во многих аптеках и продуктовых магазинах, где он используется в качестве «защитного средства для кожи». Как и многие другие медицинские товары и товары для здоровья, он продается с очень высокой наценкой, а это означает, что покупка глицерина в Интернете у определенных оптовиков на самом деле намного дешевле.
Препарат
Глицерин получают путем гидролиза или омыления растительных и животных жиров с использованием сильного основания, такого как гидроксид натрия.


 Еще недавно применялся как консервант в безалкогольных напитках, как заменитель соли в диетических продуктах, маринадах.
Еще недавно применялся как консервант в безалкогольных напитках, как заменитель соли в диетических продуктах, маринадах. Ф. Армарего и Кристина Ли Лин Чай, 2003 г.
Ф. Армарего и Кристина Ли Лин Чай, 2003 г.