Дибутиловый эфир — Справочник химика 21
из «Практикум по органическому синтезу Издание 3»
Формула СНз (СНа) 2—СНг—О—СНг— (СНг) г—СНз. [c.142]Серная кислота (d = 1,84) 7 мл Форштосс двурогий. [c.142]
Едкий натр, 3 н. раствор 200 мл Термометр. [c.142]
Хлористый кальций Холодильник Либиха. . [c.142]
Металлический натрий Воронка капельная. [c.142]
В круглодонную колбу прибора 1 вносят 62 мл бутилового спирта и при перемешивании приливают 7 мл концентрированной серной кислоты. Смесь спирта и кислоты осторожно нагревают через асбестовую сетку, следя за тем, чтобы температура отходящих паров не превышала 100—101 °С (при нарушении температурного режима могут образоваться бутилен и продукты его полимеризации, обугливания и восстановления серной кислоты до SO2). Происходит медленная отгонка дистиллята. Время от времени дистиллят отделяют от воды и переносят в капельную воронку, из которой вводят его по каплям обратно в реакционную колбу. Воду сливают в мерный цилиндр. После 3—4 ч, когда отгонится 10 мл воды, отделяют дистиллят от воды, вносят его обратно в колбу, кипятят еще 15—20 мин, а затем прекращают нагревание. [c.143]
Высушенный эфирный слой отфильтровывают и перегоняют из круглодонной колбы емкостью 110 мл с дефлегматором, собирая погон до 135 °С. Затем остаток в колбе охлаждают, вносят туда кусочек металлического натрия [защитные очки ) и перегоняют дибутиловый эфир, собирая его в пределах 140—145 °С (не перегонять досуха ввиду опасности взрыва ). [c.143]
Выход дибутилового эфира 25 г. [c.143]
Дибутиловый эфир — бесцветная жидкость мол. вес 130,22 т. кип. 141,97 °С т. пл. —95,37 °С df = 0,7688 1,3992. [c.143]
Применяется как растворитель, используется в синтезе Гриньяра. При длительном хранении дибутилового эфира образуются взрывчатые перекиси, в связи с чем перед употреблением берут пробу на их содержание. [c.143]
Вернуться к основной статье
chem21.info
Исследования закрепления органических соединений (октан, октанол-1, дибутиловый эфир) на поверхности золота.
3.1. Октан: молекулярная формула – С8Н18, структурная формула — СН3-(СН2)6-СН3, дипольный момент μ=0. Бесцветная жидкость со слабым запахом, температура плавления – 56,795° С, температура кипения – 125,665° С, он легче воды и в ней не растворяется. Октан является типичным насыщенным углеводородом с открытой углеродной цепью, в которой все атомы углерода соединены друг с другом простыми
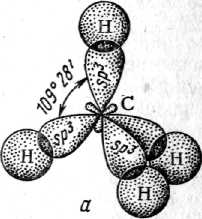
Рис. 6. sp3-гибридизация метана
Химические свойства:
В октане все атомы связаны между собой прочной ковалентной связью. Поэтому при обычных условиях октан, как и все алканы, проявляет чрезвычайно высокую химическую инертность: не вступает в реакции присоединения, не взаимодействует с кислотами и щелочами, сильными окислителями, активными металлами. Основные химические превращения октана будут происходить только при сообщении ему достаточно высокой энергии за счет нагревания, ультрафиолетового облучения и в присутствии катализатора.
1.Радикальное нитрование (реакция Коновалова):
СН3-СН2-СН2-СН2-СН2-СН2-СН2-СН3 + НNО3 =t СН3-СН2-СН2-СН2-СН2-СН-СН3 + Н2О
Октан 2-нитрооктан NО22. Крекинг – радикальный разрыв связей С – С. Протекает при нагревании и в присутствии катализаторов:
С8Н18 = С4Н10 + С4Н8
Бутан Бутилен
3. Окисление. При поджигании на воздухе октан будет гореть с выделением большого количества тепла:
2C8H18 + 25О2 = 16СО2 + 18Н2О
4. Сульфохлорирование – промышленный способ получения сульфокислот:
5. Каталитический риформинг – включает сложные процессы, такме как изомеризация, циклизация, дегидрирование, ароматизация алканов, которые приводят к перестройке углеродного скелета:
СН3-СН2-СН2-СН2-СН2-СН2-СН2-СН3 → СН3-СН2-СН2-СН2-СН2-СН-СН3 2-метилгептан
н-октан
СН3
Данная реакция протекает в присутствии катализатора Al2O3 при температуре 100° С
3.2. Октанол-1(октиловый спирт): молекулярная формула – С8Н17ОН, структурная формула – СН3-(СН2)6-СН2-ОН. Бесцветная жидкость с ароматным запахом. Температура кипения – 195,2° С, температура плавления – 16,3 С, температурные пределы воспламенения 74- 142°С. Октанол-1 является предельным одноатомным спиртом. Атомы углерода находятся в состоянии sp 3 гибридизации.
Рис. 7. Модели молекулы этилового спирта
Химические свойства: октанол-1 – это химически активное соединение, вступающее в реакции с разрывом связи R – O – H или R – OH. Разрыв происходит по ионному механизму с образованием органических катионов и анионов.
1. Реакции с щелочными металлами:
2С8Н17-ОН + 2Na = 2C8H17-ONa + H2;
2. Горение:
C8H17OH + 12О2 = 8СО2 + 9Н2О
3. Галогенирование:
C8H17OH + HBr = C8H17Br + H2O
4. Дегидратация (потеря воды):
C8H17OH → С4
Октанол-1 можно использовать в качестве пенообразователя или гетерополярного собирателя. Главным структурным элементом определяющим адсорбционные свойства у октилового спирта является функциональная группа –ОН. В этой молекуле наиболее электроотрицателен атом кислорода, поэтому связь О–Н сильно поляризована. Пара электронов смещается к кислороду, который несет частично отрицательный заряд δ- (рис4). В то же время в радикалах электронных пар связи С–Н частично смещены атомы углерода и под их влиянием смещается пара электронов. Это, в свою очередь, несколько уменьшает поляризацию связей ОН.
3.3 Дибутиловый эфир (С4Н9 – О – С4Н9) — простой эфир. Простые эфиры – это органические вещества, молекулы которых состоят из углеводородных радикалов, соединенных через атом кислорода: R ’– О – R’’, где R’ и R’’ – радикалы, которые могут быть различными и одинаковыми.
Название простых эфиров обычно связано с названием углеродных радикалов, соединенных с кислородом.
Дибутиловый эфир подвижная, крайне огнеопасная бесцветная жидкость с сильным характерным запахом. Температура кипения – 141,97°С, температура плавления – 95,37° С. В воде при температуре 17° С растворяется менее 0,01 %
Химические свойства: Простые эфиры – довольно инертные вещества. В отличие от сложных эфиров они не гидролизуются. На холоде простые эфиры не взаимодействуют с металлическим натрием и большинством разбавленных кислот. Однако концентрированные кислоты (Н2SO4;НI) даже на холоде разлагают эти эфиры, а металлический натрий при нагревании их расширяет:
С4Н9 – О – С4Н9 + Н2SO4 = С4
Дибутилсульфат
С4Н9 – О – С4Н9 + НI = С4Н9ОН + С4Н9I
С4Н9 – О – С4Н9 + 2Na =t С4Н9ОNa + С4Н9Na
бутилнатрий
Простые эфиры в природе не встречаются, их получают синтетическим путем. Дегидратация спиртов под влиянием минеральных кислот:
Н2SO4
С4Н9ОН + С4Н9ОН С4Н9 – О – С4Н9 — Дибутиловый эфир
– Н2О
Очень ограничено применяют как растворитель, используют также в синтезе гриньяра. Преимущества дибутилового эфира по сравнению с диэтиловым эфиром является меньшая летучесть. При длительном хранении образуют перекиси, в связи, с чем перед применением берут пробу на содержание этих примесей, которые вследствие устраняются встряхиванием с растворами солей двухвалентного железа или с раствором сульфата натрия.
По классификации А. В. Киселева дибутиловый эфир относится к группе В адсорбата.
Дибутиловый эфир можно является также, как и октанол-1 очень эффективным пенообразователем. Главным структурным элементом определяющим адсорбционные свойства у дибутилового эфира является функциональная группа – О –. В этой молекуле наиболее электроотрицателен атом кислорода, поэтому связь –О– с углеводородными радикалами сильно поляризована. Пара электронов смещается к кислороду, который несет частично отрицательный заряд δ- (рис4). В то же время в радикалах электронных пар связи С–Н частично смещены атомы углерода и под их влиянием смещается пара электронов в связи С — О.
ЗАКЛЮЧЕНИЕ
В данной курсовой работе было подробно рассмотрено золото, а также флотационные реагенты, применяемые в процессе флотационного извлечения этого благородного металла. Было установлено, что из всех известных реагентов-собирателей, наиболее распостранены для флотации золота – ксантогенаты и дитиофосфаты, а среди пенообразователей – сосновое масло, Т-66, Т-80, ОПСБ.
Без понимания адсорбционных свойств невозможен правильный и грамотный подбор реагентов. В процессе изучения адсорбционных способностей поверхности золота – выяснили, что адсорбция реагентов происходит путем химической адсорбции.
БИБЛИОГРАФИЧЕСКИЙ СПИСОК
1. Гумилевский С.А., Киршов В.М. Кристаллография и минералогия. Москва: «Высшая школа», 1972.
2. Виноградов А.Н. Металлы и минералы. Ростов-на-Дону: «Феникс», 2004.
3. Паддефет Р. Химия золота. Москва: «Мир», 1982.
4. Соболевский В.И. Благородные металлы. Золото. Москва: «Знание», 1970.
5. Хан. Г.А., Габриелова Л.И. Флотационные реагенты и их применение. Москва: «Недра», 1986.
6. Гольман А.М., Дмитриева И.Л. Флотационные реагенты. Москва: «Наука», 1986.
7. Дуденков С.В., Шафеев Э.Ш. Флотореагентщик. Москва: «Недра», 1968.
8. Полькин С.И. Обогащение руд и россыпей редких и благородных металлов. Москва: «Недра», 1987.
9. Абрамов А.А. Переработка, обогащение и комплексное использование полезных ископаемых. Т2. Москва: МГГУ, 2004.
10. Бочаров В.А., Игнаткина В.А. Технология обогащения полезных ископаемых. Т1, Т2. Москва: «Руда и металлы», 2007.
11. Горлова О.Е., Фадеева Н. В. Химия флотореагентов. Магнитогорск: МГТУ им. Г. И. Носова, 2007.
infopedia.su
Дибутиловый эфир — Большая Энциклопедия Нефти и Газа, статья, страница 1
Дибутиловый эфир
Cтраница 1
Дибутиловый эфир ( 1-бутоксибутан, бутиловый эфир) — бесцветная жидкость, смешивается с этиловым спиртом и ци-этиловым эфиром, в воде нерастворим. [1]
Дибутиловый эфир ( 1-бутоксибутан) — бесцветная жидкость, смешивается с этиловым спиртом, диэтиловым эфиром, в воде не растворяется. [2]
Дибутиловый эфир Р образовывает взрывчатые перекиси, особенно в безводном состоянии. [3]
Дибутиловый эфир О 8-дитиоугольной кислоты представляет собой маслянистое вещество ( пл. [4]
Дибутиловый эфир 4-нитросалициловойкислоты получался в тех же условиях, как и описанный выше Дибутиловый эфир 5-нитросалициловой кислоты. Из реакционной смеси продукт был выделен в виде коричневого масла с выходом 88 % от теоретического. [5]
Технический дибутиловый эфир подвергают тонкому фракционированию. Среднюю фракцию еще раз очищают повторным фракционированием. После этого дистиллят пропускают через колонку с окисью алюминия. [7]
Дибутиловый эфир метилфосфоновой кислоты используется как растворитель и пластификатор с повышенной огнестойкостью. [8]
Дибутиловый эфир метилфосфи-новой кислоты растворяется в спирте, эфире, бензоле, толуоле, не растворяется в воде. [9]
Дибутиловый эфир метилфосфоновой кислоты используется как растворитель и пластификатор с повышенной огнестойкостью. [10]
Дибутиловый эфир метилфосфи-новой кислоты растворяется в спирте, эфире, бензоле, толуоле, не растворяется в воде. [11]
Дибутиловый эфир декандикарбоновой кислоты применяется в качестве пластификатора для поливинилхлорида, придавая ему морозостойкость от — 60 до — 70 С. [12]
Свежеперегнанный дибутиловый эфир циклопентадиенилфосфинистой кислоты ( VII) представляет собой бесцветную жидкость, почти мгновенно темнеющую на воздухе. [13]
Система дибутиловый эфир — уксусная кислота — вода. [14]
Высушивают дибутиловый эфир хлоридом кальция. [15]
Страницы: 1 2 3 4
www.ngpedia.ru
Дибутиловый эфир фталевой кислоты — Справочник химика 21
Дибутилфталат (дибутиловый эфир фталевой кислоты) [c.173]Дибутиловый эфир фталевой кислоты, дибутилфталат, бутилфталат [c.13]
Дибутиловый эфир фталевой кислоты [c.162]
Дибутиловый эфир фталевой кислоты — не менее 99,5 [c.125]
Какие структурные формулы имеют следующие соединения а) фталевый ангидрид, б) фталимид калия, в) п-фталевая (терефталевая) кислота, г) диамид фталевой кислоты, д) дибутиловый эфир фталевой кислоты [c.194]
Аппаратура и реактивы фарфоровая чашка № 3 или № 4 (ГОСТ 9147—73) микробюретка (ГОСТ 20292—74) вместимостью 1—2 мл лопатка стеклянная (угол наклона 120°, диаметр 20 мм, толщина 2—8 мм) дибутиловый эфир фталевой кислоты (дибутилфталат) (ГОСТ 2102—67), ч. [c.189]
Из возможных изомеров дибутилового эфира фталевой кислоты очень широкое распространение получил -бутиловый эфир, который обычно и называется дибутилфталатом. Дибутилфталат играет очень большую роль в технике. Обычно, когда возникает необходимость в пластификаторе, применяют этот эфир. Он выпускается в продажу под очень большим числом торговых названий. Отдельные сорта дибутилфталата мало отличаются друг от друга. [c.747]
Дибутиловый эфир фталевой кислоты Г5,1,103 Д 1,188 О Дибу- тират стирилгликоля М3,226. О Октиловый эфир фталевой кис лоты Г8,590. о 2-Октиловый и о,ь-2-октиловый эфиры фталевой кислоты А4,7б М13,389 и 02,11,427. [c.222]
Так, например, при взаимодействии бензоилиодида с этилбензоатом образовывались этилиодид и бензойный ангидрид. Взаимодействие ацетилиодида с дибутиловым эфиром фталевой кислоты привело к получению бутилиодида, уксусного и фталевого ангидрида. [c.36]
Благодаря нерастворимости дибутилового эфира фталевой кислоты в воде, высокой температуре кипения и относительной химической инертности его очистка не представляет большого труда. Дибутилфталат можно освободить от спирта промыванием водой, а от кислот и монобутилфталата — обработкой разбавленным раствором соды. Тщательное фракционирование при пониженном давлении позволяет получить продукт, который, в пределах точности анализа методом омыления, содержит 100% дибутилфталата [1551]. [c.382]
Токсикология. Результаты опытов над крысами, в ходе которых дибутиловый эфир фталевой кислоты вводили в течение длительного времени в пищу этих животных как в больших дозах, так и в малых, свидетельствуют об очень низкой его токсичности [1702а]. [c.382]
Дибутиловый эфир фталевой кислоты 16h36U4. См. Дибутилфталат [c.794]
Диметиловые, диэтиловые и дибутиловые эфиры фталевой кислоты применяются для отпугивания комаров и гнуса (репеленты) [c.504]
В качестве рабочего вещества для насосов этого типа Бэрч [72] воспользовался высококипящими производными нефти и получил разрежение порядка 10 бара. Хайк-мэн и Сэнфорд [73] применили дибутиловый эфир фталевой кислоты и бутилбензоловый эфир той же кислоты. Геде рекомендует применение апьезонова масла , но считает, что ещё лучше рафинированное в течение нескольких дней на насосе машинное масло [74]. В настоящее время, в паромасляных диффузионных насосах приме- М [c.41]
Дибутилфталат, или дибутиловый эфир фталевой кислоты [СбН4(СООС4Нэ)2] — прозрачная бесцветная маслянистая жидкость со слабым запахом. Удельный вес 1,0465, температура кипения 340°. В воде растворяется плохо (0,04% при 25°), хорошо в органических растворителях (этиловом спирте, эфире, ацетоне, бензоле). [c.205]
Напишите структурные формулы следующих соединений а) кальциевая соль пропионовой кислоты, б) ангидрид изовалериановой кислоты, в) пропиловый, эфир валериановой кислоты, е) винилацетат, д) акрилонитрил, е) а-бромкротоно-вая кислота, ж) хлорангидрид бензойной кислоты, з) бензиловый эфир бензойной кислоты, и) амид глутаровой кислоты, к) дибутиловый эфир фталевой кислоты. [c.77]
При определении температур плавления веществ, плавящихся выше 150° С, в качестве нагревающей жидкости, кроме концентрированной серной кислоты, применяют фЪсфорную кислоту или раствор 4 вес. ч. сульфата калия в 6 вес. ч.> серной кислоты. Из органических жидкостей для нагревающей бани пригоден, например, дибутиловый эфир фталевой кислоты. Для нагревательных бань до температур выше 400° С рекомендуются силиконовые масла, например полисил-оксановые . Неоднократно рекомендованные сплавы солей, затвердевающие при комнатной температуре, оказались не очень удобными. Наиболее пригодной является смесь нитратов калия, натрия и рубидия, которая отличается прозрачностью и низкой температурой плавления. [c.810]
Дибутиловый эфир фталевой кислоты (дибутнлфталат) [c.1000]
chem21.info
Дибутиловый эфир, 99% | Himexenterprises
ДИБУТИЛОВЫЙ (БУТИЛОВЫЙ) ЭФИР
Dibutyl ether
Синонимы:
n-Butyl ether
Di-n-butyl ether
Di-n-butyl ether
n-Бутиловый эфир
Ди-n-бутиловый эфир
Ди-n-бутиловый эфир
Производитель: Acros
ДИБУТИЛОВЫЙ (БУТИЛОВЫЙ) ЭФИР | |
Каталожный номер | 14969 |
Квалификация | 99 % |
CAS | 142-96-1 |
Молекулярная формула | C8H18O |
Молярный вес | 130.23 |
Tкипения | 141 °С |
Плотность | 0.768 g/mL |
Фасовки | 1 л, 2.5 л |
Производитель: Merck
ДИБУТИЛОВЫЙ (БУТИЛОВЫЙ) ЭФИР | |
Каталожный номер | 802892 |
Квалификация | 99 % |
CAS | 142-96-1 |
Молекулярная формула | C8H18O |
Молярный вес | 130.23 |
Tкипения | 140-143 °С |
Плотность | 0.77 g/mL |
Фасовки | 100 мл, 1 л, 2.5 л |
Производитель: Aldrich
ДИБУТИЛОВЫЙ (БУТИЛОВЫЙ) ЭФИР | |
Каталожный номер | 271454 |
Квалификация | 99.3 % |
CAS | 142-96-1 |
Молекулярная формула | [CH3(CH2)3]2O |
Молярный вес | 130.23 |
Tкипения | |
Плотность | 0.764 g/mL |
Фасовки | 100 мл, 1 л, 2 л, 8 л |
ДИБУТИЛОВЫЙ (БУТИЛОВЫЙ) ЭФИР
Узнать ценуhimexenterprises.com
SammaS — Дибутилфталат (ДБФ) — Пластификаторы
Дибутилфталат (ДБФ)
Дибутилфталат (ДБФ) – дибутиловый эфир фталевой кислоты, химическая формула C16H22O4. Представляет собой бесцветную или слегка желтоватую прозрачную маслянистую жидкость со слабым фруктовым запахом. Малолетуч, почти не растворим в воде (не более 1% при 20oC), при обычных условиях устойчив к гидролизу и к воздействию кислорода. Хорошо растворим в этаноле, ацетоне и других органических растворителях.
Применяется в качестве пластификатора для композиций на основе поливинилхлорида, каучуков, эпоксидных смол, некоторых эфиров целлюлозы и как высококипящий растворитель (температура кипения 340oC, с разложением).
Этот пластификатор обычно применяют от 1 до 10% от массы смолы – чем больше пластификатора, тем более пластичное и упругое получается готовое изделие.
Следует учитывать тот момент, что при введении пластификатора дибутилфталат в эпоксидную смолу вязкость смолы снижается. Для повышения вязкости и улучшения тиксотропности эпоксидной смолы в неё можно добавить различные наполнители аэросил, мел, каолин, белую сажу.
При относительно невысокой цене ДБФ имеет одну технологическую особенность: он достаточно плохо реагирует с эпоксидной смолой, поэтому для достижения результата, смола с дибутилфталатом требует «варки», т.е. необходимо нагревать смесь на паровой бане до 50-60°С, при этом интенсивно перемешивать в течении 2-3 часов.
Работу с пластификатором проводить с использованием средств индивидуальной защиты кожи, глаз и органов дыхания. Предельно допустимая концентрация паров в воздухе рабочей зоны производственных помещений — 0,5 мг/м3. ДБФ является высокоопасным веществом, при несоблюдении техники безопасности обращения с веществом, может вызывать токсический гепатит. Хранить в герметично закрытой таре, обеспечивающей защиту от попадания влаги и воздействия прямых солнечных лучей.
sammas.ru
Дибутилфталат — Википедия (с комментариями)
Материал из Википедии — свободной энциклопедии
Дибутилфталат (дибутилбензол-1,2-дикарбонат) C6H4(COOC4H9)2 — дибутиловый эфир фталевой кислоты.
Свойства
Дибутилфталат представляет собой бесцветную маслянистую жидкость, tкип 340 °C (с разложением) (206 °C при 10 мм рт. ст.), хорошо растворимую в органических растворителях (этаноле, бензоле, ацетоне), малорастворим в воде (~0,1 % при 20 °C).
Проявляет химические свойства, характерные для сложных эфиров.
Синтез и свойства
Дибутилфталат синтезируют этерификацией н-бутилового спирта и фталевым ангидридом в присутствии кислотных катализаторов (бензолсульфокислота или другие сульфокислоты) при 120—140 °C.
Промышленное применение
Применяется как Пластификатор (ГОСТ 8728-88) композиций на основе поливинилхлорида, каучуков, эпоксидных смол, некоторых эфиров целлюлозы и как высококипящий растворитель. Входит в состав клея БФ-6.
Дибутилфталат применяется также в качестве репеллента (код P03BX03 в системе ВОЗ ATC (Anatomical Therapeutic Chemical Classification System))
Напишите отзыв о статье «Дибутилфталат»
Литература
- Даффа реакция — Меди// Химическая энциклопедия в 5 томах. — М.: Большая Российская Энциклопедия, 1990. — Т. 2. — 671 с.
Отрывок, характеризующий Дибутилфталат
Действия русского и французского войск во время обратной кампании от Москвы и до Немана подобны игре в жмурки, когда двум играющим завязывают глаза и один изредка звонит колокольчиком, чтобы уведомить о себе ловящего. Сначала тот, кого ловят, звонит, не боясь неприятеля, но когда ему приходится плохо, он, стараясь неслышно идти, убегает от своего врага и часто, думая убежать, идет прямо к нему в руки.Сначала наполеоновские войска еще давали о себе знать – это было в первый период движения по Калужской дороге, но потом, выбравшись на Смоленскую дорогу, они побежали, прижимая рукой язычок колокольчика, и часто, думая, что они уходят, набегали прямо на русских.
При быстроте бега французов и за ними русских и вследствие того изнурения лошадей, главное средство приблизительного узнавания положения, в котором находится неприятель, – разъезды кавалерии, – не существовало. Кроме того, вследствие частых и быстрых перемен положений обеих армий, сведения, какие и были, не могли поспевать вовремя. Если второго числа приходило известие о том, что армия неприятеля была там то первого числа, то третьего числа, когда можно было предпринять что нибудь, уже армия эта сделала два перехода и находилась совсем в другом положении.
Одна армия бежала, другая догоняла. От Смоленска французам предстояло много различных дорог; и, казалось бы, тут, простояв четыре дня, французы могли бы узнать, где неприятель, сообразить что нибудь выгодное и предпринять что нибудь новое. Но после четырехдневной остановки толпы их опять побежали не вправо, не влево, но, без всяких маневров и соображений, по старой, худшей дороге, на Красное и Оршу – по пробитому следу.
wiki-org.ru
