1
H
1,008
1s1
2,1
Бесцветный газ
t°пл=-259°C
t°кип=-253°C
2
He
4,0026
1s2
4,5
Бесцветный газ
t°кип=-269°C
3
Li
6,941
2s1
0,99
Мягкий серебристо-белый металл
t°пл=180°C
t°кип=1317°C
4
Be
9,0122
2s2
1,57
Светло-серый металл
t°пл=1278°C
t°кип=2970°C
5
B
10,811
2s2 2p1
2,04
Темно-коричневое аморфное вещество
t°пл=2300°C
t°кип=2550°C
6
C
12,011
2s2 2p2
2,55
Прозрачный (алмаз) / черный (графит) минерал
t°пл=3550°C
t°кип=4830°C
7
N
14,007
2s2 2p3
3,04
Бесцветный газ
t°пл=-210°C
t°кип=-196°C
8
O
15,999
2s2 2p4
3,44
Бесцветный газ
t°пл=-218°C
t°кип=-183°C
9
F
18,998
2s2 2p5
3,98
Бледно-желтый газ
t°пл=-220°C
t°кип=-188°C
10
Ne
20,180
2s2 2p6
4,4
Бесцветный газ
t°пл=-249°C
t°кип=-246°C
11
Na
22,990
3s1
0,98
Мягкий серебристо-белый металл
t°пл=98°C
t° кип=892°C
12
Mg
24,305
3s2
1,31
Серебристо-белый металл
t°пл=649°C
t°кип=1107°C
13
Al
26,982
3s2 3p1
1,61
Серебристо-белый металл
t°пл=660°C
t°кип=2467°C
14
Si
28,086
3s2 3p2
1,9
Коричневый порошок / минерал
t°пл=1410°C
t°кип=2355°C
15
P
30,974
3s2 3p3
2,2
Белый минерал / красный порошок
t°пл=44°C
t°кип=280°C
16
S
32,065
3s2 3p4
2,58
Светло-желтый порошок
t°пл=113°C
t°кип=445°C
17
Cl
35,453
3s2 3p5
3,16
Желтовато-зеленый газ
t°пл=-101°C
t°кип=-35°C
18
Ar
39,948
3s2 3p6
4,3
Бесцветный газ
t°пл=-189°C
t°кип=-186°C
19
K
39,098
4s1
0,82
Мягкий серебристо-белый металл
t°пл=64°C
t°кип=774°C
20
Ca
40,078
4s2
1,0
Серебристо-белый металл
t°пл=839°C
t°кип=1487°C
21
Sc
44,956
3d1 4s2
1,36
Серебристый металл с желтым отливом
t°пл=1539°C
t°кип=2832°C
22
Ti
47,867
3d2 4s2
1,54
Серебристо-белый металл
t°пл=1660°C
t°кип=3260°C
23
V
50,942
3d3 4s2
1,63
Серебристо-белый металл
t°пл=1890°C
t°кип=3380°C
24
Cr
51,996
3d5 4s1
1,66
Голубовато-белый металл
t°пл=1857°C
t°кип=2482°C
25
Mn
54,938
3d5 4s2
1,55
Хрупкий серебристо-белый металл
t°пл=1244°C
t°кип=2097°C
26
Fe
55,845
3d6 4s2
1,83
Серебристо-белый металл
t°пл=1535°C
t°кип=2750°C
27
Co
58,933
3d7 4s2
1,88
Серебристо-белый металл
t°пл=1495°C
t°
28
Ni
58,693
3d8 4s2
1,91
Серебристо-белый металл
t°пл=1453°C
t°кип=2732°C
29
Cu
63,546
3d10 4s1
1,9
Золотисто-розовый металл
t°пл=1084°C
t°кип=2595°C
30
Zn
65,409
3d10 4s2
1,65
Голубовато-белый металл
t°пл=420°C
t°кип=907°C
31
Ga
69,723
4s2 4p1
1,81
Белый металл с голубоватым оттенком
t°пл=30°C
t°кип=2403°C
32
Ge
72,64
4s2 4p2
2,0
Светло-серый полуметалл
t°пл=937°C
t°кип=2830°C
33
As
74,922
4s2 4p3
2,18
Зеленоватый полуметалл
t°субл=613°C
(сублимация)
34
Se
78,96
4s2 4p4
2,55
Хрупкий черный минерал
t°пл=217°C
t°кип=685°C
35
Br
79,904
4s2 4p5
2,96
Красно-бурая едкая жидкость
t°пл=-7°C
t°кип=59°C
36
Kr
83,798
4s2 4p6
3,0
Бесцветный газ
t°пл=-157°C
t°кип=-152°C
37
Rb
85,468
5s1
0,82
Серебристо-белый металл
t°пл=39°C
t°кип=688°C
38
Sr
87,62
5s2
0,95
Серебристо-белый металл
t°кип=1384°C
39
Y
88,906
4d1 5s2
1,22
Серебристо-белый металл
t°пл=1523°C
t°кип=3337°C
40
Zr
91,224
4d2 5s2
1,33
Серебристо-белый металл
t°пл=1852°C
t°кип=4377°C
41
Nb
92,906
4d4 5s1
1,6
Блестящий серебристый металл
t°пл=2468°C
t°кип=4927°C
42
Mo
95,94
4d5 5s1
2,16
Блестящий серебристый металл
t°пл=2617°C
t°кип=5560°C
43
Tc
98,906
4d6 5s1
1,9
Синтетический радиоактивный металл
t°пл=2172°C
t° кип=5030°C
44
Ru
101,07
4d7 5s1
2,2
Серебристо-белый металл
t°пл=2310°C
t°кип=3900°C
45
Rh
102,91
4d8 5s1
2,28
Серебристо-белый металл
t°пл=1966°C
t°кип=3727°C
46
Pd
106,42
4d10
2,2
Мягкий серебристо-белый металл
t°пл=1552°C
t°кип=3140°C
47
Ag
107,87
4d10 5s1
1,93
Серебристо-белый металл
t°пл=962°C
t°кип=2212°C
48
Cd
112,41
4d10 5s2
1,69
Серебристо-серый металл
t°пл=321°C
t°кип=765°C
49
In
114,82
5s2 5p1
1,78
Мягкий серебристо-белый металл
t°пл=156°C
t°кип=2080°C
50
Sn
118,71
5s2 5p2
1,96
Мягкий серебристо-белый металл
t°пл=232°C
t°кип=2270°C
51
Sb
121,76
5s2 5p3
2,05
Серебристо-белый полуметалл
t°пл=631°C
t°кип=1750°C
52
Te
127,60
5s2 5p4
2,1
Серебристый блестящий неметалл
t°пл=450°C
t°кип=990°C
53
I
126,90
5s2 5p5
2,66
Черно-серые кристаллы
t°пл=114°C
t°кип=184°C
54
Xe
131,29
5s2 5p6
2,6
Бесцветный газ
t°пл=-112°C
t°кип=-107°C
55
Cs
132,91
6s1
0,79
Мягкий серебристо-желтый металл
t°пл=28°C
t°кип=690°C
56
Ba
137,33
6s2
0,89
Серебристо-белый металл
t°пл=725°C
t°кип=1640°C
57
La
138,91
5d1 6s2
1,1
Серебристый металл
t°пл=920°C
t°кип=3454°C
58
Ce
140,12
f-элемент
Серебристый металл
t°пл=798°C
t°кип=3257°C
59
Pr
140,91
f-элемент
Серебристый металл
t°пл=931°C
t°кип=3212°C
60
Nd
144,24
f-элемент
Серебристый металл
t°пл=1010°C
t°кип=3127°C
61
Pm
146,92
f-элемент
Светло-серый радиоактивный металл
t°пл=1080°C
t°кип=2730°C
62
Sm
150,36
f-элемент
Серебристый металл
t°пл=1072°C
t°кип=1778°C
63
Eu
151,96
f-элемент
Серебристый металл
t°пл=822°C
t°кип=1597°C
64
Gd
157,25
f-элемент
Серебристый металл
t°пл=1311°C
t°кип=3233°C
65
Tb
158,93
f-элемент
Серебристый металл
t°пл=1360°C
t°кип=3041°C
66
Dy
162,50
f-элемент
Серебристый металл
t°пл=1409°C
t°кип=2335°C
67
Ho
164,93
f-элемент
Серебристый металл
t°пл=1470°C
t°кип=2720°C
68
Er
167,26
f-элемент
Серебристый металл
t°пл=1522°C
t°кип=2510°C
69
Tm
168,93
f-элемент
Серебристый металл
t°пл=1545°C
t°кип=1727°C
70
Yb
173,04
f-элемент
Серебристый металл
t°пл=824°C
t°кип=1193°C
71
Lu
174,96
f-элемент
Серебристый металл
t°пл=1656°C
t°кип=3315°C
72
Hf
178,49
5d2 6s2
Серебристый металл
t°пл=2150°C
t°кип=5400°C
73
Ta
180,95
5d3 6s2
Серый металл
t°пл=2996°C
t°кип=5425°C
74
W
183,84
5d4 6s2
2,36
Серый металл
t°пл=3407°C
t°кип=5927°C
75
Re
186,21
5d5 6s2
Серебристо-белый металл
t°пл=3180°C
t°кип=5873°C
76
Os
190,23
5d6 6s2
Серебристый металл с голубоватым оттенком
t°пл=3045°C
t°кип=5027°C
77
Ir
192,22
5d7 6s2
Серебристый металл
t°пл=2410°C
t°кип=4130°C
78
Pt
195,08
5d9 6s1
2,28
Мягкий серебристо-белый металл
t°пл=1772°C
t°кип=3827°C
79
Au
196,97
5d10 6s1
2,54
Мягкий блестящий желтый металл
t°пл=1064°C
t°кип=2940°C
80
Hg
200,59
5d10 6s2
2,0
Жидкий серебристо-белый металл
t°пл=-39°C
t°кип=357°C
81
Tl
204,38
6s2 6p1
Серебристый металл
t°пл=304°C
t°кип=1457°C
82
Pb
207,2
6s2 6p2
2,33
Серый металл с синеватым оттенком
t°пл=328°C
t°кип=1740°C
83
Bi
208,98
6s2 6p3
Блестящий серебристый металл
t°пл=271°C
t°кип=1560°C
84
Po
208,98
6s2 6p4
Мягкий серебристо-белый металл
t°пл=254°C
t°кип=962°C
85
At
209,98
6s2 6p5
2,2
Нестабильный элемент, отсутствует в природе
t°пл=302°C
t°кип=337°C
86
Rn
222,02
6s2 6p6
2,2
Радиоактивный газ
t°пл=-71°C
t°кип=-62°C
87
Fr
223,02
7s1
0,7
Нестабильный элемент, отсутствует в природе
t°пл=27°C
t°кип=677°C
88
Ra
226,03
7s2
0,9
Серебристо-белый радиоактивный металл
t°пл=700°C
t°кип=1140°C
89
Ac
227,03
6d1 7s2
1,1
Серебристо-белый радиоактивный металл
t°пл=1047°C
t°кип=3197°C
90
Th
232,04
f-элемент
Серый мягкий металл
91
Pa
231,04
f-элемент
Серебристо-белый радиоактивный металл
92
U
238,03
f-элемент
1,38
Серебристо-белый металл
t°пл=1132°C
t°кип=3818°C
93
Np
237,05
f-элемент
Серебристо-белый радиоактивный металл
94
Pu
244,06
f-элемент
Серебристо-белый радиоактивный металл
95
Am
243,06
f-элемент
Серебристо-белый радиоактивный металл
96
Cm
247,07
f-элемент
Серебристо-белый радиоактивный металл
97
Bk
247,07
f-элемент
Серебристо-белый радиоактивный металл
98
Cf
251,08
f-элемент
Нестабильный элемент, отсутствует в природе
99
Es
252,08
f-элемент
Нестабильный элемент, отсутствует в природе
100
Fm
257,10
f-элемент
Нестабильный элемент, отсутствует в природе
101
Md
258,10
f-элемент
Нестабильный элемент, отсутствует в природе
102
No
259,10
f-элемент
Нестабильный элемент, отсутствует в природе
103
Lr
266
f-элемент
Нестабильный элемент, отсутствует в природе
104
Rf
267
6d2 7s2
Нестабильный элемент, отсутствует в природе
105
Db
268
6d3 7s2
Нестабильный элемент, отсутствует в природе
106
Sg
269
6d4 7s2
Нестабильный элемент, отсутствует в природе
107
Bh
270
6d5 7s2
Нестабильный элемент, отсутствует в природе
108
Hs
277
6d6 7s2
Нестабильный элемент, отсутствует в природе
109
Mt
278
6d7 7s2
Нестабильный элемент, отсутствует в природе
110
Ds
281
6d9 7s1
Нестабильный элемент, отсутствует в природе
Металлы
Неметаллы
Щелочные
Щелоч-зем
Благородные
Галогены
Халькогены
Полуметаллы
s-элементы
p-элементы
d-элементы
f-элементы
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
1
H
1,008
1s1
2,1
Бесцветный газ
t°пл=-259°C
t°кип=-253°C
2
He
4,0026
1s2
4,5
Бесцветный газ
t°кип=-269°C
3
Li
6,941
2s1
0,99
Мягкий серебристо-белый металл
t°пл=180°C
t°кип=1317°C
4
Be
9,0122
2s2
1,57
Светло-серый металл
t°пл=1278°C
t°кип=2970°C
5
B
10,811
2s2 2p1
2,04
Темно-коричневое аморфное вещество
t°пл=2300°C
t°кип=2550°C
6
C
12,011
2s2 2p2
2,55
Прозрачный (алмаз) / черный (графит) минерал
t°пл=3550°C
t°кип=4830°C
7
N
14,007
2s2 2p3
3,04
Бесцветный газ
t°пл=-210°C
t°кип=-196°C
8
O
15,999
2s2 2p4
3,44
Бесцветный газ
t°пл=-218°C
t°кип=-183°C
9
F
18,998
2s2 2p5
3,98
Бледно-желтый газ
t°пл=-220°C
t°кип=-188°C
10
Ne
20,180
2s2 2p6
4,4
Бесцветный газ
t°пл=-249°C
t°кип=-246°C
11
Na
22,990
3s1
0,98
Мягкий серебристо-белый металл
t°пл=98°C
t°кип=892°C
12
Mg
24,305
3s2
1,31
Серебристо-белый металл
t°пл=649°C
t°кип=1107°C
13
Al
26,982
3s2 3p1
1,61
Серебристо-белый металл
t°пл=660°C
t°кип=2467°C
14
Si
28,086
3s2 3p2
1,9
Коричневый порошок / минерал
t°пл=1410°C
t°кип=2355°C
15
P
30,974
3s2 3p3
2,2
Белый минерал / красный порошок
t°пл=44°C
t°кип=280°C
16
S
32,065
3s2 3p4
2,58
Светло-желтый порошок
t°пл=113°C
t°кип=445°C
17
Cl
35,453
3s2 3p5
3,16
Желтовато-зеленый газ
t°пл=-101°C
t°кип=-35°C
18
Ar
39,948
3s2 3p6
4,3
Бесцветный газ
t°пл=-189°C
t°кип=-186°C
19
K
39,098
4s1
0,82
Мягкий серебристо-белый металл
t°пл=64°C
t°кип=774°C
20
Ca
40,078
4s2
1,0
Серебристо-белый металл
t°пл=839°C
t°кип=1487°C
21
Sc
44,956
3d1 4s2
1,36
Серебристый металл с желтым отливом
t°пл=1539°C
t°кип=2832°C
22
Ti
47,867
3d2 4s2
1,54
Серебристо-белый металл
t°пл=1660°C
t°кип=3260°C
23
V
50,942
3d3 4s2
1,63
Серебристо-белый металл
t°пл=1890°C
t°кип=3380°C
24
Cr
51,996
3d5 4s1
1,66
Голубовато-белый металл
t°пл=1857°C
t°кип=2482°C
25
Mn
54,938
3d5 4s2
1,55
Хрупкий серебристо-белый металл
t°пл=1244°C
t°кип=2097°C
26
Fe
55,845
3d6 4s2
1,83
Серебристо-белый металл
t°пл=1535°C
t°кип=2750°C
27
Co
58,933
3d7 4s2
1,88
Серебристо-белый металл
t°пл=1495°C
t°кип=2870°C
28
Ni
58,693
3d8 4s2
1,91
Серебристо-белый металл
t°пл=1453°C
t°кип=2732°C
29
Cu
63,546
3d10 4s1
1,9
Золотисто-розовый металл
t°пл=1084°C
t°кип=2595°C
30
Zn
65,409
3d10 4s2
1,65
Голубовато-белый металл
t°пл=420°C
t°кип=907°C
31
Ga
69,723
4s2 4p1
1,81
Белый металл с голубоватым оттенком
t°пл=30°C
t°кип=2403°C
32
Ge
72,64
4s2 4p2
2,0
Светло-серый полуметалл
t°пл=937°C
t°кип=2830°C
33
As
74,922
4s2 4p3
2,18
Зеленоватый полуметалл
t°субл=613°C
(сублимация)
34
Se
78,96
4s2 4p4
2,55
Хрупкий черный минерал
t°пл=217°C
t°кип=685°C
35
Br
79,904
4s2 4p5
2,96
Красно-бурая едкая жидкость
t°пл=-7°C
t°кип=59°C
36
Kr
83,798
4s2 4p6
3,0
Бесцветный газ
t°пл=-157°C
t°кип=-152°C
37
Rb
85,468
5s1
0,82
Серебристо-белый металл
t°пл=39°C
t°кип=688°C
38
Sr
87,62
5s2
0,95
Серебристо-белый металл
t°пл=769°C
t°кип=1384°C
39
Y
88,906
4d1 5s2
1,22
Серебристо-белый металл
t°пл=1523°C
t°кип=3337°C
40
Zr
91,224
4d2 5s2
1,33
Серебристо-белый металл
t°пл=1852°C
t°кип=4377°C
41
Nb
92,906
4d4 5s1
1,6
Блестящий серебристый металл
t°пл=2468°C
t°кип=4927°C
42
Mo
95,94
4d5 5s1
2,16
Блестящий серебристый металл
t°пл=2617°C
t°кип=5560°C
43
Tc
98,906
4d6 5s1
1,9
Синтетический радиоактивный металл
t°пл=2172°C
t°кип=5030°C
44
Ru
101,07
4d7 5s1
2,2
Серебристо-белый металл
t°пл=2310°C
t°кип=3900°C
45
Rh
102,91
4d8 5s1
2,28
Серебристо-белый металл
t°пл=1966°C
t°кип=3727°C
46
Pd
106,42
4d10
2,2
Мягкий серебристо-белый металл
t°пл=1552°C
t°кип=3140°C
47
Ag
107,87
4d10 5s1
1,93
Серебристо-белый металл
t°пл=962°C
t°кип=2212°C
48
Cd
112,41
4d10 5s2
1,69
Серебристо-серый металл
t°пл=321°C
t°кип=765°C
49
In
114,82
5s2 5p1
1,78
Мягкий серебристо-белый металл
t°пл=156°C
t°кип=2080°C
50
Sn
118,71
5s2 5p2
1,96
Мягкий серебристо-белый металл
t°пл=232°C
t°кип=2270°C
51
Sb
121,76
5s2 5p3
2,05
Серебристо-белый полуметалл
t°пл=631°C
t°кип=1750°C
52
Te
127,60
5s2 5p4
2,1
Серебристый блестящий неметалл
t°пл=450°C
t°кип=990°C
53
I
126,90
5s2 5p5
2,66
Черно-серые кристаллы
t°пл=114°C
t°кип=184°C
54
Xe
131,29
5s2 5p6
2,6
Бесцветный газ
t°пл=-112°C
t°кип=-107°C
55
Cs
132,91
6s1
0,79
Мягкий серебристо-желтый металл
t°пл=28°C
t°кип=690°C
56
Ba
137,33
6s2
0,89
Серебристо-белый металл
t°пл=725°C
t°кип=1640°C
57
La
138,91
5d1 6s2
1,1
Серебристый металл
t°пл=920°C
t°кип=3454°C
58
Ce
140,12
f-элемент
Серебристый металл
t°пл=798°C
t°кип=3257°C
59
Pr
140,91
f-элемент
Серебристый металл
t°пл=931°C
t°кип=3212°C
60
Nd
144,24
f-элемент
Серебристый металл
t°пл=1010°C
t°кип=3127°C
61
Pm
146,92
f-элемент
Светло-серый радиоактивный металл
t°пл=1080°C
t°кип=2730°C
62
Sm
150,36
f-элемент
Серебристый металл
t°пл=1072°C
t°кип=1778°C
63
Eu
151,96
f-элемент
Серебристый металл
t°пл=822°C
t°кип=1597°C
64
Gd
157,25
f-элемент
Серебристый металл
t°пл=1311°C
t°кип=3233°C
65
Tb
158,93
f-элемент
Серебристый металл
t°пл=1360°C
t°кип=3041°C
66
Dy
162,50
f-элемент
Серебристый металл
t°пл=1409°C
t°кип=2335°C
67
Ho
164,93
f-элемент
Серебристый металл
t°пл=1470°C
t°кип=2720°C
68
Er
167,26
f-элемент
Серебристый металл
t°пл=1522°C
t°кип=2510°C
69
Tm
168,93
f-элемент
Серебристый металл
t°пл=1545°C
t°кип=1727°C
70
Yb
173,04
f-элемент
Серебристый металл
t°пл=824°C
t°кип=1193°C
71
Lu
174,96
f-элемент
Серебристый металл
t°пл=1656°C
t°кип=3315°C
72
Hf
178,49
5d2 6s2
Серебристый металл
t°пл=2150°C
t°кип=5400°C
73
Ta
180,95
5d3 6s2
Серый металл
t°пл=2996°C
t°кип=5425°C
74
W
183,84
5d4 6s2
2,36
Серый металл
t°пл=3407°C
t°кип=5927°C
75
Re
186,21
5d5 6s2
Серебристо-белый металл
t°пл=3180°C
t°кип=5873°C
76
Os
190,23
5d6 6s2
Серебристый металл с голубоватым оттенком
t°пл=3045°C
t°кип=5027°C
77
Ir
192,22
5d7 6s2
Серебристый металл
t°пл=2410°C
t°кип=4130°C
78
Pt
195,08
5d9 6s1
2,28
Мягкий серебристо-белый металл
t°пл=1772°C
t°кип=3827°C
79
Au
196,97
5d10 6s1
2,54
Мягкий блестящий желтый металл
t°пл=1064°C
t°кип=2940°C
80
Hg
200,59
5d10 6s2
2,0
Жидкий серебристо-белый металл
t°пл=-39°C
t°кип=357°C
81
Tl
204,38
6s2 6p1
Серебристый металл
t°пл=304°C
t°кип=1457°C
82
Pb
207,2
6s2 6p2
2,33
Серый металл с синеватым оттенком
t°пл=328°C
t°кип=1740°C
83
Bi
208,98
6s2 6p3
Блестящий серебристый металл
t°пл=271°C
t°кип=1560°C
84
Po
208,98
6s2 6p4
Мягкий серебристо-белый металл
t°пл=254°C
t°кип=962°C
85
At
209,98
6s2 6p5
2,2
Нестабильный элемент, отсутствует в природе
t°пл=302°C
t°кип=337°C
86
Rn
222,02
6s2 6p6
2,2
Радиоактивный газ
t°пл=-71°C
t°кип=-62°C
87
Fr
223,02
7s1
0,7
Нестабильный элемент, отсутствует в природе
t°пл=27°C
t°кип=677°C
88
Ra
226,03
7s2
0,9
Серебристо-белый радиоактивный металл
t°пл=700°C
t°кип=1140°C
89
Ac
227,03
6d1 7s2
1,1
Серебристо-белый радиоактивный металл
t°пл=1047°C
t°кип=3197°C
90
Th
232,04
f-элемент
Серый мягкий металл
91
Pa
231,04
f-элемент
Серебристо-белый радиоактивный металл
92
U
238,03
f-элемент
1,38
Серебристо-белый металл
t°пл=1132°C
t°кип=3818°C
93
Np
237,05
f-элемент
Серебристо-белый радиоактивный металл
94
Pu
244,06
f-элемент
Серебристо-белый радиоактивный металл
95
Am
243,06
f-элемент
Серебристо-белый радиоактивный металл
96
Cm
247,07
f-элемент
Серебристо-белый радиоактивный металл
97
Bk
247,07
f-элемент
Серебристо-белый радиоактивный металл
98
Cf
251,08
f-элемент
Нестабильный элемент, отсутствует в природе
99
Es
252,08
f-элемент
Нестабильный элемент, отсутствует в природе
100
Fm
257,10
f-элемент
Нестабильный элемент, отсутствует в природе
101
Md
258,10
f-элемент
Нестабильный элемент, отсутствует в природе
102
No
259,10
f-элемент
Нестабильный элемент, отсутствует в природе
103
Lr
266
f-элемент
Нестабильный элемент, отсутствует в природе
104
Rf
267
6d2 7s2
Нестабильный элемент, отсутствует в природе
105
Db
268
6d3 7s2
Нестабильный элемент, отсутствует в природе
106
Sg
269
6d4 7s2
Нестабильный элемент, отсутствует в природе
107
Bh
270
6d5 7s2
Нестабильный элемент, отсутствует в природе
108
Hs
277
6d6 7s2
Нестабильный элемент, отсутствует в природе
109
Mt
278
6d7 7s2
Нестабильный элемент, отсутствует в природе
110
Ds
281
6d9 7s1
Нестабильный элемент, отсутствует в природе
Металлы
Неметаллы
Щелочные
Щелоч-зем
Благородные
Галогены
Халькогены
Полуметаллы
s-элементы
p-элементы
d-элементы
f-элементы
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
Дибутиловый эфир — Справочник химика 21
из «Практикум по органическому синтезу Издание 3»
Формула СНз (СНа) 2—СНг—О—СНг— (СНг) г—СНз. [c.142]Серная кислота (d = 1,84) 7 мл Форштосс двурогий. [c.142]
Едкий натр, 3 н. раствор 200 мл Термометр. [c.142]
Хлористый кальций Холодильник Либиха. . [c.142]
Металлический натрий Воронка капельная. [c.142]
В круглодонную колбу прибора 1 вносят 62 мл бутилового спирта и при перемешивании приливают 7 мл концентрированной серной кислоты. Смесь спирта и кислоты осторожно нагревают через асбестовую сетку, следя за тем, чтобы температура отходящих паров не превышала 100—101 °С (при нарушении температурного режима могут образоваться бутилен и продукты его полимеризации, обугливания и восстановления серной кислоты до SO2). Происходит медленная отгонка дистиллята. Время от времени дистиллят отделяют от воды и переносят в капельную воронку, из которой вводят его по каплям обратно в реакционную колбу. Воду сливают в мерный цилиндр. После 3—4 ч, когда отгонится 10 мл воды, отделяют дистиллят от воды, вносят его обратно в колбу, кипятят еще 15—20 мин, а затем прекращают нагревание. [c.143]
Содержимое колбы охлаждают, при перемешивании и охлаждении вносят 30 мл 3 н. раствора едкого натра и переносят в делительную воронку. Промывание раствором щелочи ведут до тех пор, пока промывные воды не будут показывать щелочную реакцию. Затем эфирный слой промывают 30 мл воды и 30 мл насыщенного раствора хлористого кальция. Тщательно отделив эфирный слой в сухую склянку, сушат его хлористым кальцием. [c.143]
Высушенный эфирный слой отфильтровывают и перегоняют из круглодонной колбы емкостью 110 мл с дефлегматором, собирая погон до 135 °С. Затем остаток в колбе охлаждают, вносят туда кусочек металлического натрия [защитные очки ) и перегоняют дибутиловый эфир, собирая его в пределах 140—145 °С (не перегонять досуха ввиду опасности взрыва ). [c.143]
Выход дибутилового эфира 25 г. [c.143]
Дибутиловый эфир — бесцветная жидкость мол. вес 130,22 т. кип. 141,97 °С т. пл. —95,37 °С df = 0,7688 1,3992. [c.143]
Применяется как растворитель, используется в синтезе Гриньяра. При длительном хранении дибутилового эфира образуются взрывчатые перекиси, в связи с чем перед употреблением берут пробу на их содержание. [c.143]
Вернуться к основной статье
дибутиловый эфир — Dibutyl ether
 | |
| имена | |
|---|---|
| Предпочтительное название IUPAC | |
Другие имена
| |
| Идентификаторы | |
| 3D модель ( JSmol ) | |
| ChemSpider | |
| ИКГВ InfoCard | 100.005.069 |
| |
| свойства | |
| С 8 Н 18 О | |
| Молярная масса | 7002130231000000000 ♠130,231 г · моль -1 |
| Внешность | Бесцветная жидкость |
| запах | Фруктовый |
| плотность | 0,77 г / см 3 (20 ° С) |
| Температура плавления | -95 ° С (-139 ° F, 178 К) |
| Точка кипения | 141 ° С (286 ° F, 414 К) |
| 0,3 г / л | |
| 1,3992 | |
| вязкость | 0,741 сП (15 ° С) |
| Состав | |
| 1,18 D | |
| опасности | |
| точка возгорания | 25 ° С (77 ° F, 298 К) |
| 175 ° С (347 ° F, 448 К) | |
| Смертельная доза или концентрация ( LD , LC ): | |
| 7400 мг / кг (перорально, крыса) | |
| За исключением случаев, когда указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| ссылки Infobox | |
Дибутиловый эфир представляет собой химическое соединение , принадлежащее к эфирным семейству с молекулярной формулой С
8 Н
18 вывода. Это бесцветное, летучее и легковоспламеняющаяся жидкость и имеет специфический запах эфирный.
Жидкий дибутиловый эфир легче , чем вода. С другой стороны, пар тяжелее воздуха. Это не растворим в воде, но растворим в ацетоне и многих других органических растворителях. Благодаря этому свойству, дибутиловый эфир использует в качестве растворителя в различных химических реакциях и процессах. Так , например, фениллития являются коммерчески доступными в виде приблизительно 1,8 М раствор в дибутиловом эфире.
Из-за образования пероксидов, он должен быть защищен от тепла, света и воздуха.
Синтез
Дибутиловый эфир получают из дегидратации 1-бутанола с помощью серной кислоты в качестве катализатора и дегидратирующего агента:
- 2 С
4 Н
9 ОН→С
8 Н
18 О+Н
2 O
Промышленно, дибутиловый эфир может быть получен путем дегидратации 1-бутанола на окиси алюмини при температуре 300 ° С.
Реакции
Это соединение, как правило, устойчиво к окислению, восстановлению, и основанию. Сильные кислоты, такие как HI и HBr могут расщеплять этот эфир. В присутствии кислорода, дибутиловый эфир окисляется до перекиси или гидроперекиси.
Приложения
Рекомендации
<img src=»https://en.wikipedia.org//en.wikipedia.org/wiki/Special:CentralAutoLogin/start?type=1×1″ alt=»» title=»»>3.1. Октан: молекулярная формула – С8Н18, структурная формула — СН3-(СН2)6-СН3, дипольный момент μ=0. Бесцветная жидкость со слабым запахом, температура плавления – 56,795° С, температура кипения – 125,665° С, он легче воды и в ней не растворяется. Октан является типичным насыщенным углеводородом с открытой углеродной цепью, в которой все атомы углерода соединены друг с другом простыми G-связями и находятся в состоянии sp3 гибридизации, углы между связями 109,5°.
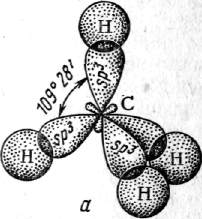
Рис. 6. sp3-гибридизация метана
Химические свойства:
В октане все атомы связаны между собой прочной ковалентной связью. Поэтому при обычных условиях октан, как и все алканы, проявляет чрезвычайно высокую химическую инертность: не вступает в реакции присоединения, не взаимодействует с кислотами и щелочами, сильными окислителями, активными металлами. Основные химические превращения октана будут происходить только при сообщении ему достаточно высокой энергии за счет нагревания, ультрафиолетового облучения и в присутствии катализатора.
1.Радикальное нитрование (реакция Коновалова):
СН3-СН2-СН2-СН2-СН2-СН2-СН2-СН3 + НNО3 =t СН3-СН2-СН2-СН2-СН2-СН-СН3 + Н2О
Октан 2-нитрооктан NО2 2. Крекинг – радикальный разрыв связей С – С. Протекает при нагревании и в присутствии катализаторов:
С8Н18 = С4Н10 + С4Н8
Бутан Бутилен
3. Окисление. При поджигании на воздухе октан будет гореть с выделением большого количества тепла:
2C8H18 + 25О2 = 16СО2 + 18Н2О
4. Сульфохлорирование – промышленный способ получения сульфокислот:
5. Каталитический риформинг – включает сложные процессы, такме как изомеризация, циклизация, дегидрирование, ароматизация алканов, которые приводят к перестройке углеродного скелета:
СН3-СН2-СН2-СН2-СН2-СН2-СН2-СН3 → СН3-СН2-СН2-СН2-СН2-СН-СН3 2-метилгептан
н-октан
СН3
Данная реакция протекает в присутствии катализатора Al2O3 при температуре 100° С
3.2. Октанол-1(октиловый спирт): молекулярная формула – С8Н17ОН, структурная формула – СН3-(СН2)6-СН2-ОН. Бесцветная жидкость с ароматным запахом. Температура кипения – 195,2° С, температура плавления – 16,3 С, температурные пределы воспламенения 74- 142°С. Октанол-1 является предельным одноатомным спиртом. Атомы углерода находятся в состоянии sp3 гибридизации.

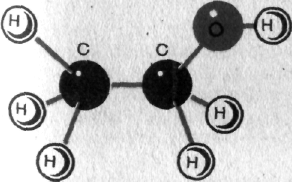
Рис. 7. Модели молекулы этилового спирта
Химические свойства: октанол-1 – это химически активное соединение, вступающее в реакции с разрывом связи R – O – H или R – OH. Разрыв происходит по ионному механизму с образованием органических катионов и анионов.
1. Реакции с щелочными металлами:
2С8Н17-ОН + 2Na = 2C8H17-ONa + H2;
2. Горение:
C8H17OH + 12О2 = 8СО2 + 9Н2О
3. Галогенирование:
C8H17OH + HBr = C8H17Br + H2O
4. Дегидратация (потеря воды):
C8H17OH → С4Н8=С4Н8 + Н2О с присутствием катализатора H2SO4; t0
Октанол-1 можно использовать в качестве пенообразователя или гетерополярного собирателя. Главным структурным элементом определяющим адсорбционные свойства у октилового спирта является функциональная группа –ОН. В этой молекуле наиболее электроотрицателен атом кислорода, поэтому связь О–Н сильно поляризована. Пара электронов смещается к кислороду, который несет частично отрицательный заряд δ- (рис4). В то же время в радикалах электронных пар связи С–Н частично смещены атомы углерода и под их влиянием смещается пара электронов. Это, в свою очередь, несколько уменьшает поляризацию связей ОН.
3.3 Дибутиловый эфир (С4Н9 – О – С4Н9) — простой эфир. Простые эфиры – это органические вещества, молекулы которых состоят из углеводородных радикалов, соединенных через атом кислорода: R’– О – R’’, где R’ и R’’ – радикалы, которые могут быть различными и одинаковыми.
Название простых эфиров обычно связано с названием углеродных радикалов, соединенных с кислородом.
Дибутиловый эфир подвижная, крайне огнеопасная бесцветная жидкость с сильным характерным запахом. Температура кипения – 141,97°С, температура плавления – 95,37° С. В воде при температуре 17° С растворяется менее 0,01 %
Химические свойства: Простые эфиры – довольно инертные вещества. В отличие от сложных эфиров они не гидролизуются. На холоде простые эфиры не взаимодействуют с металлическим натрием и большинством разбавленных кислот. Однако концентрированные кислоты (Н2SO4;НI) даже на холоде разлагают эти эфиры, а металлический натрий при нагревании их расширяет:
С4Н9 – О – С4Н9 + Н2SO4 = С4Н9О – SO2 – OС4Н9 + H2O (1. с. 199-202)
Дибутилсульфат
С4Н9 – О – С4Н9 + НI = С4Н9ОН + С4Н9I
С4Н9 – О – С4Н9 + 2Na =t С4Н9ОNa + С4Н9Na
бутилнатрий
Простые эфиры в природе не встречаются, их получают синтетическим путем. Дегидратация спиртов под влиянием минеральных кислот:
Н2SO4
С4Н9ОН + С4Н9ОН С4Н9 – О – С4Н9 — Дибутиловый эфир
– Н2О
Очень ограничено применяют как растворитель, используют также в синтезе гриньяра. Преимущества дибутилового эфира по сравнению с диэтиловым эфиром является меньшая летучесть. При длительном хранении образуют перекиси, в связи, с чем перед применением берут пробу на содержание этих примесей, которые вследствие устраняются встряхиванием с растворами солей двухвалентного железа или с раствором сульфата натрия.
По классификации А. В. Киселева дибутиловый эфир относится к группе В адсорбата.
Дибутиловый эфир можно является также, как и октанол-1 очень эффективным пенообразователем. Главным структурным элементом определяющим адсорбционные свойства у дибутилового эфира является функциональная группа – О –. В этой молекуле наиболее электроотрицателен атом кислорода, поэтому связь –О– с углеводородными радикалами сильно поляризована. Пара электронов смещается к кислороду, который несет частично отрицательный заряд δ- (рис4). В то же время в радикалах электронных пар связи С–Н частично смещены атомы углерода и под их влиянием смещается пара электронов в связи С — О.
ЗАКЛЮЧЕНИЕ
В данной курсовой работе было подробно рассмотрено золото, а также флотационные реагенты, применяемые в процессе флотационного извлечения этого благородного металла. Было установлено, что из всех известных реагентов-собирателей, наиболее распостранены для флотации золота – ксантогенаты и дитиофосфаты, а среди пенообразователей – сосновое масло, Т-66, Т-80, ОПСБ.
Без понимания адсорбционных свойств невозможен правильный и грамотный подбор реагентов. В процессе изучения адсорбционных способностей поверхности золота – выяснили, что адсорбция реагентов происходит путем химической адсорбции.
БИБЛИОГРАФИЧЕСКИЙ СПИСОК
1. Гумилевский С.А., Киршов В.М. Кристаллография и минералогия. Москва: «Высшая школа», 1972.
2. Виноградов А.Н. Металлы и минералы. Ростов-на-Дону: «Феникс», 2004.
3. Паддефет Р. Химия золота. Москва: «Мир», 1982.
4. Соболевский В.И. Благородные металлы. Золото. Москва: «Знание», 1970.
5. Хан. Г.А., Габриелова Л.И. Флотационные реагенты и их применение. Москва: «Недра», 1986.
6. Гольман А.М., Дмитриева И.Л. Флотационные реагенты. Москва: «Наука», 1986.
7. Дуденков С.В., Шафеев Э.Ш. Флотореагентщик. Москва: «Недра», 1968.
8. Полькин С.И. Обогащение руд и россыпей редких и благородных металлов. Москва: «Недра», 1987.
9. Абрамов А.А. Переработка, обогащение и комплексное использование полезных ископаемых. Т2. Москва: МГГУ, 2004.
10. Бочаров В.А., Игнаткина В.А. Технология обогащения полезных ископаемых. Т1, Т2. Москва: «Руда и металлы», 2007.
11. Горлова О.Е., Фадеева Н. В. Химия флотореагентов. Магнитогорск: МГТУ им. Г. И. Носова, 2007.
1
H
1,008
1s1
2,1
Бесцветный газ
t°пл=-259°C
t°кип=-253°C
2
He
4,0026
1s2
4,5
Бесцветный газ
t°кип=-269°C
3
Li
6,941
2s1
0,99
Мягкий серебристо-белый металл
t°пл=180°C
t°кип=1317°C
4
Be
9,0122
2s2
1,57
Светло-серый металл
t°пл=1278°C
t°кип=2970°C
5
B
10,811
2s2 2p1
2,04
Темно-коричневое аморфное вещество
t°пл=2300°C
t°кип=2550°C
6
C
12,011
2s2 2p2
2,55
Прозрачный (алмаз) / черный (графит) минерал
t°пл=3550°C
t°кип=4830°C
7
N
14,007
2s2 2p3
3,04
Бесцветный газ
t°пл=-210°C
t°кип=-196°C
8
O
15,999
2s2 2p4
3,44
Бесцветный газ
t°пл=-218°C
t°кип=-183°C
9
F
18,998
2s2 2p5
3,98
Бледно-желтый газ
t°пл=-220°C
t°кип=-188°C
10
Ne
20,180
2s2 2p6
4,4
Бесцветный газ
t°пл=-249°C
t°кип=-246°C
11
Na
22,990
3s1
0,98
Мягкий серебристо-белый металл
t°пл=98°C
t°кип=892°C
12
Mg
24,305
3s2
1,31
Серебристо-белый металл
t°пл=649°C
t°кип=1107°C
13
Al
26,982
3s2 3p1
1,61
Серебристо-белый металл
t°пл=660°C
t°кип=2467°C
14
Si
28,086
3s2 3p2
1,9
Коричневый порошок / минерал
t°пл=1410°C
t°кип=2355°C
15
P
30,974
3s2 3p3
2,2
Белый минерал / красный порошок
t°пл=44°C
t°кип=280°C
16
S
32,065
3s2 3p4
2,58
Светло-желтый порошок
t°пл=113°C
t°кип=445°C
17
Cl
35,453
3s2 3p5
3,16
Желтовато-зеленый газ
t°пл=-101°C
t°кип=-35°C
18
Ar
39,948
3s2 3p6
4,3
Бесцветный газ
t°пл=-189°C
t°кип=-186°C
19
K
39,098
4s1
0,82
Мягкий серебристо-белый металл
t°пл=64°C
t°кип=774°C
20
Ca
40,078
4s2
1,0
Серебристо-белый металл
t°пл=839°C
t°кип=1487°C
21
Sc
44,956
3d1 4s2
1,36
Серебристый металл с желтым отливом
t°пл=1539°C
t°кип=2832°C
22
Ti
47,867
3d2 4s2
1,54
Серебристо-белый металл
t°пл=1660°C
t°кип=3260°C
23
V
50,942
3d3 4s2
1,63
Серебристо-белый металл
t°пл=1890°C
t°кип=3380°C
24
Cr
51,996
3d5 4s1
1,66
Голубовато-белый металл
t°пл=1857°C
t°кип=2482°C
25
Mn
54,938
3d5 4s2
1,55
Хрупкий серебристо-белый металл
t°пл=1244°C
t°кип=2097°C
26
Fe
55,845
3d6 4s2
1,83
Серебристо-белый металл
t°пл=1535°C
t°кип=2750°C
27
Co
58,933
3d7 4s2
1,88
Серебристо-белый металл
t°пл=1495°C
t°кип=2870°C
28
Ni
58,693
3d8 4s2
1,91
Серебристо-белый металл
t°пл=1453°C
t°кип=2732°C
29
Cu
63,546
3d10 4s1
1,9
Золотисто-розовый металл
t°пл=1084°C
t°кип=2595°C
30
Zn
65,409
3d10 4s2
1,65
Голубовато-белый металл
t°пл=420°C
t°кип=907°C
31
Ga
69,723
4s2 4p1
1,81
Белый металл с голубоватым оттенком
t°пл=30°C
t°кип=2403°C
32
Ge
72,64
4s2 4p2
2,0
Светло-серый полуметалл
t°пл=937°C
t°кип=2830°C
33
As
74,922
4s2 4p3
2,18
Зеленоватый полуметалл
t°субл=613°C
(сублимация)
34
Se
78,96
4s2 4p4
2,55
Хрупкий черный минерал
t°пл=217°C
t°кип=685°C
35
Br
79,904
4s2 4p5
2,96
Красно-бурая едкая жидкость
t°пл=-7°C
t°кип=59°C
36
Kr
83,798
4s2 4p6
3,0
Бесцветный газ
t°пл=-157°C
t°кип=-152°C
37
Rb
85,468
5s1
0,82
Серебристо-белый металл
t°пл=39°C
t°кип=688°C
38
Sr
87,62
5s2
0,95
Серебристо-белый металл
t°пл=769°C
t°кип=1384°C
39
Y
88,906
4d1 5s2
1,22
Серебристо-белый металл
t°пл=1523°C
t°кип=3337°C
40
Zr
91,224
4d2 5s2
1,33
Серебристо-белый металл
t°пл=1852°C
t°кип=4377°C
41
Nb
92,906
4d4 5s1
1,6
Блестящий серебристый металл
t°пл=2468°C
t°кип=4927°C
42
Mo
95,94
4d5 5s1
2,16
Блестящий серебристый металл
t°пл=2617°C
t°кип=5560°C
43
Tc
98,906
4d6 5s1
1,9
Синтетический радиоактивный металл
t°пл=2172°C
t°кип=5030°C
44
Ru
101,07
4d7 5s1
2,2
Серебристо-белый металл
t°пл=2310°C
t°кип=3900°C
45
Rh
102,91
4d8 5s1
2,28
Серебристо-белый металл
t°пл=1966°C
t°кип=3727°C
46
Pd
106,42
4d10
2,2
Мягкий серебристо-белый металл
t°пл=1552°C
t°кип=3140°C
47
Ag
107,87
4d10 5s1
1,93
Серебристо-белый металл
t°пл=962°C
t°кип=2212°C
48
Cd
112,41
4d10 5s2
1,69
Серебристо-серый металл
t°пл=321°C
t°кип=765°C
49
In
114,82
5s2 5p1
1,78
Мягкий серебристо-белый металл
t°пл=156°C
t°кип=2080°C
50
Sn
118,71
5s2 5p2
1,96
Мягкий серебристо-белый металл
t°пл=232°C
t°кип=2270°C
51
Sb
121,76
5s2 5p3
2,05
Серебристо-белый полуметалл
t°пл=631°C
t°кип=1750°C
52
Te
127,60
5s2 5p4
2,1
Серебристый блестящий неметалл
t°пл=450°C
t°кип=990°C
53
I
126,90
5s2 5p5
2,66
Черно-серые кристаллы
t°пл=114°C
t°кип=184°C
54
Xe
131,29
5s2 5p6
2,6
Бесцветный газ
t°пл=-112°C
t°кип=-107°C
55
Cs
132,91
6s1
0,79
Мягкий серебристо-желтый металл
t°пл=28°C
t°кип=690°C
56
Ba
137,33
6s2
0,89
Серебристо-белый металл
t°пл=725°C
t°кип=1640°C
57
La
138,91
5d1 6s2
1,1
Серебристый металл
t°пл=920°C
t°кип=3454°C
58
Ce
140,12
f-элемент
Серебристый металл
t°пл=798°C
t°кип=3257°C
59
Pr
140,91
f-элемент
Серебристый металл
t°пл=931°C
t°кип=3212°C
60
Nd
144,24
f-элемент
Серебристый металл
t°пл=1010°C
t°кип=3127°C
61
Pm
146,92
f-элемент
Светло-серый радиоактивный металл
t°пл=1080°C
t°кип=2730°C
62
Sm
150,36
f-элемент
Серебристый металл
t°пл=1072°C
t°кип=1778°C
63
Eu
151,96
f-элемент
Серебристый металл
t°пл=822°C
t°кип=1597°C
64
Gd
157,25
f-элемент
Серебристый металл
t°пл=1311°C
t°кип=3233°C
65
Tb
158,93
f-элемент
Серебристый металл
t°пл=1360°C
t°кип=3041°C
66
Dy
162,50
f-элемент
Серебристый металл
t°пл=1409°C
t°кип=2335°C
67
Ho
164,93
f-элемент
Серебристый металл
t°пл=1470°C
t°кип=2720°C
68
Er
167,26
f-элемент
Серебристый металл
t°пл=1522°C
t°кип=2510°C
69
Tm
168,93
f-элемент
Серебристый металл
t°пл=1545°C
t°кип=1727°C
70
Yb
173,04
f-элемент
Серебристый металл
t°пл=824°C
t°кип=1193°C
71
Lu
174,96
f-элемент
Серебристый металл
t°пл=1656°C
t°кип=3315°C
72
Hf
178,49
5d2 6s2
Серебристый металл
t°пл=2150°C
t°кип=5400°C
73
Ta
180,95
5d3 6s2
Серый металл
t°пл=2996°C
t°кип=5425°C
74
W
183,84
5d4 6s2
2,36
Серый металл
t°пл=3407°C
t°кип=5927°C
75
Re
186,21
5d5 6s2
Серебристо-белый металл
t°пл=3180°C
t°кип=5873°C
76
Os
190,23
5d6 6s2
Серебристый металл с голубоватым оттенком
t°пл=3045°C
t°кип=5027°C
77
Ir
192,22
5d7 6s2
Серебристый металл
t°пл=2410°C
t°кип=4130°C
78
Pt
195,08
5d9 6s1
2,28
Мягкий серебристо-белый металл
t°пл=1772°C
t°кип=3827°C
79
Au
196,97
5d10 6s1
2,54
Мягкий блестящий желтый металл
t°пл=1064°C
t°кип=2940°C
80
Hg
200,59
5d10 6s2
2,0
Жидкий серебристо-белый металл
t°пл=-39°C
t°кип=357°C
81
Tl
204,38
6s2 6p1
Серебристый металл
t°пл=304°C
t°кип=1457°C
82
Pb
207,2
6s2 6p2
2,33
Серый металл с синеватым оттенком
t°пл=328°C
t°кип=1740°C
83
Bi
208,98
6s2 6p3
Блестящий серебристый металл
t°пл=271°C
t°кип=1560°C
84
Po
208,98
6s2 6p4
Мягкий серебристо-белый металл
t°пл=254°C
t°кип=962°C
85
At
209,98
6s2 6p5
2,2
Нестабильный элемент, отсутствует в природе
t°пл=302°C
t°кип=337°C
86
Rn
222,02
6s2 6p6
2,2
Радиоактивный газ
t°пл=-71°C
t°кип=-62°C
87
Fr
223,02
7s1
0,7
Нестабильный элемент, отсутствует в природе
t°пл=27°C
t°кип=677°C
88
Ra
226,03
7s2
0,9
Серебристо-белый радиоактивный металл
t°пл=700°C
t°кип=1140°C
89
Ac
227,03
6d1 7s2
1,1
Серебристо-белый радиоактивный металл
t°пл=1047°C
t°кип=3197°C
90
Th
232,04
f-элемент
Серый мягкий металл
91
Pa
231,04
f-элемент
Серебристо-белый радиоактивный металл
92
U
238,03
f-элемент
1,38
Серебристо-белый металл
t°пл=1132°C
t°кип=3818°C
93
Np
237,05
f-элемент
Серебристо-белый радиоактивный металл
94
Pu
244,06
f-элемент
Серебристо-белый радиоактивный металл
95
Am
243,06
f-элемент
Серебристо-белый радиоактивный металл
96
Cm
247,07
f-элемент
Серебристо-белый радиоактивный металл
97
Bk
247,07
f-элемент
Серебристо-белый радиоактивный металл
98
Cf
251,08
f-элемент
Нестабильный элемент, отсутствует в природе
99
Es
252,08
f-элемент
Нестабильный элемент, отсутствует в природе
100
Fm
257,10
f-элемент
Нестабильный элемент, отсутствует в природе
101
Md
258,10
f-элемент
Нестабильный элемент, отсутствует в природе
102
No
259,10
f-элемент
Нестабильный элемент, отсутствует в природе
103
Lr
266
f-элемент
Нестабильный элемент, отсутствует в природе
104
Rf
267
6d2 7s2
Нестабильный элемент, отсутствует в природе
105
Db
268
6d3 7s2
Нестабильный элемент, отсутствует в природе
106
Sg
269
6d4 7s2
Нестабильный элемент, отсутствует в природе
107
Bh
270
6d5 7s2
Нестабильный элемент, отсутствует в природе
108
Hs
277
6d6 7s2
Нестабильный элемент, отсутствует в природе
109
Mt
278
6d7 7s2
Нестабильный элемент, отсутствует в природе
110
Ds
281
6d9 7s1
Нестабильный элемент, отсутствует в природе
Металлы
Неметаллы
Щелочные
Щелоч-зем
Благородные
Галогены
Халькогены
Полуметаллы
s-элементы
p-элементы
d-элементы
f-элементы
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
Строение, изомерия и номенклатура простых эфиров
Простые эфиры – это органические вещества, в которых два углеводородных радикала соединены с атомом кислорода. Их можно представить как соединения, образованные замещением обоих атомов водорода молекулы воды двумя алкильными радикалами или замещением гидроксильного водорода спиртов одним алкильным радикалом. Далее рассмотрим каково Строение, изомерия и номенклатура простых эфиров.
Атомы углерода в насыщенных простых эфирах находятся в состоянии sp3— гибридизации, если углеводородный радикал имеет двойную связь – в состоянии sp2-гибридизации. В качестве примера приведем строение диэтилового эфира:
Подробно образование sp3— гибридных атомов рассмотрены в разделе Алканы, sp2-гибридных атомов — в разделе Алкены. Также общие принципы гибридизации атомных орбиталей рассмотрены в разделе Химическая связь и строение молекул/Метод валентных связей.
Классификация простых эфиров
Различают симметричные и несимметричные (смешанные) простые эфиры. В симметричных простых эфирах углеводородные остатки (радикалы) имеют одинаковое строение, а в смешанных – различное, например, дибутиловый эфир — симметричный, а метилбутиловый эфир — смешанный:
Кроме этого, существует классификация, построенная на различии в строении углеводородного радикала. Согласно этой классификации углеводородная цепь простых эфиров может быть:
- Открытая:
- Замкнутая (циклическая):
А сами углеводородные радикалы:
- Насыщенные:
- Ненасыщенные:
- Ароматические:
Изомерия и номенклатура простых эфиров
Общая формула простых эфиров CnH2n+2O. В другом виде общую формулу можно представить как R-O-R или R-O-R`, где R и R`— алкильные радикалы (насыщенные, ненасыщенные или ароматические).
По общей формуле видно, что простые эфиры изомерны спиртам, например, изомерами являются соединения с брутто формулой С5Н12О 2-пентанол и этилизопропиловый эфир:
Кроме обычных видов изомерии, для простых эфиров характерна и метамерия – это вид изомерии, которая заключается в существовании нескольких эфиров с одинаковой общей формулой, но в структуре которых алкильные радикалы отличаются числом углеродных атомов, например, этилбутиловый эфир и дипропиловый эфир:
Номенклатура простых эфиров обусловлена характером алкильных радикалов. Низшие эфиры обычно называют в соответствии с правилами рациональной номенклатуры, т.е. сначала дают названия радикалов, к которым затем прибавляют слово эфир. Если радикалы одинаковые, то к названию радикала прибавляют приставку -ди, если разные, то называют каждый из радикалов:
Простые эфиры, имеющие более сложное строение, называют по номенклатуре ИЮПАК как алкоксиалканы или алкоксиарены:
ди-н-бутиловый эфир | 142-96-1
Ди-н-бутиловый эфир Химические свойства, применение, Производство
Химические свойства
Ди-н-бутиловый эфир — бесцветная жидкость с эфироподобным запахомХимические свойства
Ди-н-бутиловый эфир представляет собой легковоспламеняющуюся бесцветную жидкость со слабым эфирным запахом.Использует
Растворитель для углеводородов, жировых материалов; экстрагент, используемый специально для отделения мета- als, очистка растворителем, органический синтез (реакция средний).Общее описание
Ди-н-бутиловый эфир — прозрачная бесцветная жидкость с эфирным запахом. Температура вспышки ниже 141 ° F. Менее плотный, чем вода и нерастворимый в воде. Пары тяжелее воздуха. Раздражает глаза, нос, горло и дыхательные пути.Реакции воздуха и воды
Легковоспламеняющиеся. Легко окисляется в воздухе с образованием нестабильных пероксидов, которые могут самопроизвольно взрываться [Bretherick 1979 p.151-154, 164]. Смесь жидкого воздуха и диэтилового эфира взорвалась самопроизвольно [История болезни MCA 616 1960].Нерастворим в воде.Реактивность профиля
Эфиры, такие как BUTYL ETHER, могут действовать как основания. Они образуют соли с сильными кислотами и комплексы присоединения с кислотами Льюиса. Комплекс между диэтиловым эфиром и трифторидом бора является примером. Эфиры могут бурно реагировать с сильными окислителями. В других реакциях, которые обычно включают разрыв углерод-кислородной связи, простые эфиры являются относительно инертными.Опасность
Токсичен при длительном вдыхании.Огнеопасно, умеренный пожарный риск. Может образовывать взрывоопасные пероксиды, особенно в безводной форме.Опасность для здоровья
Вдыхание вызывает раздражение носа и горла. Жидкость раздражает глаза и может раздражать кожу при длительном контакте. Проглатывание вызывает раздражение рта и желудка.Пожарная опасность
Поведение в огне: пар тяжелее воздуха и может пролететь значительное расстояние до источника возгорания и вспыхнуть.Химическая реактивность
Реакционная способность с водой Нет реакции; Реакционная способность с общими материалами: нет реакции; Стабильность при транспортировке: стабильная; Нейтрализующие агенты для кислот и щелочей: не уместно; Полимеризация: не уместно; Ингибитор полимеризации: не имеет отношения.Промышленное использование
н-бутиловый эфир используется в реакции синтеза, которые требуют безводного, инертного растворителя. Этот эфир является ценным экстракционный растворитель для водных растворов из-за его низкой растворимости в воде. н-бутил простой эфир при смешивании с этанолом или бутанолом является отличным растворителем для этилцеллюлозы.Профиль безопасности
Мягко токсичен вдыхание, проглатывание и попадание на кожу. Системные эффекты человека при вдыхании: раздражение конъюнктивы и неуточненный нос последствия.Экспериментальная кожа и человек раздражитель глаз. Смотрите также Эфиры. опасно пожароопасность при воздействии тепла, пламени или окислителей. Несовместимо с NCL и окисляющие материалы. Чтобы бороться с огнем, используйте алкоголь пена, сухой химикат. При нагревании до разложение испускает едкий дым и испарения.Потенциальная экспозиция
Ди-н-бутиловый эфир используется в качестве растворителя для углеводородов, жирных материалов; экстрагент в отделении использованных металлов; очистка растворителей, изготовление других химикатов.Несовместимость: Может образовывать взрывоопасную смесь с воздухом. Может накапливать статические электрические заряды и может вызвать воспламенение его паров. Несовместим с сильными кислотами; окислители. При контакте с воздухом или светом могут образовываться нестабильные и взрывоопасные пероксиды, особенно безводные.Доставка
UN1149 Бутиловые эфиры и дибутиловые эфиры, Опасность Класс: 3; Метки: 3 — легковоспламеняющаяся жидкостьМетоды очистки
Пероксиды (определяемые по выделению йода из слабокислых растворов HCl с 2% KI) можно удалить встряхиванием 1 л эфира с 5-10 мл раствора, содержащего 6.0 г сульфата железа и 6 мл концентрированной воды и 110 мл воды, с водным Na2SO3 или подкисленным NaI, водой, затем водным Na2S2O3. После промывки разбавленным NaOH, KOH или Na2CO3, затем водой, эфир сушат над CaCl2 и перегоняют. Затем его можно высушить перегонкой из Cah3 или Na (после сушки с помощью P2O5) и хранить в темноте с Na или NaH. Эфир также может быть очищен путем обработки CS2 и NaOH, удаляя избыток сульфида нагреванием. Затем эфир промывают водой, сушат с помощью NaOH и перегоняют [Kusama & Koike J Chem Soc Jpn, Pure Chem Sect 72 229 1951].Другие процедуры очистки включают прохождение через колонку с активированным оксидом алюминия для удаления пероксидов или через колонку с силикагелем и дистилляцию после добавления примерно 3% (об. / Об.) 1М раствора MeMgI в н-бутиловом эфире. [Beilstein 1 IV 1520.]Утилизация отходов
Растворить или смешать материал с горючим растворителем и сжигать в химическом мусоросжигателе, оборудованном форсажной камерой и скруббером. Все федеральные, государственные и местные экологические нормы должны быть наблюдаемый.Продукты приготовления ди-н-бутилового эфира и сырье
Сырье
Продукты для приготовления
,дибутилфталат | 84-74-2
Дибутилфталат Химические свойства, Применение, Производство
Описание
Дибутилфталат включен в качестве средства от насекомых в некоторые аэрозольные баллончики используются для лечения ударов мух у овец. Это бесцветная маслянистая жидкость с очень слабым ароматическим запахом.Химические свойства
Дибутилфталат встречается в виде вязкой жидкости без запаха, маслянистой, бесцветной или очень слегка желтого цвета.Физические свойства
Бесцветная или бледно-желтая, маслянистая, вязкая жидкость со слабым ароматическим запахомИспользует
Ди-н-бутилфталат был использован в качестве средства от насекомых.Использует
Дибутилфталат используется в пластификаторах, косметике, безопасном стекле, инсектицидах, печатных красках, бумажных покрытиях, клеях, эластомерах и взрывчатых веществах; растворитель в полисульфидные оттискные материалы; растворитель для парфюмерных масел; парфюмерный фиксатор; текстильный смазочный агент; твердотопливный ракетный двигатель; смягчающее средство в виде аэрозольных антиперспирантов; отпугиватель насекомых; пластификатор в различных пластиковых материалах.Использует
Метаболит фталата с генотоксическим эффектом.Использует
Пластификатор; растворитель для маслорастворимых красителей, инсектицидов и других органических веществ; пеногаситель; смазка для текстильных волокон; закрепитель аромата; средство от насекомых.Определение
ChEBI: сложный эфир фталевой кислоты, который представляет собой сложный диэфир, полученный формальной конденсацией карбоксигрупп фталевой кислоты с двумя молекулами бутан-1-ола.Методы производства
Дибутилфталат получают из н-бутанола и фталевого ангидрида в реакции образования сложного эфира.Общее описание
Дибутилфталат представляет собой бесцветную маслянистую жидкость. Дибутилфталат нерастворим в воде. Основной опасностью является угроза окружающей среде. Должны быть предприняты немедленные меры для ограничения его распространения в окружающей среде. Поскольку дибутилфталат является жидким, дибутилфталат может легко проникать в почву и загрязнять грунтовые воды и близлежащие потоки. Дибутилфталат является горючим веществом, хотя дибутилфталату может потребоваться некоторое усилие для его воспламенения.Дибутилфталат используется в красках и пластмассах, а также в качестве реакционной среды для химических реакций.Реакции воздуха и воды
Нерастворим в воде.Реактивность профиля
Дибутилфталат является сложным эфиром. Сложные эфиры реагируют с кислотами, выделяя тепло вместе со спиртами и кислотами. Сильные окисляющие кислоты могут вызывать бурную реакцию, которая является достаточно экзотермической, чтобы зажечь продукты реакции. Тепло также вырабатывается при взаимодействии сложных эфиров с растворами каустика.Легковоспламеняющийся водород образуется при смешивании сложных эфиров с щелочными металлами и гидридами. Избегать контакта с сильными окислителями и сильными основаниями. Не полимеризуется. [USCG, 1999]. Может генерировать электростатические заряды. [Безопасное обращение с химическими веществами 1980. с. 250].Опасность для здоровья
Токсичность этого соединения очень низкая. Нечеловеческие, пероральный прием дибутилфталата на уровне дозы 150 мг / кг может вызвать тошноту, рвоту, головокружение, галлюцинации, искаженное зрение, слезотечение и конъюнктивит с быстрым выздоровлением.Он метаболизируется до монобутилового эфира и фталевой кислоты и выделяется с мочой. Ингаляционная токсичность должна быть незначительной из-за незначительного низкого давления пара [значение LD50, оральное (для мышей): 5300 мг / кг.Пожарная опасность
Горюче.Фармацевтические применения
Дибутилфталат используется в фармацевтических составах в качестве пластификатора в пленочных покрытиях. Он был оценен как порообразующий агент в новых системах доставки.Он также широко используется в качестве растворителя, особенно в косметических составах, таких как антиперспиранты, шампуни для волос и лаки для волос. В дополнение к ряду промышленных применений дибутилфталат используется в качестве средства от насекомых, хотя он не так эффективен, как диметилфталат.Контактные аллергены
В основном используется в качестве нереакционноспособного эпоксидного разбавителя.Профиль безопасности
Умеренно токсичен внутрибрюшинные и внутривенные пути.Мягко токсичен при проглатывании. Человек системный глазные эффекты при проглатывании, галлюцинации, искаженное восприятие, тошнота или рвота, и изменения в почках, мочеточниках или мочевом пузыре. Экспериментальный тератогенный и репродуктивный последствия. Данные мутации сообщили. Горючий при воздействии тепла или пламя; может реагировать с окислителями. Бурная реакция с Cl2. Несовместима с хлора. Чтобы бороться с огнем, используйте CO2, сухой химическое вещество. При нагревании разложить его испускает едкий дым и пары. Смотрите также Эфиры, фталевая кислота и н БУТИЛОВЫЙ АЛКОГОЛЬ.Безопасность
Дибутилфталат обычно рассматривается как относительно нетоксичный материал, хотя иногда сообщалось, что он вызывает реакции гиперчувствительности. Это широко используется в актуальных косметических и некоторых оральных фармацевтических составах.LD50 (мышь, IV): 0,72 г / кг
LD50 (мышь, оральный): 5,3 г / кг
LD50 (крыса, оральный): 8,0 г / кг
LD50 (крыса, IP): 3,05 мл / кг
Источник
Обнаружен в дистиллированной водорастворимой фракции нового и использованного моторного масла в концентрациях от 38 до 43 и от 15 до 23 мкг / л соответственно (Chen et al., 1994). Выщелачивание из гибкого пластика в контакт с водой. Лабораторный загрязнитель.Экологическая Судьба
Биологический. В аэробных условиях с использованием пресноводного гидрозоля, моно-н-бутилфталата и фталевая кислота были получены. В анаэробных условиях фталевая кислота не была настоящее время (Verschueren, 1983). В анаэробном иле ди-н-бутилфталат разлагается следующим образом: от монобутилфталата к фталевой кислоте к протокатеховой кислоте с последующим расщеплением кольца и минерализация (Shelton et al.1984). Энгельгардт и соавт. (1975) сообщили, что множество микроорганизмы были способны разлагать ди-н-бутилфталат и предположили следующая схема разложения: от ди-н-бутилфталата до моно-н-бутилфталата до фталевой кислоты до 3,4-дигидроксибензойной кислоты и других неопознанных продуктов. Ди-н-бутилфталат разлагался до бензойной кислоты культурами суспензии клеток томатов (Lycopericon lycopersicum) (Pogány et al., 1990).В скрининговом тесте в статических культуральных колбах ди-н-бутилфталат показал значительное биоразложение с быстрой адаптацией.Эфир (5 и 10 мг / л) статически инкубировали в темный при 25 ° С с дрожжевым экстрактом и осевшим инокулятом бытовых сточных вод. Через 7 дней Было достигнуто 100% биоразложение (Tabak et al., 1981).
Почва. В аэробных условиях используется гидрозоль пресной воды, моно-н-бутилфталат и фталевая кислота были получены. Однако в анаэробных условиях фталевая кислота не сформирован (Verschueren, 1983).
Фотолитик. Водный раствор, содержащий диоксид титана и подвергнутый УФ Излучение (l> 290 нм) приводит к образованию гидроксифталатов и дигидроксифталатов в качестве промежуточных соединений. (Hustert and Moza, 1988).
Химический / Физический. Пиролиз ди-н-бутилфталата в присутствии поливинила хлорид при 600 ° С давал следующие соединения: инден, метилинден, нафталин, 1- метилнафталин, 2-метилнафталин, бифенил, диметилнафталин, аценафтен, флуорен, метилаценафтен, метилфлуорен и шесть неопознанных соединений (Bove and Dalven, 1984).
В щелочных условиях ди-н-бутилфталат будет первоначально гидролизоваться до н-бутила фталат водорода и н-бутанол. Моноэфир подвергнется дальнейшему образованию гидролиза о-фталевая кислота и н-бутанол (Kollig, 1993).
хранилище
Дибутилфталат следует хранить в хорошо укупоренной таре в прохладном, сухом месте. Контейнеры могут быть опасными в пустом состоянии, поскольку они могут содержать остатки продукта, такие как пары и жидкости.Методы очистки
Промойте DBP водой (для освобождения от спирта), затем разбавьте NaOH (для удаления бутилгидрофталата или кислоты), водным NaHCO3 (уголь), затем дистиллированной водой. Сушат его (CaCl2), дистиллируют при 10торр или менее и хранят в эксикаторе над P2O5.[Beilstein 9 II 586, 9 III 4102, 9 IV 3175.]Оценка токсичности
Острый оральный LD 50 для крыс:> 6000 мг / кгНесовместимости
Дибутилфталат бурно реагирует с хлором. Он также реагирует с окислителями, кислотами, основаниями и нитратами.Нормативный статус
Включено в базу данных неактивных ингредиентов FDA (пероральные капсулы, замедленное действие, таблетки с энтеросолюбильным покрытием и таблетки с контролируемым высвобождением).Входит в непарентеральные препараты, лицензированные в Великобритании (оральные капсулы, таблетки, гранулы; актуальные кремы и растворы).Дибутилфталат Препараты и сырье
Сырье
Продукты для приготовления
,Описание продукта
Веб-сайт продукта: http://www.finerchem.com
