Алюминия гидроксид — описание вещества, фармакология, применение, противопоказания, формула
Содержание
- Структурная формула
- Русское название
- Английское название
- Латинское название вещества Алюминия гидроксид
- Брутто формула
- Фармакологическая группа вещества Алюминия гидроксид
- Нозологическая классификация
- Код CAS
- Фармакологическое действие
- Характеристика
- Фармакология
- Применение вещества Алюминия гидроксид
- Побочные действия вещества Алюминия гидроксид
- Взаимодействие
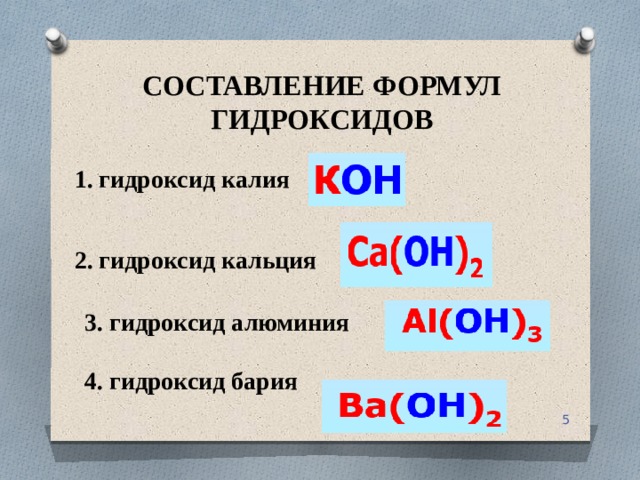
Структурная формула
Русское название
Алюминия гидроксид
Английское название
Aluminium hydroxide
Латинское название вещества Алюминия гидроксид
Aluminii hydroxydum (род. Aluminii hydroxydi)
Aluminii hydroxydi)
Брутто формула
AlH3O3
Фармакологическая группа вещества Алюминия гидроксид
Антациды
Нозологическая классификация
Список кодов МКБ-10
- K29 Гастрит и дуоденит
- K25 Язва желудка
- K31.8.2* Гиперацидность желудочного сока
- K86.
 8.3* Синдром Золлингера-Эллисона
8.3* Синдром Золлингера-Эллисона - K29.6.1* Гастрит гиперацидный
- K26 Язва двенадцатиперстной кишки
Код CAS
21645-51-2
Фармакологическое действие
Фармакологическое действие — адсорбирующее, антацидное, обволакивающее, противоязвенное.
Характеристика
Аморфный рыхлый белый порошок. Практически нерастворим в воде (образует гель). Растворим при нагревании в разбавленных кислотах и растворах едких щелочей.
Фармакология
Нейтрализует соляную кислоту желудка с образованием хлорида алюминия и воды. pH желудочного сока постепенно повышается до 3,4–4,4 и остается на этом уровне в течение нескольких часов, что сопровождается снижением протеолитической активности желудочного сока. В щелочном содержимом кишечника образует нерастворимые соединения алюминия. Даже при длительном лечении не отмечается развития алкалоза.
Применение вещества Алюминия гидроксид
Гиперацидность желудочного сока, гиперацидный гастрит, язвенная болезнь желудка и двенадцатиперстной кишки, дуоденит.
Побочные действия вещества Алюминия гидроксид
Запор (при длительном применении).
Взаимодействие
Окись магния усиливает антацидный эффект, снижая вероятность запоров.
Способ применения и дозы
Внутрь, в виде суспензии в воде, обычно по 1–2 ч. ложки 4–6 раз в день.
ложки 4–6 раз в день.
Антацид — frwiki.wiki
Антацид это вещество , как правило , основным (например), который нейтрализует кислоту желудка или ограничивает производство кислоты в желудке (ингибиторы протонного насоса; сукралфат и т.д.). Его назначают против желудочного рефлюкса ( обратный ток кислоты из желудка в пищевод), источника изжоги.
Резюме
- 1 Источник аллергического риска?
- 2 Примеры
- 3 Примечания и ссылки
- 4 См. Также
- 4.1 Связанные статьи
Источник аллергического риска?
Антациды долгое время считались препаратами с низким риском, но есть опасения по поводу их чрезмерного использования, и недавно было показано, что пациенты, которым была назначена антацидная терапия, примерно в два раза чаще получают такие препараты, как антациды. В качестве антигистаминных препаратов, предназначенных для лечения респираторная аллергия ( сенная лихорадка , астма ). В исследовании пока не говорится, вызывает ли аллергию антацидный препарат, но это еще один ключ в пользу причинно-следственной связи (исследование, опубликованное в 2018 году, сделало такое же наблюдение у младенцев, пострадавших от рефлюкса и получающих антацидное лечение). Объясняющая гипотеза состоит в том, что в менее кислой среде желудка некоторые недостаточно деградированные белки могут вызвать сенсибилизацию иммунной системы и / или вызвать аллергию у пациента, страдающего пищевой аллергией. Это наблюдалось у лабораторных мышей с аллергией.
Объясняющая гипотеза состоит в том, что в менее кислой среде желудка некоторые недостаточно деградированные белки могут вызвать сенсибилизацию иммунной системы и / или вызвать аллергию у пациента, страдающего пищевой аллергией. Это наблюдалось у лабораторных мышей с аллергией.
В Австрии , согласно исследованию, опубликованному в 2019 году, люди старше 60 лет в пять раз чаще получали противоаллергический препарат, если они ранее принимали антациды (по сравнению с пациентами, не получавшими антациды). Менее чувствительны к этому риску (среди них лишь в 1,5 раза выше) лица до 20 лет. Это исследование включало респираторную аллергию, тогда как более ранние исследования на животных моделях искали пищевые и не респираторные аллергии.
Другие исследования показывают, что они могут ухудшить иммунную функцию и увеличить риск бактериальных инфекций (вероятно, потому, что они могут нарушить баланс кишечной флоры).
Примеры
- Гидроксид алюминия / гидроксид магния ( «Маалокс» )
- Бикарбонат натрия
- Гидроксид магния ( «молоко магнезии» )
- Альгинат натрия ( «Гевискон» )
Примечания и ссылки
- ↑ a b c d и e (ru) Могут ли антациды повышать риск аллергии? — Дженнифер Кузин-Франкель, Science , 30 июля 2019 г.

- ↑ (in) Э. Митр, А. Сьюзи, THE Kropp, DJ Schwartz, GH Gorman и CM Nylund, «Ассоциация между использованием кислотоподавляющих препаратов и антибиотиков в младенчестве и аллергических заболеваний в раннем детстве», в JAMA Pediatrics , 172 (6), 2018, [ читать онлайн ] [PDF] .
Смотрите также
Статьи по Теме
- Повязка желудка
- Гастроэзофагеальный рефлюкс
Антациды | |
|---|---|
| Магний |
|
| Алюминий |
|
| Кальций |
|
| Натрий |
|
<img src=»//fr. wikipedia.org/wiki/Special:CentralAutoLogin/start?type=1×1″ alt=»» title=»»>
wikipedia.org/wiki/Special:CentralAutoLogin/start?type=1×1″ alt=»» title=»»>
гидроксид алюминия
- Главная
- Результаты для «гидроксида алюминия»
| ID | КАС | Имя | Синонимы | Молекулярная формула | Категория |
|---|---|---|---|---|---|
| 1 | 1330-44-5 | ALUMINUM HYDROXIDE HYDRATE | AlH5O4 | ||
| 2 | 1327-41-9 | Polyaluminium Chloride | Aluminum chlorohydrate (anhydrous) Aluminum hydroxychloride Оксихлорид алюминия ACH 325 ACH 331 ACH 7-321 Алоксиколл Алюминол ACH Хлоргидрат алюминия Хлоргидроксид алюминия Гидроксид алюминия хлорид Гидроксид алюминия хлорид, основной Aluminum chloride oxide Aluminum chlorohydrol Aluminum chlorohydroxide Aluminum hydroxide chloride Aquarhone 18 Astringen Astringen 10 Basic aluminum chloride Basic aluminum chloride, hydrate Berukotan AC-P Cartafix LA Cawood 5025 Chlorhydrol Chlorhydrol Micro-Dry Chlorhydrol Micro-Dry SUF Диалюминий-хлорид-пентагидроксид E 200 E 200 (коагулянт) Gelsica HPB 5025 Hessidrex WT Hydral Hydrofugal Kempac 10 Kempac 20 Kemwater PAX 14 Locron Locron P Locron S Nalco 8676 OCAL Oulupac 180 PAC PAC (salt) PAC 250A PAC 250AD PACK 300M PALC Paho 2S Sansudor UNII-HPN8MZW13M Wickenol cps 325 Хлорид алюминия основной [AL2(OH)nCL6-n]m Трихлорид алюминия Полихлорид алюминия Полихлорид алюминия 0029 | AlClh3O | Катализаторы и вспомогательные вещества; Реагенты для обработки воды |
| 3 | 21645-51-2 | Гидроксид алюминия | C. I. 77002 I. 77002 Гидроксид алюминия , высушенный [ЯНВАРЬ] Гидроксид алюминия Тригидрат оксида алюминия Гидрат алюминия Тригидрат алюминия | Al(OH)3 | Неорганическая химия; Неорганическая щелочь |
| 4 | 142-03-0 | Субацетат алюминия | Ацетат алюминия Ацетат алюминия, основной Алюминий-уксусная кислота (1:2) гидрат | Al(OH)C4H6O4 | Органические материалы; Organometallic compounds |
| 5 | 300-92-5 | Aluminium distearate (light) | Aluminium distearate,light Hydroxyaluminum distearate hydroxybis(octadecanoato-o)-aluminum ALUMINUM DISTEARATE ALUMINIUM STEARATE, DI aluminiumdistearate Aluminum,hydroxybis(octadecanoato-O)- aluminumhydroxidedistearate aluminumhydroxydistearate Aluminium Distearate aluminum hydroxide octadecanoate (1:1:2) aluminum trioctadecanoate octadecanoic acid-aluminum (2:1) hydrate | C36H71AlO5 | Органические материалы; Металлоорганические соединения |
| 6 | 882-09-7 | 2-(4-Хлорфенокси)-2-метилпропионовая кислота | Клофибриновая кислота 2-(4-Хлорфенокси)изомасляная кислота R(+)-2-(4-хлор-2-метилфенокси)пропионовая кислота 4-Хлорфенокси-изо-масляная кислота 2-(4-хлорфенокси) )-2-метилпропановая кислота 3-(4-хлорфенокси)-2-метилпропановая кислота 2-(4-хлорфенокси)-2-метилпропаноат гидроксид алюминия 2-(4-хлорфенокси)-2-метилпропаноат (1: 1:2) 2-(п-Хлорфенокси)-2-метилпропионовая кислота Клофибрат алюминия | C10h21O3Cl | Органическое сырье; Соединения карбоновых кислот |
| ID | КАС | Название продукта | Поставщики | Описания |
|---|---|---|---|---|
| 1 | 21645-51-2 | Гидроксид алюминия | Hubei Longxin Chemical Industry Co. TEL:15335994747 | |
| 2 | 1330-44-5 | ALUMINUM HYDROXIDE HYDRATE | Shanghai Yuanye Bio-Technology Co., Ltd. ПРЕМИУМ ПОСТАВЩИКИ Мобильный:13371865682 | ГИДРОКСИД АЛЮМИНИЯ 2029 юанье 909299 909294 909294
Какова химическая формула гидроксида алюминия класса 11 химии CBSEОтвет Проверено 229,5 тыс.+ просмотров Подсказка: Мы знаем, что ионные соединения состоят из катионов и анионов. Сумма зарядов в ионном соединении всегда равна нулю (в целом). Ионные связи удерживают ионы вместе, образуя ионные соединения. Благодаря наличию между ними ионных связей они имеют высокие температуры плавления и кипения. Полный пошаговый ответ: $\следовательно $ Вариант (B) правильный. Примечание: Мы можем использовать гидроксид алюминия в качестве огнезащитного наполнителя. Он используется в качестве предшественника соединений алюминия, а также используется в фармацевтике. Обладает низкой токсичностью. Он амфотерный. |

 , Ltd
, Ltd