Применение этилена. Свойства этилена
Этилен является простейшим из органических соединений, известных как алкены. Это бесцветный горючий газ, имеющий сладковатый вкус и запах. Природные источники включают природный газ и нефть, он также является естественным гормоном в растениях, в которых он ингибирует рост и способствует созреванию плодов. Применение этилена является распространенным явлением в промышленной органической химии. Он производится путем нагревания природного газа, температура плавления составляет 169,4 °С, кипения — 103, 9 °С.
Этилен: особенности структуры и свойства
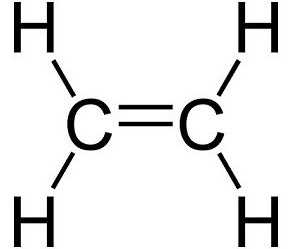
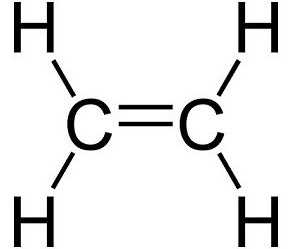
Углеводороды представляют собой молекулы, содержащие водород и углерод. Они сильно различаются с точки зрения количества одинарных и двойных связей и структурной ориентации каждого компонента. Одним из простейших, но биологически и экономически выгодных углеводородов является этилен. Он поставляется в газообразном виде, является бесцветным и легковоспламеняющимся. Он состоит из двух двойных скрепленных атомов углерода с атомами водорода. Химическая формула имеет вид C2H4. Структурная форма молекулы является линейной из-за наличия двойной связи в центре.
Этилен имеет сладковатый мускусный запах, который позволяет легко идентифицировать вещество в воздухе. Это касается газа в чистом виде: запах может исчезать при смешивании с другими химическими веществами.
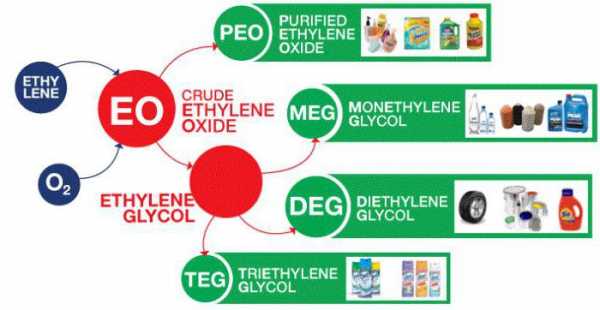
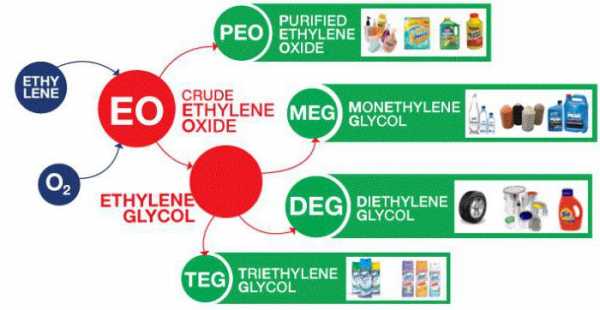
Схема применения этилена
Этилен используют в двух основных категориях: в качестве мономера, из которого построены большие углеродные цепи, и в качестве исходного материала для других двух-углеродных соединений. Полимеризации — это повторяющиеся объединения множества мелких молекул этилена в более крупные. Этот процесс происходит при высоких давлениях и температурах. Области применения этилена многочисленны. Полиэтилен – это полимер, который используется особенно массово в производстве упаковочных пленок, проволочных покрытий и пластиковых бутылок. Еще одно применение этилена в качестве мономера касается формирования линейных α-олефинов. Этилен является исходным материалом для приготовления ряда двух-углеродных соединений, таких как этанол (технический спирт), окись этилена (антифриз, полиэфирные волокна и пленки), ацетальдегида и винил хлорида. Кроме этих соединений, этилен с бензолом образует этилбензол, который используется в производстве пластмасс и синтетического каучука. Рассматриваемое вещество является одним из простейших углеводородов. Однако свойства этилена делают его биологически и хозяйственно значимым.
Коммерческое использование
Свойства этилена дают хорошую коммерческую основу для большого количества органических (содержащих углерод и водород) материалов. Одиночные молекулы этилена могут быть соединены вместе для получения полиэтилена (что означает много молекул этилена). Полиэтилен используется для изготовления пластмасс. Кроме того, он может быть использован для изготовления моющих средств и синтетических смазочных материалов, которые представляют собой химические вещества, используемые для уменьшения трения. Применение этилена для получения стиролов актуально в процессе создания резины и защитной упаковки. Кроме того, он используется в обувной промышленности, особенно это касается спортивной обуви, а также при производстве автомобильных покрышек. Применение этилена является коммерчески важным, а сам газ является одним из наиболее часто производимых углеводородов в глобальном масштабе.
Опасность для здоровья
Этилен представляет опасность для здоровья прежде всего потому, что он является легковоспламеняющимся и взрывоопасным. Он также может действовать как наркотик при низких концентрациях, вызывая тошноту, головокружение, головные боли и потерю координации движения. При более высоких концентрациях он действует как анестетик, вызывая потерю сознания, нечувствительность к боли и другим раздражителям. Все эти негативные моменты могут быть причиной для беспокойства в первую очередь для людей, непосредственно работающих с газом. Количество этилена, с которым большинство людей сталкивается в повседневной жизни, как правило, сравнительно небольшое.
Реакции этилена
1) Окисление. Это добавление кислорода, например, при окислении этилена до окиси этилена. Он используется в производстве этиленгликоля (1,2-этандиола), который применяется в качестве незамерзающей жидкости и в производстве полиэфиров путем конденсационной полимеризации.
2) Галогенирование — реакции с этиленом фтора, хлора, брома, йода.
3) Хлорирование этилена в виде 1,2-дихлорэтана и последующая конверсия 1,2-дихлорэтана в винилхлорид мономер. 1,2-дихлорэтан является полезным органическим растворителем, а также является ценным предшественником в синтезе винилхлорида.
 4) Алкилирование — добавление углеводородов по двойной связи, например, синтез этилбензола из этилена и бензола с последующим преобразованием в стирол. Этилбензол является промежуточным для производства стирола, одного из наиболее широко используемых виниловых мономеров. Стирол — мономер, используемый для производства полистирола.
4) Алкилирование — добавление углеводородов по двойной связи, например, синтез этилбензола из этилена и бензола с последующим преобразованием в стирол. Этилбензол является промежуточным для производства стирола, одного из наиболее широко используемых виниловых мономеров. Стирол — мономер, используемый для производства полистирола.5) Горение этилена. Газ получается путем нагревания этилового спирта и концентрированной серной кислоты.
6) Гидратация – реакция с добавлением воды к двойной связи. Наиболее важным промышленным применением этой реакции является превращение этилена в этанол.
Этилен и горение
Этилен – это газ без цвета, который плохо растворяется в воде. Горение этилена в воздухе сопровождается образованием углекислого газа и воды. В чистом виде газ горит световым диффузионным пламенем. Смешанный с небольшим количеством воздуха, он дает пламя, состоящее из трех отдельных слоев – внутреннего сердечника — несгоревшего газа, сине-зеленого слоя и внешнего конуса, где частично окисленный продукт из предварительно перемешанного слоя сгорают в диффузионном пламени. Результирующее пламя показывает сложную серию реакций, а если к газовой смеси добавляется больше воздуха, постепенно диффузионный слой исчезает.
Полезные факты
1) Этилен является природным растительным гормоном, он влияет на рост, развитие, созревание и старение всех растений.
2) Газ не вреден и не токсичен для человека в определенной концентрации (100-150 мг).
3) Он используется в медицине в качестве обезболивающего средства.
4) Действие этилена замедляется при низких температурах.
5) Характерным свойством является хорошая проникающая способность через большинство веществ, например через картонные упаковочные коробки, деревянные и даже бетонные стены.
6) В то время как он имеет неоценимое значение благодаря своей способности инициировать процесс созревания, он также может быть очень вредным для многих фруктов, овощей, цветов и растений, ускоряя процесс старения и снижая качество продукта и его срок годности. Степень повреждения зависит от концентрации, продолжительности воздействия и температуры.
7) Этилен взрывоопасен при высоких концентрациях.
8) Этилен используется в производстве стекла специального назначения для автомобильной промышленности.
9) Изготовление металлоконструкций: газ используется в качестве кислородно-топливного газа для резки металла, сварки и высокой скорости термического напыления.
10) Нефтепереработка: этилен используется в качестве хладагента, особенно на производстве по сжижению природного газа.
11) Как уже говорилось ранее, этилен является очень реактивным веществом, кроме того, он еще и очень легко воспламеняется. Из соображений безопасности, его обычно транспортируют по специальному отдельному газопроводу.
12) Одним из самых распространенных продуктов, изготовленных непосредственно из этилена, является пластмасса.
fb.ru
Этилен — это… Что такое Этилен?
Этиле́н (по ИЮПАК: этен) — органическое химическое соединение, описываемое формулой С2H4. Является простейшим алкеном (олефином), изологом этана. При нормальных условиях — бесцветный горючий газ со слабым запахом. Частично растворим в воде (25,6 мл в 100 мл воды при 0°C), этаноле (359 мл в тех же условиях). Хорошо растворяется в диэтиловом эфире и углеводородах. Содержит двойную связь и поэтому относится к ненасыщенным или непредельным углеводородам. Играет чрезвычайно важную роль в промышленности, а также является фитогормоном. Этилен — самое производимое органическое соединение в мире[1]; общее мировое производство этилена в 2008 году составило 113 миллионов тонн и продолжает расти на 2—3 % в год[2]. Этилен обладает наркотическим действием. Класс опасности — четвёртый[3].
Применение
Этилен является ведущим продуктом основного органического синтеза и применяется для получения следующих соединений (перечислены в алфавитном порядке):
Этилен в смеси с кислородом использовался в медицине для наркоза вплоть до середины 80-х годов ХХ века в СССР и на ближнем Востоке. Этилен является фитогормоном практически у всех растений[4], среди прочего[5] отвечает за опадание иголок у хвойных.
Электронное и пространственное строение молекулы
Атомы углерода находятся во втором валентном состоянии (sр2-гибридизация). В результате, на плоскости под углом 120° образуются три гибридных облака, которые образуют три сигма-связи с углеродом и двумя атомами водорода. Р-электрон, который не участвовал в гибридизации, образует в перпендикулярной плоскости -связь с р-электроном соседнего атома углерода. Так образуется двойная связь между атомами углерода. Молекула имеет плоскостное строение.
- CH2=CH2
Основные химические свойства
Этилен — химически активное вещество. Так как в молекуле между атомами углерода имеется двойная связь, то одна из них, менее прочная, легко разрывается, и по месту разрыва связи происходит присоединение, окисление, полимеризация молекул.
- Галогенирование:
- CH2=CH2 + Br2 → CH2Br—CH2Br
- Происходит обесцвечивание бромной воды. Это качественная реакция на непредельные соединения.
- Гидрирование:
- CH2=CH2 + H — H → CH3 — CH3 (под действием Ni)
- Гидрогалогенирование:
- CH2=CH2 + HBr → CH3 — CH2Br
- CH2=CH2 + HOH → CH3CH2OH (под действием катализатора)
- Эту реакцию открыл A.M. Бутлеров, и она используется для промышленного получения этилового спирта.
- Этилен легко окисляется. Если этилен пропускать через раствор перманганата калия, то он обесцветится. Эта реакция используется для отличия предельных и непредельных соединений.
- Окись этилена — непрочное вещество, кислородный мостик разрывается и присоединяется вода, в результате образуется этиленгликоль:
- C2H4 + 3O2 → 2CO2 + 2H2O
- nCH2=CH2 → (-CH2-CH2-)n
Примечания
| В этой статье не хватает ссылок на источники информации. Информация должна быть проверяема, иначе она может быть поставлена под сомнение и удалена. Вы можете отредактировать эту статью, добавив ссылки на авторитетные источники. Эта отметка установлена 15 мая 2011. |
dic.academic.ru
Применение этилена. Свойства этилена
Образование 27 марта 2016Этилен является простейшим из органических соединений, известных как алкены. Это бесцветный горючий газ, имеющий сладковатый вкус и запах. Природные источники включают природный газ и нефть, он также является естественным гормоном в растениях, в которых он ингибирует рост и способствует созреванию плодов. Применение этилена является распространенным явлением в промышленной органической химии. Он производится путем нагревания природного газа, температура плавления составляет 169,4 °С, кипения — 103, 9 °С.
Этилен: особенности структуры и свойства
Углеводороды представляют собой молекулы, содержащие водород и углерод. Они сильно различаются с точки зрения количества одинарных и двойных связей и структурной ориентации каждого компонента. Одним из простейших, но биологически и экономически выгодных углеводородов является этилен. Он поставляется в газообразном виде, является бесцветным и легковоспламеняющимся. Он состоит из двух двойных скрепленных атомов углерода с атомами водорода. Химическая формула имеет вид C2H4. Структурная форма молекулы является линейной из-за наличия двойной связи в центре.
Этилен имеет сладковатый мускусный запах, который позволяет легко идентифицировать вещество в воздухе. Это касается газа в чистом виде: запах может исчезать при смешивании с другими химическими веществами.
Схема применения этилена
Этилен используют в двух основных категориях: в качестве мономера, из которого построены большие углеродные цепи, и в качестве исходного материала для других двух-углеродных соединений. Полимеризации — это повторяющиеся объединения множества мелких молекул этилена в более крупные. Этот процесс происходит при высоких давлениях и температурах. Области применения этилена многочисленны. Полиэтилен – это полимер, который используется особенно массово в производстве упаковочных пленок, проволочных покрытий и пластиковых бутылок. Еще одно применение этилена в качестве мономера касается формирования линейных α-олефинов. Этилен является исходным материалом для приготовления ряда двух-углеродных соединений, таких как этанол (технический спирт), окись этилена (антифриз, полиэфирные волокна и пленки), ацетальдегида и винил хлорида. Кроме этих соединений, этилен с бензолом образует этилбензол, который используется в производстве пластмасс и синтетического каучука. Рассматриваемое вещество является одним из простейших углеводородов. Однако свойства этилена делают его биологически и хозяйственно значимым.
Коммерческое использование
Свойства этилена дают хорошую коммерческую основу для большого количества органических (содержащих углерод и водород) материалов. Одиночные молекулы этилена могут быть соединены вместе для получения полиэтилена (что означает много молекул этилена). Полиэтилен используется для изготовления пластмасс. Кроме того, он может быть использован для изготовления моющих средств и синтетических смазочных материалов, которые представляют собой химические вещества, используемые для уменьшения трения. Применение этилена для получения стиролов актуально в процессе создания резины и защитной упаковки. Кроме того, он используется в обувной промышленности, особенно это касается спортивной обуви, а также при производстве автомобильных покрышек. Применение этилена является коммерчески важным, а сам газ является одним из наиболее часто производимых углеводородов в глобальном масштабе.
Опасность для здоровья
Этилен представляет опасность для здоровья прежде всего потому, что он является легковоспламеняющимся и взрывоопасным. Он также может действовать как наркотик при низких концентрациях, вызывая тошноту, головокружение, головные боли и потерю координации движения. При более высоких концентрациях он действует как анестетик, вызывая потерю сознания, нечувствительность к боли и другим раздражителям. Все эти негативные моменты могут быть причиной для беспокойства в первую очередь для людей, непосредственно работающих с газом. Количество этилена, с которым большинство людей сталкивается в повседневной жизни, как правило, сравнительно небольшое.
Реакции этилена
1) Окисление. Это добавление кислорода, например, при окислении этилена до окиси этилена. Он используется в производстве этиленгликоля (1,2-этандиола), который применяется в качестве незамерзающей жидкости и в производстве полиэфиров путем конденсационной полимеризации.
2) Галогенирование — реакции с этиленом фтора, хлора, брома, йода.
3) Хлорирование этилена в виде 1,2-дихлорэтана и последующая конверсия 1,2-дихлорэтана в винилхлорид мономер. 1,2-дихлорэтан является полезным органическим растворителем, а также является ценным предшественником в синтезе винилхлорида.  4) Алкилирование — добавление углеводородов по двойной связи, например, синтез этилбензола из этилена и бензола с последующим преобразованием в стирол. Этилбензол является промежуточным для производства стирола, одного из наиболее широко используемых виниловых мономеров. Стирол — мономер, используемый для производства полистирола.
4) Алкилирование — добавление углеводородов по двойной связи, например, синтез этилбензола из этилена и бензола с последующим преобразованием в стирол. Этилбензол является промежуточным для производства стирола, одного из наиболее широко используемых виниловых мономеров. Стирол — мономер, используемый для производства полистирола.
5) Горение этилена. Газ получается путем нагревания этилового спирта и концентрированной серной кислоты.
6) Гидратация – реакция с добавлением воды к двойной связи. Наиболее важным промышленным применением этой реакции является превращение этилена в этанол.
Этилен и горение
Этилен – это газ без цвета, который плохо растворяется в воде. Горение этилена в воздухе сопровождается образованием углекислого газа и воды. В чистом виде газ горит световым диффузионным пламенем. Смешанный с небольшим количеством воздуха, он дает пламя, состоящее из трех отдельных слоев – внутреннего сердечника — несгоревшего газа, сине-зеленого слоя и внешнего конуса, где частично окисленный продукт из предварительно перемешанного слоя сгорают в диффузионном пламени. Результирующее пламя показывает сложную серию реакций, а если к газовой смеси добавляется больше воздуха, постепенно диффузионный слой исчезает.
Полезные факты
1) Этилен является природным растительным гормоном, он влияет на рост, развитие, созревание и старение всех растений.
2) Газ не вреден и не токсичен для человека в определенной концентрации (100-150 мг).
3) Он используется в медицине в качестве обезболивающего средства.
4) Действие этилена замедляется при низких температурах.
5) Характерным свойством является хорошая проникающая способность через большинство веществ, например через картонные упаковочные коробки, деревянные и даже бетонные стены.
6) В то время как он имеет неоценимое значение благодаря своей способности инициировать процесс созревания, он также может быть очень вредным для многих фруктов, овощей, цветов и растений, ускоряя процесс старения и снижая качество продукта и его срок годности. Степень повреждения зависит от концентрации, продолжительности воздействия и температуры.
7) Этилен взрывоопасен при высоких концентрациях.
8) Этилен используется в производстве стекла специального назначения для автомобильной промышленности.
9) Изготовление металлоконструкций: газ используется в качестве кислородно-топливного газа для резки металла, сварки и высокой скорости термического напыления.
10) Нефтепереработка: этилен используется в качестве хладагента, особенно на производстве по сжижению природного газа.
11) Как уже говорилось ранее, этилен является очень реактивным веществом, кроме того, он еще и очень легко воспламеняется. Из соображений безопасности, его обычно транспортируют по специальному отдельному газопроводу.
12) Одним из самых распространенных продуктов, изготовленных непосредственно из этилена, является пластмасса.
Источник: fb.rumonateka.com
Этиленгликоль: свойства и область применения
Этиленгликоль и его применение в промышленности
Сегодня большинство промышленных предприятий используют в своем производстве такое вещество, как этиленгликоль, как правило, для производства незамерзающих жидкостей и жидкостей теплоносителей. Спрос на подобного рода продукцию весьма высок. Многие компании, такие как ТК Апрель, работают именно на то, чтобы удовлетворить потребность производств данного вида продукции.
Общие данные и свойства этиленгликоля
- Сам этилен – это олефин, то есть алкеном. Это ненасыщенное соединение, которое содержит двойную связь, очень часто используется в промышленности, поэтому и получило свою популярность.
- Часто этиленгликоль относится к ряду фитогормонов.
- Сам этилен является одним из самых «популярных» органических соединений. Каждый год общее количество его производства растет на 5-7%, а 10 лет назад количество произведенного этилена составило 107 миллионов тонн. Пиролиз этана, бутана, пропана и других газах, которые выделяются в результате нефтедобычи и являются источником, с помощью которого вырабатывается такое большое количество данного олефина.
- Выход этого вещества равняется 30% из всех вырабатываемых газов, что объясняет его большое количество.

Где применяется этилен?
- Данный компонент является одним из основных элементов современной промышленной химии. Самое популярное его применение – это мономер, который используется в процессе применения обычного полиэтилена. Данный мономер, в зависимости от различных условий, предоставляет как полиэтилены высокого, так и полиэтилены низкого давления.
- Этиленгликоль используют также для того, чтобы получить сополимер. Этот элемент часто используется со стиролом, пропиленом и другими подобными этим элементами.
- Также этилен активно используют для производства таких веществ как этилбензола, триэтилбензол и другие компоненты, содержащие этилбензол.
- Наиболее распространенный вариант использования этилена – это производство ацетальдегида и обычного этилового спирта. Еще этиленгликоль используется для хлористого этила в чистом виде.
- В промышленности его используют в качестве сырья для стирола, хлористого винила и тому подобных веществ.
Таким образом, выяснив все положительные характеристики данного вещества, можно с уверенностью сказать, что в современной промышленности этилен http://tk-april.ru/ethylene и пропилен http://tk-april.ru/propyleneglycol — это самые востребованные в производстве вещества, которые на сегодняшний день служат основным сырьем для получения полиэтилена.
nvph.ru
Общие свойства этилена и его применение
Этилен является простейшим из органических соединений, известных как алкены. Это бесцветный горючий газ, имеющий сладковатый вкус и запах. Природные источники включают природный газ и нефть, он также является естественным гормоном в растениях, в которых он ингибирует рост и способствует созреванию плодов. Применение этилена является распространенным явлением в промышленной органической химии. Он производится путем нагревания природного газа, температура плавления составляет 169,4 °С, кипения — 103, 9 °С.
Этилен: особенности структуры и свойства
Углеводороды представляют собой молекулы, содержащие водород и углерод. Они сильно различаются с точки зрения количества одинарных и двойных связей и структурной ориентации каждого компонента. Одним из простейших, но биологически и экономически выгодных углеводородов является этилен. Он поставляется в газообразном виде, является бесцветным и легковоспламеняющимся. Он состоит из двух двойных скрепленных атомов углерода с атомами водорода. Химическая формула имеет вид C2H4. Структурная форма молекулы является линейной из-за наличия двойной связи в центре.
Этилен имеет сладковатый мускусный запах, который позволяет легко идентифицировать вещество в воздухе. Это касается газа в чистом виде: запах может исчезать при смешивании с другими химическими веществами.
Схема применения этилена
Этилен используют в двух основных категориях: в качестве мономера, из которого построены большие углеродные цепи, и в качестве исходного материала для других двух-углеродных соединений. Полимеризации — это повторяющиеся объединения множества мелких молекул этилена в более крупные. Этот процесс происходит при высоких давлениях и температурах. Области применения этилена многочисленны. Полиэтилен – это полимер, который используется особенно массово в производстве упаковочных пленок, проволочных покрытий и пластиковых бутылок. Еще одно применение этилена в качестве мономера касается формирования линейных α-олефинов. Этилен является исходным материалом для приготовления ряда двух-углеродных соединений, таких как этанол (технический спирт), окись этилена (антифриз, полиэфирные волокна и пленки), ацетальдегида и винил хлорида. Кроме этих соединений, этилен с бензолом образует этилбензол, который используется в производстве пластмасс и синтетического каучука. Рассматриваемое вещество является одним из простейших углеводородов. Однако свойства этилена делают его биологически и хозяйственно значимым.
Коммерческое использование
Свойства этилена дают хорошую коммерческую основу для большого количества органических (содержащих углерод и водород) материалов. Одиночные молекулы этилена могут быть соединены вместе для получения полиэтилена (что означает много молекул этилена). Полиэтилен используется для изготовления пластмасс. Кроме того, он может быть использован для изготовления моющих средств и синтетических смазочных материалов, которые представляют собой химические вещества, используемые для уменьшения трения. Применение этилена для получения стиролов актуально в процессе создания резины и защитной упаковки. Кроме того, он используется в обувной промышленности, особенно это касается спортивной обуви, а также при производстве автомобильных покрышек. Применение этилена является коммерчески важным, а сам газ является одним из наиболее часто производимых углеводородов в глобальном масштабе.
Опасность для здоровья
Этилен представляет опасность для здоровья прежде всего потому, что он является легковоспламеняющимся и взрывоопасным. Он также может действовать как наркотик при низких концентрациях, вызывая тошноту, головокружение, головные боли и потерю координации движения. При более высоких концентрациях он действует как анестетик, вызывая потерю сознания, нечувствительность к боли и другим раздражителям. Все эти негативные моменты могут быть причиной для беспокойства в первую очередь для людей, непосредственно работающих с газом. Количество этилена, с которым большинство людей сталкивается в повседневной жизни, как правило, сравнительно небольшое.
Реакции этилена
1) Окисление. Это добавление кислорода, например, при окислении этилена до окиси этилена. Он используется в производстве этиленгликоля (1,2-этандиола), который применяется в качестве незамерзающей жидкости и в производстве полиэфиров путем конденсационной полимеризации.
2) Галогенирование — реакции с этиленом фтора, хлора, брома, йода.
3) Хлорирование этилена в виде 1,2-дихлорэтана и последующая конверсия 1,2-дихлорэтана в винилхлорид мономер. 1,2-дихлорэтан является полезным органическим растворителем, а также является ценным предшественником в синтезе винилхлорида.
4) Алкилирование — добавление углеводородов по двойной связи, например, синтез этилбензола из этилена и бензола с последующим преобразованием в стирол. Этилбензол является промежуточным для производства стирола, одного из наиболее широко используемых виниловых мономеров. Стирол — мономер, используемый для производства полистирола.
5) Горение этилена. Газ получается путем нагревания этилового спирта и концентрированной серной кислоты.
6) Гидратация – реакция с добавлением воды к двойной связи. Наиболее важным промышленным применением этой реакции является превращение этилена в этанол.
Этилен и горение
Этилен – это газ без цвета, который плохо растворяется в воде. Горение этилена в воздухе сопровождается образованием углекислого газа и воды. В чистом виде газ горит световым диффузионным пламенем. Смешанный с небольшим количеством воздуха, он дает пламя, состоящее из трех отдельных слоев – внутреннего сердечника — несгоревшего газа, сине-зеленого слоя и внешнего конуса, где частично окисленный продукт из предварительно перемешанного слоя сгорают в диффузионном пламени. Результирующее пламя показывает сложную серию реакций, а если к газовой смеси добавляется больше воздуха, постепенно диффузионный слой исчезает.
Полезные факты
1) Этилен является природным растительным гормоном, он влияет на рост, развитие, созревание и старение всех растений.
2) Газ не вреден и не токсичен для человека в определенной концентрации (100-150 мг).
3) Он используется в медицине в качестве обезболивающего средства.
4) Действие этилена замедляется при низких температурах.
5) Характерным свойством является хорошая проникающая способность через большинство веществ, например через картонные упаковочные коробки, деревянные и даже бетонные стены.
6) В то время как он имеет неоценимое значение благодаря своей способности инициировать процесс созревания, он также может быть очень вредным для многих фруктов, овощей, цветов и растений, ускоряя процесс старения и снижая качество продукта и его срок годности. Степень повреждения зависит от концентрации, продолжительности воздействия и температуры.
7) Этилен взрывоопасен при высоких концентрациях.
8) Этилен используется в производстве стекла специального назначения для автомобильной промышленности.
9) Изготовление металлоконструкций: газ используется в качестве кислородно-топливного газа для резки металла, сварки и высокой скорости термического напыления.
10) Нефтепереработка: этилен используется в качестве хладагента, особенно на производстве по сжижению природного газа.
11) Как уже говорилось ранее, этилен является очень реактивным веществом, кроме того, он еще и очень легко воспламеняется. Из соображений безопасности, его обычно транспортируют по специальному отдельному газопроводу.
12) Одним из самых распространенных продуктов, изготовленных непосредственно из этилена, является пластмасса.
autogear.ru
Первый представитель алкенов — этилен. Физические свойства, получение, применение этилена
Яркий представитель непредельных углеводородов — этен (этилен). Физические свойства: бесцветный горючий газ, взрывоопасный в смеси с кислородом и воздухом. В значительных количествах этилен получают из нефти для последующего синтеза ценных органических веществ (одноатомных и двухатомных спиртов, полимеров, уксусной кислоты и других соединений).
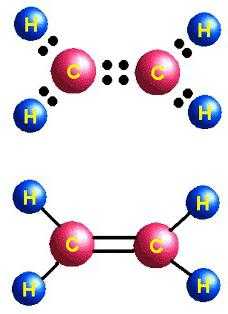
Углеводороды, сходные по строению и свойствам с этеном, называются алкенами. Исторически закрепился еще один термин для этой группы — олефины. Общая формула CnH2n отражает состав всего класса веществ. Первый его представитель — этилен, в молекуле которого атомы углерода образуют не три, а всего две õ-связи с водородом. Алкены — непредельные или ненасыщенные соединения, их формула C2H4. Смешиваются по форме и энергии только 2 p- и 1 s-электронное облако атома углерода, всего формируются три õ-связи. Это состояние называется sp2-гибридизацией. Четвертая валентность углерода сохраняется, в молекуле возникает π-связь. В структурной формуле особенность строения находит отражение. Но символы для обозначения разных типов связи на схемах обычно используются одинаковые — черточки или точки. Строение этилена определяет его активное взаимодействие с веществами разных классов. Присоединение воды и других частиц происходит благодаря разрыву непрочной π-связи. Освободившиеся валентности насыщаются за счет электронов кислорода, водорода, галогенов.
Этилен: физические свойства вещества
Этен при обычных условиях (нормальном атмосферном давлении и температуре 18°C) — бесцветный газ. Он обладает сладким (эфирным) запахом, его вдыхание оказывает наркотическое действие на человека. Затвердевает при –169,5°C, плавится при таких же температурных условиях. Кипит этен при –103,8°C. Воспламеняется при нагревании до 540°C. Газ хорошо горит, пламя светящееся, со слабой копотью. Этилен растворяется в эфире и ацетоне, значительно меньше — в воде и спирте. Округленная молярная масса вещества — 28 г/моль. Третий и четвертый представители гомологического ряда этена — тоже газообразные вещества. Физические свойства пятого и следующих алкенов отличаются, они являются жидкостями и твердыми телами.
Получение и свойства этилена
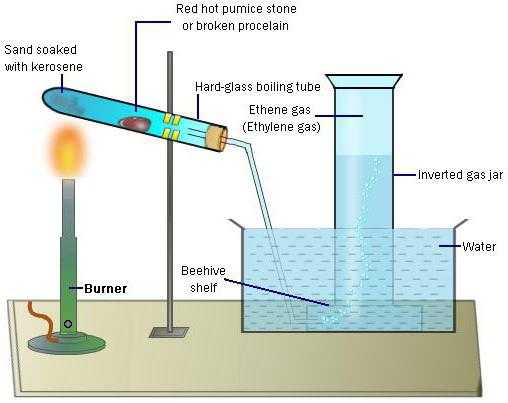
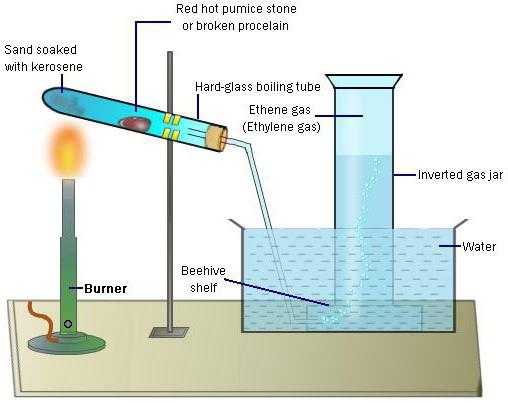
Немецкий химик Иоган Бехер случайно использовал этиловый спирт в опытах с концентрированной серной кислотой. Так впервые был получен этен в лабораторных условиях (1680 год). В середине XIX века А.М. Бутлеров дал соединению название этилен. Физические свойства и химические реакции также были описаны известным русским химиком. Бутлеров предложил структурную формулу, отражающую строение вещества. Способы его получения в лаборатории:
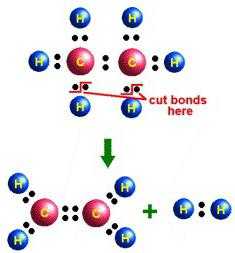
- Каталитическое гидрирование ацетилена.
- Дегидрогалогенирование хлорэтана в реакции с концентрированным спиртовым раствором сильного основания (щелочи) при нагревании.
- Отщепление воды от молекул этилового спирта (дегидратация). Проходит реакция в присутствии серной кислоты. Ее уравнение: Н2С–СН2–OH → Н2С=СН2 + Н2О
Промышленное получение:
- переработка нефти — крекинг и пиролиз углеводородного сырья;
- дегидрирование этана в присутствии катализатора. H3C–CH3 → H2C=CH2 + H2
Строение этилена объясняет его типичные химические реакции — присоединение частиц атомами C, которые находятся при кратной связи:
- Галогенирование и гидрогалогенирование. Продуктами этих реакций являются галогенопроизводные.
- Гидрирование (насыщение водородом), получение этана.
- Окисление до двухатомного спирта этиленгликоля. Его формула: OH–h3C–Ch3–OH.
- Полимеризация по схеме: n(h3C=Ch3) → n(-h3C–Ch3-).
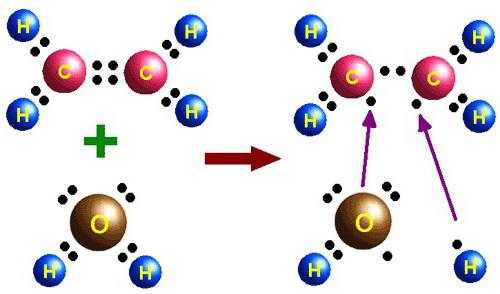
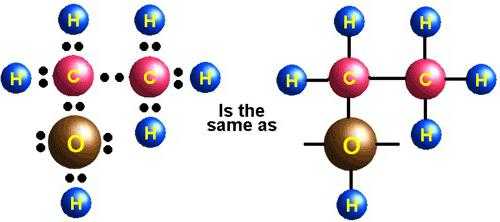
Области применения этилена
При фракционной перегонке нефти в больших объемах получают этилен. Физические свойства, строение, химическая природа вещества позволяют использовать его в производстве этилового спирта, галогенопроизводных, спиртов, оксида, уксусной кислоты и других соединений. Этен — мономер полиэтилена, а также исходное соединение для полистирола.
Дихлорэтан, который получают из этена и хлора, является хорошим растворителем, используется в производстве поливинилхлорида (ПВХ). Из полиэтилена низкого и высокого давления изготавливают пленку, трубы, посуду, из полистирола — футляры для CD-дисков и другие детали. ПВХ — это основа линолеума, непромокаемых плащей. В сельском хозяйстве этеном обрабатываются плоды перед уборкой урожая для ускорения созревания.
fb.ru
Вопрос 10 § 48-54 Химия Рудзитис, Фельдман 9 класс
Этилен — непредельный углеводород, простей-
ший алкен, имеет формулу С2Н4. Представляет
хом. Хорошо растворим в диэтиловом эфире и
углеводородах. Частично растворим в воде и эта-
ноле. Химически активен. Вступает в следующие
реакции:
1. Галогенирование:
2. Гидрирование:
3. Гидрогалогенирование:
4. Гидратация:
5. Горение:
6. Полимеризация:
В результате образуется полимер — полиэтилен
(-СН2-СН2-)n, который является самым распро-
страненным пластиком в мире. Полиэтилен при-
меняют в качестве упаковочной пленки (пакеты,
скотч), тары (бутылки, канистры), для изготовле-
ния труб (канализационные, водоснабжения), как
электроизоляционный материал. Полимер пропиле-
на (пропена) называют полипропиленом. Его по-
лучают полимеризацией пропилена в присутствии
катализаторов:
и используют для производства пленок, тары,
труб, деталей технической аппаратуры, предметов
домашнего обихода, в строительстве для вибро- и
шумоизоляции.
Этилен применяют в качестве мономера при
получении полиэтилена, как исходный материал
для синтеза органических веществ (этилацетата,
хлористого винила, 1,2-дихлорэтана и др.), для
ускорения созревания плодов.
class.rambler.ru