59. Глюкоза. Физические свойства
Глюкоза – бесцветное кристаллическое вещество, хорошо растворимое в воде, сладкое на вкус (лат. «глюкос» – сладкий):
1) она встречается почти во всех органах растения: в плодах, корнях, листьях, цветах;
2) особенно много глюкозы в соке винограда и спелых фруктах, ягодах;
3) глюкоза есть в животных организмах;
4) в крови человека ее содержится примерно 0,1 %.
Особенности строения глюкозы
1. Состав глюкозы выражается формулой: С6Н12O6, она принадлежит к многоатомным спиртам.
2. Если раствор этого вещества прилить к свежеосажденному гидроксиду меди (II), образуется ярко-синий раствор, как в случае глицерина.
Опыт подтверждает принадлежность глюкозы к многоатомным спиртам.
3. Существует сложный эфир глюкозы, в молекуле которого пять остатков уксусной кислоты. Из этого следует, что в молекуле углевода пять гидроксильных групп. Этот факт объясняет, почему глюкоза хорошо растворяется в воде и имеет сладкий вкус.
Если раствор глюкозы нагреть с аммиачным раствором оксида серебра (I), то получится характерное «серебряное зеркало».
Шестой атом кислорода в молекуле вещества входит в состав альдегидной группы.
4. Чтобы составить полное представление о строении глюкозы, надо знать, как построен скелет молекулы. Поскольку все шесть атомов кислорода входят в состав функциональных групп, следовательно, атомы углерода, образующие скелет, соединены друг с другом непосредственно.
5. Цепь атомов углерода прямая, а не разветвленная.
6. Альдегидная группа может находиться только в конце неразветвленной углеродной цепи, и гидроксильные группы могут быть устойчивы, находясь лишь у разных атомов углерода.
7. Глюкоза одновременно и альдегид, и многоатомный спирт: она альдегидоспирт.
8. В растворе глюкозы содержатся молекулы не только с открытой цепью атомов, но и циклические, в которых нет альдегидной группы.
9. Процесс превращения альдегидной формы в циклическую обратим. В растворе существует подвижное равновесие между ними. Данное явление называется мутаротацией.
Молекул, которые содержат альдегидную группу, недостаточно, чтобы ярко проявилась реакция глюкозы с фуксинсернистой кислотой.
60. Химические свойства глюкозы и ее применение
Химические свойства альдегидной формы глюкозы:
а) глюкоза – это вещество с двойственной химической природой;
б) как многоатомный спирт глюкоза образует сложные эфиры;
в) как альдегид она окисляется. Окислительное действие аммиачного раствора оксида серебра (I) на глюкозу можно записать следующим образом:
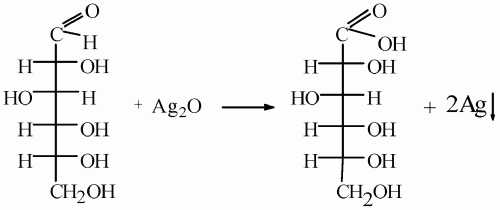
г) окислителем альдегидной группы глюкозы может служить и гидроксид меди (II). Если к небольшому количеству свежеосажденного гидроксида меди (II) прилить раствор глюкозы и смесь нагреть, то образуется красный оксид меди (I). Уравнение реакции окисления глюкозы гидроксидом меди (II) аналогично уравнению для альдегидов;
д) альдегидная группа глюкозы может быть восстановлена.
Тогда образуется шестиатомный спирт (сорбит): СН2ОН-СНОН-СНОН-СНОН-СНОН-СН2ОН.
Виды брожения.
1. Спиртовое брожение идет под действием фермента дрожжей: С6Н12O6 → 2С2Н5ОН + 2СO2.
2. Под действием фермента молочнокислых бактерий происходит молочнокислое брожение глюкозы: C6H12O6 → 2СН3-СН(ОН) – СOОН – молочная кислота.
Особенности молочной кислоты:
1) это соединение с двойственной химической функцией, в ней сочетаются свойства спирта и карбоновой кислоты;
2) процесс образования молочной кислоты происходит при скисании молока;
3) появление кислоты в молоке можно установить при помощи лакмуса;
4) молочнокислое брожение имеет большое значение в переработке сельскохозяйственных продуктов;
5) с ним связано получение молочных продуктов: простокваши, творога, сметаны, сыра;
6) молочная кислота образуется в процессе квашения капусты, силосования кормов и выполняет при этом консервирующую роль.
Способы применения глюкозы.
1. Глюкоза – ценное питательное вещество.
2. Крахмал пищи в пищеварительном тракте превращается в глюкозу, которая кровью разносится по всем тканям и клеткам организма.
3. Как вещество, легко усваиваемое организмом и дающее ему энергию, глюкоза находит и непосредственное применение в качестве укрепляющего лечебного средства.
4. Сладкий вкус обусловил применение ее в кондитерском деле (в составе патоки) при изготовлении мармелада, карамели, пряников и т. д.
studfiles.net
глюкоза и сахароза » mozok.click
Понятие об углеводах и их классификация
В природе большое значение имеют углеводы (сахариды) — органические соединения с общей формулой Cn(h3O)m (m, n > 3).. Название этого класса соединений происходит от их свойства разлагаться на углерод и воду при нагревании или под действием концентрированной сульфатной кислоты, что также отображено в их общей формуле (рис. 36.1).
Рис. 36.1. Под действием концентрированной сульфатной кислоты углеводы разлагаются на углерод и воду
Углеводы делятся на простые (моносахариды) и сложные (дисахариды и полисахариды) (схема 6). Принципиально они отличаются тем, что сложные углеводы при определенных условиях гидролизуются до простых (разлагаются), а простые уже гидролизоваться не могут. Молекулы дисахаридов состоят из двух, а полисахаридов — из большого количества остатков молекул моносахаридов.
Схема 6. Классификация углеводов
Глюкоза
Глюкоза C6H12O6 — самый распространенный углевод в живой природе, именно она является одним из продуктов процесса фотосинтеза, в результате которого растения накапливают энергию Солнца.
Глюкоза — бесцветное кристаллическое вещество без запаха, плотность — 1,54 г/см3, температура плавления — 146 °С. При нагревании выше этой температуры вещество разлагается, не доходя до точки кипения. Глюкоза сладкая на вкус, но в полтора раза менее сладкая, чем сахароза. Хорошо растворяется в воде: в 100 г воды при 0 °С растворяется 32 г глюкозы, а при 25 °С — 82 г, плохо растворяется в органических растворителях. Ее растворы не проводят электрический ток (глюкоза — неэлектролит).
Молекула глюкозы содержит несколько групп -OH, как глицерол, поэтому, подобно ему, она может взаимодействовать со свежеосажденным купрум(П) гидроксидом (рис. 36.2, а и б):
При нагревании глюкоза разлагается, как и все углеводы, на углерод и воду:
Глюкоза — один из основных продуктов обмена веществ в живых организмах. В природе она образуется в зеленых частях растений в процессе фотосинтеза, который происходит с поглощением солнечного света:
Возможна также и обратная реакция:
Этим уравнением можно описать суммарный процесс, в результате которого все животные получают энергию для своей жизнедеятельности: глюкоза попадает в наш организм вместе с пищей, кислород мы вдыхаем легкими, а продукт реакции — углекислый газ — выдыхаем. Также это уравнение описывает процесс горения и взрыва глюкозы. Поджечь глюкозу достаточно сложно, она горит только в присутствии катализатора, а взрывается при очень сильном измельчении (см. § 20).
В растениях глюкоза превращается в сложные углеводы — крахмал и целлюлозу:
Рис. 36.2. Качественная реакция на глюкозу: а — свежеосажденный купрум(И) гидроксид; б — при наличии глюкозы осадок исчезает, образуется соединение темно-синего цвета
Синтезировать глюкозу методами органической химии гораздо сложнее. Впервые этот синтез реализовал Эмиль Фишер.
С растительной пищей углеводы попадают в организм животных, где они являются основным источником энергии. Так, из 1 г углеводов организм получает около 17 кДж (4 ккал). Если эта энергия не расходуется полностью, организм откладывает ее «про запас», направляя на синтез жиров.
Впервые глюкозу выделили из винограда, поэтому ее также называют виноградным сахаром. В чистом виде глюкоза содержится в сладких ягодах и фруктах: она обусловливает сладость некоторых частей растений (ягод, плодов, корнеплодов и др.). Вместе с фруктозой она содержится в составе меда.
Содержание глюкозы в крови человека составляет около 0,1 %, отклонение этого показателя от нормы свидетельствует о заболевании сахарным диабетом. Содержание глюкозы в крови (часто этот показатель называют просто «сахар в крови») контролируют, проводя клинический анализ крови. Этот анализ можно сделать и дома с помощью специального устройства — глюкометра (рис. 36.4).
Немецкий химик-органик, лауреат Нобелевской премии по химии 1902 года. Высшее образование получил в университетах Бонна и Страсбурга. В 22 года, после защиты диссертации, стал преподавателем Страсбургского университета. Фишер впервые определил строение некоторых органических веществ: кофеина, пурина, мочевой кислоты, глюкозы и фруктозы. Открыл методы их синтеза. Установил особенности реакций с участием ферментов, предложил классификацию белков. За исследования и синтез сахаридов и производных пурина получил Нобелевскую премию. В его честь Немецкое химическое общество учредило медаль Эмиля Фишера.
В промышленности глюкозу добывают гидролизом крахмала или целлюлозы. Но чистая глюкоза не имеет широкого применения. Такую глюкозу используют в различных биологических и биохимических исследованиях. В медицине ее используют для проведения глюкозотолерантного теста — исследования, позволяющего диагностировать сахарный диабет. При некоторых заболеваниях раствор глюкозы вводят человеку внутривенно. В пищевой промышленности в качестве подсластителя ее используют мало: она дороже и менее сладкая, чем сахар.
Для глюкозы характерна реакция брожения. Под действием молочнокислых бактерий из глюкозы образуется молочная кислота:
Эта реакция происходит при скисании молока и является основой изготовления различных молочнокислых продуктов — простокваши, йогуртов, сыра, сметаны и др. Молочнокислое брожение происходит при квашении капусты и других овощей, предотвращает развитие гнилостных бактерий и способствует длительному хранению продуктов. Этот процесс также может происходить в ротовой полости, что вызывает кариес зубов.
Сахароза
Наибольшее значение среди дисахаридов имеет сахароза C12H22O1r Это химическое название обычного сахара, получаемого из сахарной свеклы или сахарного тростника.
Сахароза — бесцветное кристаллическое вещество без запаха, плотность — 1,59 г/см3, температура плавления — 186 °С. Сахароза сладкая на вкус (в полтора раза слаще глюкозы). Очень хорошо растворяется в воде: в 100 г воды при 0 °С растворяется 179 г сахарозы, а при 100 °С — 487 г.
Как и глюкоза, сахароза разлагается при нагревании:
Эта реакция происходит при изготовлении карамели и выпекании пирожных и тортов, благодаря ей образуется сладкая карамелизирован-ная корочка со специфическим привкусом жженого сахара (рис. 36.5).
Как и большинство органических веществ, сахароза может гореть с образованием углекислого газа и воды:
Но если просто пытаться поджечь сахар, то он не воспламенится: для этого нужен катализатор — соли Лития. Сильно измельченный сахар может не только гореть — его взвесь в воздухе может взорваться, о чем говорилось в § 20.
Рис. 36.5. Плавление сахарозы сопровождается изменением цвета и появлением специфического запаха карамели
Сахарозу называют дисахаридом, поскольку молекула сахарозы состоит из остатков молекул двух моносахаридов — глюкозы и фруктозы, соединенных между собой.
При гидролизе сахарозы в кислой среде или под действием ферментов связь между этими остатками разрывается и образуются молекулы глюкозы и фруктозы:
Такое преобразование происходит в организмах пчел: собирая нектар с цветков, они потребляют сахарозу, которая затем гидролизуется. Поэтому мед — это смесь равных количеств глюкозы и фруктозы, конечно, с примесями других веществ (рис. 36.6).
В больших количествах сахароза содержится только в трех растениях: сахарной свекле и сахарном тростнике, используемых для промышленного производства сахара, а также в сахарном клене (из него
получают кленовый сироп). Для привлечения насекомых сахароза в небольшом количестве содержится в нектаре цветов, а также во фруктах и ягодах.
В Украине сахарная промышленность — одна из старейших и самых важных отраслей пищевой промышленности, продукция которой является ценным продуктом экспорта. Значительный вклад в развитие сахарной отрасли в Украине сделал выдающийся украинский ученый Н. А. Бунге.
Выдающийся украинский химик, профессор Киевского университета. Родился в Варшаве. Окончил Киевский университет, в котором с 1870 года преподавал техническую химию. Основные научные достижения относятся к технической химии, в частности виноделию, сахарному производству. Усовершенствовал технологию производства сахара из сахарной свеклы. Исследовал технологию образования сахарных кристаллов, условия образования, состав и преобразование свекольного студня. Организовал техническую школу по сахароварению, опубликовал 33 тома «Ежегодника свеклосахарной промышленности». Был одним из организаторов газового и электрического освещения, а также водоснабжения Киева.
Сегодня в Украине около 100 сахарных заводов с общей максимальной мощностью около 7 млн тонн в год. На этих предприятиях могут производить сахар как из свеклы (местное сырье), так и из тростника (экспортируют обычно из Кубы). Самым большим заводом является Лохвицкий сахарный комбинат (Полтавская область) с ежедневной мощностью 9300 тонн сахара. В последние годы в Украине производят около 2 млн тонн сахара ежегодно, часть которого идет на экспорт.
• Коричневый сахар — это обычный тростниковый сахар, который в процессе производства недочистили от примесей. Интересно, что в его производстве меньше технологических процессов (отсутствует окончательная очистка), в производстве он дешевле, но в продаже гораздо дороже обычного белого сахара.
• Слова «сахароза» и «сахар» происходят от древнеиндийского «саркара», что означает кусочки кристаллического вещества, образующиеся при сгущении сока сахарного тростника.
ЛАБОРАТОРНЫЙ ОПЫТ № 12
Взаимодействие глюкозы с купрум(11) гидроксидом
Оборудование: штатив с пробирками.
Реактивы: растворы глюкозы и сахарозы, CuSO4, NaOH.
Правила безопасности:
• для опытов используйте небольшие количества реактивов;
• остерегайтесь попадания реактивов на кожу, в глаза, на одежду; при попадании едкого вещества смойте его большим количеством воды и протрите поврежденное место разбавленным раствором боратной кислоты.
Получите купрум(П) гидроксид: к 1-2 мл раствора щелочи в пробирке долейте несколько капель раствора купрум(П) сульфата. К образовавшемуся осадку добавляйте по капле раствор глюкозы до растворения осадка купрум(П) гидроксида. Перемешайте смесь. Что происходит? В какой цвет окрашивается раствор? Какие выводы о строении молекул глюкозы можно сделать по результатам опыта?
Повторите опыт, но вместо раствора глюкозы используйте раствор сахарозы. Есть ли отличия в ваших наблюдениях? Изменятся ли результаты опыта, если вместо глюкозы и сахарозы использовать глицерол?
Ключевая идея
Углеводы являются материальными носителями энергии, они обеспечивают перенос энергии Солнца от растений к животным.
Контрольные вопросы
437. Дайте определение класса углеводов.
438. Как классифицируют углеводы? Приведите примеры представителей каждой группы углеводов.
439. Охарактеризуйте физические свойства глюкозы и сахарозы.
440. В результате какого процесса образуется глюкоза в природе?
441. Какая реакция является качественной на глюкозу?
442. Опишите распространенность и применение глюкозы и сахарозы. Какие свойства этому причиной?
Задания для усвоения материала
443. Из приведенных формул веществ выпишите формулы углеводов: C3H8O,
C5H10O5′ C12H26O2′ C12H22O1V C6H12O‘
444. Вычислите массовые доли Карбона и воды: а) в глюкозе; б) в сахарозе. В каком из этих веществ больше Карбона, а в каком — воды?
445. Сравните количество теплоты, которое получает организм из 1 г жира и из 1 г глюкозы. Как вы считаете, почему углеводы являются основным источником энергии для животных, а жиры — только резервным источником?
446. Определите неизвестное вещество X и составьте уравнения реакций, отвечающие такой схеме превращений:
447. В медицине для инъекций используют раствор глюкозы с массовой долей около 5 %. Вычислите массу глюкозы, необходимую для приготовления такого раствора массой 1 кг.
448. При сгорании глюкозы количеством вещества 1 моль выделяется 2800 кДж энергии. Составьте термохимическое уравнение реакции.
449. По данным из предыдущего задания составьте термохимическое уравнение реакции фотосинтеза.
450. При гидролизе сахарозы образовалось 360 г смеси глюкозы и фруктозы. Определите, какие массы сахарозы и воды прореагировали.
451. Одно дерево за сутки в среднем превращает в углеводы углекислый газ массой 55 г. Какая масса глюкозы при этом образуется?
452. В процессе фотосинтеза зеленые растения нашей планеты ежегодно поглощают 200 млрд тонн углекислого газа. Какой объем кислорода (н. у.) выделяется при этом в атмосферу?
453*. В телевизионной рекламе можно услышать, что после еды в ротовой полости нарушается кислотно-щелочной баланс и чтобы его восстановить, нужно жевать резинку с карбамидом. Как вы считаете, каким образом нарушается этот баланс? В результате какого процесса он нарушается? Какова роль карбамида в восстановлении баланса?
454*. На этикетке пищевых продуктов обязательно указывают содержание питательных веществ: жиров, белков и углеводов. Рассмотрите этикетки пищевых продуктов, которые вы часто употребляете (напитки, снеки, шоколадки и др.), и оцените массу сахара, которую вы потребляете с этими продуктами ежедневно. Сравните полученную массу с рекомендованной диетологами суточной дозой углеводов.
Это материал учебника Химия 9 класс Григорович
mozok.click
Глюкоза
Кристаллы глюкозы имеют белый цвет и приятный сладкий вкус. Глюкоза хорошо усваивается организмом, быстро восстанавливая силы человека. Она менее сладкая, чем сахароза, и не маскирует аромат и вкус других веществ в пищевых продуктах. Используют глюкозу для приготовления отдельных сортов кондитерских изделий, напитков, мороженого, для подслащивания вин, при производстве продуктов для детей.
Глюкоза кристаллизуется в разных формах в зависимости от температуры и концентрации раствора. При температуре 0-50 °С выкристаллизовывается моногидратная глюкоза. Ее кристаллы относятся к моноклинической системе, имеют вид тонких пластинок. При температуре выше 50 °С и концентрации раствора более 70 % образуются кристаллы ангидридной глюкозы С6Н206 ромбической системы в виде пластинок удлиненной призматической формы (рис. 14). Температура плавления глюкозы (в °С): моногидратной — 86-90, ангидридной — 146-147 Глюкоза хорошо растворима в воде. При повышении температуры насыщенные растворы глюкозы становятся более вязкими. Понижение растворимости глюкозы при охлаждении растворов может вызвать засахаривание таких продуктов, как варенье.
Крахмалопаточная промышленность вырабатывает глюкозу разной степени очистки: кристаллическую, медицинскую, пищевую и техническую. Глюкозу получают в основном из кукурузного крахмала. Гидролизаты, полученные кислотным или ферментативным способом, после очистки уваривают. Для ускорения кристаллизации в сироп, охлажденный до 44 °С, вводят кристаллическую затравку. По мере остывания сиропа до 25 °С в течение 3-4 суток выделяются кристаллы гидратной глюкозы и сироп превращается в утфель — смесь кристаллов глюкозы и межкристалльного раствора.
Кристаллическую глюкозу отделяют на центрифугах от раствора и промывают водой. Чистые кристаллы сушат, удаляя свободную влагу, пропускают через магнитные сепараторы, просеивают на ситах с отверстиями 1-1,5 мм для отделения крупки.
Гидратная глюкоза по внешнему виду — белый кристаллический порошок. Она должна быть сладкой, не иметь посторонних привкусов и запахов. Нормируются цветность и прозрачность растворов глюкозы. Цветность — не более 0,18 ед. оптической плотности; прозрачность, светопропускание — не менее 65%. Массовая доля влаги не более 9 %, золы — не более 0,07 % в пересчете на сухое вещество. Нормы удельного вращения характеризуют содержание чистой глюкозы.
Пищевую глюкозу вырабатывают из глюкозного утфеля без выделения кристаллов. Это закристаллизованная масса желтого цвета, сладкого вкуса, без запаха. Она состоит из глюкозы, низкомолекулярных декстринов, олигосахаридов, продуктов конденсации и разложения глюкозы. Влажность пищевой глюкозы не должна превышать 20 %, содержание редуцирующих веществ должно составлять не менее 85, зольность — не более 0,8-1,2 % в пересчете на сухое вещество. Пищевую глюкозу используют вместо кристаллической в производстве антибиотиков и для других целей.
Для медицинских целей глюкоза должна иметь высокую степень чистоты, не допускается заражение ее микробами. Медицинскую глюкозу кристаллизуют из дополнительно очищенных растворов. Применяют перекристаллизацию в условиях, при которых образуется глюкоза в ангидридной форме. Она состоит из однородных кристаллов с меньшим количеством примесей.
Кристаллическую глюкозу массой по 50 кг упаковываю в тканевые мешки с бумажными вкладышами (не менее четырех слоев) или из полиэтиленовой пленки, герметически закрывающиеся путем сварки или склеивания.
Глюкозу фасуют массой 100-1000 г в мелкую тару — пакеты из неворсистой ткани или (бумажные кулаки и коробки. Особенностью маркировки является нанесение предупредительного знака «Боится сырости».
Хранят глюкозу при относительной влажности воздуха не более 75 % При увлажнении отсыревшая глюкоза комкуется, вкус и запасе ухудшаются в результате забраживания. При длительном Хранении глюкоза желтеет, особенно при повышенной температуре. Срок хранения кристаллической гидратной глюкозы — год со дня выработки.
www.comodity.ru
Глюкоза. Эволюция стиля: от начала карьеры до наших дней

Всего за несколько лет на наших глазах певица Глюкоза превратилась из угловатой девочки-подростка в очень женственную и нежную женщину и маму двоих замечательных дочек. Коротки майки, рваные джинсы и ботинки на огромной платформе сменились красивыми женственными платьями и изящными шпильками. Но, даже кардинально поменяв стиль, Наталья Ионова (настоящее имя Глюкозы) не потеряла свою индивидуальность. Она всячески подчеркивает свою стройную фигуру и предпочитает ультракороткое мини и полупрозрачные ткани.
 2003 г.
2003 г.В начале своей карьеры Глюкоза явно подражала известной певице Гвен Стефани и носила прическу в виде скрученных узелков один в один, как ее американская коллега.
 2004 г.
2004 г.Такой спортивный образ с леггинсами и наколенниками больше подходит для катания на роликах в парке, чем для выступления на сцене.
 2004 г.
2004 г.Нежно-голубое платье очень идет блондинке Наташе, но странная шапочка для душа на голове и огромные ботинки явно не вписываются в образ.
 2005 г.
2005 г.Помните, как еще недавно многие женщины и девушки ходили в велюровых спортивных костюмах Juicy Couture? Не смогла устоять перед успешным трендом и Глюкоза. Сейчас такой фасон — настоящий модный моветон.
 2005 г.
2005 г.Платье в японском стиле очень странно смотрится с джинсами и поясной сумкой. Не спасают ситуацию даже подобранные в тон сумки сапоги.
 2006 г.
2006 г.Романтическое платье на тонких бретелях подчеркивает хрупкость и юный возраст певицы. Но принт на нем мог быть более молодежным и интересным. Этот скорее напоминает рисунок на шейном платке.
 2006 г.
2006 г.Повседневный образ без особой «изюминки» — удобный и практичный.
 2007 г.
2007 г.Стройная Наташа может себе позволить пышную юбку и много драпировки. Получился образ в её любимом стиле хиппи.
 2008 г.
2008 г.Глюкозе здесь явно не хватает аксессуаров и украшений, поэтому платье смотрится немного скучно. Красные колготки и ботильоны в цвет говорят о том, что певица любит похулиганить, выбирая наряд, и не относится к своей внешности слишком серьезно.
 2008 г.
2008 г.Глюкоза выбрала наряд в стиле «Боже, храни Королеву!». В нем все продумано до мелочей — топ с британским флагом и портретом Елизаветы II, а на ногах — ботинки с традиционной шотландской клеткой.
 2009 г.
2009 г.Здесь мы наблюдаем уже изменившийся стиль певицы. Женственное платье и роскошное ожерелье очень идут Глюкозе.
 2009 г.
2009 г.Платье-бюстье с цветочным принтом — настоящая летняя классика. Босоножки с множеством ремешков делают образ более актуальным и даже бунтарским.
 2010 г.
2010 г.Длинноногая Наташа — одна из немногих наших звезд, кто осмелился выйти на публику в таком откровенном трикотажном платье от Missoni.
 2010 г.
2010 г.На презентацию Глюкоза выбрала пышное ассиметричное платье. В таком наряде очень важно подчеркнуть талию, как это сделала певица, иначе фигура будет выглядеть абсолютно бесформенной.
 2011 г.
2011 г.Строгий лаконичный смокинг Глюкоза уравновесила забавной бахромой на юбке.
 2011 г.
2011 г.Странная юбка с бесчисленными рядами рюшей смотрится очень театрально. А кожаная упряжь — агрессивно.
 2012 г.
2012 г.Для выступления на музыкальной премии Глюкоза выбрала наряд с блестящими паетками в стиле диско 80-х годов. А кожаная перчатка на одной руке напоминает сценические образы Майкла Джексона.
 2013 г.
2013 г.Сложный крой платья добавляет этому образу оригинальности, а полупрозрачная ткань подчеркивает женственность Натальи.
 2014 г.
2014 г.Нечасто Глюкозу можно увидеть в таком элегантном и сдержанном платье в пол. Здесь она выглядит как настоящая леди.
 2014 г.
2014 г.Раз в году даже взрослая девушка может нарядиться принцессой. Блестящее платье с пышным тюлем отлично подходит для новогодних мероприятий.
 2015 г.
2015 г.Роскошное платье цвета благородной бронзы подчеркивает смуглую кожу и золотистый оттенок волос Глюкозы. Изящные босоножки с тонким ремешком отлично дополняют наряд.
 2015 г.
2015 г.В начале своей карьеры Глюкоза уже примеряла сценический образ невесты. Но этот, согласитесь, гораздо элегантнее предыдущего.
www.goodhouse.ru
Углеводы. Глюкоза. Химические свойства глюкозы. Применение глюкозы на основе свойств
Доброе время суток, уважаемые десятиклассники!
Мы начинаем знакомиться с новой группой органических соединений — углеводами.Углеводы… А это те самые сладости, которые вы так любите, (фрукты, торты, конфеты, варенье, шоколад и т.д., особенно много углеводов содержит виноград). Углеводы жизненно важные вещества, которые необходимы каждому организму. Эти вещества расходуются, и человек должен постоянно пополнять их запасы. Понятно, что вещества, входящие в состав тканей организма, не похожие на те, которые он употребляет в пищу. Организм человека перерабатывает пищевые продукты и в процессе своей жизнедеятельности постоянно расходует энергию, которая, как мы знаем, выделяется при окислении в тканях организма, углеводы входят в состав нуклеиновых кислот, осуществляющих биосинтез белка и передачу наследственных признаков.
Животные и человек не синтезируют углеводы. В зеленых растениях при участии хлорофилла и солнечного света осуществляется ряд процессов преобразования поглощенной из воздуха углекислого газа и впитанной из почвы воды. Конечным продуктом этих процесса – фотосинтеза, является сложная молекула углевода.
Углеводы – важный источник энергии для организма, участвуют в обмене веществ. Основными источниками углеводов являются растительные продукты.
Физиологи установили, что при физической нагрузке, которая в 10 раз превышает привычную, человек, соблюдающий жировую диету, лишается сил уже через полчаса. А вот углеводная диета позволяет выдержать такую же нагрузку в течение четырех часов. Оказывается, получение организмом энергии из жиров – процесс длительный. Это объясняется малой реакционной способностью жиров, особенно их углеводородных цепей. Углеводы же, хотя и дают меньше энергии, чем жиры, однако выделяют ее намного быстрее. Поэтому, если предстоит основательная нагрузка, предпочтительнее подкрепиться сладким, а не жирным.
Классификация углеводов.
Углеводы – обширный класс природных соединений.Обратимся к схеме 1. “Классификация углеводов”. В зависимости от числа остатков моносахаридов в молекуле делятся на моносахариды, дисахариды и полисахариды.
Моносахариды (простые углеводы) – углеводы, которые не гидролизуются. В зависимости от числа атомов углерода подразделяются на триозы, тетрозы, пентозы, гексозы. Для человека наиболее важны глюкоза, фруктоза, галактоза, рибоза, дезоксирибоза.
Дисахариды – углеводы, которые гидролизуются с образованием двух молекул моносахаридов. Наиболее важны для человека сахароза, мальтоза и лактоза.
Полисахариды – высокомолекулярные соединения – углеводы, которые гидролизуются с образованием множества молекул моносахаридов. Они делятся на перевариваемые и неперевариваемые в желудочно-кишечном тракте. К перевариваемым относят крахмал и гликоген, из вторых для человека важны клетчатка, гемицеллюлоза и пектиновые вещества.
Углеводы часто называют сахаристыми веществами или сахарами. Они могут быть безвкусными, сладкими и горькими. Если сладость раствора сахарозы принимать за 100 %, то сладость фруктозы – 173 %, глюкозы – 81 %, мальтозы и галактозы – 32 %, лактозы – 16 %.
Качественный состав углеводов.
Углеводы – органические соединения, состоящие из углерода, водорода и кислорода, причем водород и кислород входят в соотношении (2 : 1) как в воде, отсюда и название.
На основе этой аналогии русский химик К. Шмидт в 1844 г. предложил термин углевода (углерод и вода), а общая формула углеводов Сn(Н2О)m
Итак, важнейшим представителем моносахаридов является глюкоза. При изучении, каких некоторых тем мы встречались с вами с этим веществом в курсе химии и биологии: химия – альдегиды, спирты; биология – фотосинтез, строение клетки.
Получение глюкозы.
1. Реакция фотосинтеза.6СО2 + 6H2O –> С6Н12 О6 + 6О2 +Q
2. Реакция полимеризации.
3. Гидролиз крахмала.
(С6Н10О5)n + nH2O –> nС6Н12О6
Физические свойства:
бесцветное кристаллическое вещество, хорошо растворимо в воде, сладкое на вкус, температура плавления 146оС.
Строение молекулы глюкозы. Изомерия.
Вывод: таким образом, глюкоза – альдегидоспирт, точнее – многоатомный альдегидоспирт.Установлено, что в растворе глюкозы находится не только её альдегидная форма; но и молекулы циклического строения.Установлено, что у третьего атома углерода группа – ОН расположена иначе, чем у других атомов углерода распространённое строение глюкозы выглядит так:

Превращение молекулы линейного строения в молекулу циклического строения объяснимо, если вспомнить что атомы углерода могут вращаться вокруг сигма -связей. Альдегидная группа может приблизиться к гидроксильной группе 5-го атома углерода, поскольку атом кислорода карбонильной группы несёт на себе частичный – заряд, а атом водород гидроксильной группы – частично + заряд.
Осуществляется своеобразный химический процесс: происходит разрыв -связи карбонильной труппы, к атому кислорода присоединяется атом водорода, а атом кислорода гидроксильной группы с атомом углерода замыкают цепь. Циклические формы находятся в равновесии, превращаясь альфа и бетту форму. Таким образом, в водном растворе глюкозы находятся три изомерные формы. Молекула кристаллической глюкозы альфа -форма, при растворении в воде – открытая форма, а затем снова циклическая бетта-форма. Такая изомерия называется динамической (таутомерия).
Химические свойства глюкозы.
Моносахариды вступают в химические реакции, свойственные карбонильной и гидроксильной группам.
1) Реакция “серебряного зеркала”
Доказать наличие альдегидной группы в глюкозе можно с помощью аммиачного раствора оксида серебра. Эта реакция называется реакцией серебряного зеркала. Ее используют как качественную для открытия альдегидов. Альдегидная группа глюкозы окисляется до карбоксильной группы. Глюкоза превращается в глюконовую кислоту.
СН2ОН – (СНОН)4 – СОН + Ag2O = СН2ОН – (СНОН)4 – СООН + 2Ag
(Реакцию серебряного зеркала используют в промышленности для серебрения зеркал, изготовления колб для термосов, елочных украшений).
2) Взаимодействие глюкозы с гидроксидом меди (II)
3) Гидрирование глюкозы
Альдегидная группа может быть восстановлена в гидроксильную группу действием водорода в присутствии катализатора.
4) Специфические свойства.Большое значение имеют процессы брожения глюкозы, происходящие под действием органических катализаторов-ферментов (они вырабатываются микроорганизмами).
а) спиртовое брожение (под действием дрожжей)
С6Н12О6= 2С2Н5 ОН + 2СО2
б) молочнокислое брожение (под действием молочнокислых бактерий)
в) маслянокислое брожение
Применение глюкозы.
Глюкоза находит применение в различных отраслях промышленности:- в кондитерской промышленности при изготовлении мягких конфет, десертных сортов шоколада, тортов и различных диетических изделий;
- в хлебопечении глюкоза улучшает условия брожения, придает пористость и хороший вкус изделиям, замедляет очерствение;
- в производстве мороженого она занижает точку замерзания, увеличивает его твердость;
- при производстве фруктовых консервов, соков, ликеров, вин, безалкогольных напитков, так как глюкоза не маскирует аромата и вкуса;
- в молочной промышленности при изготовлении молочных продуктов и продуктов детского питания рекомендуется использовать глюкозу в определенной пропорции с сахарозой для придания этим продуктам более высокой питательной ценности;
- в ветеринарии;
- в птицеводстве;
- в фармацевтической промышленности.
Кристаллическую глюкозу целесообразно использовать для питания больных, травмированных, выздоравливающих, а также людей, работающих с большими перегрузками.
Медицинскую глюкозу применяют в антибиотиках и других лекарственных препаратах, в том числе для внутривенных вливаний, и для получения витамина С. Техническая глюкоза находит применение в качестве восстановителя в кожевенном производстве, в текстильном – при производстве вискозы, в качестве питательной среды при выращивании различных видов микроорганизмов в медицинской и микробиологической промышленности.
Закрепление:
Источник: http://festival.1september.ru/articles/532403/
alximiki.blogspot.com
Глюкоза: формула, строение и свойства
Строение глюкозы
Название «углеводы» сохранилось с тех времен, когда строение этих соединений еще не было известно, но был установлен их состав, которому соответствует формула Cn(H2O)m. Поэтому углеводы относили к гидратам углерода, т.е. к соединениям углерода и воды – «углеводам». В наше время большинство углеводов выражают формулой CnH2nOn.
1. Углеводы используются с глубокой древности — самым первым углеводом (точнее смесью углеводов), с которой познакомился человек, был мёд.
2. Родиной сахарного тростника является северо-западная Индия-Бенгалия. Европейцы познакомились с тростниковым сахаром благодаря походам Александра Македонского в 327 г. до н.э.
3. Свекловичный сахар в чистом виде был открыт лишь в 1747 г. немецким химиком А. Маргграфом.
4. Крахмал был известен ещё древним грекам.
5. Целлюлоза, как составная часть древесины, используется с глубокой древности.
6. Термин слова “сладкий” и окончание — оза- для сахаристых веществ было предложено французским химиком Ж. Дюла в 1838 г. Исторически сладость была главным признаком, по которому то или иное вещество относили к углеводам.
7. В 1811 г. русский химик Кирхгоф впервые получил глюкозу гидролизом крахмала, а впервые правильную эмпирическую формулу глюкозы предложил шведский химик Я. Берцемус в 1837 г. С6Н12О6
8. Синтез углеводов из формальдегида в присутствии Са(ОН)2 был произведён А.М. Бутлеровым в 1861 г.
Глюкоза является бифункциональным соединением, т.к. содержит функциональные группы – одну альдегидную и 5 гидроксильных. Таким образом, глюкоза — многоатомный альдегидоспирт.
Структурная формула глюкозы имеет вид:
Сокращённая формула имеет вид:
Молекула глюкозы может существовать в трех изомерных формах, причем две из них являются циклическими, одна – линейной.
Все три изомерных формы находятся в динамическом равновесии между собой:
циклическая [(альфа-форма) (37%)] <—> линейная (0,0026%) <—> циклическая [(бета-форма) (63%)]
Циклические альфа- и бета- формы глюкозы представляют собой пространственные изомеры, отличающиеся положением полуацетального гидроксила относительно плоскости кольца. В альфа-глюкозе этот гидроксил находится в транс-положении к гидроксиметильной группе -СН2ОН, в бета-глюкозе – в цис-положении.
Химические свойства глюкозы:
Свойства, обусловленные наличием альдегидной группы:
1. Реакции окисления:
а) с Cu(OH)2:
C6H12O6 + Cu(OH)2↓ ——> ярко-синий раствор
2.Реакция восстановления:
c водородом H2:
В этой реакции может принимать участие лишь линейная форма глюкозы.
Свойства обусловленные наличием нескольких гидроксильных групп (ОН):
1. Реагирует с карбоновыми кислотами с образованием сложных эфиров (пять гидроксильных групп глюкозы вступают в реакцию с кислотами):
2. Как многоатомный спирт реагирует с гидроксидом меди (II) c образованием алкоголя-та меди (II):

Специфические свойства
Большое значение имеют процессы брожения глюкозы, происходящие под действием органических катализаторов-ферментов (они вырабатываются микроорганизмами).
а) спиртовое брожение (под действием дрожжей):
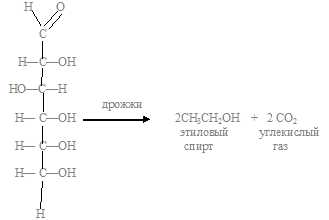
б) молочнокислое брожение (под действием молочнокислых бактерий):
в) уксуснокислое брожение:
г) лимоннокислое брожение:
д) ацетон-бутанольное брожение:
Получение глюкозы
1.Синтез глюкозы из формальдегида в присутствии гидроксида кальция (ре-акция Бутлерова):
2. Гидролиз крахмала (реакция Киргофа):
Биологическое значение глюкозы, её применение
Глюкоза — необходимый компонент пищи, один из главных участников обмена веществ в организме, очень питательна и легко усваивается. При её окислении выделяется больше трети используемой в организме энергий ресурс — жиры, но роль жиров и глюкозы в энергетике разных органов различна. Сердце в качестве топлива используется жирные кислоты. Скелетным мышцам глюкоза нужна для “запуска”, а вот нервные клетки, в том числе и клетки головного мозга работают только на глюкозе. Их потребность составляет 20-30% вырабатываемой энергии. Нервным клеткам энергия нужна каждую секунду, а глюкозу организм получает при приёме пищи. Глюкоза легко усваивается организмом, поэтому ее используют в медицине в качестве укрепляющего лечебного средства. Специфические олигосахариды определяют группу крови. В кондитерском деле для изготовления мармелада, карамели, пряников и т.д. Большое значение имеют процессы брожения глюкозы. Так, например, при квашении капусты, огурцов, молока происходит молочнокислое брожение глюкозы, также как и при силосовании кормов. На практике используется и спиртовое брожение глюкозы, например, при производстве пива.
Углеводы действительно самые распространенные органические вещества на Земле, без которых невозможно существование живых организмов. В живом организме в процессе метаболизма глюкоза окисляется с выделением большого количества энергии:
buzani.ru
Цвет глюкозы
Химики, вопрос к вам! Окраска смеси глюкозы и гидроксида меди (II) БЕЗ нагревания
Образуется синий раствор, при нагревании выпадает красно-оранжевый осадок.
Глюкоза содержит в своем составе пять гидроксильных групп и одну альдегидную группу. Поэтому она относится к альдегидоспиртам. Раствор окрашивается в ярко-синий цвет. В данном случае глюкоза растворяет гидроксид меди (II) и ведет себя как многоатомный спирт, образуя комплексное соединение. При нагревании раствора реакция с гидроксидом меди (II) демонстрирует восстановительные свойства глюкозы. Цвет раствора начинает изменяться. Сначала образуется желтый осадок Cu2O, который с течением времени образует более крупные кристаллы CuO красного цвета. Глюкоза при этом окисляется до глюконовой кислоты.
2HOСН2-(СНOH)4)-СН=O + Cu(OH)2→ 2HOСН2-(СНOH)4)-СOOH + Cu2O↓ + 2h3O
Расход воды на пробелку глюкозы составляет 20 -25 % к массе сырых кристаллов.Продукт имеет чисто белый цвет, чистый сладкий вкус и может заменять кристаллическую глюкозу в…
Катализатором каких реакций является глюкоза? приведите пожалуйста примеры. желательно чтобы с изменением цвета раствора
Распознать химическим путем порошки белого цвета: глюкоза фруктоза решение Химия
Химия. Укажите окраску раствора глюкозы при добавлении свежеприготовленного Cu(OH)2:…
Глюкозу восстанавливает гидроксид меди двухвалентный, который дает желтый осадок, а при дальнейшем нагреве выпадает красный осадок оксида меди (1)
Многие люди, ведущие здоровый образ жизни, предпочитают употреблять в качестве подсластителя глюкозу. Ее считают полезной альтернативой сахару.
Что красит йод в синий цвет? глюкоза, целюлоза, сахароза или крохмаль зарание спасибо )
Крахмал
Table . dima1985 fusion fusion articles is marked as crashed and should be repaired Table . dima1985 fusion fusion articles is marked as crashed and should be repaired Table…
Крохмаль, конечно!
Крахмал
Почему при кипячении глюкозы с NAOH р-р приобретает стадии коричневого цвета в зависимости от концентрации глюкозы?
Происходит щелочное расщепление сахаров.
Глюко за от др.-греч. сладкий C6h22O6 , или виноградный сахар, или декстроза D- глюкоза , встречается в соке многих фруктов и ягод, в том числе и винограда, от чего и произошло название этого вида сахара.
Подскажите пожалуйста, что за глюкоза добавляется в шоколад для лепки цветов.
Это просто глюкоза.
Глюкоза она и в Африке глюкоза.
Продается свободно, обычно в отделах для диабетиков.
Тест считается положительным при изменении цвета реакционной зоны. В зависимости от концентрации глюкозы в пробе исходная окраска зоны меняется.
Образование вещества синего цвета при взаимодействии раствора глюкозы с гидроксидом меди (II) обусловлено наличием ней
C6h22O6 + Cu(OH)2 = C6h20O6Cu + 2 h3O
Особенности строения глюкозы 1. Состав глюкозы выражается формулой С6Н12O6, она1. Глюкоза многоатомный спирт. Глюкоза с Cu OH 2 да т раствор синего цвета глюконат меди .
Приветик!
Ответ б) , т. к образование ярко-синего раствора при действии свежеосаждённым гидроксидом меди (II) в щелочной среде — качественная реакция на многоатомные спирты.
Удачи!
Кто знает,какие цветы можно подкармливать глюкозой.И какой концентрации должен быть рабочий раствор?
Прочитайте о «домашних подкормках» здесь: http://www.treeland.ru/article/home/plant/fertilizer.htm Лично я сомневаюсь, нужно ли это растению? Глюкоза-один из продуктов фотосинтеза. А вот для восстановления тургора листьев у орхидей-хорошее средство (но я пробовала не чистую глюкозу, а р-р сахарозы, т. е. сахар обычный).
Минимальное количество глюкозы, выделяемое почками здорового человека и не реабсорбированное в канальцах, окрашивает диагностическую зону в слегка зеленоватый цвет.
От сахаров всяких и глюкоз в земле заведутся всякие мошки. Удобрять можно, но следите, чтобы мошек в квартире не было. Иначе долго потом будете от них избавляться. А опрыскивать, думаю вреда не будет.
Я даже пиво для подкормки использую.
Химия….помогите пожалуйста!!!!
Уксусная кислота и серная имеют специфические запахи, глицерин — вязкую текстуру (он будет как бы тянуться по стенкам пробирки) , ну а то что осталось — без цвета и запаха — глюкоза
Глюкоза от лат. глюкос — сладкий углевод кристаллическое вещество без цвета и запаха, со сладковатым вкусом, хорошо растворимое в воде. Синонимы виноградный сахар, декстроза.
Подскажите интересные, может быть немного опасные химические опыты
А волбешное слово где?
Реакция основана на свойстве глюкозы восстанавливать гидрат окиси меди в щелочной среде в гидрат закиси меди желтый цвет или закись меди красный цвет .
Динамит и зажигалка)
Посмотрите эксперимент с горящей рукой:
sozvezdie21.ru
