Раздел недели: Обезжиривающие водные растворы и органические растворители. Составы для очистки и обезжиривания поверхности. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Поиск на сайте DPVA Поставщики оборудования Полезные ссылки О проекте Обратная связь Ответы на вопросы. Оглавление Таблицы DPVA.ru — Инженерный Справочник | Адрес этой страницы (вложенность) в справочнике dpva.ru: главная страница / / Техническая информация/ / Химический справочник / / Водные растворы и смеси для обработки металлов — мытья, обезжиривания, нанесения покрытий, очистки и т. Поделиться:
 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Если Вы не обнаружили себя в списке поставщиков, заметили ошибку, или у Вас есть дополнительные численные данные для коллег по теме, сообщите , пожалуйста. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Коды баннеров проекта DPVA.ru Консультации и техническая | Проект является некоммерческим. Информация, представленная на сайте, не является официальной и предоставлена только в целях ознакомления. Владельцы сайта www.dpva.ru не несут никакой ответственности за риски, связанные с использованием информации, полученной с этого интернет-ресурса. Free xml sitemap generator | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Урок «Производство чугуна и его применение»
Тема: Производство чугуна и его применение
Класс: 9
Тип урока: изучение нового материала
Цель: ознакомление учащихся с чугуном, как сплавом железа и его применением.
Задачи:
закрепить знания, об основных месторождениях железа в России, полученные на уроках географии;
познакомить с доменным процессом выплавки чугуна;
познакомить с историей чугунного литья и применением чугуна в архитектуре.
Ход урока:
I. Организационный момент
1. Вводное слово учителя, актуализация
II. Новая тема
Постановка цели урока, изложение плана урока;
Изложение материала учащимися по первому этапу урока, работа с картой;
Изложение материала учителем и учащимися по второму этапу урока;
Изложение материала учителем и учащимися по третьему этапу урока;
Изложение материала учащимися по четвёртому этапу урока;
Решение расчётной задачи на практический выход продукта реакции.

III. Заключительное слово учителя, итог урока
IV. Рефлексия
V. Домашнее задание.
Средства обучения:
Мультимедийная установка;
Диски: «Неорганическая химия», с мультимедийной презентацией;
Коллекция минералов;
Алгоритм
Схема устройства доменной печи
Методы:
По источнику информации – наглядные
По способу познавательной деятельности – проблемный
По движению мысли от незнания к знанию — дедуктивный
Часы истории человечества стали отсчитывать время быстрее, когда в его жизнь вошли металлы и, что важнее всего, их сплавы. Вся история человечества в зависимости от материала и изготовления орудий труда делится на четыре больших эпохи. И в большинстве своем, именно металлы дали названия этим эпохам: каменный век — медный век — бронзовый век — железный век. Здесь мы видим прогресс развития человечества. Слайд 1
И в большинстве своем, именно металлы дали названия этим эпохам: каменный век — медный век — бронзовый век — железный век. Здесь мы видим прогресс развития человечества. Слайд 1
Давайте сразу перенесемся в эпоху железного века. Ведь железо сыграло большую роль в развитии человеческого общества и не потеряло своего значения в настоящее время: из всех металлов оно и его сплавы наиболее широко используются в современной промышленности.
Первобытный человек начал использовать железо за несколько тысячелетий до нашей эры. В те времена он еще не добывал железо из руд, а использовал упавшие из космоса на Землю метеориты. Отсюда и древнее название железа ваасперс, что обозначает в переводе с шумерского языка – это металл, “капнувший с неба, небесный”.
Получение железа из железных руд, приходится на середину II тыс. до н.э. Данный процесс был осуществлен египтянами. Начало металлургии железа на территории нашей страны приходится на рубеж II и I тыс. до н.э. Сегодня на уроке мы поговорим о сплаве железа.
до н.э. Сегодня на уроке мы поговорим о сплаве железа.
И объектом нашего урока сегодня будет чугун.
Тема урока: «Производство чугуна и его применение». Исходя из темы, сформулируйте для себя задачи урока. Слайд 2
Предполагаемый ответ: выяснить химизм получения чугуна и познакомиться с отраслями его применения.
Чтобы реализовать поставленные вами задачи, необходим план урока. Я вам предлагаю план, по которому мы с вами будем сегодня работать. Найдите его на своих столах и положите посередине. Слайд 3
Сообщение учащегося, работа с картой Слайд 4 Железо один из самых распространенных в природе элементов. В земной коре его массовая доля составляет 5,1%, и оно уступает лишь кислороду, кремнию и алюминию. Железо входит в состав большинства горных пород в виде руд: магнетит, красный железняк, бурый железняк. Слайд 5 Демонстрация коллекции минералов. Железорудные месторождения имеются на территории всей России. Это Курская магнитная аномалия, на Урале, в Западной Сибири. Слайд 6
Слайд 5 Демонстрация коллекции минералов. Железорудные месторождения имеются на территории всей России. Это Курская магнитная аномалия, на Урале, в Западной Сибири. Слайд 6
Слово учителя У нас на территории РХ тоже имеются железорудные месторождения, их более 130. А вы можете назвать какие-нибудь? Показать.
Добыча железной руды в Хакасии ведется двумя рудниками: Абаканском и Тейском. Кроме того, месторождение в Западном Саяне: Анзасское является резервным. Слайд 7
Чистое железо из железных руд можно получить химическим способом, однако мягкость чистого металла делает его применение нецелесообразным. В промышленности и технике используют железо в виде сплавов: чугуна и стали.
Первый чугун был произведен в Китае в VI в. до н.э. В Европе чугун начали получать в ХIV в. (когда появились первые доменные печи. В России первые доменные производства открылись в ХVI столетии).
Что же такое чугун? Для этого нам нужно ответить на следующие вопросы. Слайд 8 Что такое? Какой он? Из чего состоит? Чтобы ответить на эти вопросы, мы познакомимся сначала с его производством.
3. Получение чугуна осуществляется в доменных печах, или домнах. Давайте познакомимся с их устройством. Внимание на экран. Диск «Неорганическая химия», раздел «Железо и хром», параграф «Чугун и сталь» — п.3 – устройство доменной печи или слайд 9
Самостоятельная работа учащихся со схемой в тетрадях (3мин). У вас на столах имеются таблицы с изображением доменной печи. Сделайте на них обозначения, характеризующие устройство домны. Чтобы вам было легче справиться обратите внимание на следующие термины (записаны на доске). Проверьте, верно, ли вы сделали обозначения (отвечает один ученик, показывает на слайде). Проверим ещё раз. Диск «Неорганическая химия», раздел «Железо и хром», параграф «Чугун и сталь» — п.3 – устройство доменной печи включить повторно для проверки (отвечают учащиеся). Если есть неточности в ваших работах, исправьте их.
Диск «Неорганическая химия», раздел «Железо и хром», параграф «Чугун и сталь» — п.3 – устройство доменной печи включить повторно для проверки (отвечают учащиеся). Если есть неточности в ваших работах, исправьте их.
Через колошник происходит загрузка сырья для выплавки чугуна, а снизу подается воздух.
Давайте познакомимся с химизмом выплавки чугуна в доменных печах.
4. Самостоятельная работа учащихся по алгоритму (10мин). Представьте, что вы рабочие-металлурги и вам необходимо выплавить 1т чугуна. Для этого у вас есть 1800кг Fe2O3, 800кг кокса, 300кг флюсов в виде СаСО3. По предложенному вам алгоритму получите, пожалуйста, вашу первую тонну чугуна. Слайд 10
Давайте посмотрим, получили ли вы свою первую тонну чугуна. Кто желает выйти к доске и написать уравнения реакций процессов, которые идут в доменной печи. Запись на доске. Теперь проверим, верно, ли вы написали уравнения процессов и, следовательно, получили ли чугун. Внимание на экран. Диск «Неорганическая химия», раздел «Железо и хром», параграф «Чугун и сталь» — п.4,5.или слайд11,12 Такие процессы должны пройти в доменной печи. Чтобы глубже узнать профессию металлурга, у нас в г.Абакане есть филиал КГТУ, где вы можете приобрести данную профессию.
Теперь проверим, верно, ли вы написали уравнения процессов и, следовательно, получили ли чугун. Внимание на экран. Диск «Неорганическая химия», раздел «Железо и хром», параграф «Чугун и сталь» — п.4,5.или слайд11,12 Такие процессы должны пройти в доменной печи. Чтобы глубже узнать профессию металлурга, у нас в г.Абакане есть филиал КГТУ, где вы можете приобрести данную профессию.
Мы познакомились с устройством доменной печи и процессами выплавки чугуна. Давайте теперь вернемся к нашим вопросам Что такое? Какой он? Из чего состоит? Слайд 13 и скажем, что же такое чугун. (ответы учащихся).
Чугун – определение в тетрадь. Слайд 14
Слово учителя Различают два вида чугуна: белый и серый. Белый чугун идет на производство стали, а серый используется для нужд человека.
5. Давайте выясним, где же чугун находит свое применение. Для этого слайд 15 из приведенного перечня выберите те области, в которых используются изделия из чугуна. И приведите примеры изделий из этого сплава. Работа учащихся над выбором отраслей применения чугуна.
Для этого слайд 15 из приведенного перечня выберите те области, в которых используются изделия из чугуна. И приведите примеры изделий из этого сплава. Работа учащихся над выбором отраслей применения чугуна.
В быту
Авиастроение
Мебельная промышленность
Водоснабжение
Коммунальное хозяйство
Искусство
Архитектура (ответы учащихся с примерами).
Слово учителя Но чугун используется и в искусстве, в архитектуре и скульптуре.
Сообщение учащегося об истории первых чугуноплавильных заводов на территории России.
Сообщения учащегося из Интернет-ресурсов о Каслинском литье, решётках Санкт-Петербурга, мостах и Исаакиевском соборе. Слайды по ходу сообщений 16-19
6. Решение задачи. Мы с вами сегодня выплавили в доменной печи чугун. Теперь давайте решим задачу стр.157, зад.4 и узнаем, сколько можно получить чугуна из 100т железной руды.
Решение задачи. Мы с вами сегодня выплавили в доменной печи чугун. Теперь давайте решим задачу стр.157, зад.4 и узнаем, сколько можно получить чугуна из 100т железной руды.
III. Итог Давайте вернемся к нашему плану и посмотрим, все ли пункты плана реализованы? (Ответ учащихся: все). Я согласна и тоже считаю что все. IV. Рефлексия Посмотрите на предложенные Вам вопросы и ответьте на них. Слайд 20 ответы и отзывы учащихся.
V. Домашнее задание стр. 157. зад.5, пар.56, вопр.5-10, более сильным учащимся индивидуальные карточки с заданиями в тетрадь
Спасибо за урок! Слайд 21. Я рада, что урок Вам понравился.
Используемая литература
Аликберова Л. Ю. Занимательная химия: Книга для учащихся, учителей и родителей – М.: АСТ-ПРЕСС.
 2002. – 560 с.
2002. – 560 с.Бердоносов С. С., Менделеева Е. А. Химия. Новейший справочник. – М.: Махаон, 2006.
Ф.Г.Фельдман, Г.Е. Рудзитис Химия:Учеб. Для 9 кл. сред. Общеобразоват. Учеб. Заведений. – М.: Просвещение, 2008.
Химия. – 2-е изд., перераб./ред. Коллегия: М.Аксёнова, И.Леенсон, С.Мартынова и др. – М.: Мир энциклопедий Аванта+, Астрель, 2007.
Хомченко Г.П. Химия для поступающих в ВУЗы: учеб.пособие. – 2-е изд. – М.: высш. Шк., 1993.
Электронные издания
Диск «Неорганическая химия»
Диск Химия 9 класс «Просвещение»
Учащимися использовались Интернет-ресурсы
Чугун | Металлургия для чайников
Чугун получают из чугуна, и хотя обычно он относится к серому чугуну, он также определяет большую группу ферросплавов, затвердевающих с эвтектикой. Цвет поверхности излома можно использовать для идентификации сплава. Белый чугун назван в честь его белой поверхности при изломе из-за примесей карбида, которые позволяют трещинам проходить прямо насквозь. Серый чугун назван в честь его серой изломистой поверхности, которая возникает из-за того, что графитовые чешуйки отклоняют проходящую трещину и вызывают бесчисленное количество новых трещин по мере разрушения материала.
Цвет поверхности излома можно использовать для идентификации сплава. Белый чугун назван в честь его белой поверхности при изломе из-за примесей карбида, которые позволяют трещинам проходить прямо насквозь. Серый чугун назван в честь его серой изломистой поверхности, которая возникает из-за того, что графитовые чешуйки отклоняют проходящую трещину и вызывают бесчисленное количество новых трещин по мере разрушения материала.
Чугун Автозапчасти
Углерод (C) и кремний (Si) являются основными легирующими элементами в количестве от 2,1 до 4 % масс. и от 1 до 3 % масс., соответственно. Сплавы железа с меньшим содержанием углерода известны как стали.
Хотя технически это делает эти базовые сплавы тройными сплавами Fe-C-Si, принцип затвердевания чугуна можно понять из бинарной фазовой диаграммы железо-углерод. Поскольку составы большинства чугунов находятся примерно в точке эвтектики системы железо-углерод, температуры плавления тесно связаны между собой, обычно в диапазоне от 1150 до 1200 °C (от 2102 до 2,19°С). 2 °F), что примерно на 300 °C (572 °F) ниже температуры плавления чистого железа.
2 °F), что примерно на 300 °C (572 °F) ниже температуры плавления чистого железа.
Фазовая диаграмма Сталь и чугун
Чугун имеет тенденцию быть хрупким, за исключением ковких чугунов. Благодаря относительно низкой температуре плавления, хорошей текучести, литейности, отличной обрабатываемости, устойчивости к деформации и износостойкости, чугуны стали конструкционным материалом с широким спектром применения и используются в трубах, машинах и деталях автомобильной промышленности, таких как цилиндры. головки (сокращение использования), блоки цилиндров и картеры коробок передач (сокращение использования). Он устойчив к разрушению и ослаблению при окислении (ржавчине).
Чугунные украшения
Чугун производится путем повторного плавления чугуна, часто вместе со значительным количеством железного и стального лома, и принятия различных мер для удаления нежелательных примесей, таких как фосфор и сера. В зависимости от применения содержание углерода и кремния снижается до желаемого уровня, который может составлять от 2 до 3,5% и от 1 до 3% соответственно. Затем в расплав добавляются другие элементы, прежде чем окончательная форма будет получена путем литья. После завершения плавки расплавленный чугун заливают в раздаточный котел или ковш.
Затем в расплав добавляются другие элементы, прежде чем окончательная форма будет получена путем литья. После завершения плавки расплавленный чугун заливают в раздаточный котел или ковш.
Чугун Art
Свойства чугуна изменяются путем добавления различных легирующих элементов или сплавов. После углерода кремний является наиболее важным сплавом, потому что он вытесняет углерод из раствора. Вместо этого углерод образует графит, что приводит к более мягкому железу, уменьшает усадку, снижает прочность и плотность. Сера при добавлении образует сульфид железа, препятствующий образованию графита и повышающий твердость.
Проблема с серой заключается в том, что она делает расплавленный чугун вялым, что вызывает кратковременные браки. Чтобы противодействовать воздействию серы, добавляют марганец, потому что они образуют сульфид марганца вместо сульфида железа. Сульфид марганца легче расплава, поэтому он всплывает из расплава в шлак. Количество марганца, необходимое для нейтрализации серы, составляет 1,7×содержание серы+0,3%. Если добавить больше этого количества марганца, то образуется карбид марганца, который увеличивает твердость и холодостойкость, за исключением серого чугуна, где до 1% марганца увеличивает прочность и плотность.
Если добавить больше этого количества марганца, то образуется карбид марганца, который увеличивает твердость и холодостойкость, за исключением серого чугуна, где до 1% марганца увеличивает прочность и плотность.
Железо-углеродная фазовая диаграмма
Никель является одним из наиболее распространенных сплавов, поскольку он очищает перлитную и графитовую структуру, улучшает ударную вязкость и выравнивает разницу в твердости между толщинами срезов. Хром добавляют в ковш в небольших количествах для уменьшения количества свободного графита, получения отбела и потому, что он является мощным стабилизатором карбида; никель часто добавляют вместе. Вместо 0,5% хрома можно добавить небольшое количество олова. Медь добавляется в ковш или в печь в количестве от 0,5 до 2,5% для уменьшения отбела, рафинирования графита и повышения текучести.
Кухонный гарнитур из чугуна
Молибден добавляется в количестве от 0,3 до 1% для повышения холодостойкости и улучшения структуры графита и перлита; его часто добавляют в сочетании с никелем, медью и хромом для получения высокопрочного железа. Титан добавляют в качестве дегазатора и раскислителя, но он также увеличивает текучесть. От 0,15 до 0,5% ванадия добавляют в чугун для стабилизации цементита, повышения твердости и повышения износостойкости и теплостойкости. От 0,1 до 0,3% циркония способствует образованию графита, раскислению и повышению текучести. В расплавы ковкого чугуна добавляется висмут в количестве от 0,002 до 0,01%, чтобы увеличить количество кремния, которое можно добавить. В белый чугун бор добавляется для облегчения производства ковкого железа, он также снижает огрубляющий эффект висмута.
Титан добавляют в качестве дегазатора и раскислителя, но он также увеличивает текучесть. От 0,15 до 0,5% ванадия добавляют в чугун для стабилизации цементита, повышения твердости и повышения износостойкости и теплостойкости. От 0,1 до 0,3% циркония способствует образованию графита, раскислению и повышению текучести. В расплавы ковкого чугуна добавляется висмут в количестве от 0,002 до 0,01%, чтобы увеличить количество кремния, которое можно добавить. В белый чугун бор добавляется для облегчения производства ковкого железа, он также снижает огрубляющий эффект висмута.
Механический блок из чугуна
Серый чугун
Серый чугун характеризуется графитовой микроструктурой, из-за которой изломы материала приобретают серый цвет. Это наиболее часто используемый чугун и наиболее широко используемый литой материал в зависимости от веса.
Микроструктура серого чугуна
Большинство чугунов имеют химический состав от 2,5 до 4,0% углерода, от 1 до 3% кремния, а остальную часть составляет железо. Серый чугун имеет меньшую прочность на растяжение и ударопрочность, чем сталь, но его прочность на сжатие сравнима с низко- и среднеуглеродистой сталью.
Серый чугун имеет меньшую прочность на растяжение и ударопрочность, чем сталь, но его прочность на сжатие сравнима с низко- и среднеуглеродистой сталью.
При более низком содержании кремния и более быстром охлаждении углерод в белом чугуне выделяется из расплава в виде метастабильной фазы цементита Fe3C, а не графита. Цементит, выделяющийся из расплава, образует относительно крупные частицы, обычно в эвтектической смеси, где другой фазой является аустенит (который при охлаждении может превратиться в мартенсит).
Белый чугун – это нелегированный чугун с низким содержанием углерода и кремния, структура которого представляет собой твердый хрупкий карбид железа без свободного графита. Белые чугуны широко используются в приложениях, связанных с абразивным износом, связанных с дроблением, шлифованием, измельчением и обработкой абразивных материалов
Эти эвтектические карбиды слишком велики, чтобы обеспечить дисперсионное твердение (как в некоторых сталях, где выделения цементита могут ингибировать пластическую деформацию, препятствуя движению дислокаций через ферритовую матрицу).
Скорее, они повышают объемную твердость чугуна просто за счет своей очень высокой твердости и значительной объемной доли, так что объемная твердость может быть аппроксимирована по правилу смесей. В любом случае, они предлагают жесткость за счет жесткости. Поскольку карбид составляет большую часть материала, белый чугун можно с полным основанием отнести к кермету.
Микроструктура белого чугуна
Белый чугун слишком хрупок для использования во многих конструкционных компонентах, но благодаря хорошей твердости и стойкости к истиранию и относительно низкой стоимости он находит применение в таких областях, как изнашиваемые поверхности (рабочее колесо и улитка) шламовых насосов. , вкладыши и подъемные стержни в шаровых мельницах и мельницах самоизмельчения, шары и кольца в угольных измельчителях, а также зубья ковша обратной лопаты (хотя для этого применения чаще используется литая мартенситная сталь со средним содержанием углерода).
Ковкий чугун Ковкий чугун представляет собой отливку из белого чугуна, которая затем подвергается термообработке при температуре около 900 °C (1650 °F). Графит в этом случае выделяется гораздо медленнее, так что поверхностное натяжение успевает сформировать из него сфероидальные частицы, а не чешуйки. Из-за меньшего соотношения сторон сфероиды относительно короткие и находятся далеко друг от друга, а также имеют меньшее поперечное сечение по отношению к распространяющейся трещине или фонону.
Графит в этом случае выделяется гораздо медленнее, так что поверхностное натяжение успевает сформировать из него сфероидальные частицы, а не чешуйки. Из-за меньшего соотношения сторон сфероиды относительно короткие и находятся далеко друг от друга, а также имеют меньшее поперечное сечение по отношению к распространяющейся трещине или фонону.
Ковкий чугун Микроструктура
Деталь фитинга из ковкого чугуна
Кроме того, они имеют тупые края, в отличие от чешуек, что облегчает проблемы с концентрацией напряжений, с которыми сталкивается серый чугун. В целом свойства ковкого чугуна больше напоминают мягкую сталь. Существует ограничение на то, насколько большая деталь может быть отлита из ковкого чугуна, поскольку она изготавливается из белого чугуна.
Детали из высокопрочного чугуна
Высокопрочный чугун Более поздней разработкой является шаровидный или высокопрочный чугун. Небольшие количества магния или церия, добавленные к этим сплавам, замедляют рост графитовых отложений, связываясь с краями графитовых плоскостей.
Чугун с шаровидным графитом Микроструктура
Наряду с тщательным контролем других элементов и времени это позволяет углероду отделяться в виде сфероидальных частиц по мере затвердевания материала. Свойства аналогичны ковкому чугуну, но детали можно отливать с большим сечением.
Вам нужны ссылки на книги по чугуну? здесь…
Вам также может понравиться
| Микроструктура металлов Микроструктура определяется как… | Фазовая диаграмма стали Фазовая диаграмма Fe-Fe3C, Материаловедение… | Высокопрочный чугун с аустенитным отпуском (ADI) Ковкий чугун из закаленного алюминия (ADI)… | Фазовые диаграммы Fe-Mn, Fe-Co, Fe-Mo В чистом железе А4 (1394 °С) и… |
Чугун
Диаграмма состояния железа и углерода
В своей простейшей форме стали представляют собой сплавы железа (Fe) и углерода (C). Изучение состава и структуры железа и стали начинается с фазовой диаграммы железо-углерод. Это также является основой понимания термической обработки сталей.
Изучение состава и структуры железа и стали начинается с фазовой диаграммы железо-углерод. Это также является основой понимания термической обработки сталей.
В железоуглеродной системе присутствуют некоторые важные металлургические фазы и микрокомпоненты. На низкоуглеродистом конце находятся феррит (альфа-железо) и аустенит (гамма-железо). Феррит может растворить не более 0,028 мас.% С при 727°С, а аустенит (гамма-железо) может растворить 2,11 мас.% С при 1148°С. На богатой углеродом стороне находится цементит (Fe3C).
Между однофазными полями находятся области со смесями двух фаз, таких как феррит и цементит, аустенит и цементит, феррит и аустенит. При самых высоких температурах можно обнаружить поле жидкой фазы, а под ним находятся поля двух фаз: жидкость и аустенит, жидкость и цементит и жидкость и феррит. При термообработке сталей всегда избегают жидкой фазы. Некоторым важным границам в однофазных полях даны специальные названия, облегчающие понимание диаграммы.
Основные микроструктуры железа и сталей в равновесии:
1.
2. Ферритная или альфа-железная фаза – это относительно мягкая низкотемпературная фаза и стабильная равновесная фаза. Феррит является обычным компонентом сталей и имеет объемно-центрированную кубическую (ОЦК) структуру (которая менее плотно упакована, чем ГЦК). ?-железо мягкое, пластичное, имеет низкую прочность и хорошую ударную вязкость.
3. Цементит – Fe3C или карбид железа. Это промежуточное соединение Fe и C. Имеет сложную орторомбическую структуру и является метастабильной фазой. Он твердый, хрупкий и имеет низкую прочность на растяжение, хорошую прочность на сжатие и низкую ударную вязкость
 Он представляет собой совокупность чередующихся пластинок феррита и цементита, которая после длительной выдержки ниже 723°С вырождается («сфероидизируется» или «огрубевает») в частицы цементита, диспергированные с ферритовой матрицей. Является эвтектоидом и имеет ОЦК-структуру. Это частично растворимый раствор Fe и C. Обладает высокой прочностью и низкой ударной вязкостью.
Он представляет собой совокупность чередующихся пластинок феррита и цементита, которая после длительной выдержки ниже 723°С вырождается («сфероидизируется» или «огрубевает») в частицы цементита, диспергированные с ферритовой матрицей. Является эвтектоидом и имеет ОЦК-структуру. Это частично растворимый раствор Fe и C. Обладает высокой прочностью и низкой ударной вязкостью.В случае неравновесного затвердевания системы Fe-C могут образовываться следующие основные микроструктуры.
• Бейнит представляет собой фазу между перлитом и мартенситным участком. Это твердый метастабильный микрокомпонент; непластинчатая смесь феррита и цементита в очень мелком масштабе. Верхний бейнит образуется при более высоких температурах и имеет перистый вид. Нижний бейнит образуется при более низких температурах и имеет игольчатый вид. Твердость бейнита увеличивается с понижением температуры формования. Обладает хорошей прочностью и жесткостью.
• Мартенсит образуется при быстром охлаждении и является твердым и хрупким. Это пересыщенный раствор атомов С в феррите. Он имеет структуру ОЦТ и твердую метастабильную фазу. Он имеет решетчатую морфологию при 1,0 мас.% С и смеси промежуточных значений. Он имеет высокую прочность и твердость и низкую ударную вязкость.
Это пересыщенный раствор атомов С в феррите. Он имеет структуру ОЦТ и твердую метастабильную фазу. Он имеет решетчатую морфологию при 1,0 мас.% С и смеси промежуточных значений. Он имеет высокую прочность и твердость и низкую ударную вязкость.
• Сорбит / троостит
На диаграмме железа-C есть много температур и критических точек, которые важны как с базовой, так и с практической точки зрения.
• Температура А1, при которой происходит эвтектоидная реакция, равная 723 град. С на схеме. A1 называется эвтектоидной температурой и является минимальной температурой для аустенита.
• На более низкотемпературной границе аустенитной области при низком содержании углерода находится ?/? + ? граница.
• Acm – это граница соответствия для высокого содержания углерода, то есть ?/? + граница Fe3C (граница перлита). Содержание углерода, при котором достигается минимальная температура аустенита, называется эвтектоидным содержанием углерода (0,77 мас. % С).
• Температура А4, при которой аустенит превращается в ?-железо, 1390 град.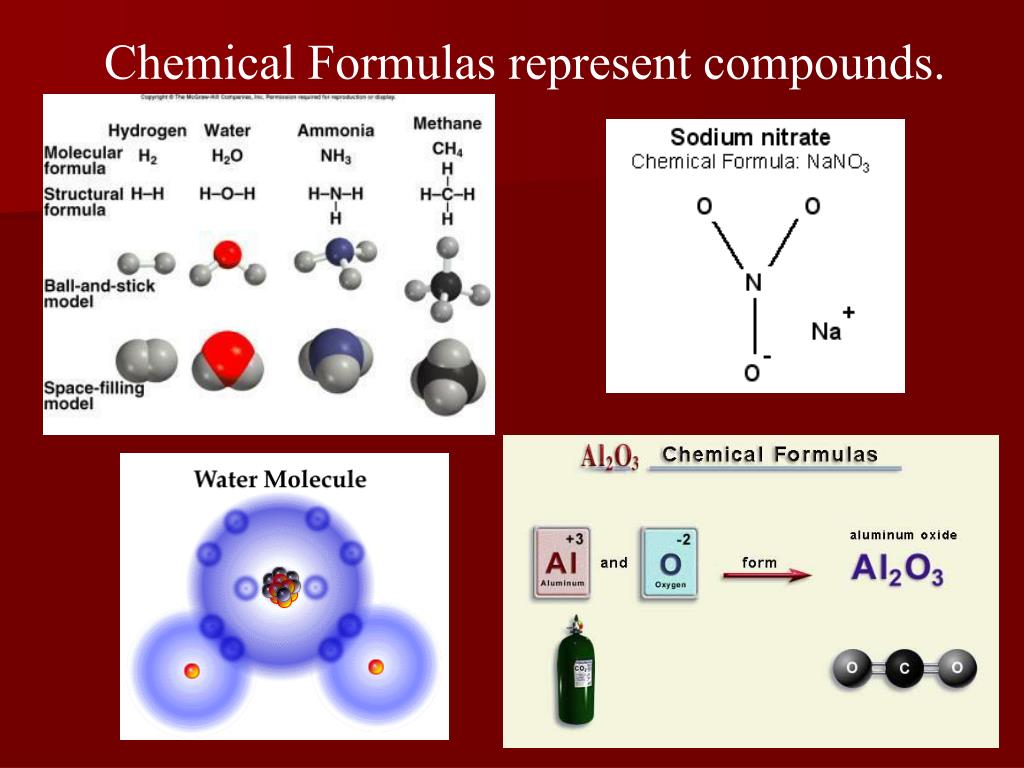 C в чистом железе, но эта температура увеличивается по мере добавления углерода.
C в чистом железе, но эта температура увеличивается по мере добавления углерода.
• Температура A2 является точкой Кюри, когда железо переходит из ферро в парамагнитное состояние. Эта температура составляет 769 градусов. C для чистого железа, но без изменения кристаллической структуры.
• Accm – температура в заэвтектоидной стали, при которой растворение цементита в аустените завершается при нагреве.
• Ac1 – это температура, при которой во время нагревания начинается образование аустенита, где c происходит от французского слова chauffant.
• Ac3 – температура, при которой завершается превращение феррита в аустенит при нагреве.
• Aecm, Ae1, Ae3 – температуры фазовых переходов при равновесии.
• Arcm – это температура в заэвтектоидной стали, температура, при которой начинается осаждение цементита во время охлаждения, где r происходит от французского refroidissant.
• Ar1 – это температура, при которой завершается превращение аустенита в феррит или в феррит плюс цементит во время охлаждения.
• Ar3 – это температура, при которой аустенит начинает превращаться в феррит при охлаждении.
• Ar4 – это температура, при которой дельта-феррит превращается в аустенит при охлаждении.
• Ms (или Ar”) – температура, при которой начинается превращение аустенита в мартенсит при охлаждении.
• Mf – температура, при которой заканчивается образование мартенсита при охлаждении.
Все изменения, кроме образования мартенсита, происходят при более низких температурах при охлаждении, чем при нагреве, и зависят от скорости изменения температуры.
Превращение аустенита в феррит
В равновесных условиях в железоуглеродистых сплавах, содержащих до 0,8% углерода, будет образовываться доэвтектоидный феррит. Реакция происходит при 910 град. C в чистом железе, но имеет место между 910 град. С и 723 град. C в железоуглеродистых сплавах.
Однако при закалке из аустенитного состояния до температур ниже эвтектоидной температуры Ae1 феррит может образовываться при температурах до 600 град. C. Имеются выраженные морфологические изменения при понижении температуры превращения, которые, следует подчеркнуть, относятся в основном к гипо- и заэвтектоидным фазам, хотя в каждом случае будут вариации из-за точной кристаллографии вовлеченных фаз. Например, те же принципы применимы к образованию цементита из аустенита, но морфологически отличить феррит от цементита нетрудно.
C. Имеются выраженные морфологические изменения при понижении температуры превращения, которые, следует подчеркнуть, относятся в основном к гипо- и заэвтектоидным фазам, хотя в каждом случае будут вариации из-за точной кристаллографии вовлеченных фаз. Например, те же принципы применимы к образованию цементита из аустенита, но морфологически отличить феррит от цементита нетрудно.
Превращение аустенита в цементит
Классификация Дьюба одинаково хорошо применима к различным морфологиям цементита, образующегося при постепенно более низких температурах превращения. Начальное развитие аллотриоморфов границ зерен очень похоже на развитие феррита, и рост боковых пластин или цементита видманстатена происходит по той же схеме. Пластинки цементита имеют более строго кристаллографическую форму, несмотря на то, что ориентационная связь с аустенитом более сложная.
Как и в случае с ферритом, большинство боковых пластин происходит из аллотриоморфов границ зерен, но в цементитной реакции больше боковых пластин зарождается на границах двойников в аустените.
Реакция аустенита и перлита
Перлит является наиболее известной микроструктурной особенностью во всей металлографии. Он был обнаружен Сорби более века назад, который правильно предположил, что это пластинчатая смесь железа и карбида железа.
Перлит является очень распространенным компонентом многих сталей, где он вносит существенный вклад в прочность. Пластинчатые эвтектоидные структуры этого типа широко распространены в металлургии, и для их описания часто используется термин перлит.
Эти структуры имеют много общего с реакциями клеточной преципитации. Оба типа реакций происходят путем зародышеобразования и роста и, следовательно, контролируются диффузией. Зародыши перлита встречаются на границах аустенитных зерен, но ясно, что они также могут быть связаны как с доэвтектоидным ферритом, так и с цементитом. В промышленных сталях перлитные конкреции могут образовываться на включениях.
Можно видеть, что нормальная диаграмма равновесия железо-углерод представляет собой метастабильное равновесие между железом и карбидом железа. Цементит метастабилен, так как истинное равновесие находится между железом и графитом. Хотя графит широко встречается в чугунах (от 2 до 4 мас.% углерода), обычно трудно получить эту равновесную фазу в сталях (0,03-1,5 мас.% углерода). Поэтому обычно рассматривается метастабильное равновесие между железом и карбидом железа, поскольку оно имеет отношение к поведению различных сталей на практике.
Цементит метастабилен, так как истинное равновесие находится между железом и графитом. Хотя графит широко встречается в чугунах (от 2 до 4 мас.% углерода), обычно трудно получить эту равновесную фазу в сталях (0,03-1,5 мас.% углерода). Поэтому обычно рассматривается метастабильное равновесие между железом и карбидом железа, поскольку оно имеет отношение к поведению различных сталей на практике.
При сравнении аустенита (гамма-железа) с ферритом (альфа-железом) замечено, что растворимость углерода больше в аустените с максимальным значением чуть более 2 мас.% при 1147 град. C. Эта высокая растворимость углерода в аустените чрезвычайно важна при термообработке, когда обработка на твердый раствор в аустените с последующей быстрой закалкой до комнатной температуры позволяет образовать пересыщенный твердый раствор углерода в железе.
Ферритовая фаза ограничена максимальной растворимостью углерода 0,02 мас.% при 723 град. C. Поскольку диапазон содержания углерода в обычных сталях составляет от 0,05 до 1,5 мас.

 п. Составы для очистки и обезжиривания поверхности и нанесения покрытий./ / Обезжиривающие водные растворы и органические растворители. Составы для очистки и обезжиривания поверхности.
п. Составы для очистки и обезжиривания поверхности и нанесения покрытий./ / Обезжиривающие водные растворы и органические растворители. Составы для очистки и обезжиривания поверхности. Любая смесь составленная самостоятельно в разы дешевле покупной смеси.
Любая смесь составленная самостоятельно в разы дешевле покупной смеси.
 Химическая формула: Na3PO4 * 12h3O
Химическая формула: Na3PO4 * 12h3O Химическая формула, Na2CO3
Химическая формула, Na2CO3