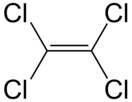
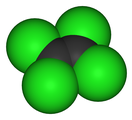
Перхлорэтилен — органическое вещество, хлорпроизводное этана и этилена с формулой C2Cl4. Химическое название — 1,1,2,2-тетрахлорэтен. В Европе этот реактив называют тетрахлорэтиленом. Получают его искусственным синтезом.
Свойства
1,1,2,2-тетрахлорэтен — прозрачная плотная жидкость с резким  запахом эфира, текучая. Не горит, не поддерживает горения, не взрывается. Почти не растворяется в воде; легко смешивается с органическими растворителями, например, с этиловым и метиловым спиртом, уксусной и муравьиной кислотой, пропанолом, бутанолом, этиленгликолем и др. Сам является растворителем для масел, жиров, воска и подобных им веществ.
запахом эфира, текучая. Не горит, не поддерживает горения, не взрывается. Почти не растворяется в воде; легко смешивается с органическими растворителями, например, с этиловым и метиловым спиртом, уксусной и муравьиной кислотой, пропанолом, бутанолом, этиленгликолем и др. Сам является растворителем для масел, жиров, воска и подобных им веществ.
Перхлорэтилен — самый стабильный реактив среди хлорпроизводных этана и этилена. Реагирует с кислородом, хлором, водой, водородом. Реакцией перхлорэтилена с хлором и фтороводородом получают фреон 113. Взаимодействие с водой приводит к образованию трихлоруксусной кислоты и соляной кислоты.
Меры предосторожности
 Хим.реактив относится к 3-му классу опасности, обладает наркотическим воздействием, токсичен, его категорически нельзя глотать. Длительное вдыхание паров или проглатывание приводит к раздражению дыхательных путей, негативному воздействию на центральную нервную систему, поражению внутренних органов, в том числе, почек и печени.
Хим.реактив относится к 3-му классу опасности, обладает наркотическим воздействием, токсичен, его категорически нельзя глотать. Длительное вдыхание паров или проглатывание приводит к раздражению дыхательных путей, негативному воздействию на центральную нервную систему, поражению внутренних органов, в том числе, почек и печени.
Нежелателен контакт перхлорэтилена с кожей, так как он может проникать через кожу и всасываться в кровь. На кожу и слизистую глаз оказывает раздражающее воздействие, при регулярном контакте с кожей может вызывать дерматит.
Кратковременное вдыхание паров вещества оказывает наркотическое воздействие; вызывает головные боли, возбуждение, головокружение, потерю координации движений, повышенное потоотделение. Затем появляется слабость, тошнота, сонливость вплоть до потери сознания.
Работа с перхлорэтиленом требует принятия мер предосторожности. Опыты с веществом следует проводить в вытяжном шкафу. Работники должны использовать средства защиты кожи, глаз, органов дыхания.
Транспортируют реактив в алюминиевых бочках по 200 л или железнодорожных цистернах. Хранят в бочках в крытых складских помещениях, в которых должны быть установлена приточно-вытяжная вентиляция.
Применение
- Больше половины всего производимого
 перхлорэтилена используется в химчистках для сухой чистки одежды.
перхлорэтилена используется в химчистках для сухой чистки одежды. - В машиностроении и металлургии для обезжиривания поверхностей металлов, промывки промышленных агрегатов.
- На предприятиях по производству игл для одноразовых шприцов.
- В качестве сырья в химпроме для синтеза хладагентов (фреона 113), треххлоруксусной кислоты, активных красителей.
- В кожевенной индустрии для выделки кож и мехов.
- В радиоэлектронике для очистки фотополимерных печатных плат.
- Как универсальный многофункциональный растворитель.
- В текстильной, деревообрабатывающей индустрии.
Достоинства перхлорэтилена как растворителя и очистителя
- Он не требует принятия строгих мер безопасности, т.к. не горит, не воспламеняется и не взрывается.
- Отлично растворяет все органические загрязнения с одежды.
- Легко проникает во все волокна, быстро разлагает загрязнения.
- Не разрушает волокна большинства тканей.
- Не вызывает повреждения окраски на тканях.
- Быстро выветривается, не оставляет остаточных запахов обработки.
- Не оказывает коррозионного воздействия на детали оборудования.
В магазине химических реактивов и лабораторного оборудования «ПраймКемикалсГрупп» вы можете купить перхлорэтилен оптом по выгодной цене и с доставкой. Покупать у нас — удобно!
Перхлорэтилен
Оптовые поставки по России и странам СНГ
Синонимы: Тетрахлорэтилен, Perchloroethylene
Формула: C2Cl4
CAS: 127-18-4
Код ТН ВЭД: 2903230000
Стандарт:
AGC Chemicals ASAHI GLASS CO., LTD, Япония
INOVYN (ранее SOLVAY), Франция
Dowper компании DOW, Германия
HG/T3262-2002, Китай
ТУ 2412-246-00203312-2004, Россия
ТУ 6-01-956-86 c изм. 1,2,3,4, Россия
 Описание:
Описание:Перхлорэтилен технический — бесцветная прозрачная жидкость без примесей эмульгированных и суспендированных частиц.
Перхлорэтилен — универсальный растворитель, применяется для обезжиривания металлов в машиностроении, приборостроении, при обработке фотополимерных печатных плат, в производстве игл к одноразовым шприцам, в текстильной, деревообрабатывающей промышленности, в производстве фреонов и активных красителей. Перхлорэтилен – эффективное средство для сухой химической чистки одежды. Отличительные особенности:
- Высокая плотность обеспечивает отличную чистящую способность благодаря повышенному механическому воздействию на вещи.
- Растворяет практически все органические вещества, находящиеся на загрязненной одежде, включая масла, жиры и воск.
- Высокая текучесть и низкое поверхностное натяжение обеспечивают быстрое проникновение в волокна одежды и эффективное разложение загрязнений.
- Не наносит ущерб большинству обычно используемых тканей, красок, отделок, которые встречаются на текстильных изделиях.
- Быстро и полностью выветривается, не оставляя остаточного запаха.
- Хорошо работает в любых машинах химической чистки.
- Стабильный показатель pH защищает оборудование и одежду и позволяет проводить многократную дистилляцию растворителя без дополнительной стабилизации и нейтрализации.
Перхлорэтилен
AGC Chemicals ASAHI GLASS CO., LTD (соответствует ТУ 6-01-956-86), Япония
| Технические характеристики | Норма |
|---|---|
| Внешний вид | Бесцветная прозрачная жидкость без эмульгированных и суспендированных частиц |
| Содержание основного вещества, %, не менее | 99,6 |
| Массовая доля воды, ppm, не более | 100 |
| Массовая доля кислот в пересчете на HCl, %, не более | 0,001 |
| Интенсивность цвета (Хазен по платиново-кобальтовой шкале) | 15 |
| Дестиляция остатков, °С: Начальная точка кипения, не более Конец кипения, не менее |
117 122 |
| Тест стабильности (с медью), мг/см2, не более | 0,5 |
| pH | 6,0-7,5 |
Перхлорэтилен упаковывают в 200 литровые стальные бочки тяжелого типа по 300кг.
Хранение:Гарантийный срок хранения Перхлорэтилена — 1 год со дня изготовления.
Перхлорэтилен
INOVYN (ранее SOLVAY), Франция
| Технические характеристики | Норма |
|---|---|
| Внешний вид | Прозрачная жидкость |
| Содержание основного вещества, %, не менее | 99,90 |
| Содержание воды, мг/кг, не более | 30 |
| Массовая доля щелочи (as NaOH), мг/кг, не более | 30 |
| Цвет, АРНА, не более | 15 |
| Плотность при 20ºС, гр/мл | 1,620 – 1,625 |
| Окисляющие вещества ( как Cl2), мг/кг, не более | 1,0 |
| 8,0 | |
| Содержание нелетучих веществ, мг/кг, не более | 30 |
Перхлорэтилен упаковывают в 200 литровые стальные бочки тяжелого типа по 330кг.
Хранение:Гарантийный срок хранения Перхлорэтилена — 2 года со дня изготовления.
Перхлорэтилен
Dowper® компании DOW, Германия
| Технические характеристики | Норма |
|---|---|
| Внешний вид | Бесцветная прозрачная жидкость без примеси эмульгированных и суспендированных частиц |
| Содержание основного вещества | 99,9 |
| Температура кипения , °C | 121°C |
| Плотность при 25°C, г/см3, в пределах | 1,6189-1,622 |
| Щелочей в пересчете на NaOH | не более 15-30 мг/кг |
| Содержание воды | 30 мг/кг |
| Молекулярный вес | 165,84 |
Перхлорэтилен упаковывают в 200 литровые стальные бочки тяжелого типа по 330кг.
Хранение:Гарантийный срок хранения Перхлорэтилена Dowper® — 2 года со дня изготовления.
Перхлорэтилен
HG/T3262-2002, Китай
| Технические характеристики | Норма |
|---|---|
| Внешний вид | Бесцветная прозрачная жидкость без примеси эмульгированных и суспендированных частиц |
| Содержание основного вещества, %, не менее | 99,6 |
| Массовая доля воды, %, не более | 0,0050 |
| Щелочность, %, не более | 0,03 |
| Плотность, г/см3 | 1,615-1,625 |
| Интенсивность цвета (Хазен по платиново-кобальтовой шкале) | 15 |
| Дестиляция остатков, %, не более | 0,005 |
Перхлорэтилен упаковывают в 200 литровые стальные бочки тяжелого типа по 300кг.
Хранение:Гарантийный срок хранения Перхлорэтилена — 2 года со дня изготовления.
Транспортировка:
Перхлорэтилен перевозится всеми видами транспорта в соответствии с правилами перевозок грузов.
Выгодно
Низкие цены за счёт прямых контрактов с производителями
Надёжно
Работаем более 20 лет (с 1997 года) под одним ИНН.
Товар на складе
Более 3 000 тонн продукции в наличии на наших складах
Качество гарантируем
Работаем только с проверенными поставщиками.
Доставим как надо
Контролируем товар на всем пути
Перхлорэтилен
Новосибирск: +7(383) 3-34-34-34,
8 (800) 200-11-66,
Иркутск: +7 (3952) 475732
Описание:
Перхлорэтилен технический — бесцветная прозрачная жидкость без примесей эмульгированных и суспендированных частиц.
Применение:
Перхлорэтилен — универсальный растворитель, применяется для обезжиривания металлов в машиностроении, приборостроении, при обработке фотополимерных печатных плат, в производстве игл к одноразовым шприцам, в текстильной, деревообрабатывающей промышленности, в производстве фреонов и активных красителей.
Перхлорэтилен – эффективное средство для сухой химической чистки одежды. Отличительные особенности:
-
Высокая плотность обеспечивает отличную чистящую способность благодаря повышенному механическому воздействию на вещи.
-
Растворяет практически все органические вещества, находящиеся на загрязненной одежде, включая масла, жиры и воск.
-
Высокая текучесть и низкое поверхностное натяжение обеспечивают быстрое проникновение в волокна одежды и эффективное разложение загрязнений.
-
Не наносит ущерб большинству обычно используемых тканей, красок, отделок, которые встречаются на текстильных изделиях.
-
Быстро и полностью выветривается, не оставляя остаточного запаха.
-
Хорошо работает в любых машинах химической чистки.
-
Стабильный показатель pH защищает оборудование и одежду и позволяет проводить многократную дистилляцию растворителя без дополнительной стабилизации и нейтрализации.
Перхлорэтилен AGC Chemicals ASAHI GLASS CO., LTD (соответствует ТУ 6-01-956-86), Япония
| Технические характеристики: | Норма |
| Внешний вид | Бесцветная прозрачная жидкость без эмульгированных и суспендированных частиц |
| Содержание основного вещества, %, не менее | 99,6 |
| Массовая доля воды, ppm, не более | 100 |
| Массовая доля кислот в пересчете на HCl, %, не более | 0,001 |
| Интенсивность цвета (Хазен по платиново-кобальтовой шкале) | 15 |
| Дестиляция остатков, °С: Начальная точка кипения, не более Конец кипения, не менее |
117 122 |
| Тест стабильности (с медью), мг/см2, не более | 0,5 |
| pH | 6,0-7,5 |
Упаковка:
Перхлорэтилен упаковывают в 200 литровые стальные бочки тяжелого типа по 300кг.
Хранение:
Гарантийный срок хранения Перхлорэтилена — 1 год со дня изготовления.
Перхлорэтилен INOVYN (ранее SOLVAY), Франция
| Технические характеристики: | Норма |
| Внешний вид | Прозрачная жидкость |
| Содержание основного вещества, %, не менее | 99,90 |
| Содержание воды, мг/кг, не более | 30 |
| Массовая доля щелочи (as NaOH), мг/кг, не более | 30 |
| Цвет, АРНА, не более | 15 |
| Плотность при 20ºС, гр/мл | 1,620 – 1,625 |
| Окисляющие вещества ( как Cl2), мг/кг, не более | 1,0 |
| pH, не менее | 8,0 |
| Содержание нелетучих веществ, мг/кг, не более | 30 |
Упаковка:
Перхлорэтилен упаковывают в 200 литровые стальные бочки тяжелого типа по 330кг.
Хранение:
Гарантийный срок хранения Перхлорэтилена — 2 года со дня изготовления.
Перхлорэтилен Dowper® компании DOW, Германия
| Технические характеристики: | Норма |
| Внешний вид | Бесцветная прозрачная жидкость без примеси эмульгированных и суспендированных частиц |
| Содержание основного вещества | 99,9 |
| Температура кипения , °C | 121°C |
| Плотность при 25°C, г/см3, в пределах | 1,6189-1,622 |
| Щелочей в пересчете на NaOH | не более 15-30 мг/кг |
| Содержание воды | 30 мг/кг |
| Молекулярный вес | 165,84 |
Упаковка:
Перхлорэтилен упаковывают в 200 литровые стальные бочки тяжелого типа по 330кг.
Хранение:
Гарантийный срок хранения Перхлорэтилена Dowper® — 2 года со дня изготовления.
Перхлорэтилен HG/T3262-2002, Китай
| Технические характеристики: | Норма |
| Внешний вид | Бесцветная прозрачная жидкость без примеси эмульгированных и суспендированных частиц |
| Содержание основного вещества, %, не менее | 99,6 |
| Массовая доля воды, %, не более | 0,0050 |
| Щелочность, %, не более | 0,03 |
| Плотность, г/см3 | 1,615-1,625 |
| Интенсивность цвета (Хазен по платиново-кобальтовой шкале) | 15 |
| Дестиляция остатков, %, не более | 0,005 |
Упаковка:
Перхлорэтилен упаковывают в 200 литровые стальные бочки тяжелого типа по 300кг.
Хранение:
Гарантийный срок хранения Перхлорэтилена — 2 года со дня изготовления.
ТУ 6-01-956-86 c изм. 1,2,3,4, Россия
— в настоящее время производство остановлено на неопределенный срок;
ТУ 2412-246-00203312-2004, Россия
— в настоящее время производство остановлено на неопределенный срок.
|
Технические характеристики: |
Перхлорэтилен ТУ 6-01-956-86 c изм. 1,2,3,4 |
Перхлорэтилен стабилизированный |
| Внешний вид | Бесцветная прозрачная жидкость без эмульгированных и суспендированных частиц | |
| Плотность при 20°C, г/см3 | 1,620-1,624 | 1,619-1,624 |
| Массовая доля хлорорганических примесей, %, не более | 0,03 | 0,1 |
| Массовая доля кислот в пересчете на HCl, %, не более | 0,0005 | — |
| Щелочей в пересчете на NaOH, %, не более | 0,0015 | pH=7-10 |
| Массовая доля воды, %, не более | 0,003 | 0,01 |
| Массовая доля остатка после выпаривания, %, не более | 0,0015 | — |
| Объемная доля (%, не менее) продукта, перегоняющегося в температурном интервале (0С) при 101,3 кПа (760 мм рт. ст.) |
95 120-122 |
95 118-122 |
Упаковка:
Перхлорэтилен упаковывают в 200 литровые стальные бочки тяжелого типа по 330кг.
Хранение:
Гарантийный срок хранения Перхлорэтилена — 1 год со дня изготовления.
Траспортировка:
Перхлорэтилен перевозится всеми видами транспорта в соответствии с правилами перевозок грузов.
Перхлорэтилен реализует компания «Логосиб».
Цены:
Несмотря на изначально низкие цены, мы делаем скидки в зависимости от объема закупаемого товара.
Если Вы имеете предложение с более низкими ценами, звоните – будем договариваться о лучших условиях для Вас.
Качество:
Мы работаем непосредственно с производителями, поэтому обеспечиваем наших клиентов товарами высокого качества.
Оформление и отгрузка:
Благодаря отлаженной работе офиса и складов, мы предоставляем быстрое оформление и отгрузку товаров.
Доставка:
Мы предлагаем доставку товаров по России:
•автотранспортом;
•железнодорожными контейнерами, вагонами;
•через транспортные компании.
Для получения подробной информации о ценах на перхлорэтилен и условиях поставки звоните нашим специалистам по телефонам:
+7 (383) 3-34-34-34 и 8-800-200-11-66 (бесплатный звонок по России).
Тетрахлорэтилен — Википедия с видео // WIKI 2
| |||
| Систематическое наименование | 1,1,2,2-тетрахлорэтен | ||
|---|---|---|---|
| Традиционные названия | перхлорэтилен | ||
| Хим. формула | C2Cl4 | ||
| Рац. формула | C2Cl4 | ||
| Состояние | бесцветная жидкость | ||
| Молярная масса | 165,83 г/моль | ||
| Плотность | 1,6230 г/см³ | ||
| Динамическая вязкость | 0,88·10-3 Па·с | ||
| Энергия ионизации | 9,32 ± 0,01 эВ[5] | ||
| Температура | |||
| • плавления | −22,4 °C | ||
| • кипения | 121 °C | ||
| • вспышки | 45 °C | ||
| Критическая точка | |||
| • температура | 340 °C | ||
| • давление | 44,3 атм | ||
| Уд. теплоёмк. | 858 Дж/(кг·К) | ||
| Энтальпия | |||
| • образования | −51,1 кДж/моль | ||
| • кипения | 34,7 кДж/моль | ||
| Давление пара | 1,86 кПа (20 °С) | ||
| Растворимость | |||
| • в воде | 0,015 г/100 мл | ||
| Диэлектрическая проницаемость | 2,20 | ||
| Показатель преломления | 1,5044 | ||
| Дипольный момент | 0 Кл·м[6] | ||
| Рег. номер CAS | 127-18-4 | ||
| PubChem | 31373 | ||
| Рег. номер EINECS | 204-825-9 | ||
| SMILES | |||
| InChI | |||
| RTECS | KX3850000 | ||
| ChEBI | 17300 | ||
| Номер ООН | 1897 | ||
| ChemSpider | 13837281 | ||
| Предельная концентрация | 10 мг/м3 | ||
| Токсичность | При длительном контакте оказывает токсическое действие на ЦНС и печень | ||
| Фразы риска (R) | R40, R51/53 | ||
| Фразы безопасности (S) | R23, R36/37, R61 | ||
| Краткие характер. опасности (H) | |||
| Меры предостор. (P) | |||
| Пиктограммы СГС |   | ||
| NFPA 704 |  | ||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
 Медиафайлы на Викискладе Медиафайлы на Викискладе | |||
Тетрахлорэтилен (перхлорэтилен) — бесцветная жидкость с резким запахом, хлорорганический растворитель. Широкое применение находит в химчистке и обезжиривании металлов.
Энциклопедичный YouTube
1/5
Просмотров:639
404
31 381
40 783
2 632
✪ ПОЛИМЕРИЗАЦИЯ Органическая Тетрахлорэтилен Этен Хлорвинил Бутадиен Задание 23 Химия ЕГЭ 2016
✪ Как измерять уровень pH перхлора в машине химчистки
✪ 4.2. Алкадиены (диены): Способы получения. ЕГЭ по химии
✪ 4.3. Алкадиены (диены): Химические свойства. ЕГЭ по химии
✪ Реакции свободных радикалов
Содержание
Получение
Впервые тетрахлорэтилен был получен М. Фарадеем при термическом разложении гексахлорэтана[4].
- C C l 3 − C C l 3 → [ t ] C C l 2 = C C l 2 + C l 2 {\displaystyle {\mathsf {CCl_{3}{-}CCl_{3}{\xrightarrow[{}]{[t]}}CCl_{2}{=}CCl_{2}+Cl_{2}}}}
В промышленности тетрахлорэтилен получают несколькими способами. Первый метод, игравший важное промышленное значение в прошлом, заключается в получении тетрахлорэтилена из ацетилена через трихлорэтилен. Хлорирование трихлорэтилена в жидкой фазе при температуре 70—110 °С в присутствии FeCl3 (0,1—1% масс.) даёт пентахлорэтан, который затем подвергают жидкофазному (80—120 °С, Ca(OH)2) или каталитическому термическому крекингу (170—330 °С, активированный уголь). Общий выход достигает 90—94% по ацетилену. Однако после повышения цен на ацетилен этот метод утратил своё значение[7].
- C 2 H 2 + 2 C l 2 → C 2 H 2 C l 4 {\displaystyle {\mathsf {C_{2}H_{2}+2Cl_{2}}}\rightarrow {\mathsf {C_{2}H_{2}Cl_{4}}}}
- C 2 H 2 C l 4 → C 2 H C l 3 + H C l {\displaystyle {\mathsf {C_{2}H_{2}Cl_{4}}}\rightarrow {\mathsf {C_{2}HCl_{3}+HCl}}}
- C 2 H C l 3 + C l 2 → C 2 H C l 5 {\displaystyle {\mathsf {C_{2}HCl_{3}+Cl_{2}}}\rightarrow {\mathsf {C_{2}HCl_{5}}}}
- C 2 H C l 5 → C 2 C l 4 + H C l {\displaystyle {\mathsf {C_{2}HCl_{5}}}\rightarrow {\mathsf {C_{2}Cl_{4}+HCl}}}
Главным методом получения тетрахлорэтилена является окислительное хлорирование этилена или 1,2-дихлорэтана. Субстрат, кислород и хлор реагируют в присутствии катализатора (хлорид калия, хлорид меди(II) на силикагеле) при 420—460 °С. В результате серии реакций происходит образование трихлорэтилена и тетрахлорэтилена. Выход по хлору составляет 90—98%. Побочным процессом является окисление этилена до оксидов углерода, который ускоряется при превышении оптимальной температуры процесса. Продукты разделяются и очищаются перегонкой. Соотношение продуктов можно регулировать соотношением реагентов[8].
- C H 2 = C H 2 + C H 2 C l − C H 2 C l + 2 , 5 C l 2 + 1 , 75 O 2 → C H C l = C C l 2 + C C l 2 = C C l 2 + 3 , 5 H 2 O {\displaystyle {\mathsf {CH_{2}{=}CH_{2}+CH_{2}Cl{-}CH_{2}Cl+2,5Cl_{2}+1,75O_{2}}}\rightarrow {\mathsf {CHCl{=}CCl_{2}+CCl_{2}{=}CCl_{2}+3,5H_{2}O}}}
Высокотемпературное хлорирование углеводородов C1—C3 или их хлорпроизводных является вторым по важности источником тетрахлорэтилена. Он не требует чистого сырья и позволяет использовать отходы производства[9].
В 1985 году производство тетрахлорэтилена в США составило 380 тыс. тонн, в Европе — 450 тыс. тонн. Из-за оптимизации процесса химчистки и уменьшения выбросов вещества в атмосферу, а также по причине ужесточающихся экологических требований производство тетрахлорэтилена сокращалось с конца 1970-х годов. Уже в 1993 году объёмы производства в США оценивались в 123 тыс. тонн в год и 74 тыс. тонн в ФРГ[10].
Физические свойства
Тетрахлорэтилен негорюч, невзрывоопасен и не самовоспламеняется[1]. Он смешивается с большинством органических растворителей. С некоторыми растворителями тетрахлорэтилен образует азеотропные смеси.
| Второй компонент | Массовая доля тетрахлорэтилена | Т. кип. азеотропной смеси при 101,3 кПа, °С |
|---|---|---|
| вода | 15,9 | 87,1 |
| метанол | 63,5 | 63,8 |
| этанол | 63,0 | 76,8 |
| пропанол-1 | 48,0 | 94,1 |
| пропанол-2 | 70,0 | 81,7 |
| бутанол-1 | 29,0 | 109,0 |
| бутанол-2 | 40,0 | 103,1 |
| муравьиная кислота | 50,0 | 88,2 |
| уксусная кислота | 38,5 | 107,4 |
| пропионовая кислота | 8,5 | 119,2 |
| изомасляная кислота | 3,0 | 120,5 |
| ацетамид | 2,6 | 120,5 |
| пиррол | 19,5 | 113,4 |
| 1,1,2-трихлорэтан | 43,0 | 112,0 |
| 1-хлор-2,3-эпоксипропан | 51,5 | 110,1 |
| этиленгликоль | 6,0 | 119,1 |
Химические свойства
Тетрахлорэтилен является самым устойчивым соединением из всех хлорпроизводных этана и этилена. Он устойчив к гидролизу и меньше способствует коррозии, чем другие хлорсодержащие растворители[4].
Окисление
Окисление тетрахлорэтилена на воздухе даёт трихлорацетилхлорид и фосген, процесс протекает под действием УФ-излучения:
- 2 C C l 2 = C C l 2 + 1 , 5 O 2 → [ h v ] C C l 3 − C O C l + 2 C O C l 2 {\displaystyle {\mathsf {2CCl_{2}{=}CCl_{2}+1,5O_{2}{\xrightarrow[{}]{[hv]}}CCl_{3}{-}COCl+2COCl_{2}}}}
Этот процесс может быть замедлен при использовании аминов и фенолов в качестве стабилизаторов (обычно применяют N-метилпиррол и N-метилморфолин). Процесс, однако, может использоваться для производства трихлорацетилхлорида[4].
Хлорирование
При реакции тетрахлорэтилена с хлором в присутствии небольшого количества хлорида железа(III) FeCl3 (0,1 %) в качестве катализатора при 50-80 °С образуется гексахлорэтан[11]:
- C C l 2 = C C l 2 + C l 2 → [ F e C l 3 ] C C l 3 − C C l 3 {\displaystyle {\mathsf {CCl_{2}{=}CCl_{2}+Cl_{2}{\xrightarrow[{}]{[FeCl_{3}]}}CCl_{3}{-}CCl_{3}}}}
По реакции тетрахлорэтилена с хлором и HF в присутствии SbF5 синтезируют фреон-113[1].
- C C l 2 = C C l 2 + 3 H F + C l 2 → [ S b F 5 ] C C l F 2 − C C l 2 F + 3 H C l {\displaystyle {\mathsf {CCl_{2}{=}CCl_{2}+3HF+Cl_{2}{\xrightarrow[{}]{[SbF_{5}]}}CClF_{2}{-}CCl_{2}F+3HCl}}}
Гидролиз
Происходит только при нагревании в кислой среде (лучше всего с серной кислотой):
- C C l 2 = C C l 2 + H 2 O → [ t , H 2 S O 4 ] C C l 3 − C O O H + H C l {\displaystyle {\mathsf {CCl_{2}{=}CCl_{2}+H_{2}O{\xrightarrow[{}]{[t,H_{2}SO_{4}]}}CCl_{3}{-}COOH+HCl}}}
при этом образуется трихлоруксусная кислота.
Восстановление
Тетрахлорэтилен может быть частично или полностью восстановлен в газовой фазе в присутствии таких катализаторов как: никель, палладий, платиновая чернь и др.:
- C C l 2 = C C l 2 + 2 H 2 → [ t , k a t : N i , P d , P t O 2 ] 2 C + 4 H C l {\displaystyle {\mathsf {CCl_{2}{=}CCl_{2}+2H_{2}{\xrightarrow[{}]{[t,kat:Ni,Pd,PtO_{2}]}}2C+4HCl}}}
Применение
Около 60 % всего расходуемого тетрахлорэтилена находит применение как растворитель в химчистке. Тетрахлорэтилен заменил все другие растворители в этой области, поскольку он не горюч и может быть безопасно использован без особых мер предосторожности. Из-за своей устойчивости тетрахлорэтилен содержит низкий процент стабилизаторов и по этой же причине используется наряду с трихлорэтиленом и 1,1,1-трихлорэтаном для обезжиривания металлов, особенно, алюминия. В меньших количествах тетрахлорэтилен применяется в текстильной промышленности и производстве фреона-113[12][1].
В нефтепереработке тетрахлорэтилен наряду с дихлорэтаном применяется в процессе оксихлорирования (для восстановления активности) биметаллических катализаторов на установках каталитического риформинга и низкотемпературной изомеризации[13].
Токсичность
Перхлорэтилен токсичен. При длительном вдыхании паров перхлорэтилена человек начинает смеяться, как при реакции от оксида азота, после чего могут возникнуть признаки тошноты, склонность ко сну, видимая припухлость надбровных дуг и щек. При попадании на кожу перхлорэтилен оставляет ожог, и трескается место кожи. При попадании небольшого количества в глаза, достаточно просто промыть большим количеством воды.
Примечания
- ↑ 1 2 3 4 Химическая энциклопедия / Под ред. И. Л. Кнунянца. — М: Большая Российская энциклопедия, 1992. — Т. 4. — С. 557. — ISBN 5-85270-039-8.
- ↑ Dean J. A. Lange’s Handbook of Chemistry. — McGraw-Hill, 1999. — ISBN 0-07-016384-7.
- ↑ Sigma-Aldrich. Tetrachloroethylene, anhydrous (неопр.). Дата обращения 24 апреля 2013. Архивировано 29 апреля 2013 года.
- ↑ 1 2 3 4 5 Ullmann, 2006, p. 75.
- ↑ http://www.cdc.gov/niosh/npg/npgd0599.html
- ↑ CRC Handbook of Chemistry and Physics (англ.) / W. M. Haynes — 95 — Boca Raton: CRC Press, 2014. — P. 15—21. — ISBN 978-1-4822-0868-9
- ↑ Ullmann, 2006, p. 76.
- ↑ Ullmann, 2006, p. 74, 76.
- ↑ Ullmann, 2006, p. 77—78.
- ↑ Ullmann, 2006, p. 79—80.
- ↑ Ошин Л.А. Промышленные хлорорганические продукты. — М.: Химия, 1978. — 656 с.
- ↑ Ullmann, 2006, p. 79.
- ↑ |ISOFORM™Isomerization Grade/ Reforming Grade
Литература
- Rossberg M., Lendle W., Pfleiderer G., Tögel A., Dreher E.-L., Langer E., Rassaerts H., Kleinschmidt P., Strack H., Cook R., Beck U., Lipper K.-A., Torkelson T. R., Löser E., Beutel K. K., Mann T. Chlorinated Hydrocarbons // Ullmann’s Encyclopedia of Industrial Chemistry. — Wiley, 2006. — doi:10.1002/14356007.a06_233.pub2.
- U.S. Department of Health and Human Services. Toxicological profile for tetrachloroethylene (неопр.) (1997). Дата обращения 24 апреля 2013. Архивировано 29 апреля 2013 года.
![{\displaystyle {\mathsf {CCl_{2}{=}CCl_{2}+2H_{2}{\xrightarrow[{}]{[t,kat:Ni,Pd,PtO_{2}]}}2C+4HCl}}}](/800/600/https/wiki2.org/s/i/modif.png) Эта страница в последний раз была отредактирована 22 июля 2020 в 21:55.
Эта страница в последний раз была отредактирована 22 июля 2020 в 21:55.| Тетрахлорэтилен[1][2][3][4] | |||
|---|---|---|---|
| |||
| Систематическое наименование | 1,1,2,2-тетрахлорэтен | ||
| Традиционные названия | перхлорэтилен | ||
| Хим. формула | C2Cl4 | ||
| Рац. формула | C2Cl4 | ||
| Состояние | бесцветная жидкость | ||
| Молярная масса | 165,83 г/моль | ||
| Плотность | 1,6230 г/см³ | ||
| Динамическая вязкость | 0,88·10-3 Па·с | ||
| Энергия ионизации | 9,32 ± 0,01 эВ[5] | ||
| Температура | |||
| • плавления | −22,4 °C | ||
| • кипения | 121 °C | ||
| • вспышки | 45 °C | ||
| Критическая точка | |||
| • температура | 340 °C | ||
| • давление | 44,3 атм | ||
| Уд. теплоёмк. | 858 Дж/(кг·К) | ||
| Энтальпия | |||
| • образования | −51,1 кДж/моль | ||
| • кипения | 34,7 кДж/моль | ||
| Давление пара | 1,86 кПа (20 °С) | ||
| Растворимость | |||
| • в воде | 0,015 г/100 мл | ||
| Диэлектрическая проницаемость | 2,20 | ||
| Показатель преломления | 1,5044 | ||
| Дипольный момент | 0 Кл·м[6] | ||
| Рег. номер CAS | 127-18-4 | ||
| PubChem | |||
Перхлорэтилен очистка
Перхлорэтилен
Перхлорэтилен:
ПЕРХЛОРЭТИЛЕН — органический растворитель C2CL4. Представляет собой бесцветную жидкость с характерным эфирным запахом. Негорюч, невзрывоопасен и не самовоспламеняется.
ПЕРХЛОРЭТИЛЕН— обладает уникальными свойствами растворения большинства видов жиров. Поэтому перхлорэтилен применяется для химической чистки одежды. Более 70% всего объема перхлорэтилена (тетрахлорэтилена) находит применение в химчистке. Обладая отличными свойствами расщепления жиров, при этом являясь негорючим и безопасным растворителем он стал незаменимым материалом в текстильной промышленности. Перхлорэтилен (PCE) получают окислительным хлорированием этилена. В результате химической реакции происходит образование трихлорэтилена и тетрахлорэтилена.
Технические характеристики ПЕРХЛОРЭТИЛЕНА:
Растворимость в воде: 0,015 г/100мл
Диэлектр. прониц. 2,20
Области применения перхлорэтилена (тетрахлорэтилена):
- Перхлорэтилен широко применяется в текстильной промышленности.
- Обезжиривания металлов.
- В химчистке.
- В приборостроении.
- В нефтепереработке.
Физические свойства перхлорэтилена:
Перхлорэтилен хорошо растворим с большинством органических растворителей.
| № | Характеристики | Величина |
| 1 | Вид | Бесцветная жидкость |
| 2 | Молярная масса | 165,83 г/моль |
| 3 | Плотность | 1,62 г/см3 |
| 4 | Динамическая вязкость | 0,88*10-3 Па*с |
| 5 | Т. плав. | -22,4 |
| 6 | Т кип. | 121 |
| 7 | Т.всп. | 45 |
| 8 | Кр. темп. | 340 |
| 9 | Кр. давл | 44,3 атм |
| 10 | Уд. теплоемкость | 858 дж/кг*К |
| 11 | Энтальпия кипения | 34,7 кДж/моль |
| 12 | Давление пара | 1,86 кПа |
Очистка загрязненного перхлорэтилена
Перхлорэтилен Википедия
| Тетрахлорэтилен[1][2][3][4] | |||
|---|---|---|---|
| |||
| Систематическое наименование | 1,1,2,2-тетрахлорэтен | ||
| Традиционные названия | перхлорэтилен | ||
| Хим. формула | C2Cl4 | ||
| Рац. формула | C2Cl4 | ||
| Состояние | бесцветная жидкость | ||
| Молярная масса | 165,83 г/моль | ||
| Плотность | 1,6230 г/см³ | ||
| Динамическая вязкость | 0,88·10-3 Па·с | ||
| Энергия ионизации | 9,32 ± 0,01 эВ[5] | ||
| Температура | |||
| • плавления | −22,4 °C | ||
| • кипения | 121 °C | ||
| • вспышки | 45 °C | ||
| Критическая точка | |||
| • температура | 340 °C | ||
| • давление | 44,3 атм | ||
| Уд. теплоёмк. | 858 Дж/(кг·К) | ||
| Энтальпия | |||
| • образования | −51,1 кДж/моль | ||
| • кипения | 34,7 кДж/моль | ||
| Давление пара | 1,86 кПа (20 °С) | ||
| Растворимость | |||
| • в воде | 0,015 г/100 мл | ||
| Диэлектрическая проницаемость | 2,20 | ||
| Показатель преломления | 1,5044 | ||
| Дипольный момент | 0 Кл·м[6] | ||
| Рег. номер CAS | 127-18-4 | ||
| PubChem | 31373 | ||
| Рег. номер EINECS | 204-825-9 | ||
| SMILES | |||
| InChI | |||
| RTECS | KX3850000 | ||
| ChEBI | 17300 | ||
| Номер ООН | 1897 | ||
| ChemSpider | 13837281 | ||
| Предельная концентрация | 10 мг/м3 | ||
| Токсичность | При длительном контакте оказывает токсическое действие на ЦНС и печень | ||
| Фразы риска (R) | R40, R51/53 | ||
| Фразы безопасности (S) | R23, R36/37, R61 | ||
| Краткие характер. опасности (H) | |||
| Меры предостор. (P) | |||
| Пиктограммы СГС | |||
| NFPA 704 | |||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
| Медиафайлы на Викискладе | |||
Тетрахлорэтилен (перхлорэтилен) — бесцветная жидкость с резким запахом, хлорорганический растворитель. Широкое применение находит в химчистке и обезжиривании металлов.
Получение
Впервые тетрахлорэтилен был получен М. Фарадеем при термическом разложении гексахлорэтана[4].
- C C l 3 − C C l 3 → [ t ] C C l 2 = C C l 2 + C l 2 {\displaystyle {\mathsf {CCl_{3}{-}CCl_{3}{\xrightarrow[{}]{[t]}}CCl_{2}{=}CCl_{2}+Cl_{2}}}}
В промышленности тетрахлорэтилен получают несколькими способами. Первый метод, игравший важное промышленное значение в прошлом, заключается в получении тетрахлорэтилена из ацетилена через трихлорэтилен. Хлорирование трихлорэтилена в жидкой фазе при температуре 70—110 °С в присутствии FeCl3 (0,1—1% масс.) даёт пентахлорэтан, который затем подвергают жидкофазному (80—120 °С, Ca(OH)2) или каталитическому термическому крекингу (170—330 °С, активированный уголь). Общий выход достигает 90—94% по ацетилену. Однако после повышения цен на ацетилен этот метод утратил своё значение[7].
- C 2 H 2 + 2 C l 2 → C 2 H 2 C l 4 {\displaystyle {\mathsf {C_{2}H_{2}+2Cl_{2}}}\rightarrow {\mathsf {C_{2}H_{2}Cl_{4}}}}
- C 2 H 2 C l 4 → C 2 H C l 3 + H C l {\displaystyle {\mathsf {C_{2}H_{2}Cl_{4}}}\rightarrow {\mathsf {C_{2}HCl_{3}+HCl}}}
- C 2 H C l 3 + C l 2 → C 2 H C l 5 {\displaystyle {\mathsf {C_{2}HCl_{3}+Cl_{2}}}\rightarrow {\mathsf {C_{2}HCl_{5}}}}
- C 2 H C l 5 → C 2 C l 4 + H C l {\displaystyle {\mathsf {C_{2}HCl_{5}}}\rightarrow {\mathsf {C_{2}Cl_{4}+HCl}}}
Главным методом получения тетрахлорэтилена является окислительное хлорирование этилена или 1,2-дихлорэтана. Субстрат, кислород и хлор реагируют в присутствии катализатора (хлорид калия, хлорид меди(II) на силикагеле) при 420—460 °С. В результате серии реакций происходит образование трихлорэтилена и тетрахлорэтилена. Выход по хлору составляет 90—98%. Побочным процессом является окисление этилена до оксидов углерода, который ускоряется при превышении оптимальной температуры процесса. Продукты разделяются и очищаются перегонкой. Соотношение продуктов можно регулировать соотношением реагентов[8].
- C H 2 = C H 2 + C H 2 C l − C H 2 C l + 2 , 5 C l 2 + 1 , 75 O 2 → C H C l = C C l 2 + C C l 2 = C C l 2 + 3 , 5 H 2 O {\displaystyle {\mathsf {CH_{2}{=}CH_{2}+CH_{2}Cl{-}CH_{2}Cl+2,5Cl_{2}+1,75O_{2}}}\rightarrow {\mathsf {CHCl{=}CCl_{2}+CCl_{2}{=}CCl_{2}+3,5H_{2}O}}}
Высокотемпературное хлорирование углеводородов C1—C3 или их хлорпроизводных является вторым по важности источником тетрахлорэтилена. Он не требует чистого сырья и позволяет использовать отходы производства[9].
В 1985 году производство тетрахлорэтилена в США составило 380 тыс. тонн, в Европе — 450 тыс. тонн. Из-за оптимизации процесса химчистки и уменьшения выбросов вещества в атмосферу, а также по причине ужесточающихся экологических требований производство тетрахлорэтилена сокращалось с конца 1970-х годов. Уже в 1993 году объёмы производства в США оценивались в 123 тыс. тонн в год и 74 тыс. тонн в ФРГ[10].
Физические свойства
Тетрахлорэтилен негорюч, невзрывоопасен и не самовоспламеняется[1]. Он смешивается с большинством органических растворителей. С некоторыми растворителями тетрахлорэтилен образует азеотропные смеси.
| Второй компонент | Массовая доля тетрахлорэтилена | Т. кип. азеотропной смеси при 101,3 кПа, °С |
|---|---|---|
| вода | 15,9 | 87,1 |
| метанол | 63,5 | 63,8 |
| этанол | 63,0 | 76,8 |
| пропанол-1 | 48,0 | 94,1 |
| пропанол-2 | 70,0 | 81,7 |
| бутанол-1 | 29,0 | 109,0 |
| бутанол-2 | 40,0 | 103,1 |
| муравьиная кислота | 50,0 | 88,2 |
| уксусная кислота | 38,5 | 107,4 |
| пропионовая кислота | 8,5 | 119,2 |
| изомасляная кислота | 3,0 | 120,5 |
| ацетамид | 2,6 | 120,5 |
| пиррол | 19,5 | 113,4 |
| 1,1,2-трихлорэтан | 43,0 | 112,0 |
| 1-хлор-2,3-эпоксипропан | 51,5 | 110,1 |
| этиленгликоль | 6,0 | 119,1 |
Химические свойства
Тетрахлорэтилен является самым устойчивым соединением из всех хлорпроизводных этана и этилена. Он устойчив к гидролизу и меньше способствует коррозии, чем другие хлорсодержащие растворители[4].
Окисление
Окисление тетрахлорэтилена на воздухе даёт трихлорацетилхлорид и фосген, процесс протекает под действием УФ-излучения:
- 2 C C l 2 = C C l 2 + 1 , 5 O 2 → [ h v ] C C l 3 − C O C l + 2 C O C l 2 {\displaystyle {\mathsf {2CCl_{2}{=}CCl_{2}+1,5O_{2}{\xrightarrow[{}]{[hv]}}CCl_{3}{-}COCl+2COCl_{2}}}}
Этот процесс может быть замедлен при использовании аминов и фенолов в качестве стабилизаторов (обычно применяют N-метилпиррол и N-метилморфолин). Процесс, однако, может использоваться для производства трихлорацетилхлорида[4].
Хлорирование
При реакции тетрахлорэтилена с хлором в присутствии небольшого количества хлорида железа(III) FeCl3 (0,1 %) в качестве катализатора при 50-80 °С образуется гексахлорэтан[11]:
- C C l 2 = C C l 2 + C l 2 → [ F e C l 3 ] C C l 3 − C C l 3 {\displaystyle {\mathsf {CCl_{2}{=}CCl_{2}+Cl_{2}{\xrightarrow[{}]{[FeCl_{3}]}}CCl_{3}{-}CCl_{3}}}}
По реакции тетрахлорэтилена с хлором и HF в присутствии SbF5 синтезируют фреон-113[1].
- C C l 2 = C C l 2 + 3 H F + C l 2 → [ S b F 5 ] C C l F 2 − C C l 2 F + 3 H C l {\displaystyle {\mathsf {CCl_{2}{=}CCl_{2}+3HF+Cl_{2}{\xrightarrow[{}]{[SbF_{5}]}}CClF_{2}{-}CCl_{2}F+3HCl}}}
Гидролиз
Происходит только при нагревании в кислой среде (лучше всего с серной кислотой):
- C C l 2 = C C l 2 + H 2 O → [ t , H 2 S O 4 ] C C l 3 − C O O H + H C l {\displaystyle {\mathsf {CCl_{2}{=}CCl_{2}+H_{2}O{\xrightarrow[{}]{[t,H_{2}SO_{4}]}}CCl_{3}{-}COOH+HCl}}}
при этом образуется трихлоруксусная кислота.
Восстановление
Тетрахлорэтилен может быть частично или полностью восстановлен в газовой фазе в присутствии таких катализаторов как: никель, палладий, платиновая чернь и др.:
- C C l 2 = C C l 2 + 2 H 2 → [ t , k a t : N i , P d , P t O 2 ] 2 C + 4 H C l {\displaystyle {\mathsf {CCl_{2}{=}CCl_{2}+2H_{2}{\xrightarrow[{}]{[t,kat:Ni,Pd,PtO_{2}]}}2C+4HCl}}}
Применение
Около 60 % всего расходуемого тетрахлорэтилена находит применение как растворитель в химчистке. Тетрахлорэтилен заменил все другие растворители в этой области, поскольку он не горюч и может быть безопасно использован без особых мер предосторожности. Из-за своей устойчивости тетрахлорэтилен содержит низкий процент стабилизаторов и по этой же причине используется наряду с трихлорэтиленом и 1,1,1-трихлорэтаном для обезжиривания металлов, особенно, алюминия. В меньших количествах тетрахлорэтилен применяется в текстильной промышленности и производстве фреона-113[12][1].
В нефтепереработке тетрахлорэтилен наряду с дихлорэтаном применяется в процессе оксихлорирования (для восстановления активности) биметаллических катализаторов на установках каталитического риформинга и низкотемпературной изомеризации[13].
Токсичность
Перхлорэтилен токсичен. При длительном вдыхании паров перхлорэтилена человек начинает смеяться, как при реакции от оксида азота, после чего могут возникнуть признаки тошноты, склонность ко сну, видимая припухлость надбровных дуг и щек. При попадании на кожу перхлорэтилен оставляет ожог, и трескается место кожи. При попадании небольшого количества в глаза, достаточно просто промыть большим количеством воды.
Примечания
- ↑ 1 2 3 4 Химическая энциклопедия / Под ред. И. Л. Кнунянца. — М: Большая Российская энциклопедия, 1992. — Т. 4. — С. 557. — ISBN 5-85270-039-8.
- ↑ Dean J. A. Lange’s Handbook of Chemistry. — McGraw-Hill, 1999. — ISBN 0-07-016384-7.
- ↑ Sigma-Aldrich. Tetrachloroethylene, anhydrous (неопр.). Дата обращения 24 апреля 2013. Архивировано 29 апреля 2013 года.
- ↑ 1 2 3 4 5 Ullmann, 2006, p. 75.
- ↑ http://www.cdc.gov/niosh/npg/npgd0599.html
- ↑ CRC Handbook of Chemistry and Physics (англ.) / W. M. Haynes — 95 — Boca Raton: CRC Press, 2014. — P. 15—21. — ISBN 978-1-4822-0868-9
- ↑ Ullmann, 2006, p. 76.
- ↑ Ullmann, 2006, p. 74, 76.
- ↑ Ullmann, 2006, p. 77—78.
- ↑ Ullmann, 2006, p. 79—80.
- ↑ Ошин Л.А. Промышленные хлорорганические продукты. — М.: Химия, 1978. — 656 с.
- ↑ Ullmann, 2006, p. 79.
- ↑ |ISOFORM™Isomerization Grade/ Reforming Grade
Литература
- Rossberg M., Lendle W., Pfleiderer G., Tögel A., Dreher E.-L., Langer E., Rassaerts H., Kleinschmidt P., Strack H., Cook R., Beck U., Lipper K.-A., Torkelson T. R., Löser E., Beutel K. K., Mann T. Chlorinated Hydrocarbons // Ullmann’s Encyclopedia of Industrial Chemistry. — Wiley, 2006. — doi:10.1002/14356007.a06_233.pub2.
- U.S. Department of Health and Human Services. Toxicological profile for tetrachloroethylene (неопр.) (1997). Дата обращения 24 апреля 2013. Архивировано 29 апреля 2013 года.
Где находится перхлорэтилен (PCE, PERC)?
- Химчистка одежды — выделение небольшого количества перхлорэтилена
- Потребительские товары — клеи, пятновыводители, жидкости для коррекции пишущей машинки, лак для обуви, печатные краски, лакокрасочные материалы и бытовые чистящие средства
- Отделочники тканей
Как я могу подвергаться воздействию перхлорэтилена (PCE, PERC)?
Перхлорэтилен (PCE, PERC) обычно попадает в организм через:


Вдыхание (дыхание)
- Дыхательные выделения из одежды, подвергнутой химической чистке, или продуктов, содержащих перхлорэтилен

Контакт с кожей
- Прикосновение к химчистке одежды, изделий из перхлорэтилена или загрязненной ими почвы
- Купание в воде, загрязненной перхлорэтиленом
Что происходит, когда я подвергаюсь воздействию перхлорэтилена (PCE, PERC)?
Краткосрочные:
Дыхание высоких уровней перхлорэтилена в течение короткого времени может вызвать:
- Головокружение
- Сонливость
- Головная боль
- Тошнота и рвота
- Отсутствие координации
- Раздражение глаз и дыхательных путей
Контакт кожи с перхлорэтиленом может вызвать:
- Раздражение
- Покраснение и трещины
Долгосрочный:
Длительное воздействие перхлорэтилена может вызвать изменения в:
- настроение
- Память
- Внимание
- Время реакции
- Видение
Длительное воздействие перхлорэтилена может привести к:
Кто подвергается риску воздействия перхлорэтилена (PCE, PERC)?
- потребителей
- Химчистка одежды и некоторые потребительские товары содержат перхлорэтилен.
- Люди, которые живут недалеко от мест химчистки
- Женщины детородного возраста
- Несколько исследований на людях показали, что воздействие тетрахлорэтилена увеличивало число детей с врожденными дефектами, но эти исследования не были достаточно большими, чтобы четко ответить на вопрос.
Уменьшите свой риск
Если вы считаете, что воздействие перхлорэтилена на ваше здоровье повлияло, обратитесь к своему лечащему врачу.
Всегда тщательно мойте руки после работы с химикатами. По поводу чрезвычайных ситуаций при отравлении или вопросов о возможных ядах обращайтесь в местный токсикологический центр по телефону 1-800-222-1222.
- Химчистите ли вы свою одежду?
- Вы живете рядом с химчистками, химическими отходами или химическими хранилищами, где хранился перхлорэтилен?
- Используете ли вы продукты, которые содержат перхлорэтилен?
- Вы пользуетесь колодезной водой?
- Если ваша питьевая вода поступает из общественного источника, обратитесь в местную систему водоснабжения, чтобы выяснить, есть ли в вашей воде загрязняющие вещества.
- Регулярно проверяйте воду из скважины на предмет перхлорэтилена.
- Если в вашей колодезной воде высокий уровень перхлорэтилена, обратитесь в местное или государственное учреждение здравоохранения или в Центры по контролю и профилактике заболеваний (CDC) для получения информации о том, как уменьшить воздействие.
- Если вы выполняете химчистку одежды и думаете, что часть растворителя не была удалена, или если одежда пахнет растворителем, попросите уборщика повторно вымыть вашу одежду или отнесите ее другому уборщику для повторной чистки.
- Проветрите сухую одежду перед тем, как принести ее в дом.
- Если вы живете над химчисткой, проветривайте свой дом, открывая окна.
- Проверьте этикетки продукта для перхлорэтилена. Следуйте инструкциям на этикетке продукта, чтобы минимизировать воздействие. Храните их в сарае или вне помещения.
- Используйте надлежащую вентиляцию при использовании продуктов, содержащих перхлорэтилен.
Не позволяйте детям играть в грязи или есть грязь, если вы живете рядом с местом для отходов, содержащим перхлорэтилен.
Внешние ссылки
Национальная библиотека медицинских ресурсов и баз данных
- Тетрахлорэтилен. Банк данных по опасным веществам
Результаты поиска тетрахлорэтилена по токсикологической базе данных, которая фокусируется на токсикологии потенциально опасных химических веществ.
Дополнительные ресурсы
- Что такое перхлорэтилен (тетрахлорэтилен или PCE)?
Центр общественного здравоохранения ВМФ и Корпуса морской пехоты
Ресурс по перхлорэтилену (тетрахлорэтилену или PCE), в котором рассматриваются его свойства, виды использования, группы населения, подверженные риску неблагоприятных последствий для здоровья в результате воздействия, и распределение PCE в окружающей среде. - Тетрахлорэтилен (PERC). ToxFAQs.
Агентство по регистрации токсичных веществ и заболеваний
Информационный бюллетень с ответами на наиболее часто задаваемые вопросы о воздействии тетрахлорэтилена (PERC) и его влиянии на здоровье человека, разработанный федеральным агентством общественного здравоохранения, которое защищает общины от вредного воздействия на здоровье, связанного с воздействием природных и искусственных опасных веществ.
Перхлорэтилен — Большая Химическая Энциклопедия
Удаление огнеупорных органических веществ. Озон реагирует медленно или незначительно с некоторыми микропроизводителями в некоторых исходных водах, таких как четыреххлористый углерод, трихлорэтилен (TCE) и перхлорэтилен (PCE), а также в хлорированных водах, т. кислоты (HAA) (например, трихлоруксусная кислота). Некоторое удаление этих соединений происходит в озоновом контакторе в результате улетучивания (115).Удаление воздуха в насадочной колонне эффективно для удаления некоторых ТГМ, но не CHBr. THM могут быть адсорбированы на гранулированном активированном угле (GAG), но эффективность адсорбции низкая. [Pg.502]SO, чтобы закончить воздушную смесь в адсорбер № 2. Затем система полностью автоматическая. Растворители, которые были успешно извлечены методом адсорбции на активированном угле, включают метанол, этанол, бутанол, хлорированные углеводороды, включая перхлорэтилен, который кипит при 121 ° С (250 ° F), этиловый эфир, изопропиловый эфир, ацетаты до амилацетата, бензол, толуол, ксилол, минеральные спирты, нафта, бензин, ацетон, метилэтилкетон, гексан, сероуглерод и другие.[Pg.301]
Фосфаты кислотных эфиров с алкильной цепью до C6 имеют низкую растворимость, тогда как нейтрализованные сложные эфиры растворимы в воде. В этаноле и изопропаноле большинство эфиров фосфорной кислоты и их соли растворимы. Если продукты основаны на этоксилированных спиртах, их растворимость в воде будет увеличиваться с увеличением степени этоксилирования. Растворимость в органических растворителях, таких как бензин, бензол, перхлорэтилен и другие неполярные жидкости, уменьшается с увеличением степени этоксилирования, но увеличивается за счет более высокой алкильной цепи.[Pg.591]
Пентилэтаноат, см. Втор-Амилацетат, втор-Пентилэтаноат, см. Амилацетат Penwar, см. Пентахлорфенол Ператокс, см. Пентахлорфенол Перавин, см. Тетрахлорэтилен PERC, см. Тетрахлорэтилен перхлор, см. Тетрахлорэтиленхлорэтиленхлорэтиленхлорэтиленхлорэтиленхлорэтиленхлорэтиленхлорэтиленхлорэтиленхлорэтиленхлорэтиленхлорэтилен-перхлор, см. Гексахлорбензол Перхлорбнтадиен, см. Гексахлорбутадиен Перхлорциклопентадиен, см. Гексахлорциклопентадиен Перхлор-1,3-циклопентадиен, см. … [Pg.1504]
Сандер М., Хемпель Д.К. Chemie Ingenieur Technik 68 150-155.[Pg.79]
Bolton4 удалось объединить хлор и углерод. Он использовал вольтовую дугу между угольными электродами в атмосфере хлора. Перхлорэтан в основном производится гексахлорбензол образуется в меньшем количестве. Поскольку оба эти хлор-углеводорода получают полным хлорированием четыреххлористого углерода, Болтон предполагает их промежуточное существование, поэтому промежуточное появление газообразных или жидких соединений, таких как перхлорэтилен, не представляется невероятным. Бром и йод, по-видимому, реагируют аналогично (Bolton4) экспериментам с последними галогенами, но еще не получили научного обоснования.Они, несомненно, окажутся выгодными. [Pg.250]
Тетрахлорид углерода, 1 — это соединение, разлагаемое отдельно по схеме, аналогичной той, которая используется для хлороформа, выделяет большие количества перхлорбензола хлора, перхлорэтана (в очень незначительном количестве) и перхлорэтилена. также производится. Присутствие воды в этом случае также увеличивает выход угарного газа. Анилин приводит к трифенил-гуанидину, также образуется некоторое количество смолы. [Pg.255]
PERCHLORAETHYLEN, ПЕРЛИ (НЕМЕЦКИЙ) ПЕРХЛОРЭТИЛЕН ПЕРХЛОРЭТИЛЕН, ПЕР (французское) перклено PERCLOROETILENE (ИТАЛЬЯНСКИЙ) PERCOSOLVE PERK PERKLONE PERSEC RCRA ОТХОДОВ НОМЕР U210 TETLEN TETRACAP TETRACHLOORETHEEN (нидерландский) TETRACHLORAETHEN (НЕМЕЦКИЙ) тетрахлор-этен тетрахлорэтилен горшок , ACGIH)… [Pg.1082]
Основное использование циклических силоксанов, в частности декаметилциклопентасилоксана (D5), в продуктах личной гигиены. D5 способствует равномерному распределению средств личной гигиены и обеспечивает гладкое, шелковистое ощущение при нанесении. D5 быстро сохнет, не оставляя ощущения охлаждения или остатков. Все большее применение D5 используется для химической чистки при замене перхлорэтилена. [Pg.612]
Lean Copper Solvent Очищенная вода C2-хлор. HC, свет Хлористый водород Тяжелый C2-Chlor.Перхлорэтилен Воздух Водяной паровой кожух Двигатель Водопоглощение Масло, очищенное воздухом и хлором … [Стр.42]
Химчистка — это процесс, при котором одежда очищается без воды. Используемая чистящая жидкость представляет собой перхлорэтилен (C12C = CC12) perc или летучий синтетический растворитель четыреххлористый углерод (CC14). Эти растворители используются потому, что их молекулярные структуры аналогичны структурам масел, содержащихся в грязи и грязи. [Стр.12]
Паральдегид Пентаэритритол Перхлорэтилен Парфюмерия (отдельные продукты)… [Стр.66]
Эти шарики можно использовать при более высоком давлении. Некоторые из них, такие как гидрогель, могут выдерживать давление до 3000 ps.i. Можно использовать органические растворители, поэтому можно разделить большое разнообразие соединений. Типичными растворителями являются бензол, толуол, ксилол, четыреххлористый углерод, диметилформамид, метиленхлорид, кетоны, диметилсульфоксид, дихлорбензол, этилендихлорид, перхлорэтилен, тетрагидрофуран, трихлорбензол и хлороформ. [Ст.175]
,
Перхлорэтилен | 127-18-4 — Guidechem
Перхлорэтилен с регистрационным номером CAS 127-18-4 имеет другие названия: порклон, тетрохлорэтан, тетрахлорэтилен, безводный, 99%, тетрахлорэтилен, 99%, спектрофотометрический класс, тетрахлорэтилен. , реагент плюс 99%, тетрахлорэтилен 99,9 +%, класс ВЭЖХ, тетрахлорэтилен стабильный, тетрахлорэтан эканал.
Физические свойства этого химического вещества следующие: (1) ACD / LogP:? 2,95? ; (2) ACD / LogD (рН 5.5) 😕 2,95? ; (3) ACD / LogD (pH 7,4):? 2,95? ; (4) ACD / BCF (pH 5,5): 102,96? ; (5) ACD / BCF (pH 7,4): 102,96? ; (6) ACD / KOC (pH 5,5): 960,03? ; (7) ACD / KOC (pH 7,4):? 960,03? ; (8) показатель преломления:? 1,519? ; (9) Молярная рефракционная способность:? 30,45 см 3? ; (10) Молярный объем:? 100,3 см 3? ; (11) поляризуемость 😕 12,07 10 -24 см 3 ? ; (12) Поверхностное натяжение:? 35,6 дин / см? ; (13) Плотность 😕 1,665 г / см 3 ? ; (14) Температура вспышки:? 27,4 ° С? ; (15) Энтальпия испарения:? 34.68 кДж / моль? ; (16) Точка кипения:? ? 119,1 ° C при 760 мм рт.ст. ; (17) Давление пара:? 19,3 мм рт.ст. при 25 ° C.
Это прозрачная бесцветная жидкость с похожим запахом этилового эфира. И он растворим во многих материалах, таких как каучук, смола, жир, хлорид алюминия и т. Д. Кроме того, он может смешиваться с этиловым эфиром, этанолом, хлороформом, бензолом и так далее. Более того, он стабилен, но несовместим с сильными окислителями, щелочными металлами, алюминием, сильными основаниями.
Будучи вредным химическим веществом, он может нанести вред здоровью, что отражается на некоторых аспектах.Он токсичен при вдыхании и проглатывании или при контакте с кожей и может даже иметь очень серьезный необратимый эффект. Тогда он имеет ограниченные доказательства канцерогенного воздействия на наше здоровье. Это вредно не только для нашего здоровья, но и для окружающей среды. Это опасно для окружающей среды? для этого? может представлять непосредственную или отсроченную опасность для одного или нескольких компонентов окружающей среды; Тогда он токсичен для водных организмов и может вызывать долгосрочные неблагоприятные воздействия в водной среде. Более того, он легко воспламеняется, поскольку он может загореться при контакте с воздухом, требуя лишь краткого контакта с источником возгорания, и имеет очень низкую температуру вспышки или выделяет легковоспламеняющиеся газы при контакте с водой.?
Так что, имея дело с этим химическим веществом, вы должны быть очень осторожны. Носите подходящую защитную одежду и перчатки при контакте. Не вдыхайте газ / пары / пары / спрей (соответствующая формулировка должна быть указана производителем), и в случае аварии или если вы плохо себя чувствуете, немедленно обратитесь к врачу (по возможности, покажите этикетку). Кроме этого, избегайте попадания в окружающую среду и обратитесь к специальным инструкциям / паспорту безопасности; Хранить вдали от источников возгорания. Не курить и хранить контейнер плотно закрытым.Если вам нужна дополнительная информация о безопасности, вы можете обратиться в WGK Germany? 3.
?
Перхлорэтилен широко применяется во многих отношениях. Он в основном используется в органических растворителях, химчистках, растворителях для обезжиривания металлов и может также использоваться в качестве глистогонного средства. Кроме того, его можно применять в алифатических экстракторах, огнетушителях, отсеивающих дым, а также в трикленовых фторорганических химических веществах. И его категории продуктов включают органические вещества, аналитическую химию, стандартные растворы летучих органических соединений для анализа воды и почвы, стандартные растворы (VOC).
Кроме того, вы можете преобразовать следующую информацию данных в молекулярную структуру:
УЛЫБКИ:
Cl / C (Cl) = C (/ Cl) Cl
перхлорэтилен Wikipedia
Химическое соединение в очень широком использовании
| имен | |||
|---|---|---|---|
| ИЮПАК имя тетрахлорэтан | |||
| Другие имена перхлорэтен; перхлорэтилен; Проц; PCE | |||
| идентификаторов | |||
| ЧЕБИ | |||
| ЧЕМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.004,388 | ||
| ЕС номер | |||
| КЕГ | |||
| номер RTECS | |||
| UNII | |||
| номер ООН | 1897 | ||
| |||
| свойства | |||
| C 2 Cl 4 | |||
| Молярная масса | 165.82 г · моль -1 | ||
| Внешний вид | Прозрачная бесцветная жидкость | ||
| Запах | мягкий хлороформоподобный [1] | ||
| Плотность | 1,622 г / см 3 | ||
| Точка плавления | −19 ° C (−2 ° F; 254 К) | ||
| Точка кипения | 121,1 ° C (250,0 ° F; 394,2 К) | ||
| 0,15 г / л (25 ° C) | |||
| Давление пара | 14 мм рт.ст. (20 ° С) [1] | ||
| -81.6 · 10 −6 см 3 / моль | |||
| Вязкость | 0,89 сП при 25 ° C | ||
| опасности | |||
| Основные опасности | Вредные (Xn), Опасные для среды (N) | ||
| Паспорт безопасности | См .: страница данных Внешний MSDS | ||
| R-фразы (устаревшие) | R40 R51 / 53 | ||
| S-фраз (устаревших) | S23 S36 / 37 S61 | ||
| NFPA 704 (огненный алмаз) | |||
| Точка воспламенения | Негорючий | ||
| Смертельная доза или концентрация (LD, LC): | |||
| 4000 ч / млн (крыса, 4 часа) 5200 ч / млн (мышь, 4 часа) 4964 ч / млн (крыса, 8 часов) [2] | |||
| NIOSH (пределы воздействия на здоровье США): | |||
| TWA 100 ppm C 200 ppm (в течение 5 минут в течение любого 3-часового периода) с максимальным пиком 300 ppm [1] | |||
| Ca Минимизируйте концентрацию воздействия на рабочем месте. [1] | |||
| Ca [150 ppm] [1] | |||
| Родственные соединения | |||
| Тетрабромэтилен Тетрайодоэтилен | |||
Родственные соединения | Трихлорэтилен Дихлорэтан Тетрахлорэтан | ||
| Страница дополнительных данных | |||
| показатель преломления ( n ), диэлектрическая проницаемость (ε r ) и т. Д. | |||
Термодинамические | Фазовое поведение твердое вещество – жидкость – газ | ||
| УФ, ИК, ЯМР, МС | |||
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| N проверить (что такое YN ?) | |||
| ссылок Infobox | |||
тетрахлорэтилен , также известный под систематическим названием тетрахлорэтен или перхлорэтилен , и многие другие названия (и сокращения, такие как « перц » или « PERC » и «» PCE 9027) хлоркарбон с формулой Cl 2 C = CCl 2 .Это бесцветная жидкость, широко используемая для химической чистки тканей, поэтому ее иногда называют « для химической чистки ». Он имеет сладкий запах, обнаруживаемый большинством людей в концентрации 1 часть на миллион (1 ч / млн). В 1985 году мировое производство составило около 1 миллиона метрических тонн (980 000 длинных тонн; 1 100 000 коротких тонн). [3]
Производство []
Майкл Фарадей впервые синтезировал тетрахлорэтилен в 1821 году путем термического разложения гексахлорэтана.
- C 2 Cl 6 → C 2 Cl 4 + Cl 2
Большую часть тетрахлорэтилена получают путем высокотемпературного хлорирования легких углеводородов.Этот метод связан с открытием Фарадея, поскольку гексахлорэтан образуется и термически разлагается. [3] Побочные продукты включают четыреххлористый углерод, хлористый водород и гексахлорбутадиен.
Несколько других методов были разработаны. Когда 1,2-дихлорэтан нагревают до 400 ° С с хлором, тетрахлорэтилен получают химической реакцией:
- ClCH 2 CH 2 Cl + 3 Cl 2 → Cl 2 C = CCl 2 + 4 HCl
Эту реакцию можно катализировать смесью хлорида калия и хлорида алюминия или активированного угля.Трихлорэтилен является основным побочным продуктом, который отделяют перегонкой.
Согласно отчету Агентства США по охране окружающей среды (EPA) за 1976 г., количество тетрахлорэтилена, произведенного в Соединенных Штатах в 1973 г., составило 320 000 метрических тонн (706 млн фунтов). [4] К 1993 году объем производства в Соединенных Штатах сократился до 123 000 метрических тонн (271 млн фунтов). [5]
использует []
Тетрахлорэтилен является отличным растворителем для органических материалов.В противном случае он является летучим, высокостабильным и негорючим. По этим причинам он широко используется в химчистке. Он также используется для обезжиривания металлических деталей в автомобильной и другой металлообрабатывающей промышленности, как правило, в виде смеси с другими углеводородами. Это появляется в нескольких потребительских продуктах, включая средства для снятия краски и пятновыводители. Он также используется в аэрозольных препаратах.
Используется в детекторах нейтрино, где нейтрино взаимодействует с нейтроном в атоме хлора и преобразует его в протон с образованием аргона.
Исторические приложения []
Тетрахлорэтилен когда-то широко использовался в качестве промежуточного продукта при производстве ГФУ-134а и связанных с ним хладагентов. В начале 20 века тетрахлорэтан использовался для лечения заражения анкилостомами. [6]
Здоровье и безопасность []
Острая токсичность тетрахлорэтилена «от умеренной до низкой». «Сообщения о человеческих травмах встречаются редко, несмотря на то, что они широко используются для химической чистки и обезжиривания». [7]
Международное агентство по исследованию рака классифицирует тетрахлорэтилен как канцероген группы 2А, что означает, что он, вероятно, является канцерогенным для человека. [8] Как и многие хлорированные углеводороды, тетрахлорэтилен является депрессантом центральной нервной системы и может попасть в организм через органы дыхания или кожу. [9] Тетрахлорэтилен растворяет жиры с кожи, что может вызвать раздражение кожи.
В связи с токсичностью и рисками рака тетрахлорэтилена Калифорнийский совет по воздушным ресурсам запретил использование этого вещества в новых машинах химической чистки в 2007 году, поскольку к середине 2010 года старые машины, использующие PCE, были закрыты, а использование всех таких машин прекращено. в Калифорнии к 2023 году. [10]
Исследования на животных и исследование 99 близнецов показали, что существует «много косвенных доказательств» того, что воздействие тетрахлорэтилена увеличивает риск развития болезни Паркинсона в девять раз. Планируются более масштабные исследования населения. [11] Также было показано, что тетрахлорэтилен вызывает опухоли печени у мышей и опухоли почек у самцов крыс. [12]
При температуре выше 315 ° C (599 ° F), например, при сварке, тетрахлорэтилен может окисляться в фосген, чрезвычайно ядовитый газ. [13] [14]
Национальный институт безопасности и гигиены труда США собрал обширную информацию о здоровье и безопасности для тетрахлорэтилена, [15] [16] , включая рекомендации для предприятий химической чистки. [17] [18] [19] [20]
Воздействие тетрахлорэтилена было связано с выраженными приобретенными нарушениями цветового зрения после хронического воздействия. [21]
Тестирование на экспозицию []
Воздействие тетрахлорэтилена можно оценить с помощью дыхательного теста, аналогичного измерениям алкоголя в выдыхаемом воздухе.Поскольку тетрахлорэтилен накапливается в жировых отложениях организма и медленно выделяется в кровоток, он может обнаруживаться в дыхании в течение нескольких недель после сильного воздействия. Тетрахлорэтилен и трихлоруксусная кислота (ТСА), продукт распада тетрахлорэтилена, могут быть обнаружены в крови.
В Европе Научный комитет по пределам воздействия на рабочем месте (SCOEL) рекомендует для тетрахлорэтилена предел профессионального воздействия (средневзвешенное по времени за 8 часов) 20 ppm и предел кратковременного воздействия (15 min) 40 ppm. [22]
Загрязнение окружающей среды []
Тетрахлорэтилен является распространенным загрязнителем почвы. При удельном весе, превышающем 1, тетрахлорэтилен будет присутствовать в виде жидкой неводной фазы (DNAPL), если высвобождаются достаточные количества. Из-за его подвижности в подземных водах, его токсичности на низких уровнях и его плотности (что приводит к его погружению ниже уровня грунтовых вод), деятельность по очистке является более сложной, чем при разливе нефти: удельный вес нефти составляет менее 1.Недавние исследования загрязнения почвы и грунтовых вод тетрахлорэтиленом были сосредоточены на восстановлении на месте. Вместо выемки или извлечения для наземной обработки или утилизации загрязнение тетрахлорэтиленом успешно устраняется путем химической обработки или биоремедиации. Биоремедиация была успешной в анаэробных условиях путем восстановительного дехлорирования Dehalococcoides sp. и в аэробных условиях кометаболизмом Pseudomonas sp. [23] [24] Дочерние продукты частичного разложения включают трихлорэтилен, цис-1,2-дихлорэтан и винилхлорид; полная деградация превращает тетрахлорэтилен в этен и хлористый водород, растворенный в воде.
Согласно оценкам, 85% полученного тетрахлорэтилена выбрасывается в атмосферу; в то время как модели из ОЭСР предполагали, что 90% выбрасывается в воздух и 10% — в воду. Основываясь на этих моделях, его распределение в окружающей среде оценивается в воздухе (76.39% — 99,69%), вода (0,23% — 23,2%), почва (0,06-7%), с остатком в донных отложениях и биоте. Оценки времени жизни в атмосфере варьируются, но опрос 1987 года показал, что время жизни в воздухе составляет около 2 месяцев в южном полушарии и 5–6 месяцев в северном полушарии. Продукты разложения, наблюдаемые в лаборатории, включают фосген, трихлорацетилхлорид, хлористый водород, диоксид углерода и оксид углерода. Тетрахлорэтилен разлагается в результате гидролиза и устойчив в аэробных условиях. Ватт П. (2006). Краткий документ о международной оценке химических веществ 68: ТЕТРАХЛОРЭТЕН, Всемирная организация здравоохранения

 перхлорэтилена используется в химчистках для сухой чистки одежды.
перхлорэтилена используется в химчистках для сухой чистки одежды.