Химические формулы веществ — Ида Тен
Что такое химическая формула?
В любой науке есть своя система обозначений. Химия в этом плане не исключение. Вам уже известно, что для обозначения химических элементов используются символы, образованные от латинских названий элементов. Химические элементы способны образовывать как простые, так и сложные вещества, состав которых можно выразить химической формулой.
Чтобы написать химическую формулу простого вещества необходимо записать символ химического элемента, который образует простое вещество, и справа внизу записать цифру, показывающую количество его атомов. Данная цифра называется индексом.
Например, химическая формула кислорода – О2. Цифра 2 после символа кислорода – это индекс, указывающий, что молекула кислорода состоит из двух атомов элемента кислорода.
Индекс – число, показывающее в химической формуле количество атомов определенного типа
Чтобы написать химическую формулу сложного вещества, необходимо знать, из атомов каких элементов оно состоит (качественный состав), и число атомов каждого элемента (количественный состав).
Например, химическая формула пищевой соды – NaHCO3. В состав этого вещества входят атомы натрия, водорода, углерода, кислорода – это его качественный состав. Атомов натрия, водорода, углерода по одному, а атомов кислорода – три. Это количественный состав соды
Качественный состав вещества показывает, атомы каких элементов входят в его состав
Количественный состав вещества показывает количество атомов, которые входят в его состав
Химическая формула – условная запись состава вещества при помощи химических символов и индексов
Обратите внимание на то, что если в химической формуле присутствует только один атом одного вида, индекс 1 не ставится.
Например, формулу углекислого газа записывают так – CO2, а не С1О2.
Как правильно понимать химические формулы?
При записи химических формул нередко встречаются цифры, которые записывают перед химической формулой. Например, 2Na, или 5О2. Что обозначают эти цифры и для чего они нужны? Цифры, записанные перед химической формулой, называют коэффициентами.
Коэффициенты показывают общее количество частиц вещества: атомов, молекул, ионов. Например, запись 2Na обозначает два атома натрия. Запись 5О2 обозначает пят/
Коэффициент – число, которое показывает общее количество частиц. Коэффициент записывается перед химической формулой вещества молекул кислорода.
Обратите внимание, что молекулы не могут состоять из одного атома, минимальное количество атомов в молекуле – два. Таким образом, записи: 2Н, 4P обозначают два атома водорода и четыре атома фосфора соответственно.
Запись 2Н2 обозначает две молекулы водорода, содержащие по два атома элемента водорода. Запись
Подобная система обозначений количества частиц используется и для ионов. Запись 5K+ обозначает пять ионов калия. Стоит отметить, что ионы могут быть образованы не только атомом одного элемента. Ионы, образованные атомами одного химического элемента, называют простыми: Li+, N3−. Ионы, образованные несколькими химическими элементами, называют сложными: OH⎺, SO4 2−. Обратите внимание, что заряд иона обозначают верхним индексом.
А что будет обозначать запись 2NaCl? Если на этот вопрос ответить – две молекулы поваренной соли, то ответ не правильный. Поваренная соль, или хлорид натрия, имеет ионную кристаллическую решетку, то есть это ионное соединение и состоит из ионов Na+ и Сl⎺. Пару этих ионов называют формульной единицей вещества. Таким образом, запись 2NaCl обозначает две формульных единицы хлорида натрия. Термин формульная единица используют так же и для веществ атомного строения.
Формульная единица – наименьшая частица вещества немолекулярного строения
Ионные соединения так же электронейтральны, как и молекулярные. Значит, положительный заряд катионов полностью уравновешен отрицательным зарядом анионов. Например, какова формульная единица вещества, состоящего из ионов Ag+ и PO4 3−? Очевидно, что для компенсации отрицательного заряда иона (заряд –3), необходимо иметь заряд +3. С учетом того, что катион серебра имеет заряд +1, то таких катионов понадобиться три. Значит формульная единица (формула) данного вещества – Ag3PO4.
Таким образом, при помощи символов химических элементов, индексов и коэффициентов, можно четко составить химическую формулу вещества, которая даст информацию, как о качественном, так и о количественном составе вещества.
В завершение рассмотрим, как правильно произносить химические формулы. Например, запись 3Ca2+ произносится: «три иона кальций два плюс» или «три иона кальция с зарядом два плюс». Запись 4НСl, произносится «четыре молекулы аш хлор». Запись 2NaCl, произносится как «две формульных единицы хлорида натрия».
Закон постоянства состава вещества
Одно и то же химическое соединение можно получить различными способами. Так, например, углекислый газ, CO2, образуется при сжигании топлива: угля, природного газа. Во фруктах содержится много глюкозы. При длительном хранении фрукты начинают портиться, начинается процесс, называемый брожением глюкозы, в результате которого выделяется углекислый газ. Углекислый газ образуется и при нагревании таких горных пород, как мел, мрамор, известняк.
Химические реакции совершенно разные, но вещество, образовавшееся в результате их протекания, имеет одинаковый качественный и количественный состав – CO2.
Эта закономерность касается, в основном, веществ молекулярного строения. В случае веществ немолекулярного строения, возможны случаи, когда состав вещества зависит от методов его получения.
Закон постоянства состава веществ молекулярного строения: состав сложного вещества всегда одинаков и не зависит от способа его получения
Выводы из статьи по теме Химические формулы веществ
- Индекс – число, показывающее в химической формуле количество атомов определенного типа
- Качественный состав вещества показывает, атомы каких элементов входят в его состав
- Количественный состав вещества показывает количество атомов, которые входят в его состав
- Химическая формула – условная запись состава вещества при помощи химических символов и индексов (если нужно)
- Коэффициент – число, которое показывает общее количество частиц. Коэффициент записывается перед химической формулой вещества
- Формульная единица – наименьшая частица вещества атомного или ионного строения
idaten.ru
Учебник химии — Знаки химических элементов
Знаки химических элементов
В химии используют химическую символику, облегчающую изучение состава и свойств веществ. По предложению шведского химика Й. Берцелиуса химические элементы обозначают начальной или начальной и один из последующих букв латинского названия данного элемента. Водород (лат. Hydrogenium – гидрогениум ) обозначается буквой H, ртуть (лат. Hydrargrum – гидраргирум ) – буквами Hg и т. д.
Эти буквы латинских названий химических элементов приняты за химические знаки, или химические символы.
Выясним, что обозначает химический символ ( химический знак).
Примеры
Если требуется обозначить не один, а несколько атомов, то перед химическим знаком ставят соответствующую цифру, которая называется коэффициентом. Например, три атома водорода обозначаются 3H, пять атомов железа – 5Fe.
Химические знаки элементов, их названия, относительные атомные массы и произношение химических знаков приведены в таблице.
Название химического элемента | Химический знак | Произношение химического знака | Относительная атомная масса (округленная) |
Азот Алюминий Барий Бор Бром Водород Железо Золото Иод Калий Кальций Кислород Кремний Магний Марганец Мель Натрий Ртуть Свинец Сера Серебро Углерод Фосфор Фтор Хлор Цинк | N Al Ba B Br H Fe Au I K Ca O Si Mg Mn Cu Na Hg Pb S Ag C P F Cl Zn
| Эн Алюминий Барий Бор Бром Аш Феррум Аурум Иод Калий Кальций О Силициум Магний Марганец Купрум Натрий Гидраргиум Плюмбум Эс Аргентум Це Пэ Фтор Хлор Цинк | 14 27 137 11 80 1 56 197 127 39 40 16 28 24 55 64 23 201 207 32 108 12 31 19 35,5 65
|
sochi-nochi.narod.ru
Урок 5. Химическая формула – HIMI4KA
В уроке 5 «Химическая формула» из курса «Химия для чайников» дадим определение химическим формулам и их индексам, а также выясним различия химических формул веществ молекулярного и немолекулярного строения. Напоминаю, что в прошлом уроке «Сложные вещества» мы дали определение химическим соединениям, рассмотрели различия органических и неорганических соединений, а также выяснили, что означает качественный и количественный состав.

Состав любого вещества выражается в виде химической формулы.
Химическая формула — это условная запись состава вещества с помощью химических знаков и индексов.
Качественный состав показывается с помощью знаков (символов) химических элементов, а количественный — с помощью индексов, которые записываются справа и чуть ниже знаков химических элементов.
Индекс — число атомов данного химического элемента в формуле вещества.
Например, химическая формула простого вещества водорода записывается так:
и читается «аш-два».
Химические формулы веществ молекулярного строения
Формулы двухатомных молекул: кислорода — О2 («о-два»), хлора — Сl2 («хлор-два»), азота — N2 («эн-два»). Трехатомная молекула озона и восьмиатомная молекула серы обозначаются формулами О3 («о-три») и S8 («эс-восемь»).
Формулы молекул сложных веществ также отображают их качественный и количественный состав. Например, формула воды, как вы уже, наверное, хорошо знаете, Н2О («аш-два-о»), метана — СН4 («це-аш-четыре»), а аммиака — NH3 («эн-аш-три»). Точно так же читаются формулы любых сложных веществ. Например, формула серной кислоты — H2SO4 («аш-два-эс-о-четыре»), а глюкозы — C6H12O6 («це-шесть-аш-двенадцать-о-шесть»).
Химические формулы веществ молекулярного строения (их называют молекулярными формулами) показывают состав элементарных частей, т. е. условных «кирпичиков», из которых состоят эти вещества. Такими элементарными составными частями (элементарными структурными единицами, или просто структурными единицами) в данном случае являются молекулы.
Химические формулы веществ немолекулярного строения
А если вещество имеет немолекулярное строение? Химические формулы простых веществ такого типа (например, металлов) записывают просто знаками соответствующих элементов без индексов (или, вернее, с индексом, равным единице, которая не записывается). Так, формула простого вещества железа — Fe, меди — Cu, алюминия — Al.
Состав сложных веществ немолекулярного строения выражают с помощью формул, которые показывают простейшее соотношение чисел атомов разных химических элементов в этих веществах. Такие формулы называются простейшими. Например, простейшая формула кварца — главной составной части речного песка — SiO2. Она показывает, что в кристалле кварца на один атом кремния приходятся два атома кислорода, т. е. простейшее соотношение чисел атомов кремния и кислорода в этом веществе равно 1:2. Простейшая формула Al2O3 показывает, что в этом соединении простейшее соотношение между числами атомов алюминия и кислорода равно 2:3.
Группа атомов, состав которой соответствует простейшей формуле вещества немолекулярного строения, называется его формульной единицей.
Формульная единица, поваренной соли NaCl («натрий-хлор») — группа из одного атома натрия и одного атома хлора. Формульная единица мела CaCO3 («кальций-це-о-три») — группа из одного атома кальция, одного атома углерода и трех атомов кислорода.
Формулы более сложных соединений немолекулярного строения читаются аналогично. Дополнительно указывается только число групп атомов, заключенных в круглые скобки: Al2(SO4)3 («алюминий-два-эс-о-четыре-трижды»), Mg(NO3)2 («магний-эн-о-три-дважды») и т. д.
Таким образом, структурными единицами веществ молекулярного строения являются молекулы. Структурными единицами веществ немолекулярного строения являются их формульные единицы.
В таблице ниже показаны формульная запись и схематическое изображение состава веществ различного типа.
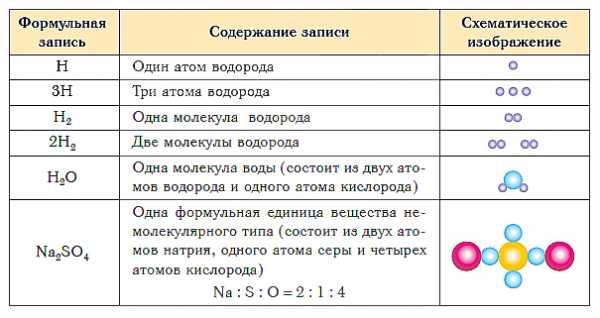
Краткие выводы урока:
- Качественный и количественный состав вещества выражается с помощью химических формул.
- Химическая формула вещества молекулярного строения показывает состав его молекулы, которая является элементарной структурной единицей данного вещества.
- Химическая формула вещества немолекулярного строения показывает простейшее соотношение атомов в его формульной единице.
Надеюсь урок 5 «Химическая формула» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.
himi4ka.ru
Химические знаки элементов — Справочник химика 21
Периодическая система химических элементов создана Д. И. Менделеевым в 1869 г. На форзацах представлена таблица Периодическая система элементов Д. И.Менделеева в современном виде. Химические знаки элементов расположены в клетках таблицы. В верхней части клетки указаны порядковые номера элементов цифры, стоящие рядом с химическим знаком элемента, обозначают атомные массы (по данным 1981 г.). Атомные массы приведены по углеродной шкале. В квадратных скобках даны массовые числа наиболее устойчивых изотопов. [c.9]Символ (химический знак) элемента Обозначение элемента одной или двумя латинскими буквами, принятое в химии [c.547]
Химические знаки элементов. В химии принято все элементы обозначать особыми знаками. Эти знаки представляют собой начальные буквы (одну или две) названия элемента на латинском языке. Например, водород па латинском языке называется Hydrogenium химический знак водорода—Н кислород—Oxigenium химический знак этого элемента—О и т. д. [c.42]
Название и химический знак элемента [c.119]
Формулами обозначаются и молекулы простых веществ, если известно, из скольких атомов состоит молекула. Например, На, Оа, F2. Однако если простое вещество имеет атомную или металлическую структуру или неизвестен атомный состав молекулы, то его изображают химическим знаком элемента. Например, Не, А1, С. Химическую формулу вещества можно установить по результатам анализа его состава (см. 1.12).
Наличие химической азбуки — знаков (символов) химических элементов — позволило ввести для всех химических индивидов химические формулы, отражающие их состав. При существовании химического индивида в атомной или молекулярной форме его химическая формула обозначается химическим знаком элемента с индексом, указывающим число атомов в атомной совокупности (единичный индекс не указывается), например благородные газы — Не, Ке, Аг, Кг, галогены — Га, С12, Вг,, Ха, белый фосфор — Р4. Если же химический индивид входит в состав атомного ассоциата или агрегата, ему приписывают химическую формулу с единичным индексом. [c.11]
Массовое число, атомный (порядковый) номер, число атомов и заряд указываются с помощью четырех индексов, расположенных симметрично около химического знака элемента в следующем порядке вверху слева — массовое число, внизу слева — атомный номер, вни у справа — число атомов, вверху справа — заряд. Например, 8 0 . Изотопы, например изотопы кислорода, нужно обозначать так 1 0, 0, 8 0. [c.174]
Химический знак элемента Физические свойства простого вещества Кислородные соединения с высшей степенью окисления [c.133]
В табл. 17 приведены физические константы некоторых неорганических веществ. Формулы соединений размещены в таблице в алфавитном порядке химических знаков элементов, которые стоят в начале формулы. Названия соединений даны преимущественно по международной номенклатуре, в некоторых случаях в скобках приведены их синонимы. Степень окисления элементов указана в скобках римскими цифрами. [c.36]
Перед химическим знаком элемента обозначен его порядковый номер Z по таблице Менделеева. Квантовые числа п—главное I—орбитальное [c.560]
С помощью записи внешних электронов в виде точек, приставленных к химическому знаку элемента. Тогда образование молекулы водорода можно показать схемой [c.40]
Как отмечалось, в периодической системе 107 элементов. В честь творца периодического закона Д. И. Менделеева 101-й хи.мический элемент назван менделевием Мс1. В Объединенном институте ядерных исследований в г. Дубне был открыт 104-элемент — курчатовий Ки, названный в честь выдающегося советского физика И. В. Курчатова. В том же институте в феврале 1970 г. открыт 105-й элемент. Первооткрыватели элемента предложили назвать его нильсборием — в честь Нильса Бора, выдающегося физика XX в. Химический знак элемента N3, массовое число 261. Это самый тяжелый из всех известных элементов. По своим химическим свойствам N3 — аналог Nb и Та (см. периодическую систему). Коллективом физиков социалистических стран, работающих в Дубне, завершен цикл экспериментов по синтезу 106-го и 107-го элементов. [c.67]
Очень часто формулы молекул изображаются графически. Поясним, как это делается. Валентность элемента изображается черточками. Число черточек, которые отходят от химического знака элемента, равно его валентности, например Н—, С1—, 0=, А1=, =С= и т. д. [c.27]
Схематически образование молекулы водорода может быть изображено следующим образом Н- -4- -Н- -Н Н. Точками на схемах при химическом знаке элемента обозначаются внешние электроны. Обобществленная пара электронов обычно заменяется черточкой —, например И—И. [c.57]
В таблице соединения размещены по алфавиту химических знаков элементов приведены названия соединений по двум, наиболее распространенным, номенклатурам. [c.40]
С атомной теорией был связан такой важнейший шаг в развитии химии, как введение химических знаков элементов. Созданная Берцелиусом химическая символика позволяла составлять эмпирические и рациональные формулы химических соединений и химические уравнения. Так возникли предпосылки для изучения строения химических соединений, выяснения порядка расположения атомов в молекуле и распределения в ней химических связей. Исследования в этом направлении и привели к созданию теории химического строения и стереохимии. [c.68]
Объяснительно-иллюстративный метод находит достаточно широкое применение, так как позволяет быстро накопить минимальную базу знаний, на которых потом можно строить поисковую деятельность учащихся. В некоторых случаях этот метод необходим. Папример, при изучении химических знаков элементов учитель показывает написание и произношение химического знака, разъясняет, что он обозначает, а затем предлагает учащимся однотипные упражнения. Упражнениям можно придать занимательный, игровой характер, использовать ТСО, но характер познавательной деятельности останется тем же. [c.68]
Наряду с проблемным обучением, постоянно используется в процессе изучения периодического закона работа с карточками, на которых учащиеся записывают известные им сведения о каждом элементе. Работа с карточками не ограничивается только этапом выведения периодического закона. Учащиеся пользуются ими постоянно в ходе изучения темы на разных дидактических этапах. На карточке отмечают химический знак элемента, характер его свойств, высшую валентность в оксидах, формулы оксидов, валентность в летучих водородных соединениях и гидридах, схемы строения атомов, степень окисления элементов и т. д. Карточки позволяют эффективно организовать самостоятельную работу. Они используются как справочные материалы, способствуют выработке умений пользоваться периодической системой. [c.228]
Выписывают химические знаки элементов, атомы или ионы которых меняют степень окисления [c.114]
Химический знак элемента Ре. Заряд ядра + 26. Распределение электронов по энергетическим уровням 2, 8, 14, 2. Атомный вес 56. Б химических соединениях железо проявляет положительную валентность, равную 2, 3 и 6. [c.174]
Понятие об окислительном числе. Под ним подразумевают заряд, который имела бы частица, если бы все связи в молекуле были ионного характера. Примеры (сверху над химическими знаками элементов указаны окислительные числа соответствующих частиц) [c.11]
Величина 6-10 (точнее 6,02-10 ) получила название числа Авогадро и обозначается буквой N (Л печатается курсивом, в отличие от прямого N—химического знака элемента азота). [c.35]
Написать рядом химические знаки элементов . …………… Р О [c.97]
Порядковый номер элемента Химический знак элемента Заряд иона Атомный ионный радиус, А [c.305]
Порядковый номер элемента Химический знак элемента Заряд [иона Атомный ионный радиус, А Порядковый номер элемента Химический знак элемента Заряд иона Атомный ионный радиус, А [c.308]
Атомный номер Химический знак элемента Ионизационный потенциал, эв Атомный номер Химический знак элемента [c.309]
В том же институте в феврале 1970 г. открыт 105-й Элемент. Первооткрыватели элемента предложили назвать его нильсборием—в честь Нильса Бора, выдающегося физика XX в. Химический знак элемента №, массовое число 261. Это самый тяжелый из всех известных элементов. По своим химическим свойствам нильсборий Ыз— аналог ниобия N5 и тантала Та. Название элемента окончательно еще не утверждено. [c.5]
ХИМИЧЕСКИЕ ЗНАКИ ЭЛЕМЕНТОВ И ФОРМУЛЫ ВЕЩЕСТВ, [c.24]
Заряд иона равен его валентности одновалентные ионы несут по одно.му заряду, двухвалентные — по два и т. д. Ионы обозначают теми же химическими знаками, что и соответствующие элементы. Если ион несет положительный заряд, справа от химического знака элемента вверху ставят знак плюс, при отрицательном заряде— минус, например Na+, С1 . [c.18]
В табл. 1 приведены названия (русские и латинские) элементов, химические знаки, порядковые номера их в периодической системе элементов Д. И. Менделеева, относительная атомная масса и год открытия. Атомные массы приведены по Международной таблице 1981 г. Звездочкой обозначены искусственно полученные элементы древн. — элемент, известный в глубокой древности средн. — элемент открыт в средние века. В квадратных скобках приведены массовые числа изотопов, обладающих наибольшим для данного радиоактивного элемента периодом полураспада. Названия и химические знаки элементов, приведенные в круглых скобках, не являются общепринятыми. [c.6]
Изображение электронов в виде символов (точек, крестиков и т. п.), поставленных у химического знака элемента. Для удобства электроны, принадлежащие разным атомам, иногда изображают разными символами. В случае полярной связи указывают направление смещения электронной плотности. Описанные выше процессы образоЕиния молекул водорода и хлороводорода отобразятся схемами [c.64]
Атомньга номера Химические знаки элементов Сродство к электрону, ае [c.310]
Для изображения связей, образованных электронными парами, постз гают так. Символом данного элемента обозначают ядро его атома и все энергетические уровни, кроме внешнего. Число электронов на наружном энергетическом уровне обозначают соответствующим числом точек около химического знака элемента, например, [c.56]
chem21.info
Химические элементы. Символы химических элементов. Экологическое воспитание
Дополнительные сочиненияКак и в любой науке, в химии существует своя система условных обозначений, свой язык. Урок посвящен знакомству с языком химической науки, изучению символов химических элементов. Вы узнаете, когда и кем были придуманы современные символы химических элементов.
Тема: Первоначальные химические представления
Урок: Символы химических элементов
1. История развития языка химии
Еще в Средневековье, во времена алхимии использовались различные знаки для обозначения веществ, в основном металлов. Ведь основной целью алхимиков было получение из различных металлов золота. Поэтому каждый из них использовал свою систему обозначений.
В 19 в. появилась необходимость использования понятной для всех ученых символики. И одним из первых такую символику предложил Джон Дальтон. Но его обозначениями было неудобно пользоваться.

Рис. 1. Джон Дальтон и его система обозначения химических элементов
2. Система обозначения химических элементов Й. Я. Берцелиуса
Современную систему химических знаков предложил в начале XIX в. шведский химик Йёнс Якоб Берцелиус. Ученый предложил обозначать химические элементы первой буквой их латинского названия. В те времена все научные статьи печатала на латинском языке, он был общепринятым и понятным для всех ученых.
Например, химический элемент кислород (по-латински Oxygenium) получил обозначение О.
А химический элемент водород (Hydrogenium) – Н. Если названия нескольких элементов начинались на одну и ту же букву, то в символе элемента указывали вторую или одну из последующих букв названия. Например, ртуть (Hydrargyrum) обозначается Hg.
Обратите внимание, что первая буква знака химического элемента всегда заглавная, если есть вторая буква – то она строчная. Необходимо запоминать не только названия элементов и их символы, но и произношение, т. е. как эти символы читаются.
Определенных правил произношения знаков химических элементов нет. Их надо учить наизусть. Знаки некоторых химических элементов произносятся так же, как и соответствующая буква: кислород – «о», сера – «эс», фосфор – «пэ», азот – «эн», углерод – «цэ».
Знаки других элементов произносятся так же, как и называются сами элементы: «натрий», «калий», «хлор», «фтор».
Произношение некоторых знаков соответствует их латинскому названию: кремний – «силициум», ртуть – «гидраргирум», медь – «купрум», железо – «феррум».
Рис. 2. Символы и названия некоторых химических элементов
3. Значение знаков химических элементов
Знак химического элемента имеет несколько значений. Во-первых, им обозначают все атомы данного элемента. Во-вторых, знаком химического элемента можно обозначить один или несколько атомов данного элемента. Например, запись O может означать: «химический элемент кислород» или «один атом кислорода».
Чтобы обозначить несколько атомов данного химического элемента, нужно перед его знаком поставить число, соответствующее количеству атомов. Например, запись 3N означает «три атома азота».
Цифра, стоящая перед знаком химического элемента, называется коэффициентом.
Список рекомендованной литературы
1. Сборник задач и упражнений по химии: 8-й класс: к учебнику П. А. Оржековского и др. «Химия, 8 класс» / П. А. Оржековский, Н. А. Титов, Ф. Ф. Гегеле. – М.: АСТ: Астрель, 2006.
2. Ушакова О. В. Рабочая тетрадь по химии: 8-й кл.: к учебнику П. А. Оржековского и др. «Химия. 8 класс» / О. В. Ушакова, П. И. Беспалов, П. А. Оржековский; под. ред. проф. П. А. Оржековского — М.: АСТ: Астрель: Профиздат, 2006. (с.19-21)
3. Химия: 8-й класс: учеб. для общеобр. учреждений / П. А. Оржековский, Л. М. Мещерякова, Л. С. Понтак. М.: АСТ: Астрель, 2005.(§8)
4. Химия: неорг. химия: учеб. для 8 кл. общеобр. учреждений / Г. Е. Рудзитис, ФюГю Фельдман. – М.: Просвещение, ОАО «Московские учебники», 2009. (§6)
5. Энциклопедия для детей. Том 17. Химия / Глав. ред. В.А. Володин, вед. науч. ред. И. Леенсон. – М.: Аванта+, 2003.
Дополнительные веб-ресурсы
1. Единая коллекция цифровых образовательных ресурсов .
2. Электронная версия журнала «Химия и жизнь» .
3. Тесты по химии (онлайн) .
Домашнее задание
с.19-21 №№ 1-5 из Рабочей тетради по химии: 8-й кл.: к учебнику П. А. Оржековского и др. «Химия. 8 класс» / О. В. Ушакова, П. И. Беспалов, П. А. Оржековский; под. ред. проф. П. А. Оржековского — М.: АСТ: Астрель: Профиздат, 2006.
Й. Я. Берцелиус Обозначение химических элементов Д. Дальтоном Таблица названий и символов некоторых химических элементов Алхимические знаки химических элементов и веществ Массовые доли химических элементов в земной коре
dp-adilet.kz
Символ — химический элемент — Большая Энциклопедия Нефти и Газа, статья, страница 3
Символ — химический элемент
Cтраница 3
Отдельные изотопы обозначают, помечая символ химического элемента сверху справа индексом, указывающим массу. [31]
В центре каждой клетки помещен символ химического элемента; ниже символа помешено русское название, а выше — порядковый номер элемента; ниже названия приведен атомный вес элемента; сбоку химического символа, вдоль вертикальной границы клетки, указано распределение электронов в электронной оболочке атома элемента. [32]
В термохимических уравнениях, помимо символов химических элементов и теплового эффекта, часто указывают агрегатное состояние реагентов и продуктов. [33]
Цифры в кружке справа от символа химического элемента обозначают ширину запрещенной зоны в кристалле данного химического элемента. Можно заметить, что ширина запрещенной зоны закономерно изменяется в этой группе: она возрастает в каждом периоде при переходе от элемента к элементу слева направо, она уменьшается в каждой группе при переходе от элемента к элементу сверху вниз. Эта закономерность не является неожиданной, так как полупроводниковые свойства вещества определяются в конечном счете структурой внешних электронных оболочек его атомов. [34]
Легирующие элементы могут обозначаться или общепринятыми символами химических элементов, или прописными буквами английского алфавита ( С — хром, М — молибден, А — азот, N — никель, К — кремний), или одновременно символами и буквами. Буква Н после цифр указывает на особенности прокаливаемости этой марки стали. В сталях специального назначения ( например, для труб) трехзначное число означает минимальное временное сопротивление разрыву ( предел прочности) в ме-гапаскалях. [35]
Для обозначения состава атомных ядер применяют символ данного химического элемента, около которого помещают два числа: слева вверху массовое число, а слева внизу — число протонов в ядре. [36]
Для обозначения состава атомных ядер применяют символ дан-ного химического элемента, около которого помещают два числа: справа вверху массовое число, а слева внизу — число протонов в ядре. [37]
При необходимости в технических требованиях чертежа указывают символ химического элемента или формулу химического соединения, используемого в качестве соосаждаемого вещества. [38]
Элемент принято обозначать Х, где X — символ химического элемента. [39]
Для удобства описания процессов радиоактивного распада слева внизу у символа химического элемента ставится его атомный номер, а справа наверху — его атомная масса. [40]
Для упрощения записей пользуются таким способом: атом обозначают символом соответствующего химического элемента, а вокруг символа ставят столько точек, сколько электронов содержится во внешнем слое. Точки условно символизируют собой электрические центры тяжести электронов, участвующих в образовании химической связи. [41]
Часто атомный номер опускают, так как он просто дублирует символ химического элемента. [42]
Для удобства пользователей в режиме работы 0 на экран выводятся символы химических элементов, которые необходимо вводить в точном соответствии с их — видом на экране терминала. В этом же разделе может быть получен перечень имеющихся в банке соединений данного элемента с элементами, которые стоят до него в списке БД. [43]
В обозначении материала композиционного покрытия указывают металл покрытия и в скобках символ химического элемента или формулу химического соединения, используемого в качестве соосаждаемого вещества. [44]
На крышке окулярного устройства сверху укрепляется шкала с выгравированными на ней символами химических элементов. Шкала 10 применяется при сортировке легированных сталей; шкала 15 служит для сортировки цветных сплавов на медной основе. [45]
Страницы: 1 2 3
www.ngpedia.ru
Что означают цифры в табл Менделеева?
В XIX веке не было никаких представлений о строении атома. Открытие Д. И. Менделеева являлось лишь обобщением опытных фактов, но их физический смысл долгое время оставался непонятным. Когда появились первые данные о строении ядра и распределении электронов в атомах, это позволило взглянуть на периодический закон и систему элементов по-новому. Таблица Д. И. Менделеева дает возможность наглядно проследить периодичность свойств элементов, встречающихся в природе. 2Каждому элементу в таблице присвоен определенный порядковый номер (H — 1, Li — 2, Be — 3 и т. д.). Этот номер соответствует заряду ядра (количеству протонов в ядре) и числу электронов, вращающихся вокруг ядра. Число протонов, таким образом, равно числу электронов, и это говорит о том, что в обычных условиях атом электрически нейтрален. 3Деление на семь периодов происходит по числу энергетических уровней атома. Атомы первого периода имеют одноуровневую электронную оболочку, второго — двухуровневую, третьего — трехуровневую и т. д. При заполнении нового энергетического уровня начинается новый период. 4Первые элементы всякого периода характеризуются атомами, имеющими по одному электрону на внешнем уровне, — это атомы щелочных металлов. Заканчиваются периоды атомами благородных газов, имеющими полностью заполненный электронами внешний энергетический уровень: в первом периоде инертные газы имеют 2 электрона, в последующих — 8. Именно по причине похожего строения электронных оболочек группы элементов имеют сходные физико-химические свойства. 5В таблице Д. И. Менделеева присутствует 8 главных подгрупп. Такое их количество обусловлено максимально возможным числом электронов на энергетическом уровне. 6Внизу периодической системы выделены лантаноиды и актиноиды в качестве самостоятельных рядов. 7С помощью таблицы Д. И. Менделеева можно пронаблюдать периодичность следующих свойств элементов: радиуса атома, объема атома; потенциала ионизации; силы сродства с электроном; электроотрицательности атома; степени окисления; физических свойств потенциальных соединений. 8К примеру, радиусы атомов, если смотреть вдоль периода, уменьшаются слева направо; растут сверху вниз, если смотреть вдоль группы. 9Четко прослеживаемая периодичность расположения элементов в таблице Д. И. Менделеева рационально объясняется последовательным характером заполнения электронами энергетических уровней.
порядковый номер
touch.otvet.mail.ru
