Метиленхлорид — популярный промышленный растворитель
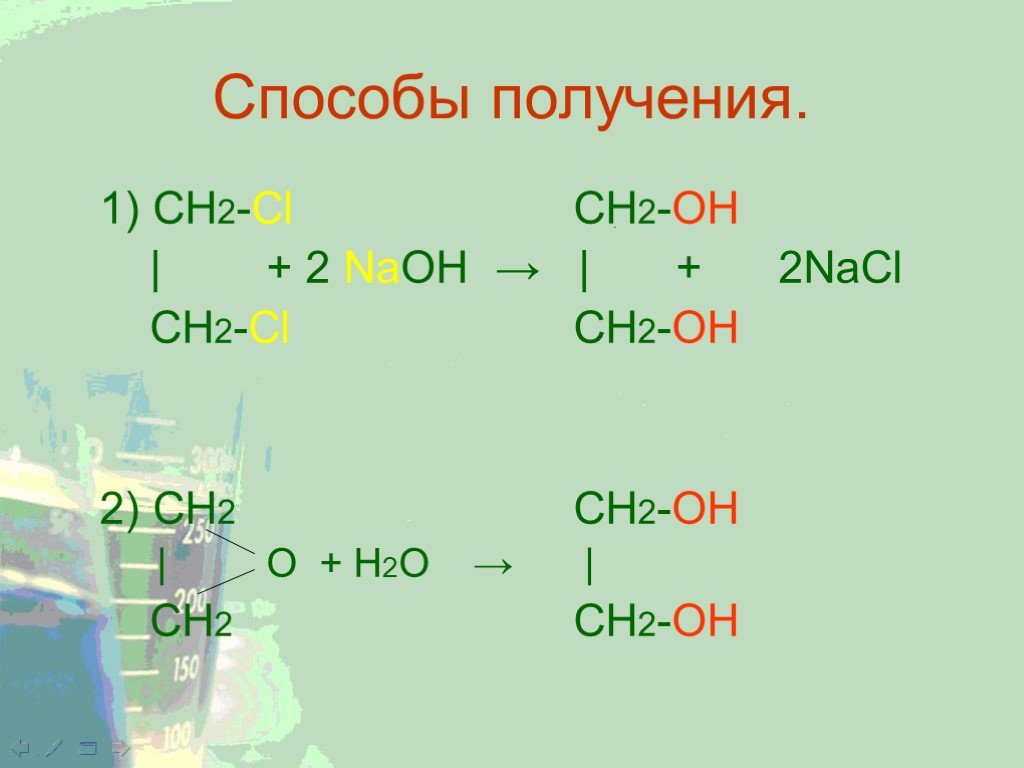
Метиленхлорид — органическое соединение, производное метана. Синонимы названия: метилен хлористый, дихлорметан, ДХМ. Формула Ch3Cl2.
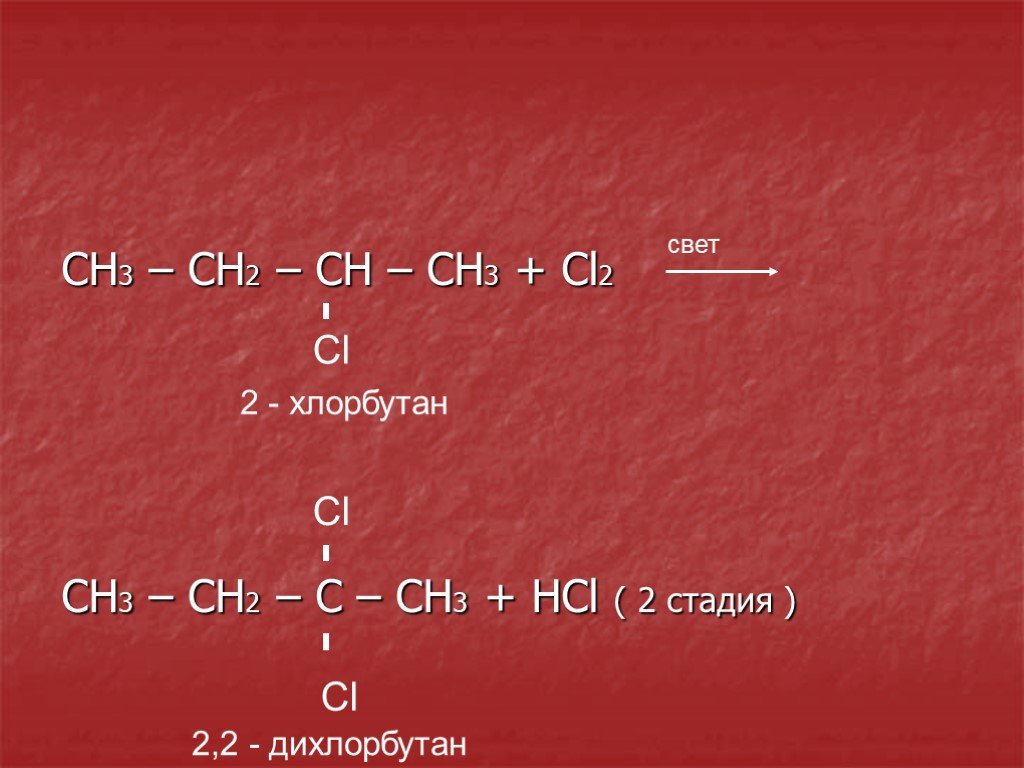
Впервые был синтезирован в 1840-м году: в лаборатории соединили газообразный хлор с хлористым метилом и выдерживали смесь на свету. Для массового производства дихлорметан получают химическим синтезом из метана, выделенного из коксовых газов, и газообразного хлора. Другой метод: получение хлорметила из метанола и соляной кислоты, с последующим хлорированием.
Свойства
Подвижная прозрачная жидкость без цвета, летучая, с характерным резким, сладковатым запахом эфира. В воде растворяется слабо, хорошо — в орг. растворителях. При растворении в горячей воде разрушается, разлагаясь на соляную кислоту и формальдегид. Малотоксичен по сравнению с другими растворителями.
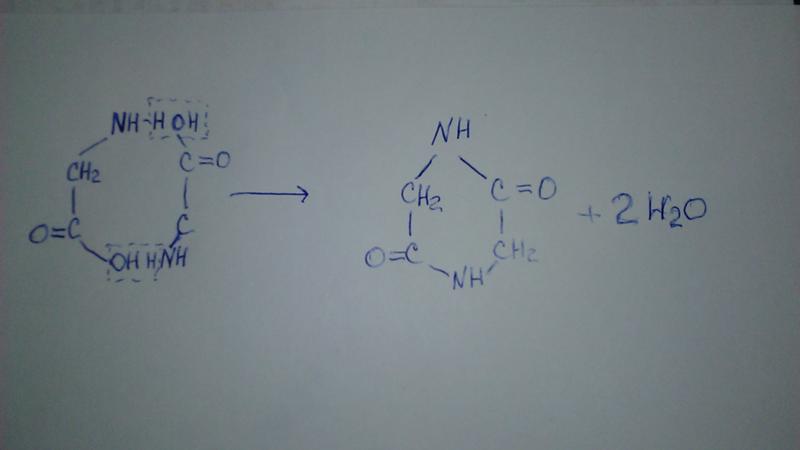
Вступает в реакцию с хлором, с получением хлороформа. Реагирует и с другими галогенами: йодом, бромом. Взаимодействует со спиртовым и водным растворами аммиака. В результате реакции с водным аммиаком получается муравьиная и соляная кислоты и метиламин. Вступает в реакции с ароматическими углеводородами, например, с бензолом.
В результате реакции с водным аммиаком получается муравьиная и соляная кислоты и метиламин. Вступает в реакции с ароматическими углеводородами, например, с бензолом.
Очень бурно реагирует (вплоть до взрыва) со щелочными металлами.
| Вытяжной шкаф ВА-102, комплектация «Стандарт» | Метиленхлорид (дихлорметан) «хч» 1000 мл |
Меры предосторожности
Реактив токсичен, плохо горит, но горение поддерживает; смеси с воздухом взрывоопасны. Обладает канцерогенным действием.
Проглатывание реактива и длительное вдыхание паров или аэрозолей приводит к раздражению слизистых глаз и органов дыхания, отравлению, головокружению и головным болям, обморокам, диарее, заболеваниям печени и поджелудочной железы. Тяжелое отравление может привести к остановке дыхания. Длительное воздействие вещества на кожу может вызвать химический ожог.
При работе с метиленхлоридом следует использовать средства защиты: очки, резиновые перчатки (не нитриловые и не латексные), одежду с длинными рукавами, респиратор. В лабораториях все эксперименты проводят в вытяжном шкафу.
В лабораториях все эксперименты проводят в вытяжном шкафу.
Хранят реактив обычно в стальных контейнерах или бочках. Допускается хранение вне помещения, под навесом. Предпочтительнее в прохладных, вентилируемых, сухих складах.
Перевозить ДХМ можно любыми видами транспорта, контейнеры и транспорт маркируются символом опасности Xn (вредное вещество).
Применение
Реагент гораздо менее токсичен, чем другие органические растворители, легко удаляется, отличается невысокой стоимостью, поэтому широко используется во многих сферах промышленности, включая пищепром и фармацевтику.
- В химпроме используется для производства синтетических полимеров, например, полиуретановых пен (вспениватель), поролона, синтетических волокон; форм из пластмассы.
- Для получения химических продуктов, производных от дихлорметана.
- Как промышленный растворитель для очистки и обезжиривания металлических поверхностей; входит в состав аэрозольных красок; для склеивания акрилового стекла и различных пластиков, исключая полиэтилен и полипропилен; растворитель жиров, смол, битумов.
- В пищепроме — растворитель при экстракциях, например, для получения кофеина из зерен кофе, хмеля.
- В фармацевтике для изготовления аскорбиновой кислоты.
- В лабораторной практике для проведения анализов качества воды на наличие в ней бензола, аммиака, нитритов и нитратов, хлора, токсичных металлов и многих других вредных примесей. В хроматографии.
- Входит в состав некоторых хладагентов.
- Для снятия старых лаков и красок с любых поверхностей.
- В фотоделе — для обработки фото-и и кинопленок.
Methylene chloride (Метиленхлорид) (CAS 75-09-2) — Chemistry For Industry — Solvents & Chemicals
€0.00 – €20.00
Другие названия: метиленхлорид, дихлорметан, хлористый метилен
Описание:
Популярный промышленный растворитель – органическое соединение, производное метана. Подвижная прозрачная жидкость без цвета, летучая, с характерным резким, сладковатым запахом эфира. Слабо растворяется в воде.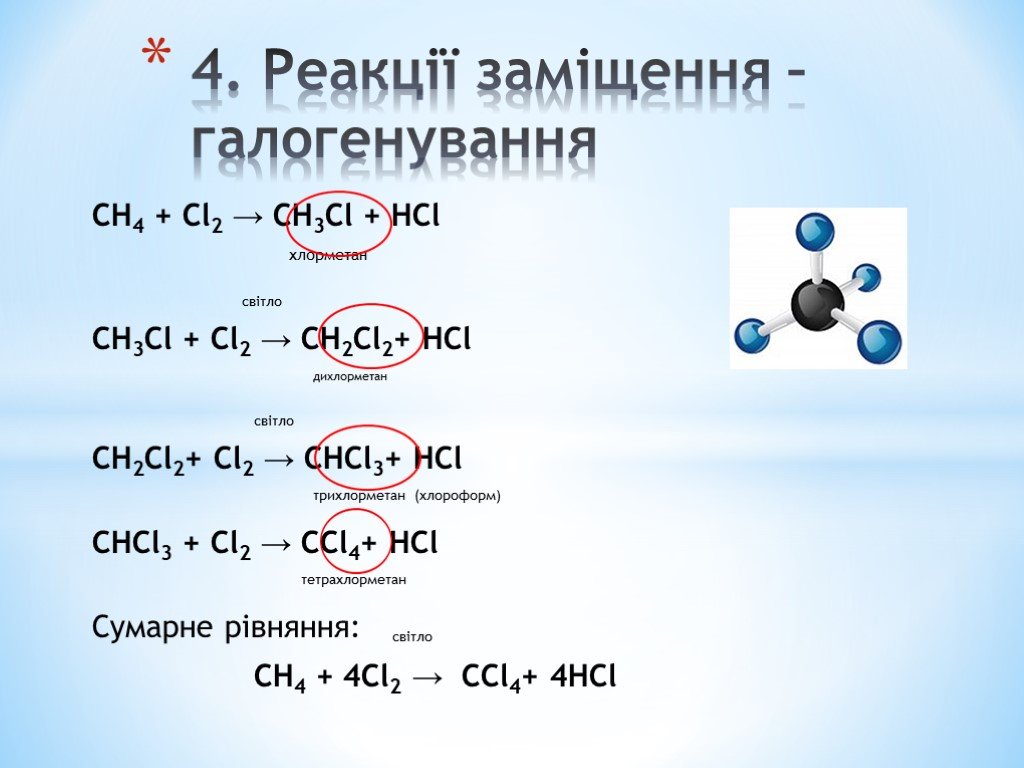 Хорошо растворяется в органических растворителях. При растворении в горячей воде разрушается, разлагаясь на соляную кислоту и формальдегид. Малотоксичен по сравнению с другими растворителями. Вступает в реакцию с хлором, с получением хлороформа. Реагирует и с другими галогенами: йодом, бромом. Взаимодействует со спиртовым и водным растворами аммиака. В результате реакции с водным аммиаком получается муравьиная и соляная кислоты и метиламин. Вступает в реакции с ароматическими углеводородами, например, с бензолом.
Хорошо растворяется в органических растворителях. При растворении в горячей воде разрушается, разлагаясь на соляную кислоту и формальдегид. Малотоксичен по сравнению с другими растворителями. Вступает в реакцию с хлором, с получением хлороформа. Реагирует и с другими галогенами: йодом, бромом. Взаимодействует со спиртовым и водным растворами аммиака. В результате реакции с водным аммиаком получается муравьиная и соляная кислоты и метиламин. Вступает в реакции с ароматическими углеводородами, например, с бензолом.
CAS: 75-09-2
Спецификация на метиленхлорид(TDS)
Артикул: Н/Д Категории: Mеталлообработка, Бытовая химия, Все товары, Дорожная химия, Печать/типография, Смолы, пластмассы, полиуретаны, Строительная промышленность, Фармацевтические препараты
- Описание
- Детали
Описание
Применение и использование:
Реагент гораздо менее токсичен, чем другие органические растворители, легко удаляется, отличается невысокой стоимостью, поэтому широко используется во многих сферах промышленности, включая пищепром и фармацевтику.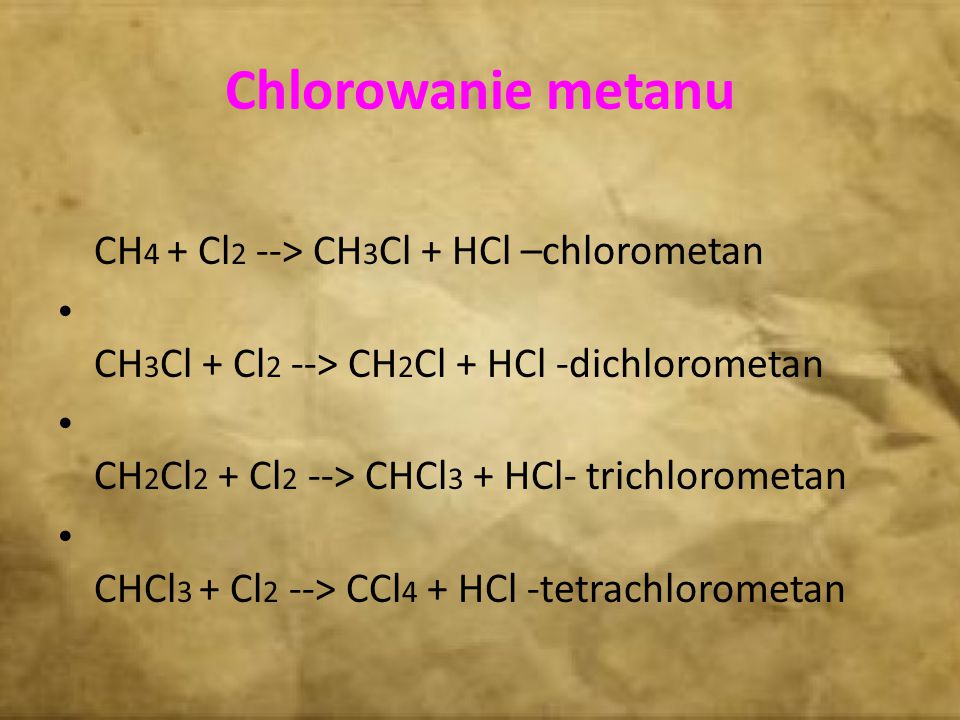
● В химпроме используется для производства синтетических полимеров, например, полиуретановых пен (вспениватель), поролона, синтетических волокон; форм из пластмассы.
● Для получения химических продуктов, производных от дихлорметана.
● Как промышленный растворитель для очистки и обезжиривания металлических поверхностей; входит в состав аэрозольных красок; для склеивания акрилового стекла и различных пластиков, исключая полиэтилен и полипропилен; растворитель жиров, смол, битумов.
● В пищепроме — растворитель при экстракциях, например, для получения кофеина из зерен кофе, хмеля.
● В фармацевтике для изготовления аскорбиновой кислоты.
● В лабораторной практике для проведения анализов качества воды на наличие в ней бензола, аммиака, нитритов и нитратов, хлора, токсичных металлов и многих других вредных примесей. В хроматографии.
● Входит в состав некоторых хладагентов.
● Для снятия старых лаков и красок с любых поверхностей.
● В фотоделе — для обработки фото-и и кинопленок.
Физические свойства
Молярная масса – 84,9 г/моль,
плотность – 1,326 г/см³.
Термосвойства:
Температура плавления -96,7 °C,
температура кипения 40 °C,
температура вспышки 14 °C
Химическая формула: Ch3Cl2
Детали
| Вес | Н/Д |
|---|
[Дихлорметан]
Общедоступно Опубликовано 2017
- EintragstypEntry Type
- Chemical Compound
- EintragsspracheEntry Language
- EnglischEnglish
- SchlagwortKeyword
Химическое соединение; Дихлорметан
- ИнЧИ
ИнЧИ=1S/Ch3Cl2/c2-1-3/h2h3; YMWUJEATGCHHMB-UHFFFAOYSA-N
| Имя ИЮПАК | дихлорметан |
| Альтернативные имена | Метиленхлорид Метилендихлорид |
| Молекулярная формула | CH 2 Класс 2 |
| Молярная масса | 84,927 г/моль |
| ИнЧИ | InChI=1S/Ch3Cl2/c2-1-3/h2h3 |
| Ключ ИнЧИ | YMWUJEATGCHHMB-UHFFFAOYSA-N |
| Номер КАС 75-09-2 | |
| PubChem ИД 6344 | |
Дихлорметан
Источник: Национальный центр биотехнологической информации. База данных соединений PubChem; CID=6344, https://pubchem.ncbi.nlm.nih.gov/compound/6344
База данных соединений PubChem; CID=6344, https://pubchem.ncbi.nlm.nih.gov/compound/6344
Дополнительную информацию см. на сайте PubChem Compound. База данных
Найти в базе данных IUPAC
Выпуск 93/2021
Конец строки Химические названия
Выпуск 85/2013
Анализ CUPRAC как роман Анализ антиоксидантной способности на основе Et и его различные модификации для Измерение емкости/активности в различных матрицах (включая биологические жидкости)
Выпуск 84/2012
Руководство по отчетности Измерения фазового равновесия
Выпуск 81/2009
Противоточная хроматография в области аналитической химии
Выпуск 79/2007
Свойства и единицы в Клинические лабораторные науки Часть XX.
 Свойства и единицы измерения в Clinical
и экологическая токсикология человека
Свойства и единицы измерения в Clinical
и экологическая токсикология человека
Выпуск 76/2004
Характеристика Полиамиды 6, 11 и 12: определение молекулярной массы по размеру Эксклюзионная хроматография
Химическая актинометрия
Выпуск 72/2000
Биологический мониторинг для Воздействие летучих органических соединений (ЛОС)
Токсикокинетика
Отбор проб и анализ Процедуры, факторы, влияющие на компоненты неопределенности, и качество гарантия
Биомониторинг Контакт
Биомониторинг Действие Уровни
Выпуск 71/1999
Критическая компиляция Шкалы параметров растворителя.
 Часть I. Чистый донор без водородной связи
Растворители
Часть I. Чистый донор без водородной связи
Растворители
Выпуск 70/1998
Определение йода Виды в экологических и биологических пробах
Определение видов олова в пробах окружающей среды
Выпуск 63/1991
Отчеты IUPAC о пестицидах, № 28: Некоторые аспекты анализа остатков дикарбоксимида Фунгициды в продуктах питания
Методы получения Ионы-радикалы в низкотемпературных матрицах для электроники Спектроскопия
Выпуск 62/1990
Определение Содержание компонентов сложноэфирных эмульгаторов после гидролиза и силилирования Газовая хроматография: результаты совместного исследования и стандартизированные Метод
Полярографическая полуволна Возможности катионов в неводных растворителях.

Выпуск 60/1988
Определение токоферолов и токотриенолы в растительных маслах и жирах с помощью High Performance Liquid Хроматография: результаты совместного исследования и стандартизированные Метод
Извлечение, очистка и Методы группового разделения в анализе следовых количеств хлорорганических соединений
Выпуск 59/1987
Электрохимический анализ Органические загрязнители
Очистка растворителей для Электроанализ: дихлорметан
Очистка растворителей для Электроанализ: 1,1-дихлорэтан и 1,2-дихлорэтан
Выпуск 58/1986
Экстракция и жидкость-жидкость Разделение
Дальнейшая очистка
Выпуск 56/1984
Рекомендации по отчетности Электродные потенциалы в неводных растворителях
Сбор, обработка и Хранение образцов для биологического мониторинга профессионального облучения к токсичным химическим веществам
Улучшенная рентабельность Подходы к анализу остатков пестицидов
Выпуск 55/1983
Термодинамические функции Перенос одиночных ионов из воды в неводные и смешанные растворители: часть I — Свободные энергии Гиббса перехода к неводным растворителям
Выпуск 54/1982
Рекомендации по отчетности Электродные потенциалы в неводных растворителях
Критическая оценка Константы равновесия с участием ацетилацетона и его металла Хелаты
Равновесия с участием Металлы
Выпуск 53/1981
Разработка и оценка Упрощенные подходы к анализу остатков
Выпуск 52/1980
Определение
Выпуск 51/1979
Обзор методов для Определение нелетучих нитрозаминов в пищевых продуктах
Общее и конкретное Стандарты идентичности SCP, используемых в качестве корма для животных
QuelleSource
- TitleTitle
- Chemical Compounds
- VerlagPublisher
- 2016
Дополнительные материалы
Пожалуйста, войдите или зарегистрируйтесь в De Gruyter, чтобы заказать этот продукт.
ВойтиРегистрация
Дихлорметан — Американское химическое общество
- Вы здесь:
- СКУД
- Молекула недели
- Молекула недели Архив
- Архив — Д
- Дихлорметан
Молекула недели Архив
04 марта 2019 г.
Предыдущий Далее
Вы беспокоитесь, что я загрязню ваш кофе без кофеина? Не будь.
Какая я молекула?
Март — месяц растворителей MOTW! Это первая из четырех статей о ключевых растворителях — прим. ред.
Дихлорметан, обычно называемый метиленхлоридом, представляет собой растворитель, который широко используется в химических исследованиях и производстве. Это очень летучая жидкость (см. таблицу быстрых фактов), но она не воспламеняется и не взрывоопасна на воздухе.
Дихлорметан обычно получают путем хлорирования метана. В процессе также образуются три других хлоруглеводорода C 1 — хлорметан, трихлорметан (хлороформ) и тетрахлорметан (четыреххлористый углерод). Эти четыре вещества разделяют перегонкой.
Хотя дихлорметан является наименее токсичным C 1 хлоруглеводородом, он представляет опасность. Вдыхание его может вызвать симптомы, варьирующиеся от сонливости до раздражения дыхательных путей и даже смерти.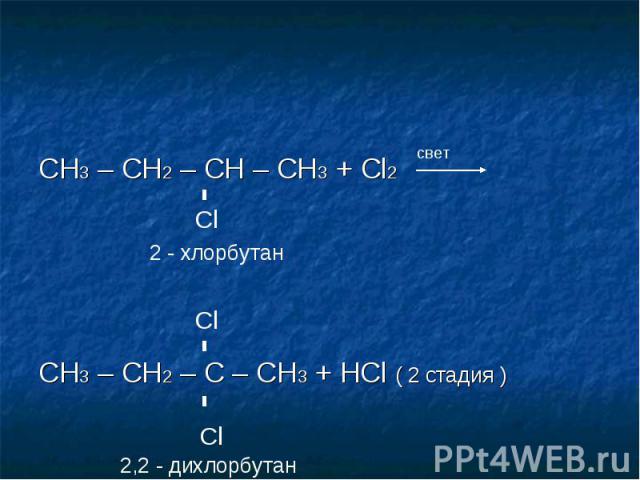 Он также может быть канцерогенным, но было проведено недостаточно исследований, чтобы установить степень воздействия, вызывающего рак.
Он также может быть канцерогенным, но было проведено недостаточно исследований, чтобы установить степень воздействия, вызывающего рак.
Несмотря на опасность для здоровья, дихлорметан является одним из основных растворителей, используемых для удаления кофеина из кофейных зерен. После удаления кофеина летучесть растворителя позволяет легко удалить остаточный растворитель. Любой оставшийся дихлорметан значительно ниже концентрации в 10 частей на миллион, разрешенной Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США.
Информация об опасности дихлорметана| Классификация СГС*: раздражение кожи, категория 2 | |
| h415 — вызывает раздражение кожи | |
| Классификация СГС: серьезное раздражение глаз, категория 2A | |
| h419 — вызывает серьезное раздражение глаз | |
| Классификация СГС: специфическая токсичность для органа-мишени, однократное воздействие, наркотическое действие, категория 3 | |
| h436 — Может вызывать сонливость или головокружение | |
| Классификация СГС: канцерогенность, категория 2 | |
| h451 — Предположительно вызывает рак | |
| Классификация СГС: опасность для водной среды, острая опасность, категория 3 | |
| h502 — Вреден для водных организмов | |
*Глобально согласованная система классификации и маркировки химических веществ. Пояснения к пиктограммам.
Пояснения к пиктограммам.
| Рег. CAS. № | 75-09-2 |
| Эмпирическая формула | CH 2 Класс 2 |
| Молярная масса | 84,93 г/моль |
| Внешний вид | Бесцветная жидкость |
| Температура кипения | 40 ºC |
| Растворимость в воде | 13 г/л |
Обновление MOTW:
01 апреля 2019 г.
Дихлорметан (он же метиленхлорид) десятилетиями был полезным растворителем; но из-за его значительных опасностей его используют в меньшем количестве приложений. В середине марта Агентство по охране окружающей среды США завершило запрет на использование дихлорметана в качестве ингредиента в средствах для удаления красок и покрытий, используемых потребителями, который вступит в силу в конце 2019 года.