Влияние Na2CO3 на стабильность двойной спирали ДНК: сильное дестабилизирующее действие анионов
. 2003 июнь; 20 (6): 801-9.
дои: 10.1080/07391102.2003.10506896.
Галюк Елена Николаевна 1 , Дмитрий Ю. Ландо, Валентина П. Егорова, Хва Дай, Юрий М. Досин
принадлежность
- 1 Институт биоорганической химии НАН Беларуси, ул. Купревича, 5/2, 220141 Минск, Беларусь.
- PMID: 12744709
- DOI: 10.1080/07391102.2003.10506896
Галюк Елена Николаевна и др. J Biomol Struct Dyn.
2003 9 июня0003
J Biomol Struct Dyn.
2003 9 июня0003
дои: 10.1080/07391102.2003.10506896.
Авторы
Галюк Елена Николаевна 1 , Дмитрий Ю. Ландо, Валентина П. Егорова, Хва Дай, Юрий М. Досин
принадлежность
- 1 Институт биоорганической химии НАН Беларуси, ул. Купревича, 5/2, 220141 Минск, Беларусь.
- PMID: 12744709
- DOI: 10.1080/07391102.2003.10506896
Абстрактный
Добавление Na(2)CO(3) к почти бессолевому раствору ДНК (5,10(-5)M ЭДТА, pH=5,7, T(m)=26,5°C) повышает как pH, так и температуру плавления ДНК (T( м)) при концентрации Na(2)CO(3) менее 0,004 М. Для 0,004 М Na(2)CO(3) максимальная Т(м)=58°С и рН=10,56. Дальнейшее увеличение концентрации приводит к монотонному уменьшению T(m) до 37°С для 1М Na(2)CO(3) (pH=10,57). Повышение рН также не является монотонным. Максимальное значение рН=10,87 достигается при 0,04 М Na(2)CO(3) (Т(м)=48,3°С). Для выявления причины такой дестабилизации ДНК, происходящей в узком интервале рН (10,56/10,87) и широком интервале концентраций Na(2)CO(3) (0,004/1М), была разработана методика определения отдельных влияний. на T(m) Na(+), pH и анионов, образованных Na(2)CO(3) (HCO(3)(-) и CO(3)(2-)). Сравнение влияния анионов, образованных Na(2)CO(3), на стабильность ДНК с Cl(-) (анион, инертный по отношению к ДНК), ClO(4)(-) (сильный дестабилизирующий ДНК «хаотропный» анион) и OH( -) было выполнено. Показано, что только Na(+) и pH влияют на T(m) в растворе Na(2)CO(3) при концентрациях ниже 0,001 М. Однако T(m) уменьшается с концентрацией для [Na(2) CO(3)]>
Для 0,004 М Na(2)CO(3) максимальная Т(м)=58°С и рН=10,56. Дальнейшее увеличение концентрации приводит к монотонному уменьшению T(m) до 37°С для 1М Na(2)CO(3) (pH=10,57). Повышение рН также не является монотонным. Максимальное значение рН=10,87 достигается при 0,04 М Na(2)CO(3) (Т(м)=48,3°С). Для выявления причины такой дестабилизации ДНК, происходящей в узком интервале рН (10,56/10,87) и широком интервале концентраций Na(2)CO(3) (0,004/1М), была разработана методика определения отдельных влияний. на T(m) Na(+), pH и анионов, образованных Na(2)CO(3) (HCO(3)(-) и CO(3)(2-)). Сравнение влияния анионов, образованных Na(2)CO(3), на стабильность ДНК с Cl(-) (анион, инертный по отношению к ДНК), ClO(4)(-) (сильный дестабилизирующий ДНК «хаотропный» анион) и OH( -) было выполнено. Показано, что только Na(+) и pH влияют на T(m) в растворе Na(2)CO(3) при концентрациях ниже 0,001 М. Однако T(m) уменьшается с концентрацией для [Na(2) CO(3)]>
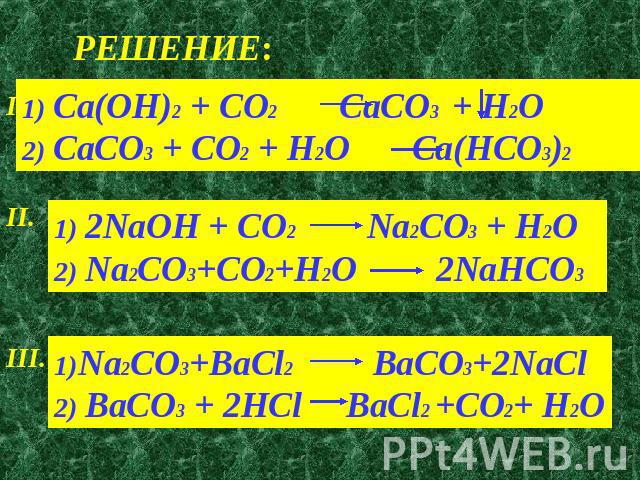 Анионы Na(2)CO(3) также оказывают сильное дестабилизирующее влияние при этих концентрациях. Для 0,1 М Na(2)CO(3) (pH=10,84, [Na(+)]=0,2M, T(m)=42,7°С) эффект дестабилизации анионов выше на 20°С. Для NaClO(4 ) (ClO(4)(-) является сильным «хаотропным» анионом), аналогичный анионный эффект возникает при гораздо более высоких концентрациях, примерно 3M. Это означает, что Na(2)CO(3) вызывает гораздо более сильный анионный эффект, чем другие соли. Эффект зависит от рН. Она снижается в пять раз при нейтральном рН после добавления HCl к 0,1 М Na(2)CO(3), а также после добавления NaOH для рН выше 11,2.
Анионы Na(2)CO(3) также оказывают сильное дестабилизирующее влияние при этих концентрациях. Для 0,1 М Na(2)CO(3) (pH=10,84, [Na(+)]=0,2M, T(m)=42,7°С) эффект дестабилизации анионов выше на 20°С. Для NaClO(4 ) (ClO(4)(-) является сильным «хаотропным» анионом), аналогичный анионный эффект возникает при гораздо более высоких концентрациях, примерно 3M. Это означает, что Na(2)CO(3) вызывает гораздо более сильный анионный эффект, чем другие соли. Эффект зависит от рН. Она снижается в пять раз при нейтральном рН после добавления HCl к 0,1 М Na(2)CO(3), а также после добавления NaOH для рН выше 11,2. Похожие статьи
Компенсация эффектов стабилизации и дестабилизации ДНК, вызванных цисплатином, частично нарушается в щелочной среде.
Галюк Е.Н., Фридман А.С., Воробьев В.И., Арутюнян С.Г., Саргсян С.А., Хаурук М.М., Ландо Д.Ю. Галюк Е.Н. и соавт.
 J Biomol Struct Dyn. 2008 февраля; 25 (4): 407-17. дои: 10.1080/07391102.2008.10507189.
J Biomol Struct Dyn. 2008.
PMID: 18092835
J Biomol Struct Dyn. 2008 февраля; 25 (4): 407-17. дои: 10.1080/07391102.2008.10507189.
J Biomol Struct Dyn. 2008.
PMID: 18092835Денатурация ДНК при замораживании в щелочной среде.
Галюк Е.Н., Вартелл Р.М., Досин Ю.М., Ландо Д.Ю. Галюк Е.Н. и соавт. J Biomol Struct Dyn. 2009 фев; 26 (4): 517-23. дои: 10.1080/07391102.2009.10507267. J Biomol Struct Dyn. 2009. PMID: 19108591
Кинетический анализ влияния нейтральных солей на термостабильность алкогольдегидрогеназы дрожжей.
Икегая К. Икегая К. Дж Биохим. 2005 март; 137(3):349-54. дои: 10.1093/jb/mvi037. Дж Биохим. 2005. PMID: 15809336
Нуклеокапсидный белок ВИЧ-1 как шаперон нуклеиновой кислоты: спектроскопическое исследование его дестабилизирующих спираль свойств, специфичности структурного связывания и активности отжига.

