Азотнокислый барий — Справочник химика 21
Прокаливание азотнокислого бария с последующим присоединением к окиси бария кислорода [c.207]Раствор, содержащий 26,1 г азотнокислого бария, смешан с 42 мл 26%-ного раствора сернокислого натрия (плотность 1,3). Какие вещества и в каком количестве остались в растворе после того, как осадок был отфильтрован [c.27]
Сколько миллилитров 0,2 и. раствора щелочного карбоната нужно прибавить к 200 мл 0,1 М раствора азотнокислого бария, чтобы полностью ссадить барий в виде карбоната бария [c.28]
Следовательно, при электролизе раствора смесн солей водород выделяется только за счет электролиза раствора Ва(МОз)а, кислород —за счет обеих солей. Значит, из 1,5 объемов кислорода (при 2 объемах водорода) 1 объем выделился при электролизе Ba(NO i)a, 0,5 объема — u(N0.-i)2. Это значит, что количество грамм-эквивалентов азотнокислого бария, а значит и его молей, было в два раза больше, чем нитрата меди.
Сколько выделится азотнокислого бария из раствора, насыщенного при 100 и охлажденного до 0°, если во взятом растворе было 50 мл воды. Растворимость азотнокислого бария при 0° равна 5 г, а при 100°—34,2 г. [c.359]
Азотнокислый барий кристаллизуется при обычных условиях без воды. Напротив, нитраты Са и 5г выделяются в виде кристаллогидратов. Последние легкорастворимы в воде, тогда как растворимость Ba(NOз)2 [и Ра (N03)2] значительно меньше. Нитрат кальция широко применяется в качестве азотсодержащего минерального удобрения. Нитраты стронция и бария служат в пиротехнике для изготовления составов, сгорающих красным (Зг) или зеленым (Ва) пламенем. [c.388]
Окись бария можно получить прокаливанием азотнокислого бария [c.68]
Менее чистый препарат можно получить при взаимодействии углекислого натрия с азотнокислым барием [c.71]
На присутствие солей серной кислоты от прибавления к раствору азотнокислого бария не должен получаться осадок сернокислого бария. [c.160]
На присутствие солей серной кислоты водный раствор уротропина не должен давать осадка сернокислого бария от прибавления раствора азотнокислого бария. [c.169]
На присутствие сернокислых солей он не должен давать мути с азотнокислым барием. [c.217]
На содержание хлористых и сернокислых солей водный раствор пиперазина, подкисленный азотной кислотой, не должен давать осадка ни с азотнокислым серебром, ни с азотнокислым барием. [c.259]
Азотнокислый барий плохо растворим в холодной воде и еще хуже в растворе азотнокислой меди. Поэтому для того, чтобы обе соли перевести в раствор, необходимо смесь нагреть. [c.302]
Барий вводится в качестве одного из компонентов катализатора, потому что он оказывает защитное действие против отравляющего действия сульфатов имеются также указания на то, что он оказывает стабилизирующее действие на катализатор в отношении его восстановления. Приведенную здесь методику можно применить также и к получению медно-хромового катализатора не содержащего бария. В этом случае не берут совсем азотнокислого бария, а азотнокислой меди берут 242 г (1 мол.). Все остальные детали синтеза сохраняются.
Перйодат натрия, приготовленный из 100 г иода (около 225 г), суспендируют в 1 л кипящей воды, содержащей 10 мл концентрированной азотной кислоты (для увеличения растворимости перйодата). Небольшой избыток (против рассчитанного по уравнению) нитрата бария (325 г) растворяют в горячей воде раствор кипятят 1,5—2 часа при энергичном перемешивании. Затем раствор нейтрализуют гидроокисью бария и оставляют охлаждаться. Выкристаллизовавшийся перйодат бария промывают несколько раз декантацией горячей водой (каждый раз перемешивая кристаллы) и затем промывают на воронке Бюхнера. Если соль окрашивает пламя горелки в желтый цвет, ее снова кипятят с раствором азотнокислого бария в присутствии азотной кислоты, как было указано выше. [c.165]
Барий азотнокислый. Бария нитрат. Ba(NOs)2. М.м. 261,35. Бесцветные кристаллы. Ядовит. ГОСТ 3777-76. [c.105]
Концентрированная соляная и азотная кислоты осаждают из достаточно концентрированных растворов бариевых солей хлористый ИЛИ азотнокислый барий. [c.298]
Пример 1. Нужно составить двойную основную смесь из азотнокислого бария и крахмала [c.8]
Во-первых, напишем реакцию разложения окислителя, т. е. азотнокислого бария [c.8]
Как видно из этого примера, при разложении окислителя — азотнокислого бария Ва(ЖЗз)2 —выделяется кислород 1 молекула его содержит 6 атомов кислорода, а в свободном виде выделяется лишь 5 атомов 1 атом кислорода остается в соединении с барием в виде окиси бария ВаО и окисляющего действия не обнаруживает.
Определить теплоту реакции взаимодействия азотнокислого бария с алюминием. [c.21]
Азотнокислый барий (нитрат бария) Ва(НОз)2, молекулярный вес 261,39 получается при реакции обменного разложения между хлористым барием в растворе и нитратом натрия при 80—90°. [c.31]
Азотнокислый барий служит окислителем во многих пиротехнических, особенно осветительных составах. Составы с азотнокислым барием значительно менее чувствительны, чем с окислителями, указанными выше. В некоторых случаях азотнокислый барий применяется в составах в смеси с другими, более активно действующими окислителями. [c.31]
В качестве окислителя для осветительных составов большей частью применяют азотнокислый барий. Прп горении составов с азотно—ки ым барием образуется окпсь бария, при температуре горения состава она излучает яркие линии и полосы в желто-зеленой части спектра. Таким образом, давая кислород для реакции горения, нитрат бария одновременно служит и пламенной добавкой. [c.56]
Опособ Кариуса состоит в сожжении навески керосяша н его, epit крепкой азотной кислотой в запаянной трубке при нагревании в течение 3. часов до 160°. Несомненно, это лучший способ, но он не-позволяет открывать незначительные количества серы, так как рискованно брать навески больше 0,4—0,5 г. Продукты окисления, ло вскрытии трубки выливаются в воду, прибавляется хлористый или азотнокислый барий, и сера определяется обычным путем-в виде BaS04. [c.207]
Бауман (146) одновременно определяет н e r, я зщр] подобным же при( ром, но сера осаждается в растворе после подкисления азотной кислотой азотнокислым барием. После отфильтро-вывания его азотнокислым Серебром осаждают хлор. Само собой разумеется, что в таком случае бромноватистую щелочь приходится заменять другими окислителями, не содержащими ни серы,. ни галоидов. Эслинг (147) употребляет для этой цели титроваийый раствор соды, избыток которой оттитровывается по оковяании опыта (326),
Кроме щелочного оксндироааиня, известно бесщелочное (кислое) оксидирование. Раствор для кислого оксидирования содержит азотнокислый барий 40—50 г на 1 дм воды и фосфорную кислоту плотности 1,55 в количестве 3—5 г на 1 дм воды. Оксидирование производится при температуре раствора 98—100°С в течение 30 мин. Коррозионная стойкость пленки из кислого раствора и другие ее свойства выше, чем у иленки, полученной при щелочном способе. [c.329]
Чтобы установить формулу хромовокалневых квасцов (лК2504 г/Сг2(804)з-2Н20), был приготовлен 1 л раствора, содержащего 99,8 г исследуемого вещества. При обработке 200 ли этого раствора избытком раствора азотнокислого бария образовалось 18,64 г осадка. При обработке такого же объема (200 мл) раствора квасцов избытком раствора гидроокиси аммония образовалось 4,12 з осадка. Определите формулу исходного вещества. [c.41]
На основании данных о растворимости, о хорошей диссоциации электролитов и об ионном характере процессов следовало бы ожидать, что при сливании растворов, например Ва(ЫОз)2 и Н ЗО , должен образоваться осадок, содержащий только ионы Ва + и 50 —.Междутем оказывается, что в осадке имеется довольно много ионов N0 (в виде азотнокислого бария). Если осаждение проводилось в большом избытке азотной кислоты,содержание азотнокислого бария в осадке может достигать 15″/ от общего веса осадка. Таким образом, азотнокислый барий, который сам по себе достаточно хорошо растворим в воде, оказался захваченным в осадок при образовании сернокислого бария. К сказанному можно еще добавить, что если чистый сернокислый барнй внести в раствор Ва(ЫОз) ,, содержащий азотную кислоту, перехода ионов КО д в осадок не обнаруживается. Для большинства случаев явления соосаждения характерно, что оно наблюдается только во время образования осадка.
БАРИа АЗОТНОКИСЛЫЙ (БАРИЙ НИТРАТ) [c.66]
Карбонаты определяются прибавлением избытка азотнокислого бария к раствору цианида, затем смесь помещают в хорошо закрытую склянку и дают осесть углекислому барию. После этого углекислыя барий отфильтровывается и промывается с принятием возможных предог сторожностей для предохранения от доступа воздуха. Промытый осадок растворяется в определенном количестве титрованной соляной кислоты, и избыток кислоты обратно оттитровывается после предварительной кипячения для удаления углекислоты. [c.37]
Метод определения Щелочного ц и а н а т а основан на свойстве цианата серебра растворяться в разбавленной азотной кислоте, в то время как цианистое и хлористое серебро нерастворимы. Навеску щелочного цианида (около 0,5 г) растворяют в воде tf прибавляют достаточно азотнокислого бария и магния в том случае, если присутствуют карбонаты и едкие Щелочи. После осаждения и отстаивания осадки фильтруются и промываются. К фильтрату прибавляется нейтральный раствор азотнокислого серебра до полного осаждения. Осадку, состоящему из цианистого серебра, хлористого серебра и циановокислого серебра, дают осесть, затем его отфильтровывают и промывают да исчезновения следов серебра в промывных водах. Осадок смывается в стакан и обрабатывается 200 см воды, к которой прибавлено 10 ел 3 разбавленной азотной кислоты (уд. вес 1,2). Стакан ставят на час на кипящую водяную баню, покрывают часовым стеклом и изредка помешивают содержимое. Цианат серебра переходит в раствор, в то время как остальные серебряные соли остаются нерастворенными в осадке. Раствор отфильтровывают от осадка, и количество серебра в фильтрате определяется объемным методом Volhard a. По количеству серебра, определяемому в растворе, может быть высчитано количество цианата. Если не соблюдать точно всех указаний этого метода, могут получиться не совсем правильные результаты вследствие заметной растворимости цианистого серебра в разбавленной азотной кислоте.
Для определения дициандиамида в таких смесях рекомендуется экстракция ацетоном, при чем дициандиамид определяется в экстракте после превращения в гуанилмочевину. В случае применения метода Harger a рекомендуется следующее видоизменение. Растирают 20 г пробы с 50 см3 воды, после чего прибавляют 100 см3 насыщенного раствора азотнокислого бария и затем гидрата окиси бария до щелочной реакции смеси по лакмусу. Доводят объем до 500 см3 и берут 200 см3 для анализа. В присутствии органических веществ, которые образуют желатинообразные осадки с пикриновой кислотой, (например, мука хлопкового семени), следует прибавить раствор уксуснокислого свинца [c.117]
Для определения аммонийных солей можно непосредственно применить отгонку с магнезией или метод аэрации Folin a. Если хотят применить титрование формолом, растворимые фосфаты должны быть удалены следующим образом Отвешивают в стакан на 400 см3 пробу, содержащую не свыше 3 г Р205. Прибавляют 150 см3 насыщенного раствора азотнокислого бария и размешивают в течение 10 минут. Помещают стакан в ледяную ванну и прибавляют из бюретки насыщенный раствор гидрата окиси бар я до тех пор, пока смесь не станет щелочной по лакмусу, и затем прибавляют еще 2 см3 избытка.-Пробуют на полноту осаждения фосфата небольшим количеством раствора азотнокислого бария. Фильтруют и промывают осадок, доводя объем фильтрата и промывочных вод до 500 см3. Помещают 25 см3 приготовленного таким образом раствора в стакан, добавляют одну каплю индикатора метилрот и делают раствор точно кислым прибавлением соляной кислоты. Продолжают анализ, как описано на стр. 115. [c.118]
Путем обработки перекиси бария кислотами выделяют перекись водорода. При этом барий осаждается в виде нерастворимой соли, иапример, сернокислой, фосфорнокислой, углекислой, или же переходит в х н1ристый или азотнокислый барий. [c.151]
Ис5пытание Раствор формальдегида не должен изменяться от прибавления раствора азотнокислого бария, от сероводорода, от раствора азотнокислого серебра (прй последней пробе надо прибаьить иредварительво несколько капель азотной кислоты). [c.52]
Смесь 26 г (0,1 мол.) азотнокислого бария и 800 мл дестиллированной воды нагревают до 70° и после полного растворения соли добавляют 218 г (0,9 мол.) химически чистой азотнокислой меди с 3 мол. кристаллизационной воды. Затем смесь перемешивают при 70 до тех пор, пока не будет получен прозрачный раствор (примечание 2). [c.301]
Другой метод описывает Адкинс . Этот метод заключается в следующем 31 г азотнокислого бария растворяют в 820 лкристаллической азотнокислой меди (3 мол. Н О) и смесь перемешивают и нагревают до полного растворения. Одновременно растворяют 151 г двухромовокислого аммония в 600 мл дестиллированной воды и к раствору добавляют 225 мл 28%-ного водного аммиака. Горячий раствор азотнокислых солей приливают тонкой струей при перемешивании к раствору хромовокислого аммония. Оранжевый осадок отфильтровывают, хорошо отжимают и отсасывают по возможности досуха. Осадок сушат в шкафу при 75—80° в течение 12 час., хорошо измельчают и разделяют на три порции. Каждую порцию разлагают в отдельности в большой фарфоровой кастрюле (диаметр 15 м), нагревая ее на голом пламени. Массу необходимо нагревать настолько, чтобы разложение протекало при возможно более низкой температуре. Во время разложения порошок непрерывно перемешивают стальным шпателем и нагревание регулируют таким образом, чтобы разложение протекало не слишком бурно. Для этого нагревают только одну сторону кастрюли и перемешивание усиливают, как только начнется разложение для того, чтобы распространить его по всей массе. Во время этого процесса окраска порошка меняется от оранжевой до бурой и в конце концов до черной. Когда вся масса станет черной, выделение 1аза прекращается, порошок вынимают из кастрюли и дают ему охладиться. После этого все количество продукта перемешивают 30 мин. с 600 мл 10%-ного раствора уксусной [c.303]
Бассэ п Додэ [131] исследовали возможность синтеза нитратов из смеси кислорода с азотом (1 2) и окислов бария, калия и кальция при 3600 атм и температурах до 900°. Им удалось обнаружить образование небольшого количества нитратов. Так, в течение 2 час. из 0,52 г окислов бария и кальция при 800° было получено соответственно 36 мг азотнокислого бария и 27,5 мг азотнокислого кальция. А. И. Дитщес, Б. А. Корндорф, С. С. Лачинов и С. Л. Лельчук [36] повторили эти опыты (с воздухом). При 2500—3000 атм ими было получено 0,08—0,1% азотнокислого бария из окиси бария. При 1000 атм, даже в течение 6 час. не образовалось аналитически определимого количества азотнокислых солей. [c.80]
Если тр етичный спирт оставить на несколько дней стоять при комнатной температуре с бромом и чистым сероуглеродом без доступа влаги, то он окисляет сероуглерод в серную кислоту за счет выделяющегося кислорода. Для определения серной кислоты ее извлекают из смеси водой и, прибавляя азотнокислый барий, осаждают в виде сернокислого бария [c.37]
Реигольм [29] тщательно исследовал растворы смесей хлористого калия с азотнокислым барием и сернокислой медью и обнаружил указанный эффект для электропроводности очень разбавленных растворов (10-з—Ю- ). Проверить уравнение (5) с помощью данных Ренгольма нельзя из-за неполной диссоциации азотнокислого бария и сернокислой меди. [c.145]
Нри горении смесей азотнокислого бария с горючими пламя окрашивается в зелены11 цвет. [c.31]
chem21.info
Азотнокислый барий — Большая Энциклопедия Нефти и Газа, статья, страница 1
Азотнокислый барий
Cтраница 1
Азотнокислый барий определяется весовым способом в виде сернокислой соли. [1]
Азотнокислый барий кристаллизуется при обычных условиях без воды. Напротив, нитраты Са и Sr выделяются в виде кристаллогидратов. Последние легко растворимы в воде, тогда как растворимость Ba ( N03h [ и Ra ( NO3) 2 ] значительно меньше. Нитрат кальция широко применяется в качестве азотсодержащего минерального удобрения. Нитраты стронция и бария служат в пиротехнике для изготовления составов, сгорающих красным ( Sr) или зеленым ( Ва) пламенем. [2]
Азотнокислый барий препятствует образованию твердых растворов га логенидов серебра или ограиичивает их образование. Разность скачка потенциала увеличивается. [4]
Азотнокислый барий плохо растворим в холодной воде и еще хуже в растворе азотнокислой меди. Поэтому для того, чтобы обе соли перевести в раствор, необходимо смесь нагреть. [5]
Азотнокислый барий применяется в пиротехнике для получения зеленых огней, при производстве некоторых взрывчатых веществ. [6]
Азотнокислый барий 301 Аконитовая кислота 15 Акр и дои 18 Акролеин 64, 65, 67 р — Аланин 20 Аллантоии 23 Аллила. [7]
Азотнокислый барий кристаллизуется из полученного раствора после его выпаривания. [8]
Азотнокислый барий кристаллизуется в виде бесцветных кристаллов кубической сингонии, умеренно растворим в воде. Растворимость азотнокислого бария обладает значительным температурным коэффициентом, в интервале температур 20 — 100 С равным 0 31 г / С. [9]
Азотнокислый барий представляет собой соль [116], растворимость которой в воде сравнительно невелика. Как видим, растворимость нитрата бария возрастает с температурой, но не очень быстро. [11]
Азотнокислый барий кристаллизуется при обычных условиях без воды, а нитраты Са и Sr выделяются в виде кристаллогидратов. Последние легкорастворимы в воде, тогда как растворимость Ba ( NO3) 2 [ и Ra ( NOa) 2 ] значительно меньше. Нитрат кальция широко применяется в качестве азотсодержащего минерального удобрения. Нитраты стронция и бария служат в пиротехнике для изготовления составов, сгорающих красным ( Sr) или зеленым ( Ва) пламенем. [12]
Азотнокислый барий кристаллизуется при обычных условиях без воды, а нитраты Са и Sr выделяются в виде кристаллогидратов. Последние легкорастворимы в воде, тогда как растворимость Ba ( NO3) 2 [ и Ra ( NO3) 2 ] значительно меньше. Нитрат кальция широко применяется в качестве азотсодержащего минерального удобрения. Нитраты стронция и бария служат в пиротехнике для изготовления составов, сгорающих красным ( Sr) или зеленым ( Ва) пламенем. [13]
Азотнокислый барий кристаллизуется при обычных условиях без воды. Напротив, нитраты Са и Sr выделяются в виде кристаллогидратов. Последние легкорастворимы в воде, тогда как растворимость Ba ( NO3) 2 [ и Ra ( NO3b ] значительно меньше. Нитрат кальция широко применяется в качестве азотсодержащего минерального удобрения. Нитраты стронция и бария служат в пиротехнике для изготовления составов, сгорающих красным ( Sr) или зеленым ( Ва) пламенем. [14]
Азотнокислый барий служит окислителем во многих пиротехнических, особенно осветительных составах. Составы с азотнокислым барием значительно менее чувствительны, чем с окислителями, указанными выше. В некоторых случаях азотнокислый барий применяется в составах в смеси с другими, более активно действующими окислителями. [15]
Страницы: 1 2 3 4
www.ngpedia.ru
Формула нитрата бария в химии
Определение и формула нитрата бария
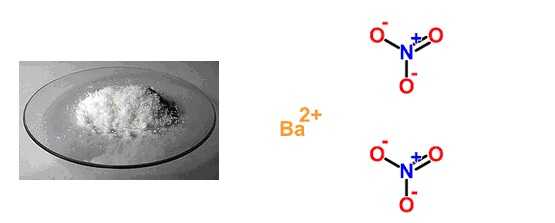
Химическая формула –
Молярная масса равна г/моль.
Физические свойства – твёрдое кристаллическое вещество белого цвета, умеренно растворимое в воде (9,2 г/100 мл при ), температура плавления равна , начинает разлагаться при плавлении, плотность кристаллической соли равна 3,24 г/см.
Химические свойства нитрата бария
Получение
В промышленности нитрат бария получают по реакции:
Лабораторным способом получения данной соли является:
Качественная реакция
Качественной реакцией на ионы бария является образование жёлтого кристаллического осадка хромата бария при добавлении к раствору хромата калия:
Применение
применяется для получения и , используется как компонент эмалей и глазурей, также находит применение в пиротехнике для окрашивания пламени в зелёный цвет.
Примеры решения задач
| Понравился сайт? Расскажи друзьям! | |||
ru.solverbook.com
ГОСТ 3777-76 Реактивы. Барий азотнокислый. Технические условия (с Изменениями N 1, 2), ГОСТ от 15 ноября 1976 года №3777-76
ГОСТ 3777-76
Группа Л51
ОКП 26 2124 0020 10
Дата введения 1977-07-01
1. РАЗРАБОТАН И ВНЕСЕН Министерством химической промышленности
РАЗРАБОТЧИКИ
В.П.Чуб, Л.К.Хайдукова, Л.М.Гартюк, Т.М.Андреева, Г.В.Грязнов, В.Г.Брудзь, И.Л.Ротенберг, З.М.Ривина, Э.П.Кравчук, И.Г.Столярова
2. УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Постановлением Государственного комитета стандартов Совета Министров СССР от 15.11.76 N 2566
3. Срок проверки — 1996 г. Периодичность проверки — 5 лет
4. ВЗАМЕН ГОСТ 3777-69
5. ССЫЛОЧНЫЕ НОРМАТИВНО-ТЕХНИЧЕСКИЕ ДОКУМЕНТЫ
6. Ограничение срока действия снято Постановлением Госстандарта СССР от 09.08.91 N 1336
7. ПЕРЕИЗДАНИЕ (июнь 1998 г.) с Изменениями N 1, 2, утвержденными в октябре 1986 г., августе 1991 г. (ИУС 1-87, 11-91)
Настоящий стандарт распространяется на азотнокислый барий, представляющий собой бесцветные кристаллы, растворимые в воде. Азотнокислый барий немного гигроскопичен.
Формула: Ва(NО).
Относительная молекулярная масса (по международным атомным массам 1985 г.) — 261,34.
Требования настоящего стандарта являются обязательными.
(Измененная редакция, Изм. N 1, 2).
1. ТЕХНИЧЕСКИЕ ТРЕБОВАНИЯ
1.1а. Азотнокислый барий должен быть изготовлен в соответствии с требованиями настоящего стандарта по технологическому регламенту, утвержденному в установленном порядке.
(Введен дополнительно, Изм. N 1).
1.1. По физико-химическим показателям азотнокислый барий должен соответствовать нормам, указанным в таблице.
Наименование показателя | Норма | ||
Химически чистый (х.ч.) | Чистый для анализа | Чистый (ч.) | |
1. Массовая доля азотнокислого бария, Ва(NО), %, не менее | 99,5 | 99,5 | 99,5 |
2. Массовая доля нерастворимых в воде веществ, %, не более | 0,005 | 0,01 | 0,02 |
3. Массовая доля хлоридов (Сl), %, не более | 0,0003 | 0,0005 | 0,002 |
4. Массовая доля железа (Fe), %, не более | 0,0002 | 0,0002 | 0,001 |
5. Массовая доля калия и натрия (K+Na), %, не более | 0,01 | 0,025 | 0,075 |
6. Массовая доля кальция и стронция (Са+Sr), %, не более | 0,05 | 0,1 | 0,2 |
7. Массовая доля тяжелых металлов (Рb), %, не более | 0,0005 | 0,0005 | 0,002 |
8. рН раствора препарата с массовой долей 5% | 5,0-7,0 | 5,0-7,0 | Не нормируется |
(Измененная редакция, Изм. N 1, 2).
2а. ТРЕБОВАНИЯ БЕЗОПАСНОСТИ
2а.1. Азотнокислый барий по степени воздействия на организм человека относится к веществам 2-го класса опасности по ГОСТ 12.1.005. Предельно допустимая концентрация продукта в воздухе рабочей зоны производственных помещений составляет 0,5 мг/м.
(Измененная редакция, Изм. N 2).
2а.2. При работе с препаратом следует применять индивидуальные средства защиты.
2а.3. Техническое оборудование, в котором перерабатывается и хранится азотнокислый барий, должно быть максимально герметизировано.
2а.4. Азотнокислый барий в смеси с горючими веществами легко воспламеняется. При загорании — тушить большим количеством воды.
Разд.2а. (Введен дополнительно, Изм. N 1).
2. ПРАВИЛА ПРИЕМКИ
2.1. Правила приемки — по ГОСТ 3885.
3. МЕТОДЫ АНАЛИЗА
3.1а. Общие указания по проведению анализа — по ГОСТ 27025.
При взвешивании применяют лабораторные весы общего назначения типов ВЛР-200 г и ВЛКТ-500 г-М или ВЛЭ-200 г.
Допускается применение других средств измерения с метрологическими характеристиками и оборудования с техническими характеристиками не хуже, а также реактивов по качеству не ниже указанных в настоящем стандарте.
(Измененная редакция, Изм. N 1, 2).
3.1. Пробы отбирают по ГОСТ 3885. Масса средней пробы должна быть не менее 135 г.
(Измененная редакция, Изм. N 2).
3.2. Определение массовой доли азотнокислого бария
Определение проводят по ГОСТ 10398 комплексонометрическим методом. При этом около 0,4000 г препарата помещают в коническую колбу вместимостью 250 см и растворяют в 100 см воды. К полученному раствору при перемешивании прибавляют из бюретки 20 см раствора трилона Б концентрации (ди-Nа-ЭДТА)=0,05 моль/дм (0,05 М), 6 см раствора гидроокиси натрия (до рН 12,2-12,3).
Масса азотнокислого бария, соответствующая 1 см раствора трилона Б концентрации точно (ди-Nа-ЭДТА)=0,05 моль/дм, — 0,01307 г.
За результат анализа принимают среднее арифметическое результатов двух параллельных определений, абсолютное расхождение между которыми не превышает допускаемое расхождение, равное 0,2%.
Допускаемая абсолютная суммарная погрешность результата анализа ±0,5% при доверительной вероятности =0,95.
(Измененная редакция, Изм. N 1,
2).
3.2.1, 3.2.2. (Исключены, Изм. N 1).
3.3. Определение массовой доли нерастворимых в воде веществ
(Измененная редакция, Изм. N 1).
3.3.1. Реактивы и аппаратура
Вода дистиллированная по ГОСТ 6709.
Стакан В(Н)-1 — 600 ТХС по ГОСТ 25336.
Тигель фильтрующий ТФ ПОР10 или ТФ ПОР16 по ГОСТ 25336.
Цилиндр 1(3) — 100 и 1 — 500 по ГОСТ 1770.
(Измененная редакция, Изм. N 1, 2).
3.3.2. Проведение анализа
20,00 г препарата помещают в стакан и растворяют при нагревании в 400 см дистиллированной воды. Стакан накрывают часовым стеклом и выдерживают на водяной бане в течение 1 ч, затем раствор фильтруют через фильтрующий тигель, предварительно высушенный до постоянной массы и взвешенный (результат взвешивания в граммах записывают с точностью до четвертого десятичного знака). Остаток на фильтре промывают 100 см горячей дистиллированной воды и сушат в сушильном шкафу при 105-110 °С до постоянной массы.
Препарат считают соответствующим требованиям настоящего стандарта, если масса остатка после высушивания не будет превышать:
для препарата химически чистый — 1 мг,
для препарата чистый для анализа — 2 мг,
для препарата чистый — 4 мг.
Допускаемая относительная суммарная погрешность результата анализа ±30% для препарата химически чистый и ±20% — для препарата чистый для анализа и чистый при доверительной вероятности =0,95.
(Измененная редакция, Изм. N 2).
3.4. Определение массовой доли хлоридов
(Измененная редакция, Изм. N 1).
3.4.1. Определение проводят по ГОСТ 10671.7. При этом 3,30 г препарата химически чистый или 2,00 г препарата чистый для анализа и чистый помещают в коническую колбу вместимостью 100 см, прибавляют 20 см воды и растворяют при нагревании на электроплитке. Затем колбу снимают с электроплитки, в горячий раствор осторожно, при перемешивании, прибавляют 4 см раствора азотной кислоты с массовой долей 25%. После охлаждения раствор с выпавшим осадком фильтруют через обеззоленный фильтр «синяя лента», промытый горячим раствором азотной кислоты с массовой долей 1%, в мерную колбу вместимостью 25 см и далее определение проводят фототурбидиметрическим методом (способ 1), не прибавляя раствора азотной кислоты.
Измерение оптической плотности анализируемого раствора проводят по отношению к контрольному раствору, содержащему 4 см раствора азотной кислоты с массовой долей 25%.
Препарат считают соответствующим требованиям настоящего стандарта, если масса хлоридов не будет превышать:
для препарата химически чистый — 0,010 мг,
для препарата чистый для анализа — 0,010 мг,
для препарата чистый — 0,040 мг.
Допускается для препарата чистый для анализа и чистый проводить определение по ГОСТ 10671.7 визуально-нефелометрическим методом (способ 2). При этом 2,00 г препарата помещают в коническую колбу вместимостью 100 см, растворяют в 37 см воды и далее определение проводят по ГОСТ 10671.7.
При разногласиях в оценке массовой доли хлоридов в препарате чистый для анализа и чистый анализ проводят фототурбидиметрическим методом.
(Измененная редакция, Изм. N 2)
.
3.5. Определение массовой доли железа
(Измененная редакция, Изм. N 1).
3.5.1. Определение проводят по ГОСТ 10555 роданидным методом с предварительным окислением железа азотной кислотой. При этом 1,00 г препарата помещают в мерную колбу вместимостью 50 см, растворяют в 20 см воды и далее определение проводят по ГОСТ 10555.
Препарат считают соответствующим требованиям настоящего стандарта, если масса железа не будет превышать:
для препарата химически чистый — 0,002 мг,
для препарата чистый для анализа — 0,002 мг,
для препарата чистый — 0,010 мг.
Допускается заканчивать определение визуально в объеме 25 см.
При разногласиях в оценке массовой доли железа анализ заканчивают фотометрически.
3.6. Определение массовой доли калия, натрия, кальция и стронция проводят по ГОСТ 26726 пламенно-фотометрическим методом. При этом для препарата чистый для анализа готовят растворы сравнения с массовой долей натрия и калия 0,05% и кальция и стронция 0,1%.
За результат анализа принимают среднее арифметическое результатов двух параллельных определений, относительное расхождение между которыми не превышает допускаемое расхождение, равное 20%.
Допускаемая относительная суммарная погрешность результата анализа ±10% при доверительной вероятности =0,95.
3.5.1, 3.6. (Измененная редакция, Изм. N 1, 2).
3.7. Определение массовой доли тяжелых металлов
(Измененная редакция, Изм. N 1).
3.7.1. Определение проводят по ГОСТ 17319 сероводородным методом. При этом 2,00 г препарата помещают в коническую колбу вместимостью 100 см с пришлифованной или резиновой пробкой и растворяют при нагревании в 30 см воды. Раствор охлаждают до комнатной температуры и далее определение проводят по ГОСТ 17319.
Препарат считают соответствующим требованиям настоящего стандарта, если наблюдаемая окраска анализируемого раствора не будет интенсивнее окраски раствора, приготовленного одновременно с анализируемым и содержащего в таком же объеме:
для препарата химически чистый — 0,01 мг Рb,
для препарата чистый для анализа — 0,01 мг Рb,
для препарата чистый — 0,04 мг Рb,
1 см уксусной кислоты, 1 см раствора уксуснокислого аммония, 10 см сероводородной воды.
3.8. Определение рН раствора препарата с массовой долей 5%
5,00 г препарата помещают в коническую колбу вместимостью 250 см (ГОСТ 25336), растворяют в 95 см дистиллированной воды, не содержащей углекислоты, приготовленной по ГОСТ 4517, и измеряют рН раствора на универсальном иономере ЭВ-74 или другом приборе с пределом допускаемой основной погрешности ±0,05 рН.
За результат анализа принимают среднее арифметическое результатов двух параллельных определений, абсолютное расхождение между которыми не превышает допускаемое расхождение, равное 0,1 рН.
Допускаемая абсолютная суммарная погрешность результата анализа ±0,1 рН при доверительной вероятности =0,95.
3.7.1, 3.8. (Измененная редакция, Изм. N 1, 2).
4. УПАКОВКА, МАРКИРОВКА, ТРАНСПОРТИРОВАНИЕ И ХРАНЕНИЕ
4.1. Препарат упаковывают и маркируют в соответствии с ГОСТ 3885.
Вид и тип тары: 2-1, 2-4, 11-1, 11-6.
Группа фасовки: IV, V, VI, VII.
На тару наносят знак опасности по ГОСТ 19433 (класс 5, подкласс 5.1, черт.5 и 6а, классификационный шифр — 5122), серийный номер ООН — 1446.
4.2. Препарат транспортируют в сухих чистых крытых железнодорожных вагонах, в закрытых палубных судах, а также автогужевым транспортом в соответствии с правилами перевозки грузов, действующими на данном виде транспорта.
4.3. Препарат хранят в закрытой таре в крытых складских помещениях.
Не допускается хранение препарата совместно с легковоспламеняющимися и горючими материалами.
5. ГАРАНТИИ ИЗГОТОВИТЕЛЯ
5.1. Изготовитель гарантирует соответствие поставляемого реактива требованиям настоящего стандарта при соблюдении условий хранения и транспортирования.
5.2. Гарантийный срок хранения препарата — три года со дня изготовления.
5.1, 5.2. (Измененная редакция, Изм. N 1).
Разд.6. (Исключен, Изм. N 1).
Электронный текст документа
подготовлен ЗАО «Кодекс» и сверен по:
официальное издание
М.: ИПК Издательство стандартов, 1998
docs.cntd.ru
Барий азотнокислый растворимость в вод
Сульфат бария значительно более растворим в кислой среде, чем в воде. Например, растворимость в 1 F растворе хлористоводородной кислоты приблизительно в 30 раз больше, чем в воде. Такое поведение аналогично описанному выше поведен-ию сульфата свинца в азотнокислом растворе. Таким образом, присутствие кислоты увеличивает растворимость сульфата бария, поскольку сульфат-ион взаимодействует с протоном. Образуя гидросульфат-анион. Если мы хотим определить сульфат-ион, добавляя ион бария к -кислому раствору пробы, то в растворе будет происходить конкуренция между Н+ я Ва + за присоединение сульфат-иона, и хотя осадок сульфата бария будет выпадать [c.243]Растворимость азотнокислого бария в пределах от О до 100° С увеличилась почти в семь раз, растворимость хлористого натрия увеличилась только на 10%, а растворимость углекислого лития уменьшилась примерно в два раза. [c.215]
Сколько выделится азотнокислого бария из раствора, насыщенного при 100 и охлажденного до 0°, если во взятом растворе было 50 мл воды. Растворимость азотнокислого бария при 0° равна 5 г, а при 100°—34,2 г. [c.359]
Азотнокислый барий кристаллизуется при обычных условиях без воды. Напротив, нитраты Са и 5г выделяются в виде кристаллогидратов. Последние легкорастворимы в воде, тогда как растворимость Ba(NOз)2 [и Ра (N03)2] значительно меньше. Нитрат кальция широко применяется в качестве азотсодержащего минерального удобрения. Нитраты стронция и бария служат в пиротехнике для изготовления составов, сгорающих красным (Зг) или зеленым (Ва) пламенем. [c.388]
Перйодат натрия, приготовленный из 100 г иода (около 225 г), суспендируют в 1 л кипящей воды, содержащей 10 мл концентрированной азотной кислоты (для увеличения растворимости перйодата). Небольшой избыток (против рассчитанного по уравнению) нитрата бария (325 г) растворяют в горячей воде раствор кипятят 1,5—2 часа при энергичном перемешивании. Затем раствор нейтрализуют гидроокисью бария и оставляют охлаждаться. Выкристаллизовавшийся перйодат бария промывают несколько раз декантацией горячей водой (каждый раз перемешивая кристаллы) и затем промывают на воронке Бюхнера. Если соль окрашивает пламя горелки в желтый цвет, ее снова кипятят с раствором азотнокислого бария в присутствии азотной кислоты, как было указано выше. [c.165]
Смешение с углекислым барием , а также неполное удаление растворимых в воде солей (хлористой и азотнокислой) и углекислого бария служило причиной смертельных отравлений. [c.120]
По правилу соосаждения, сформулированному К. Фаянсом, чем меньще растворимость соединения, образуемого радиоактивным элементом с противоположно заряженным ионом осадка, тем большее количество этого элемента захватывается осадком [1]. Так, например, изотопы висмута интенсивно захватываются осадками карбоната бария и гидроокиси железа, но не захватываются из кислых растворов осадками сульфатов бария и свинца. Изотопы свинца, количественно выделяющиеся с карбонатами и сульфатами ряда элементов, не полностью соосаждаются с галогенидами серебра и практически не соосаждаются с труднорастворимым азотнокислым нитроном. [c.94]
Вследствие небольшого периода полураспада лантана-140 (40 час) для разделения можно использовать только такие методы, которые не требуют значительной затраты времени [42—44]. Разделение при помощи ионообменников описано в раб. 23.1 [45—47]. При использовании лантана-140 для исследований с мечеными атомами целесообразно выделять радиоактивный лантан-140 тут же в лаборатории из препарата Ba /La . Активный лантан-140 накапливается в течение нескольких дней (равновесие устанавливается примерно через 20 дней) и может быть выделен в случае надобности [48]. В этом методе для отделения бария используют малую растворимость азотнокислого бария в дымящей азотной кислоте. Выделенный азотнокислый барий сохраняют для дальнейших разделений. [c.242]
Таким образом, к I группе, группе азотнокислого серебра, относятся кислоты общей формулы НХ. Ко И группе, группе нитрата бария, относятся кислоты общей формулы НгХ. К Н1 группе, группе молибденовой жидкости, относятся кислоты общей формулы НзХ. К IV группе (соли растворимы в уксусной кислоте) относятся кислоты общей формулы Н4Х — ортокислоты и Н2Х — [c.28]
Хлорат бария и азотнокислые соли стронция и свинца должны быть полностью растворимы в воде. После осаждения металлов при помощи серной кислоты растворы при выпаривании не должны давать никакого остатка. Хлорат бария в смеси с горючими веществами должен давать при нагревании сильную вспышку с зеленым пламенем. Раствор азотнокислого свинца не должен синеть от аммиака и не должен краснеть от роданистого калия. [c.719]
Впервые в 1913 г. Фаянс и Бер [Ч на основании многочисленных наблюдений установили следующее правило осаждения Радиоэлемент выпадает из крайне разведенных растворов с осадками, если последние осаждаются в условиях, при которых соответствующий радиоэлемент, присутствуя в весомых количествах, образовал бы трудно растворимую соль. Затем Фаянс и Рихтер [ ] показали, что ThB практически полностью выпадает из растворов с сернистым висмутом, углекислым марганцем и сернокислым барием, а с иодистым и хлористым серебром только частично. Вместе с тем известно, что сернистый, углекислый и сернокислый свинец — трудно растворимые соединения, азотнокислый свинец — легко растворим, а растворимость хлористого и иодистого свинца занимает промежуточное положение. Отсюда они сделали вывод о существовании ясно выраженного параллелизма между способностью радиоактивных изотопов осаждаться с различными осадками и растворимостью соединений радиоактивных изотопов с вызывающими осаждение кислотными остатками (анионами). [c.424]
Щелочноземельные металлы и их соединения. Стронций и барий, являясь нервными и мышечными ядами, обладают значительной общей токсичностью. Окиси и гидроокиси щелочноземельных металлов оказывают сильное прижигающее действие на кожу и слизистые оболочки. Соли этих металлов вызывают кожные заболевания. Соединения бария вызывают воспалительные заболевания головного мозга и мягкой его оболочки, смерть обычно наступает от паралича сердца. Ядовитость солей бария весьма зависит от их растворимости. Практически нерастворимый барий сернокислый (чистый) не ядовит, растворимые же соли хлористый, азотнокислый, уксуснокислый барий и другие — сильно токсичны. Так, 0,2—0,5 г хлористого бария вызывают отравление, смертельная доза — 0,8—0,9 г. Токсическое действие солей стронция в общем сходно с действием солей бария. Окись кальция в виде пыли раздражает слизистые оболочки, а при попадании на кожу вызывает тяжелые ожоги. Особенно опасно попадание ее в глаза. Окись стронция действует аналогично окиси кальция, но значительно сильнее. [c.95]
Налейте в пробирку раствор сернокислого алюминия Л12(804)з и добавьте раствор азотнокислого бария. Напишите уравнение реакции. Определите с помощью таблицы растворимости солей в воде, какое из полученных веществ выпало в осадок. [c.98]
Очистка азотнокислого бария. Для очистки веществ используют процесс перекристаллизации, основанный на изменении их растворимости с температурой. Если при повышенной температуре приготовить насыщенный раствор вещества, загрязненный примесями, и затем этот раствор охладить, то значительная часть основного вещества выпадает в осадок (если растворимость этого вещества уменьшается при понижении температуры). Хорошо растворимые примеси останутся при этом в растворе, так как по отношению к ним даже при низкой температуре раствор будет ненасыщенным. Понятно, что этим способом можно очищать только те вещества, у которых растворимость сильно меняется с температурой. [c.178]
И бария изменяются с температурой сравнительно мало. В то же время значение этой величины для тетраборнокислого натрия заметно возрастает. Порядок процесса образования новой фазы с увеличением температуры возрастает для всех исследованных нами солей. Для интерпретации полученных данных воспользуемся значениями растворимостей солей (табл. 2). Растворимости азотнокислого лития и тетраборнокислого натрия рассчитаны на соответствующие кристаллогидраты. Для безводных солей справед.пиво, как мы видим, утверждение о том, что с ростом растворимости величина предельного пересыщения уменьшается. Кристаллизация кристаллогидратов подчиняется той же закономерности, если сравнивать их между собой. Но в общем они более склонны к образованию пересыщенных растворов, чем безводные соли. [c.54]
Для приготовления ванны оксидирования сначала растворяют в воде азотнокислые соли. Азотнокислый кальций и препарат мажеф растворяют при комнатной температуре. Азотнокислый кальций обычно готовят в цехе растворением извести в азотной кислоте. Азотнокислый барий добавляют в горячую воду при интенсивном перемешивании. Перекись марганца, или как ее называют пиролюзит, мало растворима и при работе ванны взмучивается. Во избежание взмучивания порошок пиролюзита насыпают в мешочки из хлопчатобумажной ткани, которые укладывают на дно ванны. [c.13]
Растворимость азотнокислого бария в 100 см воды при 0° — [c.47]
Метод основан на обменной реакции между трех-замещенным кислым иоднокислым барием и азотной кислотой, которая протекает благодаря плохой растворимости азотнокислого бария в концентрированной азотной кислоте. [c.181]
Распределение по логарифмическому закону наблюдается еще такн е при осанадении из гомогенного раствора. Метод основан на том принципе, что осаждающий реагент ностепенно образуется во всем объеме раствора за счет гидролиза соответствующего соединения. Раствор становится слегка пересыщенным, что влечет за собой выделение твердой фазы. Это было показано в работе Салутского с сотрудниками на примере фракционного осанодения хромата бария—радия. Растворимость хроматов, как известно, уменьшается с уменьшением концентрации кислоты в растворе. Гомогенное осаждение в этой системе достигалось постепенной нейтрализацией азотнокислого раствора хромата бария аммиаком, образующимся при самопроизвольном гидролизе мочевины или цианата калия. Рассчитанные из экспериментальных данных значения ) и X приведены в табл. 64. [c.223]
На основании данных о растворимости, о хорошей диссоциации электролитов и об ионном характере процессов следовало бы ожидать, что при сливании растворов, например Ва(ЫОз)2 и Н ЗО , должен образоваться осадок, содержащий только ионы Ва + и 50 —.Междутем оказывается, что в осадке имеется довольно много ионов N0 (в виде азотнокислого бария). Если осаждение проводилось в большом избытке азотной кислоты,содержание азотнокислого бария в осадке может достигать 15″/ от общего веса осадка. Таким образом, азотнокислый барий, который сам по себе достаточно хорошо растворим в воде, оказался захваченным в осадок при образовании сернокислого бария. К сказанному можно еще добавить, что если чистый сернокислый барнй внести в раствор Ва(ЫОз) ,, содержащий азотную кислоту, перехода ионов КО д в осадок не обнаруживается. Для большинства случаев явления соосаждения характерно, что оно наблюдается только во время образования осадка. [c.57]
Метод определения Щелочного ц и а н а т а основан на свойстве цианата серебра растворяться в разбавленной азотной кислоте, в то время как цианистое и хлористое серебро нерастворимы. Навеску щелочного цианида (около 0,5 г) растворяют в воде tf прибавляют достаточно азотнокислого бария и магния в том случае, если присутствуют карбонаты и едкие Щелочи. После осаждения и отстаивания осадки фильтруются и промываются. К фильтрату прибавляется нейтральный раствор азотнокислого серебра до полного осаждения. Осадку, состоящему из цианистого серебра, хлористого серебра и циановокислого серебра, дают осесть, затем его отфильтровывают и промывают да исчезновения следов серебра в промывных водах. Осадок смывается в стакан и обрабатывается 200 см воды, к которой прибавлено 10 ел 3 разбавленной азотной кислоты (уд. вес 1,2). Стакан ставят на час на кипящую водяную баню, покрывают часовым стеклом и изредка помешивают содержимое. Цианат серебра переходит в раствор, в то время как остальные серебряные соли остаются нерастворенными в осадке. Раствор отфильтровывают от осадка, и количество серебра в фильтрате определяется объемным методом Volhard a. По количеству серебра, определяемому в растворе, может быть высчитано количество цианата. Если не соблюдать точно всех указаний этого метода, могут получиться не совсем правильные результаты вследствие заметной растворимости цианистого серебра в разбавленной азотной кислоте. [c.37]
Для определения аммонийных солей можно непосредственно применить отгонку с магнезией или метод аэрации Folin a. Если хотят применить титрование формолом, растворимые фосфаты должны быть удалены следующим образом Отвешивают в стакан на 400 см3 пробу, содержащую не свыше 3 г Р205. Прибавляют 150 см3 насыщенного раствора азотнокислого бария и размешивают в течение 10 минут. Помещают стакан в ледяную ванну и прибавляют из бюретки насыщенный раствор гидрата окиси бар я до тех пор, пока смесь не станет щелочной по лакмусу, и затем прибавляют еще 2 см3 избытка.-Пробуют на полноту осаждения фосфата небольшим количеством раствора азотнокислого бария. Фильтруют и промывают осадок, доводя объем фильтрата и промывочных вод до 500 см3. Помещают 25 см3 приготовленного таким образом раствора в стакан, добавляют одну каплю индикатора метилрот и делают раствор точно кислым прибавлением соляной кислоты. Продолжают анализ, как описано на стр. 115. [c.118]
Бергстром [498] получил 2-аминохинолин с выходом порядка 80% при взаимодействии хинолина с амидом бария в жидком аммиаке при комнатной температуре. Реакция в заметной степени катализируется растворимыми бариевыми солями. Бергстром обнаружил также, что при действии на хинолин амида калия в жидком аммиаке в присутствии азотнокислого калия или [c.113]
Даже в тех случаях, когда осложнения, связанные с ассоциацией ионов, сведены к минимуму, как, например, в очень разбавленных водных растворах, коэффициенты активности обнаруживают весьма специфические особенности при некоторых комбинациях электролитов со сложным типом валентности. Это явление было впервые исследовано Бренстедом и Петерсеном [14] и позднее Ла-Мером [15]. На рис. 119 показаны результаты, полученные Ла-Мером и Мэзоном путем определения растворимости 1,3-валентной соли (лютеодинитродиаммино-оксало-кобальтиата) вводных растворах различных солей при 25°. Как видно из рисунка, в случае азотнокислого калия и хлористого бария получаются кривые, которые [c.419]
Панет совместно с Горовицем [ ] в результате изучения адсорбции радиоактивных изотопов различными осадками установили правило адсорбции, аналогичное правилу осаждения Те радиоэлементы хорошо адсорбируются, соединения которых с электроотрицательной составной частью (кислотным остатком) адсорбирующего твердого тела трудно растворимы в соответствующем растворителе . Таким образом, правило адсорбции оказалось аналогичным правилу осаждения Фаянса и Вера, но в правиле осаждения не решался вопрос о том, где должен находиться электроотрицательный остаток, дающий с радиоактивным изотопом труднорастворимое соединение, в растворе или в осадке. По правилу же адсорбции Панета решающим фактором является в первую очередь состав адсорбирующего осадка, а не раствора. Достоверность этого представления подтверждается, например, тем, что в растворе, содержащим сернокислый аммоний, ThB (изотоп свинца) не осаждается с осадком азотнокислого нитрона. Следовательно, для процесса адсорбции недостаточно, чтобы ион SO4 содержался в растворе, а необходимо, чтобы он, как например в случае сернокислого бария, находился в осадке. [c.425]
К азотнокислому раствору урана добавляется серная кислота, в результате чего в осадок выпадают сернокислые соли свинца, бария и радия, а уран в виде нитрата уранила U02(N0з)2 остается в растворе. При прибавлении к раствору соды уран переходит в растворимый карбонатный комплекс с шестивалентным ураном Na4[U02 0з]2, а в осадок переходят такие элементы, как железо, алюминий, хром, цинк и другие металлы, в виде нерастворимых Карбонатов, гидроокисей и основных карбонатов. Прибавлением вновь азотной кислоты получают раствор нитрата уранила, содержащий очень небольшое количество примеси. Для окончательного отделения примесей производят экстракцию нитрата уранила эфиром, при этом верхний слой представляет собой эфирный раствор нитрата уранила, а нижний более тяжелый водный раствор, содержащий примеси, который спускается из колонны. Эфирный раствор нитрата уранила разделяется промывкой водой на эфир, возвращаемый снова в цикл, и чистый раствор нитрата уранила, С помощью перекиси водорода из раствора осаж- [c.421]
Металлический рутений не растворяется в кислотах и царской водке, не реагирует с КН504. При сплавлении с едкими щелочами и окислителями рутений превращается в растворимый в воде рутенат, МегКи04. Для сплавления применяют следующие смеси щелочь и селитра или хлорат натрия, углекислый калий и селитра, перекись бария и азотнокислый барий. При нагревании рутения с перекисью натрия образуется зеленый перрутенат натрия Ма1 и04, растворимый в воде. Рутений растворяется в растворах щелочных гипохлоритов с образованием летучей Ри04. С гипохлоритом натрия реакция происходит энергичней, чем с гипохлоритом калия. Подобно родию и иридию, рутений может быть переведен в раствор после хлорирования в смеси с хлористым натрием при нагревании. [c.11]
Сернокислый барий не растворяется ни в соляной кислоте, ни в воде этим его свойством пользуются для количественного определения бария, действуя на растворимые соли его (хлористые или азотнокислые) серной кислотой, и определяют его в виде Ва304. [c.49]
Из этого анализа видно, что в отходах производства сернистого бария содержится значительное количество растворимых в кислотах солей бария (BaSiOs, ВаСОз и BaS), вследствие чего этот отбросный продукт может быть использован для получения хлористого и азотнокислого бария. [c.209]
Этот случай был изучен 1 ] на системе Ка(МОз)2— РЬ(КОз)2—Н2О при 25° в присутствии и в отсутствие НаСзНзОа иНСаНдОг, которые образуют со свинцом стойкие мало диссоциирующие основные соли и таким путем понижают его активность. Радий же, подобно барию, образует в этих условиях неустойчивые комплексы или малодиссоциирующие основные соли. Поэтому прибавление уксуснокислых солей должно оказать влияние как на К, так и на в сторону повышения их значения, причем значение В должно больше возрастать, чем К, так как в присутствии уксуснокислых солей повышается растворимость азотнокислого свинца. В табл. 71 приводятся полз енные данные, связанные с комплексообразованием макрокомпонента. [c.231]
Используя далее табл. 2 растворимости солей и оснований в воде (см. приложение 1) и имея в виду, чтр исходные соли должны быть растворимы в воде, что одна из получаемых солей (BaS04) должна выпадать в виде осадка и что вторая исходная соль должна быть растворимой солью бария, придти к выводу, что для реакции можно взять хлористый барий ВаСЬ или азотнокислый барий Ba(N03)2 [c.37]
На практике также выявлено, что химические добавки при известных концентрациях ускоряют схватывание и твердение бетона, а взятые в других количествах, наоборот, замедляют, и их воздействие зависит и от сорта применяемого цемента. Отсюда следует, что объяснение причин ускорения бетона не является простым делом. Поэтому наиболее точными показателями влияния этих добавок до сих пор считают только практические технологические испытания, проведенные в условиях, полностью отвечающих строительной практике и данным реальной внешней среды. Все же в общих чертах можно сказать, что схватывание и твердение портландцемента и шлакопортландцемента практически можно ускорять всеми солями щелочных металлов, металлов щелочных земель и многовалентных металлов. Большое значение имеют и анионы (ионы с отрицательным зарядом) этих солей. Известно, например, что азотнокислые соли (нитраты) меют только малое влияние, в то время как хлориды, гидроокиси и растворимые углекислые соли являются очень действенными. Подобно солям этих веществ ведут себя и некоторые кислоты, например соляная и угольная [89]. Поэтому к активным ускорителям схватывания и твердения бетона можем отнести следующие вещества хлориды натрия, кальция, магния, бария, цинка, алюминия, железа, а затем углекислый натрий, гидрат окиси натрия, кремнекислый натрий, сульфаты натрия, кальция, цинка, алюминия и т. п. Однако в этих случаях всегда необходимо устанавливать, и подходящую концентрацию таких веществ. Одновременно нужно следить за тем, чтобы примененное к мичество выбранной добавки не ухудшало других по- [c.10]
При этом предполагается, что во всех случаях исходным раствором является азотнокислый раствор, в котором уран присутствует в виде UO2 (N03)2 плутоний — в виде смеси четырех-и шестивалентных солей церий — в виде смеси трех- и четырехвалентных соединений цезий, стронций, барий, все редкоземельные элементы, иттрий, родий — в виде нитратов цирконий — в виде нитрата циркония ниобий — в виде нитрата или взвеси пятиокиси ниобия рутений в виде растворимого нитрозонц-7Q [c.76]
Карбонаты, сульфаты, сульфиты, фториды и фосфаты кальция, стронция и б шя отличаются весьма малой растворимостью. В отличие от них нитраты и хлориды растворимы в воде. Нитрат кальцня раствории, кроме того, в крепкой азотной кислоте, смеси равных объемов абсолютного спирта и эфира /4/ и в ацетдае. Азотнокислые соли бария и стронция при этом практически нерастворимы. На этом свойстве основан птан из наиболее часто применяемых методов отделения кальция от бария и стронция /4- /. Гидроокиси этих элементов растворимы в воде и их растворы имеют щелочную реакцию. [c.7]
chem21.info
Азотнокислый барий — Большая Энциклопедия Нефти и Газа, статья, страница 2
Азотнокислый барий
Cтраница 2
Азотнокислый барий плохо растворим в холодной воде и еще хуже в растворе азотнокислой меди. Поэтому для того, чтобы обе соли перевести в раствор, необходимо смесь нагреть. [16]
Азотнокислый барий, мелко растертый, по извлечении 95 / 0-ым спиртом не должен показывать красноватого окрашивания пламени ( см. также стр. [17]
Азотнокислый барий Ва ( МО3Ь служит для приготовления зеленых бенгальских огней. [18]
Прибавка азотнокислого бария, как показывает опыт, благоприятствует быстрому установлению потенциала, что в свою очередь приводит к более резко выраженному изменению потенциала в эквивалентной точке. [20]
Растворимость азотнокислого бария в пределах от 0 до 100 С увеличилась почти в семь раз, растворимость хлористого натрия увеличилась только на 10 %, а растворимость углекислого лития уменьшилась примерно в два раза. [21]
Получается прокаливанием азотнокислого бария с последующим окислением окиси бария кислородом. [22]
Форма кристаллов азотнокислого бария в значительной мере зависит от присутствующих в растворе примесей. Так, введение в жидкую фазу метиленовой сини [20] приводит к тому, что ромбовидные кристаллы нитрата бария превращаются в пластинчатые — в осадок выпадают кристаллы в виде шестиугольных пластинок. [23]
При горении смесей азотнокислого бария с горючими пламя окрашивается в зеленый цвет. [24]
Карбонаты определяются прибавлением избытка азотнокислого бария к раствору цианида, затем смесь помещают в хорошо закрытую склянку и дают осесть углекислому барию. После этого углекислыя барий отфильтровывается и промывается с принятием возможных предог сторожностей для предохранения от доступа воздуха. Промытый осадок растворяется в определенном количестве титрованной соляной кислоты, и избыток кислоты обратно оттитровывается после предварительной кипячения для удаления углекислоты. [25]
Раствор 2 6 г азотнокислого бария в 100 г воды кипит при 100, 122 С. [26]
Перед концом титрования раствор азотнокислого бария следует добавлять осторожно, тщательно перемешивая содержимое колбы. [27]
Изыскание оптимальных условий получения чистого азотнокислого бария, Отч. [28]
Для приготовления некоторых эмалей применяется углекислый и азотнокислый барий. [29]
В горячем растворе 5 г азотнокислого бария в 150 мл воды при перемешивании растворяют 45 г азотнокислой меди и к горячему раствору добавляют теплый раствор 25 г двухромовокислого аммония в смеси 100 мл воды и 35 мл концентрированного водного аммиака. Перемешивают смесь в течение нескольких минут и дают ей охладиться. Осадок собирают на воронке Бюхнера диаметром 7 см, промывают его 200 мл воды, переносят в стакан и смешивают с таким количеством воды, чтобы консистенция смеси напоминала жидкую сметану. Добавляют 150 г пемзы, просеянной через сито 3 — 8 меш, тщательно перемешивают до тех пор, пока пемза не покроется равномерным слоем, переносят массу на чистую железную сковороду. Осторожно нагревают массу, перемешивая ее стеклянной палочкой, чтобы выпарить воду. Скоро зерна пемзы перестают прилипать одно к другому и образуется сыпучая масса. Продолжают нагревание и перемешивание до тех пор, пока масса не почернеет. [30]
Страницы: 1 2 3 4
www.ngpedia.ru
Барий азотнокислый — это… Что такое Барий азотнокислый?
- Барий азотнокислый
или азотнобаритовая соль — см. Барий и его соединения (9).
Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона. — С.-Пб.: Брокгауз-Ефрон. 1890—1907.
- Барий (хим.) (дополнение к статье)
- Барий марганцовокислый
Смотреть что такое «Барий азотнокислый» в других словарях:
барий азотнокислый — bario nitratas statusas T sritis chemija formulė Ba(NO₃)₂ atitikmenys: angl. barium nitrate rus. барий азотнокислый; бария нитрат ryšiai: sinonimas – bario bis(trioksonitratas) … Chemijos terminų aiškinamasis žodynas
Барий — I (хим. обозн. Ва, атомный вес 137) принадлежит к группе щелочноземельных металлов и по своим свойствам в особенности близок к кальцию и стронцию. Металлическая природа его доказана Берцелиусом, получившим амальгаму бария, из которой Дэви в 1808… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
азотнокислый барий — нитрат бария … Cловарь химических синонимов I
71.040.30 — Хімічні реактиви ГОСТ 8.134 98 ГСИ. Шкала рН водных растворов. Взамен ГОСТ 8.134 74 ГОСТ 8.315 97 ГСИ. Стандартные образцы состава и свойств веществ и материалов. Основные положения. Взамен ГОСТ 8.315 91 ГОСТ 61 75 Кислота уксусная. Технические… … Покажчик національних стандартів
71.060.50 — Солі ГОСТ 201 76 Тринатрийфосфат. Технические условия. Взамен ГОСТ 201 58 ГОСТ 244 76 Натрия тиосульфат кристаллический. Технические условия. Взамен ГОСТ 5.1189 72, ГОСТ 244 68 ГОСТ 246 76 Гидросульфит натрия технический. Технические условия.… … Покажчик національних стандартів
1713 — ГОСТ 1713{ 79} Барий азотнокислый технический. Технические условия. ОКС: 71.060.50 КГС: Л14 Соли Взамен: ГОСТ 1713 72 Действие: С 01.01.82 Изменен: ИУС 10/84, 7/86, 3/89 Примечание: переиздание 1993 Текст документа: ГОСТ 1713 «Барий азотнокислый… … Справочник ГОСТов
3777 — ГОСТ 3777{ 76} Барий азотнокислый. Технические условия. ОКС: 71.040.30 КГС: Л51 Неорганические реактивы Взамен: ГОСТ 3777 69 Действие: С 01.07.77 Изменен: ИУС 1/87, 11/91 Примечание: переиздание 1998 Текст документа: ГОСТ 3777 «Барий азотнокислый … Справочник ГОСТов
ГОСТ 1713-79 — 20 с. (4) Барий азотнокислый технический. Технические условия Взамен: ГОСТ 1713 72 Изменение №1/ИУС 10 1984 Изменение №2/ИУС 7 1986 Изменение №3/ИУС 3 1989 раздел 71.060.50 … Указатель национальных стандартов 2013
ГОСТ 3777-76 — 7 с. (2) Реактивы. Барий азотнокислый. Технические условия Взамен: ГОСТ 3777 69 Изменение №1/ИУС 1 1987 Изменение №2/ИУС 11 1991 раздел 71.040.30 … Указатель национальных стандартов 2013
bario nitratas — statusas T sritis chemija formulė Ba(NO₃)₂ atitikmenys: angl. barium nitrate rus. барий азотнокислый; бария нитрат ryšiai: sinonimas – bario bis(trioksonitratas) … Chemijos terminų aiškinamasis žodynas
dic.academic.ru
