Анод и катод — что это и как правильно определить?
Про анод и катод источника питания необходимо знать тем, кто занимается практической электроникой. Что и как называют? Почему именно так? Будет углублённое рассмотрение темы с точки зрения не только радиолюбительства, но и химии. Наиболее популярное объяснение звучит следующим образом: анод – это положительный электрод, а катод – отрицательный. Увы, это не всегда верно и неполно. Чтобы уметь определить анод и катод, необходимо иметь теоретическую базу и знать, что да как. Давайте рассмотрим это в рамках статьи.
Анод
 Обратимся к ГОСТ 15596-82, который занимается химическими источниками тока. Нас интересует информация, размещённая на третьей странице. Согласно ГОСТу, отрицательным электродом химического источника тока является именно анод. Вот так да! А почему именно так? Дело в том, что именно через него электрический ток входит из внешней цепи в сам источник. Как видите, не всё так легко, как кажется на первый взгляд. Можно посоветовать внимательно рассматривать представленные в статье картинки, если содержимое кажется слишком сложным – они помогут понять, что же автор хочет вам донести.
Обратимся к ГОСТ 15596-82, который занимается химическими источниками тока. Нас интересует информация, размещённая на третьей странице. Согласно ГОСТу, отрицательным электродом химического источника тока является именно анод. Вот так да! А почему именно так? Дело в том, что именно через него электрический ток входит из внешней цепи в сам источник. Как видите, не всё так легко, как кажется на первый взгляд. Можно посоветовать внимательно рассматривать представленные в статье картинки, если содержимое кажется слишком сложным – они помогут понять, что же автор хочет вам донести.
Катод
Обращаемся всё к тому же ГОСТ 15596-82. Положительным электродом химического источника тока является тот, при разряде из которого он выходит во внешнюю цепь. Как видите, данные, содержащиеся в ГОСТ 15596-82, рассматривают ситуацию с другой позиции. Поэтому при консультировании с другими людьми насчет определённых конструкций необходимо быть очень осторожным.
Возникновение терминов
 Их ввёл ещё Фарадей в январе 1834 года, чтобы избежать неясности и добиться большей точности. Он предлагал и свой вариант запоминания на примере с Солнцем. Так, у него анод – это восход. Солнце движется вверх (ток входит). Катод – это заход. Солнце движется вниз (ток выходит).
Их ввёл ещё Фарадей в январе 1834 года, чтобы избежать неясности и добиться большей точности. Он предлагал и свой вариант запоминания на примере с Солнцем. Так, у него анод – это восход. Солнце движется вверх (ток входит). Катод – это заход. Солнце движется вниз (ток выходит).
Пример радиолампы и диода
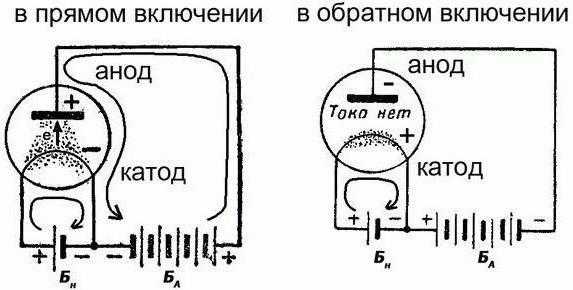
 Продолжаем разбираться, что для обозначения чего используется. Допустим, один из данных потребителей энергии у нас имеется в открытом состоянии (в прямом включении). Так, из внешней цепи диода в элемент по аноду входит электрический ток. Но не путайтесь благодаря такому объяснению с направлением электронов. Через катод во внешнюю цепь из используемого элемента выходит электрический ток. Та ситуация, что сложилась сейчас, напоминает случаи, когда люди смотрят на перевёрнутую картину. Если данные обозначения сложные – помните, что разбираться в них таким образом обязательно исключительно химикам. А сейчас давайте сделаем обратное включение. Можно заметить, что полупроводниковые диоды практически не будут проводить ток. Единственное возможное здесь исключение – обратный пробой элементов. А электровакуумные диоды (кенотроны, радиолампы) вообще не будут проводить обратный ток. Поэтому и считается (условно), что он через них не идёт. Поэтому формально выводы анод и катод у диода не выполняют свои функции.
Продолжаем разбираться, что для обозначения чего используется. Допустим, один из данных потребителей энергии у нас имеется в открытом состоянии (в прямом включении). Так, из внешней цепи диода в элемент по аноду входит электрический ток. Но не путайтесь благодаря такому объяснению с направлением электронов. Через катод во внешнюю цепь из используемого элемента выходит электрический ток. Та ситуация, что сложилась сейчас, напоминает случаи, когда люди смотрят на перевёрнутую картину. Если данные обозначения сложные – помните, что разбираться в них таким образом обязательно исключительно химикам. А сейчас давайте сделаем обратное включение. Можно заметить, что полупроводниковые диоды практически не будут проводить ток. Единственное возможное здесь исключение – обратный пробой элементов. А электровакуумные диоды (кенотроны, радиолампы) вообще не будут проводить обратный ток. Поэтому и считается (условно), что он через них не идёт. Поэтому формально выводы анод и катод у диода не выполняют свои функции.
Почему существует путаница?
Специально, чтобы облегчить обучение и практическое применение, было решено, что диодные элементы названия выводов не будут менять зависимо от своей схемы включения, и они будут «прикреплены» к физическим выводам. Но это не относится к аккумуляторам. Так, у полупроводниковых диодов всё зависит от типа проводимости кристалла. В электронных лампах этот вопрос привязан к электроду, который эмитирует электроны в месте расположения нити накала. Конечно, тут есть определённые нюансы: так, через такие полупроводниковые приборы, как супрессор и стабилитрон, может немного протекать обратный ток, но здесь существует специфика, явно выходящая за рамки статьи.
Разбираемся с электрическим аккумулятором
 Это по-настоящему классический пример химического источника электрического тока, что является возобновляемым. Аккумулятор пребывает в одном из двух режимов: заряд/разряд. В обоих этих случаях будет разное направление электрического тока. Но обратите внимание, что полярность электродов при этом меняться не будет. И они могут выступать в разных ролях:
Это по-настоящему классический пример химического источника электрического тока, что является возобновляемым. Аккумулятор пребывает в одном из двух режимов: заряд/разряд. В обоих этих случаях будет разное направление электрического тока. Но обратите внимание, что полярность электродов при этом меняться не будет. И они могут выступать в разных ролях:
- Во время зарядки положительный электрод принимает электрический ток и является анодом, а отрицательный его отпускает и именуется катодом.
- При отсутствии движения о них разговор вести нет смысла.
- Во время разряда положительный электрод отпускает электрический ток и является катодом, а отрицательный принимает и именуется анодом.
Об электрохимии замолвим слово
Здесь используют немного другие определения. Так, анод рассматривается как электрод, где протекают окислительные процессы. И вспоминая школьный курс химии, можете ответить, что происходит в другой части? Электрод, на котором протекают восстановительные процессы, называется катодом. Но здесь нет привязки к электронным приборам. Давайте рассмотрим ценность окислительно-восстановительных реакций для нас:
- Окисление. Происходит процесс отдачи частицей электрона. Нейтральная превращается в положительный ион, а отрицательная нейтрализуется.
- Восстановление. Происходит процесс получения частицей электрона. Положительная превращается в нейтральный ион, а потом в отрицательный при повторении.
- Оба процесса являются взаимосвязанными (так, количество электронов, что отданы, равняется присоединённому их числу).
Также Фарадеем для обозначения были введены названия для элементов, что принимают участие в химических реакциях:
- Катионы. Так называются положительно заряженные ионы, что двигаются в растворе электролита в сторону отрицательного полюса (катода).
- Анионы. Так называются отрицательно заряженные ионы, что двигаются в растворе электролита в сторону положительного полюса (анода).
Как происходят химические реакции?
 Окислительная и восстановительная полуреакции являются разделёнными в пространстве. Переход электронов между катодом и анодом осуществляется не непосредственно, а благодаря проводнику внешней цепи, на котором создаётся электрический ток. Здесь можно наблюдать взаимное превращение электрической и химической форм энергии. Поэтому для образования внешней цепи системы из проводников разного рода (коими являются электроды в электролите) и необходимо пользоваться металлом. Видите ли, напряжение между анодом и катодом существует, как и один нюанс. И если бы не было элемента, что мешает им напрямую произвести необходимый процесс, то ценность источников химического тока была бы весьма низка. А так, благодаря тому, что заряду необходимо пройтись по той схеме, была собрана и работает техника.
Окислительная и восстановительная полуреакции являются разделёнными в пространстве. Переход электронов между катодом и анодом осуществляется не непосредственно, а благодаря проводнику внешней цепи, на котором создаётся электрический ток. Здесь можно наблюдать взаимное превращение электрической и химической форм энергии. Поэтому для образования внешней цепи системы из проводников разного рода (коими являются электроды в электролите) и необходимо пользоваться металлом. Видите ли, напряжение между анодом и катодом существует, как и один нюанс. И если бы не было элемента, что мешает им напрямую произвести необходимый процесс, то ценность источников химического тока была бы весьма низка. А так, благодаря тому, что заряду необходимо пройтись по той схеме, была собрана и работает техника.
Что есть что: шаг 1
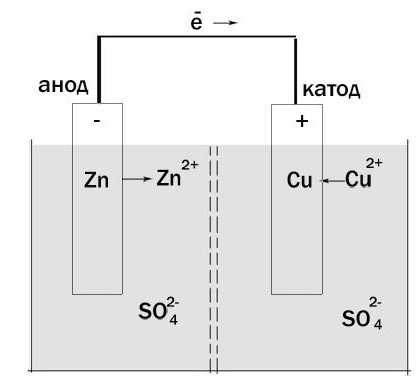 Теперь давайте будем определять, что есть что. Возьмём гальванический элемент Якоби-Даниэля. С одной стороны он состоит из цинкового электрода, который опущен в раствор сульфата цинка. Затем идёт пористая перегородка. И с другой стороны имеется медный электрод, который расположен в растворе сульфата меди. Они соприкасаются между собой, но химические особенности и перегородка не дают смешаться.
Теперь давайте будем определять, что есть что. Возьмём гальванический элемент Якоби-Даниэля. С одной стороны он состоит из цинкового электрода, который опущен в раствор сульфата цинка. Затем идёт пористая перегородка. И с другой стороны имеется медный электрод, который расположен в растворе сульфата меди. Они соприкасаются между собой, но химические особенности и перегородка не дают смешаться.
Шаг 2: Процесс
Происходит окисление цинка, и электроны по внешней цепи двигаются к меди. Так получается, что гальванический элемент имеет анод, заряженный отрицательно, и катод — положительный. Причем данный процесс может протекать только в тех случаях, когда электронам есть куда «идти». Дело в том, что попасть напрямую от электрода к другому мешает наличие «изоляции».
Шаг 3: Электролиз
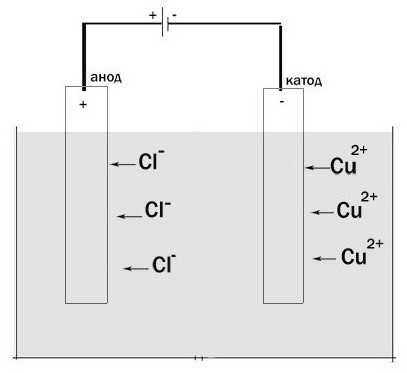 Давайте рассмотрим процесс электролиза. Установка для его прохождения является сосудом, в котором имеется раствор или расплав электролита. В него опущено два электрода. Они подключены к источнику постоянного тока. Анод в этом случае – это электрод, который подключен к положительному полюсу. Здесь происходит окисление. Отрицательно заряженный электрод – это катод. Здесь протекает реакция восстановления.
Давайте рассмотрим процесс электролиза. Установка для его прохождения является сосудом, в котором имеется раствор или расплав электролита. В него опущено два электрода. Они подключены к источнику постоянного тока. Анод в этом случае – это электрод, который подключен к положительному полюсу. Здесь происходит окисление. Отрицательно заряженный электрод – это катод. Здесь протекает реакция восстановления.
Шаг 4: Напоследок
Поэтому при оперировании данными понятиями всегда необходимо учитывать, что анод не в 100% случаев используется для обозначения отрицательного электрода. Также катод периодически может лишаться своего положительного заряда. Всё зависит от того, какой процесс на электроде протекает: восстановительный или окислительный.
Заключение
Вот таким всё и является – не очень сложно, но не скажешь, что и просто. Мы рассмотрели гальванический элемент, анод и катод с точки зрения схемы, и сейчас проблем с соединением источников питания с наработками у вас быть не должно. И напоследок нужно оставить ещё немного ценной для вас информации. Всегда приходится учитывать разницу, которую имеет потенциал катода/потенциал анода. Дело в том, что первый всегда будет немного большим. Это из-за того, что коэффициент полезного действия не работает с показателем в 100 % и часть зарядов рассеивается. Именно из-за этого можно увидеть, что аккумуляторы имеют ограничение на количество раз заряда и разряда.
fb.ru
что это такое, как их определить и запомнить
Среди терминов в электрике встречаются такие понятия как анод и катод. Это касается источников питания, гальваники, химии и физики. Термин встречается также в вакуумной и полупроводниковой электронике. Им обозначают выводы или контакты устройств и каким электрическим знаком они обладают. В этой статье мы расскажем, что это такое анод и катод, а также как определить где они находятся в электролизере, диоде и у батарейки, что из них плюс, а что минус.
Электрохимия и гальваника
В электрохимии есть два основных раздела:
- Гальванические элементы – производство электричества за счет химической реакции. К таким элементам относятся батарейки и аккумуляторы. Их часто называют химическими источниками тока.
- Электролиз – воздействие на химическую реакцию электроэнергией, простыми словами – с помощью источника питания запускается какая-то реакция.
Рассмотрим окислительно-восстановительную реакцию в гальваническом элементе, тогда какие процессы протекают на его электродах?
- Анод – электрод на котором наблюдается окислительная реакция, то есть он отдаёт электроны. Электрод, на котором происходит окислительная реакция – называется восстановителем.
- Катод – электрод на котором протекает восстановительная реакция, то есть он принимает электроны. Электрод, на котором происходит восстановительная реакция – называется окислителем.
Отсюда возникает вопрос – где плюс, а где минус у батарейки? Исходя из определения, у гальванического элемента анод отдаёт электроны.
Важно! В ГОСТ 15596-82 дано официальное определение названий выводов химических источников тока, если кратко, то плюс на катоде, а минус на аноде.
В данном случае рассматривается протекание электрического тока по проводнику внешней цепи от окислителя (катода) к восстановителю (аноду). Так как электроны в цепи текут от минуса к плюсу, а электрический ток наоборот, тогда катод – это плюс, а анод – это минус.

Внимание: ток всегда втекает в анод!
Или то же самое на схеме:

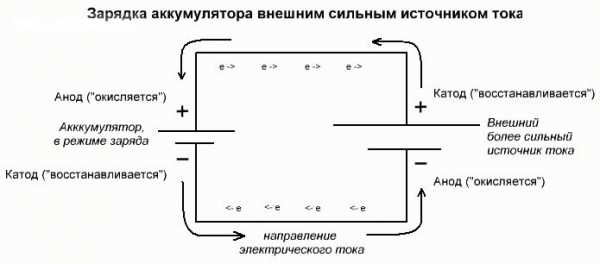
Процесс электролиза или зарядки аккумулятора
Эти процессы похожи и обратны гальваническому элементу, поскольку здесь не энергия поступает за счет химической реакции, а наоборот – химическая реакция происходит за счет внешнего источника электричества.
В этом случае плюс источника питания всё также называется катодом, а минус анодом. Зато контакты заряжаемого гальванического элемента или электроды электролизера уже будут носить противоположные названия, давайте разберемся почему!
Важно! При разряде гальванического элемента анод – минус, катод – плюс, при зарядке наоборот.
Так как ток от плюсового вывода источника питания поступает на плюсовой вывод аккумулятора – последний уже не может быть катодом. Ссылаясь на вышесказанное можно сделать вывод, что в этом случае электроды аккумулятора при зарядке условно меняются местами.
Тогда через электрод заряжаемого гальванического элемента, в который втекает электрический ток, называют анодом. Получается, что при зарядке у аккумулятора плюс становится анодом, а минус катодом.
Гальванотехника
Процессы осаждения металлов в результате химической реакции под воздействием электрического тока (при электролизе) называют гальванотехникой. Таким образом мир получил посеребренные, золоченные, хромированные или покрытые другими металлами украшения и детали. Этот процесс используют как в декоративных, так и в прикладных целях – для улучшения стойкости к коррозии различных узлов и агрегатов механизмов.
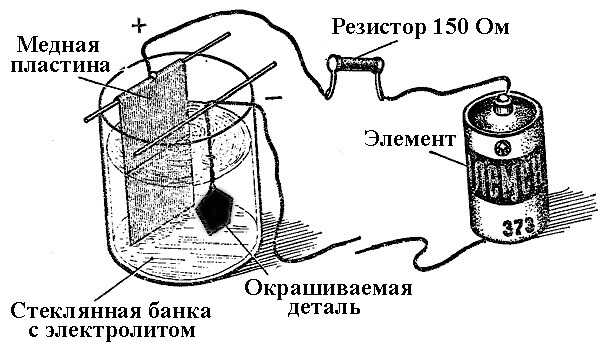
Принцип действия установок для нанесения гальванического покрытия лежит в использовании растворов солей элементов, которыми будут покрывать деталь, в качестве электролита.
В гальванике анод также является электродом, к которому подключаются плюсовой вывод источника питания, соответственно катод в этом случае – это минус. При этом металл осаждается (восстанавливается) на минусовом электроде (реакция восстановления). То есть если вы хотите сделать позолоченное кольцо своими руками – подключите к нему минусовой вывод блока питания и поместите в ёмкость с соответствующим раствором.
В электронике
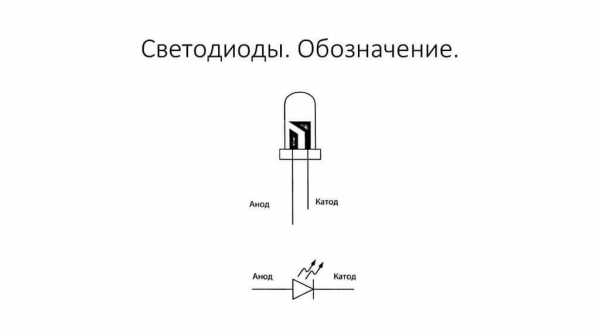
Электроды или ножки полупроводниковых и вакуумных электронных приборов тоже часто называют анодом и катодом. Рассмотрим условное графическое обозначение полупроводникового диода на схеме:

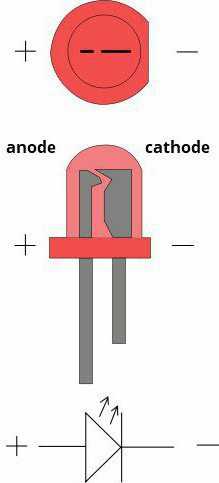
Как мы видим, анод у диода подключается к плюсу батареи. Он так называется по той же причине – в этот вывод у диода в любом случае втекает ток. На реальном элементе на катоде есть маркировка в виде полосы или точки.

У светодиода аналогично. На 5 мм светодиодах внутренности видны через колбу. Та половина, что больше — это катод.
Также обстоит ситуация и с тиристором, назначение выводов и «однополярное» применение этих трёхногих компонентов делают его управляемым диодом:
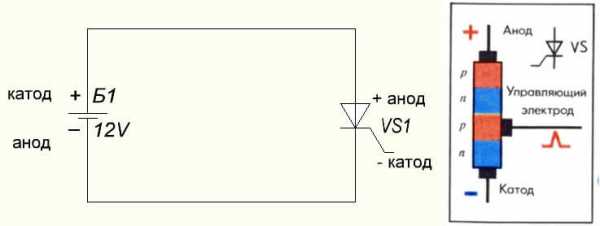
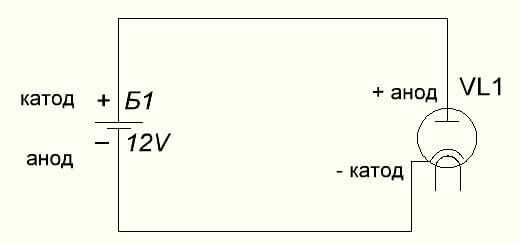
У вакуумного диода анод тоже подключается к плюсу, а катод к минусу, что изображено на схеме ниже. Хотя при приложении обратного напряжения – названия этих элементов не изменятся, несмотря на протекание электрического тока в обратном направлении, пусть и незначительного.
С пассивными элементами, такими как конденсаторы и резисторы дело обстоит иначе. У резистора не выделяют отдельно катод и анод, ток в нём может протекать в любом направлении. Вы можете дать любые названия его выводам, в зависимости от ситуации и рассматриваемой схемы. У обычных неполярных конденсаторов также. Реже такое разделение по названиям контактов наблюдается в электролитических конденсаторах.

Заключение
Итак, подведем итоги, ответив на вопрос: как запомнить где плюс, где минус у катода с анодом? Есть удобное мнемоническое правило для электролиза, заряда аккумуляторов, гальваники и полупроводниковых приборов. У этих слов с аналогичными названиями одинаковое количество букв, что проиллюстрировано ниже:
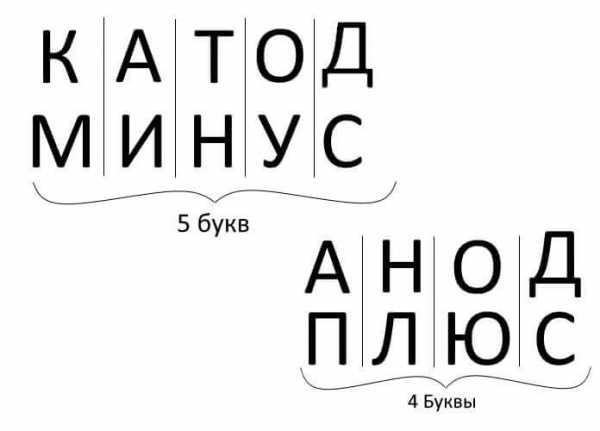
Во всех перечисленных случаях ток вытекает из катода, а втекает в анод.
Пусть вас не собьёт с толку путаница: «почему у аккумулятора катод положительный, а когда его заряжают – он становится отрицательным?». Помните у всех элементов электроники, а также электролизеров и в гальванике – в общем у всех потребителей энергии анодом называют вывод, подключаемый к плюсу. На этом отличия заканчиваются, теперь вам проще разобраться что плюс, что минус между выводами элементов и устройств.
Напоследок рекомендуем просмотреть полезное видео по теме статьи:
Теперь вы знаете, что такое анод и катод, а также как запомнить их достаточно быстро. Надеемся, предоставленная информация была для вас полезной и интересной!
Материалы по теме:
Нравится(0)Не нравится(0)samelectrik.ru
Катоды и аноды отрицательно и положительно заряженные электроды
Катод – это электрод устройства, который подключен к отрицательному полюсу источнику тока. Анод – противоположность ему. Это электрод прибора, подключенный к положительному полюсу источника тока.
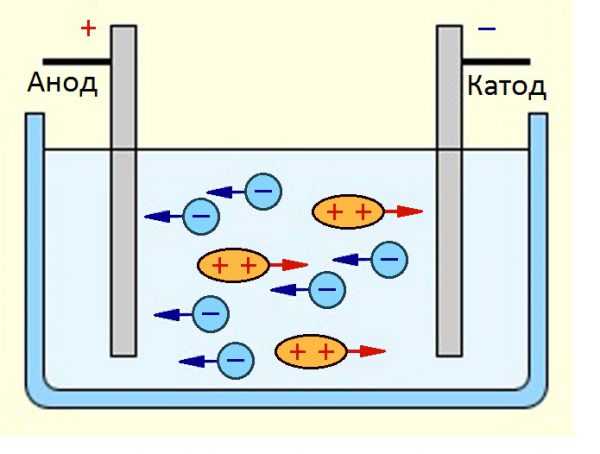
Окислительно-восстановительный процесс на электродах
Обратите внимание! Чтобы легче запомнить разницу между ними, используют шпаргалку. В словах «катод»-«минус», «анод»-«плюс» одинаковое число букв.
Применение в электрохимии
В этом разделе химии катод – это отрицательно заряженный электрический проводник (электрод), притягивающий к себе положительно заряженные ионы (катионы) во время процессов окисления и восстановления.
Электролитическое рафинирование – это электролиз сплавов и водных растворов. Большинство цветных металлов подвергаются такой очистке. При помощи электролитической очистки получается металл с высокой чистотой. Так, степень чистоты меди после рафинирования достигает 99,99%.
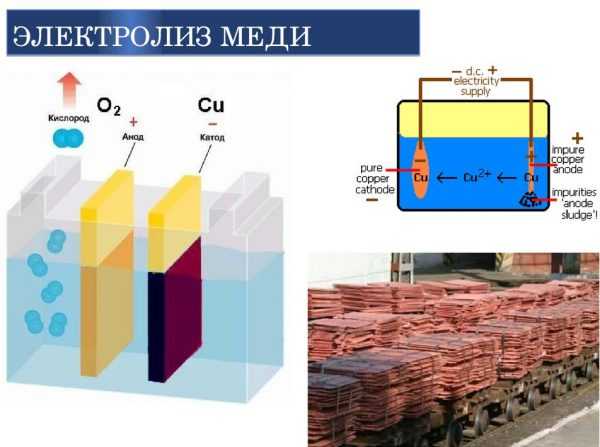
Электролиз меди
На положительном электрическом проводнике во время рафинирования или очистки проходит электролитический процесс. Во время него металл с примесями помещают в электролизер и делают анодом. Такие процессы проводятся при помощи внешнего источника электрической энергии и называются реакциями электролиза. Осуществляются в электролизерах. Он выполняет функцию электронасоса, нагнетающего отрицательно заряженные частицы (электроны) в отрицательный проводник и удаляющего его из анода. Откуда исходит ток, неважно.
На катоде очищается металл от посторонних примесей. Простой катод изготавливается из вольфрама, иногда – из тантала. Достоинством вольфрамового отрицательного электрода является стойкость его изготовления. Из недостатков – имеет низкую эффективность и неэкономичность. Сложные катоды имеют разное устройство. У многих таких типов проводников на чистый металл сверху наносится специальный слой, который активирует получение большей производительности при относительно низких температурах. Они очень экономичны. Их недостаток состоит в небольшой устойчивости производительности.
Готовый чистый металл тоже называется катодом. Например, цинковый или платиновый катод. На производстве отрицательный проводник отделяют от катодной основы при помощи катодосдирочных машин.
При удалении отрицательно заряженных частиц из электрического проводника на нем создается анод, а при нагнетании отрицательно заряженных частиц на электрический проводник – катод. При электролизе очищаемого металла его положительные ионы притягивают к себе отрицательно заряженные частицы на отрицательном проводнике, и происходит восстановительный процесс. Чаще всего используют такие аноды:
- цинковые;
- кадмиевые;
- медные;
- никелевые;
- оловянные;
- золотые;
- серебряные;
- платиновые.
Чаще всего на производстве используют цинковые аноды.
- катанные;
- литые;
- сферические.
Больше всего применяют катанные цинковые аноды. Еще используют никелевые и медные. А вот кадмиевые почти не используются из-за их токсичности для экологии. Бронзовые и оловянные аноды применяют при изготовлении радиоэлектронных печатных плат.
Гальванизация (гальваностегия) – процесс нанесения тонкого слоя металла на другой предмет с целью предотвращения коррозии изделия, окисления контактов в электронике, износостойкости, декорации. Суть процесса такая же, как при рафинировании.
Цинк и олово используют для повышения стойкости изделия при коррозии. Цинкование бывает холодным, горячим, гальваническим, газотермическим и термодиффузионным. Золото используют в основном в защитно-декоративных целях. Серебро повышает стойкость контактов электроприборов к окислению. Хром – для увеличения износостойкости и защиты от коррозии. Хромирование придает изделиям красивый и дорогой вид. Используется для нанесения на ручки, краны, колесные диски и т.д. Процесс хромирования токсичен, поэтому строго регламентируется законодательством разных стран. Ниже на картинке представлен метод гальванизации при помощи никеля.
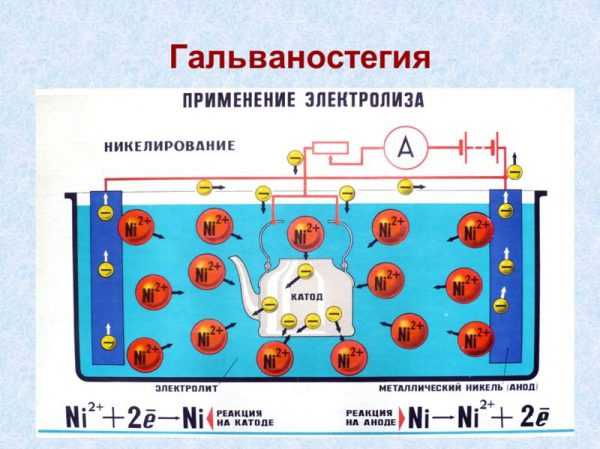
Никелирование чайника методом гальванизации
Применение в вакуумных электронных приборах
Здесь катод выступает источником свободных электродов. Они образуются в ходе их выбивания из металла при высоких температурах. Положительно заряженный электрод притягивает электроны, выпущенные отрицательным проводником. В разных аппаратах он в разной степени собирает их в себя. В электронных трубках он полностью притягивает отрицательно заряженные частицы, а в электронно-лучевых приборах – частично, формируя в завершении процесса электронный луч.
Маркировка
Стандартно катод маркируют как «-». Знак анода – «+». А вот в гальванике, из-за того, что отрицательный заряд на проводнике снабжается не источником тока извне, а реакцией окисления металла, катод получит положительный заряд электрического проводника. Поэтому в аккумуляторах, когда ток меняет направление, происходит смена знаков «+» и «-».
Эти свойства катодов и анодов нашли широкое применение в промышленности при очистке металла и в гальваностегии.
Видео
Оцените статью:elquanta.ru
Анод — Википедия
Полупроводниковый прибор — диод Полупроводниковый прибор — тиристор Розлив черновой меди в аноды на заводе «Уралэлектромедь» Металлургические аноды и катоды в цехе электролиза Анод электронной лампыАно́д (др.-греч. ἄνοδος — движение вверх) — электрод некоторого прибора, присоединённый к положительному полюсу источника питания. Электрический потенциал анода положителен по отношению к потенциалу катода (кроме гальванических элементов).[источник не указан 1362 дня]
Содержание
- 1 Анод в электрохимии
- 2 Анод в вакуумных электронных приборах
- 3 Анод у полупроводниковых приборов
- 4 Знак анода и катода
- 5 См. также
- 6 Литература
- 7 Ссылки
ru.wikipedia.org
Катод и анод — единство и борьба противоположностей
Катод и анод – это две составляющие одного процесса: протекания электрического тока. Все материалы можно разделить на два типа – это проводники, в структуре которых большой избыток свободных электронов, и диэлектрики (в них свободных электронов практически нет).
Понятие электрического тока
 Электрический ток – это упорядоченное перемещение заряженных элементарных частиц в структуре вещества под воздействием электромагнитного напряжения. Если приложить к проводнику постоянное напряжение, то свободные электроны, имеющие отрицательный заряд, начнут упорядоченно двигаться в сторону анода (положительно заряженного электрода) от катода (отрицательно заряженного электрода). Ток же, соответственно, будет течь в обратном направлении. А катод и анод – это два электрода, между которыми образовался перепад (разница) электромагнитного напряжения.
Электрический ток – это упорядоченное перемещение заряженных элементарных частиц в структуре вещества под воздействием электромагнитного напряжения. Если приложить к проводнику постоянное напряжение, то свободные электроны, имеющие отрицательный заряд, начнут упорядоченно двигаться в сторону анода (положительно заряженного электрода) от катода (отрицательно заряженного электрода). Ток же, соответственно, будет течь в обратном направлении. А катод и анод – это два электрода, между которыми образовался перепад (разница) электромагнитного напряжения.
Проводники и диэлектрики
Проводники и диэлектрики могут быть твердыми, жидкими и газообразными веществами. Это для протекания электрического тока совсем не принципиально. При длительном приложении электромагнитного напряжении к материалу на катоде будет образовываться избыток электронов, а на аноде – его недостача. Если напряжение прилагается достаточно долго, то из структуры материала, из которого сделан анод, будут вырываться связанные электроны вместе с атомами, а сам материал начнет вступать в химическую реакцию с химически активными веществами из окружающей среды. Такой процесс носит название электролиза.
Электролиз
Катод и анод в электрохимии являются двумя полюсами приложенного к солевым растворам или расплавам постоянного электромагнитного напряжения. При возникновении тока от избытка электронов анод начинает разрушаться, т.е. сами положительно заряженные атомы вещества будут попадать в соляной раствор (окружающую среду) и переноситься на катод, где оседать в очищенном виде. Этот процесс носит название гальванического. С помощью гальваники покрывают тонким слоем цинка, меди, золота, серебра и других металлов различные изделия.

Что такое катод и каковы задачи, которые он выполняет в электролизе? Это можно понять при выполнении следующих действий: если сделать анод из бронзы или олова, то на катоде получится печатная плата, покрытая тонким слоем меди или олова (используется в радиоэлектронной промышленности). Этим же способом получают позолоченные ювелирные украшения, омедненные и даже позолоченные алюминиевые наконечники для электротехники в целях повышения электропроводности.
Ответы на вопросы о том, что такое анод и катод, при электролизе очевидны: анод в результате протекания постоянного тока через соляной раствор разрушается, а катод принимает на себя анодный материал. Даже термин такой возник в среде гальваников – «анодирование катода». Физического смысла он не несет, но фактическую суть вопроса отображает прекрасно.
Полупроводники
Полупроводники представляют собой материалы, которые в структуре не имеют свободных электронов, а атомные держатся на своих местах плохо. Если такой материал в жидком или газообразном состоянии поместить в магнитное поле, а затем дать ему затвердеть, то получится электрически структурированный полупроводник, который будет пропускать ток только в одну сторону.  Из этого материала, используя вышеназванное свойство, делают диоды. Они бывают двух видов:
Из этого материала, используя вышеназванное свойство, делают диоды. Они бывают двух видов:
а) с «p-n-p» проводимостью;
б) с «n-p-n» проводимостью.
На практике эта тонкость структуры диодов значения не имеет. Важно правильно подключить в электрическую схему диод. Где анод, где катод – вопрос, которым многие озадачены. На диоде есть специальные обозначения: или А и К, или + и –. Можно подключить диод только двумя способами к электрической схеме постоянного тока. В одном случае исправный диод будет проводить ток, а в другом – не будет. Поэтому необходимо взять прибор, на котором заведомо известно, где катод, а где анод, и подключить его к диоду. Если устройство покажет наличие тока, то диод подключен правильно. Значит, катод прибора и катод диода, а также анод прибора и анод диода совпали. В противном случае нужно поменять соединения местами.
1. Если диод не пропускает ток в обе стороны, то он перегоревший, ремонту не подлежит.
2. Если наоборот, пропускает, то он пробитый. Его необходимо выбросить.
Проверяются диоды тестерами и пробниками. В диодах катод и анод жестко привязаны к их материальному исполнению в отличие от гальванических источников питания (аккумуляторов, батареек и т. п.).
 Катодом в полупроводниковых элементах (диодах) электрической схемы является электрод (ножка), из которого выходит положительный (+) потенциал. Через схему он связан с отрицательным потенциалом источника питания. Значит, ток непосредственно в полупроводнике диода протекает по направлению от анода к катоду. На электрических схемах этот процесс символически так и обозначается.
Катодом в полупроводниковых элементах (диодах) электрической схемы является электрод (ножка), из которого выходит положительный (+) потенциал. Через схему он связан с отрицательным потенциалом источника питания. Значит, ток непосредственно в полупроводнике диода протекает по направлению от анода к катоду. На электрических схемах этот процесс символически так и обозначается.
Если диод одной ножкой (электродом) подключить к переменному напряжению, то на втором электроде мы получим положительную или отрицательную полусинусоиду. Если соединить два диода в мост, то будем наблюдать выпрямленный электрический практически постоянный ток.
Гальванические источники постоянного тока – аккумуляторы (батареи)
Катод и анод в этих изделиях меняются местами в зависимости от направления протекания электрического тока, потому что в одном случае к ним напряжение не приходит, а они сами за счет химической реакции служат источниками постоянного тока. Тут отрицательным электродом уже будет анод, а положительным – катод. В другом же случае в аккумуляторе происходит обычный процесс электролиза.
Когда аккумулятор разрядился и химическая реакция, которая служила источником электрического тока, прекратилась, его необходимо зарядить с помощью внешнего источника питания. Таким образом, мы запускаем процесс электролиза, т.е. восстановления первоначальных свойств гальванической батареи. На катод аккумулятора необходимо приложить уже отрицательный заряд, а на анод – положительный, тогда батарея будет заряжаться.
Таким образом, ответ на вопрос о том, как определить катод и анод в гальваническом элементе, зависит от того, заряжается он или служит источником питания электрическим током.
Вывод
Как суммирование всего вышесказанного, катод – это электрод, на котором появляется избыток электронов, а анод – это электрод, на котором появляется недостача электронов. Но плюс или минус на конкретном электроде элемента электрической схемы определяется направлением протекания электрического тока.
fb.ru
Анод — это… Что такое Анод?
Ано́д (др.-греч. ἄνοδος — движение вверх) — электрод некоторого прибора, присоединённый к положительному полюсу источника питания. Электрический потенциал анода положителен по отношению к потенциалу катода.
Анод в электрохимии
При процессах электролиза (получение элементов из солевых растворов и расплавов под действием постоянного электрического тока), анод — электрически положительный полюс, на нём происходят окислительно-восстановительные реакции (окисление), результатом которых, в определённых условиях, может быть разрушение (растворение) анода, что используется, к примеру, при электрорафинировании металлов.
Аноды — множественное число слова «анод»; эта форма применяется преимущественно в металлургии, где применяются аноды для гальваники, используемые для нанесения на поверхность изделия слоя металла электрохимическим способом, либо для электрорафинирования, где металл с примесями растворяется на аноде и осаждается в очищенном виде на катоде. Основное распространение получили аноды из цинка (бывают сферические, литые и катаные, чаще используются последние), никеля, меди (среди которых отдельно выделяют медно-фосфористые, марки АМФ), кадмия (применение которых сокращается из-за экологической вредности), бронзы, олова (применяются при производстве печатных плат в радиоэлектронной промышленности), сплава свинца и сурьмы, серебра, золота и платины. Аноды из недрагоценных металлов применяются для повышения коррозионной стойкости, повышения эстетических свойств предметов и др. целей. Аноды из драгоценных металлов применяются гальваническим производством для повышения электропроводности изделий и др.
Анод в вакуумных электронных приборах
В вакуумных электронных приборах анод — электрод, который притягивает к себе летящие электроны, испущенные катодом. В электронных лампах и рентгеновских трубках конструкция анода такова, что он полностью поглощает электроны. А в электронно-лучевых приборах анод является элементом электронной пушки. Он поглощает лишь часть летящих электронов, формируя после себя электронный луч.
Анод у полупроводниковых приборов
Электрод полупроводникового прибора (диода, тиристора), подключённый к положительному полюсу источника тока, когда прибор открыт (то есть имеет маленькое сопротивление), называют анодом, подключённый к отрицательному полюсу — катодом.
Знак анода и катода
В литературе встречается различное обозначение знака анода — «+» или «-», что определяется, в частности, особенностями рассматриваемых процессов.
В электрохимии принято считать, что катод — электрод, на котором происходит процесс восстановления, а анод — тот, где протекает окисление[1]. При работе электролизера (например, при рафинировании меди) внешний источник тока обеспечивает на одном из электродов избыток электронов (отрицательный заряд), здесь происходит восстановление металла, это катод. На другом электроде обеспечивается недостаток электронов и окисление металла, это анод.
В то же время при работе гальванического элемента (к примеру, медно-цинкового), избыток электронов (и отрицательный заряд) на одном из электродов обеспечивается не внешним источником тока, а собственно реакцией окисления металла (растворения цинка), то есть здесь отрицательным, если следовать приведённому определению, будет уже анод. Электроны, проходя через внешнюю цепь, расходуются на протекание реакции восстановления (меди), то есть катодом будет являться положительный электрод.
В соответствии с таким толкованием, для аккумулятора анод и катод меняются местами в зависимости от направления тока внутри аккумулятора[2][3].
В электротехнике анод — положительный электрод, ток течет от анода к катоду, электроны, соответственно, наоборот.
См. также
Литература
- ↑ Антропов Л. И. Теоретическая электрохимия : Учеб. для хим.-технолог. спец. вузов. — 4-е изд., перераб. и доп. — М. : Высш. шк., 1984. — С. 13.
- ↑ Левин А. И. Теоретические основы электрохимии. — М.: Металлургиздат, 1963. — С. 131.
- ↑ Справочник по электрохимии / Под ред. А. М. Сухотина. — Л. : Химия, 1981. — С. 405.
Ссылки
dic.academic.ru
Катод и анод — это плюс или минус?
Изучение таких отраслей, как электрохимия и цветная металлургия, невозможно без понимания в полной мере терминов катод и анод. В то же время эти термины являются неотъемлемой частью вакуумных и полупроводниковых электронных приборов.

Вакуумные и полупроводниковые компоненты
Катод и анод в электрохимии
Под электрохимией следует понимать раздел физической химии, изучающий химические процессы, вызываемые воздействием электрического тока, а также электрические явления, вызываемые химическими процессами. Существует два основных вида электрохимических операций:
- Процедура преобразования электрического воздействия в химическую реакцию, называемая электролизом;
- Процедура преобразования химической реакции в электрический ток, называемая гальваническим процессом.
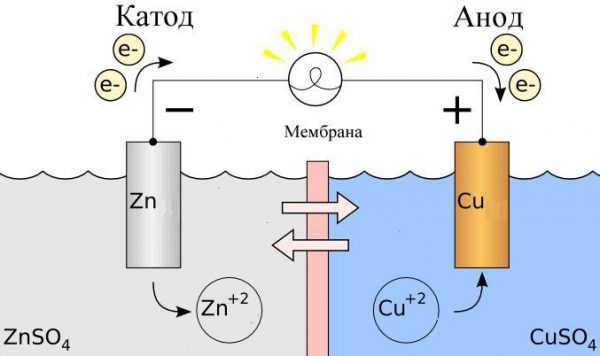
Гальванический элемент в электрохимии
В электрохимии под терминами анод и катод понимают следующее:
- Электрод, на котором проходит окислительная реакция, называется анодом;
- Электрод, на котором осуществляется процедура восстановления, называется катодом.
Под процессами окисления стоит понимать процедуру, при которой частица отдает электроны. Восстановительный процесс подразумевает процедуру принятия электронов частицей. Соответственно, частицы, которые отдают электроны, именуются «восстановителями», и они подвержены окислению. Частицы, которые принимают электроны, именуются «окислителями», они восстанавливаются.
Цветная металлургия широко использует процесс электролиза для выделения металлов из добытых руд и дальнейшей очистки. В процедуре электролиза применяются растворимые и нерастворимые аноды, а сами процессы называются электрорафинированием и электроэкстракцией, соответственно.
Катод в вакуумных приборах
Одной из разновидностей электровакуумных приборов является электронная лампа. Предназначение электроламп – регулирование потока электронов, дрейфующих в вакууме между другими электродами. Конструктивно электролампа выглядит как герметичный сосуд-баллон, с помещенными в середине мелкими металлическими выводами. Численность выводов зависит от вида радиолампы.

Устройство электронной лампы
В составе любой радиолампы такие элементы:
- Катод;
- Анод;
- Сетка.
Катодом электролампы подразумевается разогретый электрод, подключенный к «минусу» блока питания и испускающий электроны, будучи накаленным. Эти электроны движутся к аноду, подключенному к «плюсу». Процесс испускания электронов разогретым катодом называется термоэмиссией, а возникший при этом ток именуется током термоэмиссии. Метод нагрева обуславливает разновидности катодов:
- Катод прямого разогрева;
- Катод непрямого разогрева.
Катодом непосредственного накала является прочный вольфрамовый проводник большого сопротивления. Прогревание катода проходит путем подвода к нему напряжения.
Важно! К особенностям электронных ламп непосредственного нагрева относятся быстрый запуск лампы в работу при меньшем потреблении мощности, хотя за счет срока службы. Поскольку питающий ток таких ламп является постоянным, то ограничено их применение в среде переменного тока.
Электролампы, у которых внутри катода, выполненного в виде цилиндра, размещена нагревающая нить, называются радиолампами косвенного нагрева.
Конструктивно анод выглядит в виде пластины либо коробочки, размещенной вокруг катода с сеткой и имеющей потенциал, обратный катоду. Дополнительные электроды, размещенные между анодом и катодом, называются сеткой и применяются для регулировки потока электронов.
Катод у полупроводниковых приборов
К полупроводниковым приборам относятся устройства, состоящие из вещества, удельное электрическое сопротивление которого больше сопротивления проводника, но меньше сопротивления диэлектрика. К особенностям таких приборов относится большая зависимость электропроводимости от концентрации добавок и влияния электрическим током. Свойства p-n перехода определяют принципы работы большей части полупроводниковых компонентов.
Наиболее простым представителем полупроводниковых компонентов является диод. Это элемент, имеющий два вывода и один p-n переход, отличительной особенностью которого выступает протекание тока в одном направлении.
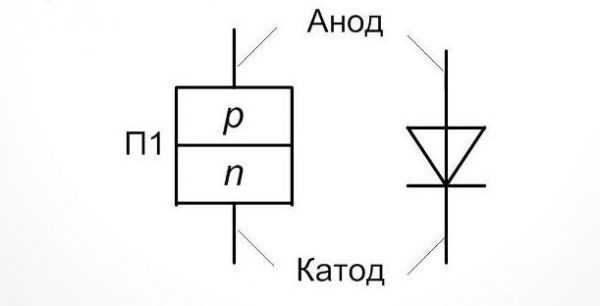
Диод полупроводниковый
Отводы компонента называются анод и катод. Протекание тока по элементу возможно при подключении «плюса» к аноду и «минуса» – к катоду. При противоположном подсоединении элемент запирается, и ток не протекает.
Такие словосочетания, как анод и катод, в полной мере применяются в приборостроении и индустрии, будь то электрохимия, вакуумные приборы или полупроводниковые приборы. Усвоение многих процессов затруднительно или невозможно без понимания терминов анод и катод.
Видео
Оцените статью:elquanta.ru

