Ангидрид хромовый, хромовая кислота, трехокись хрома
Ангидрид хромовый (хромовая кислота, трехокись хрома, оксид хрома(VI)) ГОСТ 2548-77
это соединение хрома с кислородом; кристаллы, чешуйки или гранулы темно-красного или малиново-красного цвета с фиолетовым оттенком.Плотность — 2,8 г/см³. Температура плавления — 196° С. Гигроскопичен, расплывается на воздухе. Растворимость в воде — 166г/100г (15° С), 199г/100г (100° С). С водой образует хромовые кислоты. Сильный окислитель, может вызывать воспламенение бумаги, спирта. Ядовит.
Химическая формула: CrO3
В зависимости от назначения хромовый ангидрид выпускают марок А, Б и В.
Широко применяется в машиностроительной, металлургической, химической, нефтехимической и других отраслях промышленности для:
— производства металлического хрома высокой чистоты, сверхтвердых материалов, некоторых катализаторов для процессов хромирования, хроматирования и пассивирования (марка А).
— производства электролитического хрома, производства катализаторов (марка Б).
— производства литья в составе формовочных и стержневых смесей, для процессов травления и других целей (марка В).
Его применяют также, как окислитель в органической химии (в производстве изатина, индиго и т.д.). В смеси с кизельгуром применяется для очистки ацетилена под названием «эпурит». Физико-химические показатели хромового ангидрида:
| Наименование показателя | Норма для марки | ||
| А | Б | В | |
| 1. Внешний вид | Чешуйки или гранулы малиново-красного цвета, для марки В допускается оттенок черного цвета и включение комочков слипшихся гранул или чешуек | ||
| 2. Массовая доля хромового ангидрида (CrO3), %, не менее | 99,7 | 98,8 | 98,0 |
| 3. Массовая доля веществ, нерастворимых в воде, %, не более | 0,02 | 0,05 | не нормируется |
| 4. Массовая доля сульфатов (SO 42-), %, не более | 0,06 | 0,18 | не нормируется |
5. Массовая доля натрия (Na+), %, не более Массовая доля натрия (Na+), %, не более | 0,05 | не нормируется | не нормируется |
Технический хромовый ангидрид является сильным окислителем, при соприкосновении с горючими веществами вызывает загорание или взрыв.
По степени воздействия на организм относится к веществам 1-го класса опасности.
Технический хромовый ангидрид упаковывают в cертифицированные неокрашенные металлические барабаны для химических продуктов. Хранят в закрытом складском помещении в неповрежденной упаковке. Контейнеры хранят на контейнерных площадках. Хранение продукта вместе с горючими веществами не допускается. Гарантийный срок хранения продукта — 1 год со дня изготовления.
| Класс опасности | 1 |
| Основные свойства и виды опасности | |
| Основные свойства | Чешуйки или гранулы малиново-красного цвета. |
| Взрыво- и пожароопасность | Технический хромовый ангидрид является сильным окислителем, при соприкосновении с горючими веществами вызывает загорание или взрыв. |
| Опасность для человека | При поступлении в организм в значительных количествах вызывает тяжелые отравления. |
| Индивидуальные средства защиты | Спецодежда, спецобувь, средства защиты органов дыхания, лица и глаз. |
| Необходимые действия в аварийных ситуациях | |
| Общего характера. При утечке и россыпи | |
| При пожаре | |
| При возгорании | |
| Меры первой помощи | |
ООО “Компани “Плазма”® осуществляет поставки химической продукции со склада в Харькове в сроки и, на выгодных для Вас условиях.
Хромовый ангидрид — База химической продукции Югреактив
Хромовый ангидрид
Синонимы: Хром VI окись, трёхокись хрома, оксид хрома, хром оксид
Спецификация |
|
|---|---|
Молекулярный вес | 99,99 |
Температура плавления | 197 |
Растворимость в воде | 166 г/100 г (15 °C), 199 г/100 г (100 °C) |
Плотность | 2,8 г/см3 |
Чистота,%, не менее | 99. |
Содержание сульфатов,%, не более | 0.15% |
Нерастворимость в воде, %, не более | 0.025% |
Хромовый ангидрид, этот реактив также имеет название хром оксид, хром окись VI или трёхокись хрома — это чёрно-красные с фиолетовым оттенком кристаллы — пластины или иголки. Хромовый ангидрид гигроскопичен, расплывается на воздухе, является очень сильным окислителем: может вызывать воспламенение бумаги, спирт также вспыхивает при соприкосновении с кристаллами CrO3.
При нагревании препарат чернеет, при 196 °С плавится в красно-бурую жидкость. Выше 250 °С разлагается с отщеплением кислорода и образованием Cr2O3, при 435 °С разложение заканчивается. Хромовый ангидрид хорошо растворяется в воде (62,58% при 20 °С), при этом образуется раствор хромовой кислоты h3CrO4.
Получение
Хромовый ангидрид или Хром VI окись можно получить путем обработки раствора K2Cr2O7 концентрированной h3SO4.
Применение
Хромовый ангидрид (оксид хрома) используется для
• получения хрома электролизом, электролитического хромирования,
• в качестве сильного окислителя, изредка в пиросоставах.
• как окислитель в органической химии (в производстве изатина, индиго и т. д.).
• в смеси с кизельгуром применяется для очистки ацетилена под названием «эпурит».
• растворы хромового ангидрида (или, чаще, дихромата калия) в серной кислоте широко используются в лабораторной практике для очистки посуды от органических загрязнений (хромовая смесь).
Электролиты для хромирования
Основными составляющими электролитов являются хромовый ангидрид и серная кислота. Хромовый ангидрид СгО3 — плавленая кристаллическая масса вишнево-красного цвета. Растворимость в воде при 20 °С до 625 г/л. Хромовый ангидрид, оставленный на воздухе в барабане или в кусках на полу, легко соединяется с влагой воздуха, превращаясь в хромовую кислоту, и как энергичный окислитель быстро разрушает все органические вещества, с которыми он соприкасается.
Технический хромовый ангидрид может содержать до 0,4 % SO4 в пересчете на H2SO4, что следует учитывать при приготовлении и корректировании ванн хромирования. Поэтому при зарядке сначала в ванну закладывают полностью расчетное количество хромового ангидрида, заливают водой до заданного объема и дают полностью раствориться. После перемешивания раствора отбирают пробу для анализа на содержание иона SO 4- и лишь после получения результата вводят в ванну недостающее количество серной кислоты.
Серная кислота H2SO4 (ГОСТ 4204) — химически чистая, вязкая бесцветная жидкость, плотность — 1,84 г/см3. Приливание кислоты в ванну хромирования следует производить в расчетном количестве, при энергичном перемешивании.
Стандартный электролит
Ориентировочный состав стандартного электролита содержит, г/л:
хромовый ангидрид — 150-250; серная кислота — 1,5-2,5.
При наличии целого ряда ценных свойств стандартный электролит обладает и некоторыми недостатками. Так, он чувствителен к колебаниям температуры, допуская отклонения от рабочего интервала температур лишь в пределах ±2 °С в течение всего времени процесса хромирования, длящегося обычно несколько часов. Если отклонение от заданной температуры превысит норму во время осаждения, то возникнут внутренние напряжения в хромовом покрытии, которые могут привести к его отслаиванию. Аналогичное действие оказывают и колебания плотности тока.
Так, он чувствителен к колебаниям температуры, допуская отклонения от рабочего интервала температур лишь в пределах ±2 °С в течение всего времени процесса хромирования, длящегося обычно несколько часов. Если отклонение от заданной температуры превысит норму во время осаждения, то возникнут внутренние напряжения в хромовом покрытии, которые могут привести к его отслаиванию. Аналогичное действие оказывают и колебания плотности тока.
Кроме того, поддержание правильного соотношения между концентрациями хромового ангидрида и серной кислоты, равного 100:1, связано с частыми корректированиями и с введением добавок серной кислоты. Катодный выход по току весьма низок и находится в пределах 12-13 %, вследствие чего необходимо затрачивать большое количество времени и электроэнергии для получения износостойкого слоя хрома достаточной толщины.
Саморегулирующийся электролит
Этих недостатков лишен «саморегулирующийся» электролит, который имеет следующий состав (г/л) и режим работы (ГОСТ 9. 047):
047):
хромовый ангидрид — 225-300; сернокислый стронций — 5,5-6,5; кремнефтористый калий — 18-20; хром трехвалентный — 3-10; температура, °С — 55-65; плотность тока, А/дм2 — 40-70; выход по току, % — 18.
Характерной особенностью этого электролита является, прежде всего, постоянная концентрация аниона SO2-, составляющая 2,5 г/л. Это явление связано с тем, что сернокислый стронций и кремнефтористый калий имеют весьма ограниченную растворимость в воде и в рабочем диапазоне температур поддерживают в растворе заданную концентрацию аниона SO2-. Так как в электролит вводится заведомо большее количество сернокислого стронция и кремнефтористого калия, то частично они находятся в виде осадка на дне ванны и частично — в растворе в виде ионов. По мере уноса раствора осадок растворяется и пополняет убыль аниона SO2-.
Электролит менее чувствителен к возможным колебаниям температур и плотностей тока, чем стандартный, и, следовательно, не вызывает отслаивания хрома при невольных нарушениях режима. Наконец, электролит позволяет при той же силе тока, что и в стандартном, производить осаждение хрома в 1,4—1,5 раза быстрее за счет более высокого выхода по току.
Наконец, электролит позволяет при той же силе тока, что и в стандартном, производить осаждение хрома в 1,4—1,5 раза быстрее за счет более высокого выхода по току.
Несмотря на свои высокие достоинства, саморегулирующиеся электролиты не получили широкого применения, так как имеют весьма существенные недостатки, основным из которых является наличие агрессивного аниона F— в составе электролита. Это обстоятельство приводит к быстрому разрушению свинцовой футеровки хромовых ванн, особенно по сварочным швам. В результате, взамен рольного свинца футеровку ванн необходимо производить керамикой, винипластом, пентапластом, поливинилхлоридом и прочими материалами. По этой же причине непригодны и свинцовые аноды. Взамен им приходится применять аноды из свинцово-оловянного сплава, с содержанием олова — от 6 до 10 %.
Тетрахроматный электролит
Из электролитов, не требующих подогрева, некоторое промышленное применение получил так называемый тетрахроматный электролит, для которого рекомендуются следующий состав (г/л) и режим работы (ГОСТ 9. 047):
047):
хромовый ангидрид — 350—400; серная кислота — 2,5—3,0; едкий натр —40—60; хром трехвалентный — 10—15; температура, °С — 15—30; плотность тока, А/дм2 — 10—60; выход по току, % — 25—30.
Электролит отличается повышенной рассеивающей способностью, но хромовые покрытия имеют серый, матовый вид и в 2— 3 раза меньшую твердость, чем осадки из стандартного электролита. Поэтому хромовые покрытия из тетрахромового электролита применяют лишь в качестве защитного покрытия с использованием меди, никеля или цинка в качестве подслоя.
Для скорейшего образования трехвалентного хрома в необходимом количестве для правильной эксплуатации в представленный электролит вводят при приготовлении до 0,5-0,6 г/л сахара. Электролит менее агрессивен, чем стандартный, и в нем можно непосредственно хромировать детали из латуни, цинковых сплавов и других химически нестойких металлов. Так как электролит не требует подогрева, то в качестве поплавков для предохранения электролита от уноса в вентиляционные отсосы можно использовать кусочки дерева, пропитанные парафином. В связи с тем, что плотности тока при хромировании весьма велики, электролит может перегреваться выше допустимых температур (23-24 °С).
В связи с тем, что плотности тока при хромировании весьма велики, электролит может перегреваться выше допустимых температур (23-24 °С).
Электролит для реверсирования
При электроосаждении периодическое изменение направления постоянного тока существенно изменяет некоторые свойства покрытий. Одна из характерных особенностей хромирования с применением реверсирования тока — возможность получения покрытия толщиной 800 мкм и более с малыми внутренними напряжениями. Хромирование проводят при следующем составе (г/л) и режимах:
хромовый ангидрида — 200-250; серная кислота — 2-2,5; температура электролита, °С — 50-60; катодная плотность тока, А/дм2 — 120 длительность катодного периода, мин — 1-5; длительность анодного периода, с — 5-25.
Реверсирование позволяет ускорить процесс осаждения хрома в 1,5-2 раза по сравнению с обычными электролитами.
При покрытии деталей хромом в проточном электролите при тех же плотностях тока возможно получить осадок высокого качества и значительной толщины. Процесс нанесения покрытия при этом ускоряется в 6-10 раз по сравнению с обычным хромированием. С увеличением скорости протекания электролита от 0 до 200 см/с микротвердость осажденного металла повышается от 7000 до 10000 МПа при ведении процесса с плотностью тока 45 А/дм2 и температуре электролита 45 °С. Равномерность осаждения и износостойкость хрома при наращивании в проточном электролите выше, чем при хромировании в непроточном электролите. Особенно эффективно применение проточного электролита для наращивания внутренних поверхностей деталей.
Процесс нанесения покрытия при этом ускоряется в 6-10 раз по сравнению с обычным хромированием. С увеличением скорости протекания электролита от 0 до 200 см/с микротвердость осажденного металла повышается от 7000 до 10000 МПа при ведении процесса с плотностью тока 45 А/дм2 и температуре электролита 45 °С. Равномерность осаждения и износостойкость хрома при наращивании в проточном электролите выше, чем при хромировании в непроточном электролите. Особенно эффективно применение проточного электролита для наращивания внутренних поверхностей деталей.
К типу многослойных покрытий может быть отнесено так называемое двухслойное хромовое покрытие. Последнее получают при нанесении различных осадков хрома с изменяющимися свойствами. Если необходимо защитить деталь от коррозии при одновременном увеличении ее износостойкости, наносят два слоя хрома: нижний — беспористый молочный и верхний — блестящий.
Таблица 5.2. Скорость наращивания хрома, мкм/ч.
|
Плотность тока, А/дм2 |
Катодный выход по току, % |
|||
|
12 |
14 |
16 |
18 |
|
|
20 |
11,6 |
13,5 |
15,5 |
17,5 |
|
40 |
23,2 |
27,0 |
31,0 |
35,0 |
|
60 |
34,9 |
40,6 |
46,5 |
52,5 |
|
80 |
46,5 |
54,2 |
62,0 |
70,0 |
|
100 |
58,1 |
67,7 |
77,3 |
86,9 |
Слой молочного хрома толщиной 15 мкм осаждают при температуре 70 °С и плотности тока 30 А/дм2. Затем непромытая деталь переносится в ванну с более низкой температурой электролита, где на матовый слой наносится слой блестящего износостойкого хрома толщиной 35 мкм и более. Температура электролита — 50 °С, плотность тока — 50 А/дм2. Хромирование производят в двух ваннах с электролитом одинакового состава (250 г/л хромового ангидрида и 1-5 г/л серной кислоты).
Затем непромытая деталь переносится в ванну с более низкой температурой электролита, где на матовый слой наносится слой блестящего износостойкого хрома толщиной 35 мкм и более. Температура электролита — 50 °С, плотность тока — 50 А/дм2. Хромирование производят в двух ваннах с электролитом одинакового состава (250 г/л хромового ангидрида и 1-5 г/л серной кислоты).
Скорость наращивания хрома ориентировочно можно определить по данным табл. 5.2.
Возможно Вас так же заинтересуют следующие статьи: comments powered by HyperCommentsХромовый ангидрид
Технология минеральных солей (удоБрений, пестицидов, промышленных солей, окислов и кислот)
Применяемые методы получения хромового ангидрида основаны на обработке хромпиков концентрированной серной кислотой:
Na2Cr207 + 2h3S04 = 2Cr03 + 2NaHS04 + h30
В стальной реактор с мешалкой и наружным электрообогревом загружают плав бихромата натрия (60—65% СгОз) и добавляют 92—93%-ную серную кислоту (несколько меньше стехиометрического количества). Реакционную массу нагревают в течение 1,5— 2 ч, при этом вначале она вспенивается в результате интенсивного удаления водяного пара, с которым уходят и образующиеся (из содержащейся в исходном бихромате примеси NaCl) газы — С12. НС1 и Сг02С12; отходящий газ для улавливания этих веществ промывают в скрубберах раствором соды. По окончании вспенивания добавляют остальное количество серной кислоты (до ~105% от стехиометрического) и поднимают температуру в реакторе немного выше 200°. Это обусловлено температурами плавления бисульфата натрия (186°) и хромового ангидрида (~200°), Нагревание массы выше 205° приводит к быстрому разложению Сг03 с выделением кислорода и образованием соединений СгОз с Сг2038’194.
Реакционную массу нагревают в течение 1,5— 2 ч, при этом вначале она вспенивается в результате интенсивного удаления водяного пара, с которым уходят и образующиеся (из содержащейся в исходном бихромате примеси NaCl) газы — С12. НС1 и Сг02С12; отходящий газ для улавливания этих веществ промывают в скрубберах раствором соды. По окончании вспенивания добавляют остальное количество серной кислоты (до ~105% от стехиометрического) и поднимают температуру в реакторе немного выше 200°. Это обусловлено температурами плавления бисульфата натрия (186°) и хромового ангидрида (~200°), Нагревание массы выше 205° приводит к быстрому разложению Сг03 с выделением кислорода и образованием соединений СгОз с Сг2038’194.
Реакция образования Сг03 на самом деле сложнее, чем приведенная выше, так как в системе Na20—Cr03—S03—Н20 могут существовать при разных температурах, помимо представленных в уравнении, и другие соединения, например, Na2S04, Na3H(S04)2- •Н20, Na3H(S04)2177. Кроме того, в небольшой мере идут побочные реакции диссоциации СгОз и образования сульфата хрома и его двойных соединений с сульфатом натрия и серной кислотой. Соединения трехвалентного хрома появляются вследствие реакций: 2Na2Cr207 + 10H, S04 = 2Cr2(S04)3 + 4NaHS04 + 8h30 + 302 4Cr03 + 6h3S04 = 2Cr2(S04)3 + 6h30 + 302
Соединения трехвалентного хрома появляются вследствие реакций: 2Na2Cr207 + 10H, S04 = 2Cr2(S04)3 + 4NaHS04 + 8h30 + 302 4Cr03 + 6h3S04 = 2Cr2(S04)3 + 6h30 + 302
Сульфат хрома образует с серной кислотой нерастворимые безводные кислые сульфаты хрома 2Cr2(S04)3 • h3S04, Cr2(S04b — •h3S04 и другие, а также соли Na[Cr(S04)2] и Na3[Cr(S04b] и кислые соли х Na2S04 • у Cr2(S04)3 • г h3S04.
После завершения реакции плав сливают в отстойник, снабженный наружными электроподогревателями. Вследствие разности плотностей расплавленных хромового ангидрида и бисульфата натрия (при 200° плотность Сг03 —2,30 г/см3, плотность NaHS04 ~ 2,05 г/см3) и незначительной взаимной растворимости этих веществ, они расслаиваются. Скапливающийся в низу отстойника
жидкий хромовый ангидрид направляют на охлаждаемые изнутри водой полые барабаны — вальцы, на поверхности которых он застывает и снимается ножами в виде чешуйчатого продукта, который укупоривают в стальные барабаны. После слива хромового ангидрида из отстойника выпускают бисульфат натрия — его используют для травки хромата натрия, которую осуществляют в этом случае здесь же, в цехе хромового ангидрида ввиду трудности транспорта расплавленного бисульфата в бихроматный цех. Из 1 т хромового ангидрида получают более 1,5 т бисульфата натрия. Он содержит ~3,5% Сг08, 2% Сг203 и 32—33% титруемой H2S04.
После слива хромового ангидрида из отстойника выпускают бисульфат натрия — его используют для травки хромата натрия, которую осуществляют в этом случае здесь же, в цехе хромового ангидрида ввиду трудности транспорта расплавленного бисульфата в бихроматный цех. Из 1 т хромового ангидрида получают более 1,5 т бисульфата натрия. Он содержит ~3,5% Сг08, 2% Сг203 и 32—33% титруемой H2S04.
Полученный продукт содержит более 99% СЮ3. Использование хрома составляет ~96%- На 1 г хромового ангидрида (98% СгОз) расходуется: 1,52 т бихромата натрия (67,1% Сг03) и 1,29 т серной кислоты (100%).
Применение бихроматного плава с содержанием 68—70% Сг03 (вместо 63%) позволяет сократить продолжительность плавки на 20—40%, а замена купоросного масла олеумом (103—104% h3S04) приводит к сокращению продолжительности процесса в 3 раза 195.
Предложено производить очистку хромового ангидрида добавкой к нему кристаллического бихромата и его насыщенного водного раствора и нагреванием массы до плавления. При этом плаБ расслаивается, — в нижний слой переходит чистый Сг03, а в верхний — загрязнения 196.
При этом плаБ расслаивается, — в нижний слой переходит чистый Сг03, а в верхний — загрязнения 196.
Из общего количества Сг203, содержащейся в бисульфате, до 0,5% (абсол.) находится в форме водорастворимых соединений. Можно уменьшить их содержание (до 0,05% Сг203) выдерживанием бисульфата в смеси с 15% Na2S04 (для предотвращения разложения Сг03) при 185° в течение 1 ч. При этом разлагается лишь 5—!0% от содержавшегося в бисульфате Сг03, а Сг203 почти полностью переходит в нерастворимые соединения, которые могут ■быть отделены при приготовлении раствора бисульфата 197. При использовании бисульфата для травки желтого щелока содержащиеся в нем нерастворимые примеси отделяются после травки вместе с выделяющимся сульфатом натрия. Оставшиеся в щелоке водорастворимые соединения Сг3+ окисляют гипохлоритом 198»».
За рубежом запатентован и осуществлен, так же как и в СССР, непрерывный способ производства хромового ангидрида 200.201. Бихромат и серная кислота смешиваются и взаимодействуют, проходя последовательно шнековые аппараты, в последнем из которых поддерживают температуру выше точки плавления СгОз, за» тем плав разделяется в непрерывно действующем отстойнике; из него хромовый ангидрид поступает на охлаждаемые вальцы для получения чешуйчатого продукта, а бисульфат используется для травки хроматного щелока. Непрерывный способ обеспечивает возможность полной автоматизации производства.
Непрерывный способ обеспечивает возможность полной автоматизации производства.
Хромовый ангидрид может быть получен из монохроматных (желтых) щелоков через хромат кальция по следующей схеме: хромат кальция осаждают обработкой хроматного щелока хлоридом кальция при кипячении; отфильтрованный и промытый хромат кальция разлагают серной кислотой, причем образуются гипс и раствор Сг03; гипс отделяют на фильтре и раствор выпаривают для получения твердого Сг03202. Материалом для выпарного аппарата может служить титан.
Описано много других путей получения СгОз (например, разложение хромата натрия азотной кислотой 195), но они пока не имеют промышленного значения.
Родентициды это средства защиты от грызунов. Их применяют для уничтожения крыс, мышей и некоторых видов диких хомяков. Применять их в качестве уничтожителя начинают в том случае, если грызуны становятся стихийным …
При взаимодействии хлорита натрия с хлором происходит образование хлористого натрия и выделяется двуокись хлора: 2NaC102 + С12 = 2NaCl + 2 СЮ2 Этот способ ранее был основным для получения двуокиси …
На рис. 404 представлена схема производства диаммонитро — фоски (типа TVA). Фосфорная кислота концентрацией 40—42,5% Р2О5 из сборника 1 насосом 2 подается в напорный бак 3, из которого она непрерывно …
404 представлена схема производства диаммонитро — фоски (типа TVA). Фосфорная кислота концентрацией 40—42,5% Р2О5 из сборника 1 насосом 2 подается в напорный бак 3, из которого она непрерывно …
Способ получения хромового ангидрида
Изобретение относится к получению хромового ангидрида и может быть использовано в химической промышленности. Способ получения хромового ангидрида из высококонцентрированного раствора бихромата натрия включает взаимодействие бихромата натрия с серной кислотой в реакторе при непосредственном контакте реакционной массы с дымовым газом, полученным при сжигании природного газа, сопровождающееся плавлением образующегося хромового ангидрида и бисульфата натрия, и последующее разделение хромового ангидрида и бисульфата натрия путем отстаивания. При этом высококонцентрированный раствор бихромата натрия обрабатывают дымовым газом от сжигания природного газа при непосредственном контакте дымового газа и раствора с образованием твердой фазы, состоящей из безводных кристаллов бихромата натрия. Изобретение позволяет сократить время контакта реакционной массы и дымового газа в реакторе, снизить габаритные размеры реактора, увеличить интенсивность процесса и выход продукта, улучшить коррозионные условия работы реактора. 6 з.п. ф-лы, 2 ил.
Изобретение позволяет сократить время контакта реакционной массы и дымового газа в реакторе, снизить габаритные размеры реактора, увеличить интенсивность процесса и выход продукта, улучшить коррозионные условия работы реактора. 6 з.п. ф-лы, 2 ил.
Настоящее изобретение относится к технологии неорганических соединений, в частности к технологии соединений хрома, и может быть использовано в химической промышленности.
Известен способ получения хромового ангидрида, основанный на взаимодействии бихромата натрия и серной кислоты с доведением температуры реакционной смеси примерно до 200°С. Образующийся при этом жидкий хромовый ангидрид и жидкий бисульфат натрия мало растворимы друг в друге и легко разделяются механически благодаря разнице удельных весов. Исходный бихромат натрия поступает в производство хромового ангидрида в виде высококонцентрированного раствора (содержание бихромата натрия в исходном растворе составляет не менее 925 г /литр в пересчете на СrO3). Собственно производство хромового ангидрида включает в себя концентрирование исходного раствора (предварительная упарка раствора до ~1100 г/литр в пересчете на Сr2О3 и последующее удаление влаги с получением плава с концентрацией 60-65% СrO3), разложение плава серной кислотой (стадия выплавки), отстаивание и разделение хромового ангидрида и бисульфата натрия (см., например, Т.Д.Авербух и П.Г.Павлов. «Технология соединений хрома». Изд. «Химия», Л.О., 1967 год, с.236-251).
Собственно производство хромового ангидрида включает в себя концентрирование исходного раствора (предварительная упарка раствора до ~1100 г/литр в пересчете на Сr2О3 и последующее удаление влаги с получением плава с концентрацией 60-65% СrO3), разложение плава серной кислотой (стадия выплавки), отстаивание и разделение хромового ангидрида и бисульфата натрия (см., например, Т.Д.Авербух и П.Г.Павлов. «Технология соединений хрома». Изд. «Химия», Л.О., 1967 год, с.236-251).
Данный способ имеет ряд существенных недостатков, основные из которых состоят в периодическом характере проходящих процессов, высоких затратах тепловой энергии, в сниженном качестве продукта, в высоких эксплуатационных затратах и малой интенсивности процесса.
Известен способ получения хромового ангидрида, включающий взаимодействие бихромата натрия и серной кислоты, причем оба компонента находятся в безводном состоянии (см. патент США №1872588 от 16 августа 1932 года; см. также указанный выше источник, с. 253-254). Сложные технологические и коррозионные условия не позволили данному способу найти промышленное применение.
253-254). Сложные технологические и коррозионные условия не позволили данному способу найти промышленное применение.
Наиболее близким к настоящему изобретению является способ получения хромового ангидрида путем взаимодействия бихромата натрия с серной кислотой, сопровождающийся плавлением продуктов реакции и последующим их разделением в расплавленном виде, причем процесс взаимодействия проводят при непосредственном контакте реакционной массы с газообразным теплоносителем (см. авторское свидетельство СССР №292459, дата опубликования 05.05.1972 года, бюллетень №15). Согласно приведенному в описании примеру и опыту эксплуатации установки, реализующей данный способ, исходными веществами являются концентрированный раствор бихромата натрия и техническая серная кислота, а собственно процесс взаимодействия проводят во вращающемся барабанном реакторе, причем в качестве газообразного теплоносителя используют дымовой газ от сжигания природного газа.
Данный способ получения хромового ангидрида отличается рядом преимуществ, основными из которых является реализация непрерывного процесса и снижение энергетических и эксплуатационных затрат.
Однако данному способу присущ и ряд недостатков. Из-за необходимости удаления влаги, поступающей с исходными реагентами, возрастает время пребывания реакционной массы в барабанном реакторе. При этом снижается интенсивность процесса и увеличивается время пребывания реакционной массы в реакторе, что в свою очередь приводит к снижению качества продукта из-за разложения хромового ангидрида. Соответственно, при увеличении времени пребывания реакционной массы в барабанном реакторе увеличиваются габариты последнего. Ухудшаются и коррозионные условия работы реактора из-за разбавления серной кислоты в начале процесса при смешении исходных компонентов.
Техническая задача настоящего изобретения состоит в создании модернизированного способа получения хромового ангидрида.
Технический результат настоящего изобретения состоит в сокращении времени контакта реакционной массы и дымового газа в реакторе, соответственно в снижении габаритов и увеличении интенсивности процесса, в увеличении выхода продукта и улучшении коррозионных условий работы реактора.
Для достижения указанного технического результата в способе получения хромового ангидрида из высококонцентрированного раствора бихромата натрия, включающем взаимодействие бихромата натрия с серной кислотой в реакторе при непосредственном контакте реакционной массы с дымовым газом, полученным при сжигании природного газа, сопровождающееся плавлением образующегося хромового ангидрида и бисульфата натрия, и последующее разделение хромового ангидрида и бисульфата натрия в расплавленном состоянии путем отстаивания, высококонцентрированный раствор бихромат натрия обрабатывают дымовым газом от сжигания природного газа при непосредственном контакте дымового газа и раствора с образованием твердой фазы, состоящей из безводных кристаллов бихромата натрия. Обработку высококонцентрированного раствора бихромата натрия дымовым газом от сжигания природного газа проводят в распылительной сушилке или в аппарате кипящего слоя, полученные безводные кристаллы бихромата натрия в сухом виде смешивают с серной кислотой в смесителе механического типа, а полученную реакционную массу направляют в реактор. В другом варианте обработку высококонцентрированного раствора бихромата натрия дымовым газом от сжигания природного газа проводят в прямоточном распыливающем скруббере, полученную суспензию, твердой составляющей которой являются безводные кристаллы бихромата натрия, разделяют на центрифуге, снятый с центрифуги осадок смешивают с серной кислотой в смесителе механического типа, полученную реакционную массу направляют в реактор, а маточный раствор возвращают на орошение прямоточного распыливающего скруббера. Реактор выполняют в виде тарельчатого барботажного массообменного аппарата. Отработанный дымовой газ используют для нагревания воздуха, поступающего на сжигание природного газа, или исходных реагентов. Температуру дымового газа перед подачей на обработку высококонцентрированного раствора в аппарате кипящего слоя или распылительной сушилке поддерживают на уровне не выше 400°С, а после обработки — не ниже 120-150°С. Температуру высококонцентрированного раствора в ходе обработки его дымовым газом в прямоточном распыливающем скруббере поддерживают на уровне не ниже 85°С за счет регулирования температуры дымового газа перед обработкой.
В другом варианте обработку высококонцентрированного раствора бихромата натрия дымовым газом от сжигания природного газа проводят в прямоточном распыливающем скруббере, полученную суспензию, твердой составляющей которой являются безводные кристаллы бихромата натрия, разделяют на центрифуге, снятый с центрифуги осадок смешивают с серной кислотой в смесителе механического типа, полученную реакционную массу направляют в реактор, а маточный раствор возвращают на орошение прямоточного распыливающего скруббера. Реактор выполняют в виде тарельчатого барботажного массообменного аппарата. Отработанный дымовой газ используют для нагревания воздуха, поступающего на сжигание природного газа, или исходных реагентов. Температуру дымового газа перед подачей на обработку высококонцентрированного раствора в аппарате кипящего слоя или распылительной сушилке поддерживают на уровне не выше 400°С, а после обработки — не ниже 120-150°С. Температуру высококонцентрированного раствора в ходе обработки его дымовым газом в прямоточном распыливающем скруббере поддерживают на уровне не ниже 85°С за счет регулирования температуры дымового газа перед обработкой.
Сущность настоящего изобретения состоит в следующем.
Предлагаемый способ и известные способы получения хромового ангидрида основаны на следующей реакции:
Na2Cr2O7+2H2SO4=2NaHSO4+2СrO3+Н2O.
При доведении температуры примерно до 200°С образующиеся бисульфат натрия и хромовый ангидрид находятся в жидком виде и благодаря малой растворимости друг в друге и разнице удельных весов легко разделяются механически.
Необходимый для реакции бихромат натрия поступает в производство хромового ангидрида в виде раствора. Для сокращения времени пребывания и снижения габаритов реактора при применении периодического процесса исходный раствор обычно упаривают в выпарных аппаратах до содержания в растворе основного вещества на уровне 1100 г/литр в пересчете на СrО3, а далее в уварочных котлах доводят раствор до состояния плава с содержанием бихромата натрия на уровне 60-65% в расчете на СrO3. Процесс концентрирования мало интенсивен и сопровождается затратой достаточно дорогого пара и значительными потерями тепловой энергии.
Процесс концентрирования мало интенсивен и сопровождается затратой достаточно дорогого пара и значительными потерями тепловой энергии.
В известном непрерывном способе получения хромового ангидрида процессы взаимодействия исходных реагентов и плавления конечных продуктов проходят в барабанном вращающемся реакторе, нагреваемом дымовым газом от сжигания природного газа. Непрерывный способ получения хромового ангидрида принципиально позволяет применять непосредственно исходный раствор без его предварительной подготовки. При этом важно отметить следующее.
В барабанном реакторе, как и в емкостных реакторах периодического действия, основное время пребывания реакционной массы определяется необходимостью удаления воды, как поступающей с исходными веществами, так и образующейся в ходе реакции. Учитывая, что одновременно с образованием хромового ангидрида проходит и его термическая диссоциация, связанная со снижением качества и выхода продукта, целесообразно снижение времени пребывания реакционной массы в реакторе. Для достижения этого в непрерывном процессе получения хромового ангидрида в реактор целесообразно подавать бихромат натрия в безводном виде. При малом содержании воды в исходной серной кислоте в этом случае из реактора необходимо удалять в основном воду, образованную в ходе реакции.
Для достижения этого в непрерывном процессе получения хромового ангидрида в реактор целесообразно подавать бихромат натрия в безводном виде. При малом содержании воды в исходной серной кислоте в этом случае из реактора необходимо удалять в основном воду, образованную в ходе реакции.
Получение собственно безводного бихромата натрия в настоящее время также основано на использовании исходного раствора, содержащего не менее 925 г/литр в пересчете на СrО3 бихромата натрия, концентрировании исходного раствора до содержания основного вещества на уровне 1100 г/литр в пересчете на СrО3 и последующей уварке в котлах с получением суспензии, твердой составляющей которой является безводный бихромат натрия. Полученную суспензию разделяют на центрифугах. Из-за затрат дорогого пара и соответственно высокой стоимости безводного бихромата натрия применение полученного подобным образом безводного бихромата натрия в производстве хромового ангидрида нецелесообразно. Настоящее изобретение в целом основано на предварительной обработке исходного раствора бихромата натрия дымовым газом от сжигания природного газа в ходе их непосредственного контакта.
Основные преимущества предлагаемых способов получения хромового ангидрида целесообразно изложить в ходе описания собственно технологических схем и их работы.
Принципиальная технологическая схема, реализующая первый вариант настоящего изобретения, приведена на фиг.1.
Исходный раствор бихромата натрия из бака 1 подают в аппарат кипящего слоя или распылительную сушилку 2, где его обрабатывают дымовым газом от сжигания природного газа. Отработанный дымовой газ очищают от твердых включений в системе сухого пылеулавливания 3. Безводный бихромат натрия в сухом виде из аппарата 2 и системы сухого пылеулавливания 3 подают в смеситель 4 механического типа. В качестве такового может быть принят, например, широко известный двухвальный смеситель шнекового типа или лопастный смеситель с выгрузочным шнеком. В смеситель 4 одновременно подают серную кислоту из бака 5. Из смесителя 4 реакционную смесь направляют в реактор 6, который на фиг.1 показан в виде традиционного вращающегося барабана. В реактор одновременно подают дымовой газ от сжигания природного газа из другого источника. Из реактора 6 бисульфат натрия и хромовый ангидрид в расплавленном состоянии подают в отстойник 7, где происходит разделение полученного плава.
В реактор одновременно подают дымовой газ от сжигания природного газа из другого источника. Из реактора 6 бисульфат натрия и хромовый ангидрид в расплавленном состоянии подают в отстойник 7, где происходит разделение полученного плава.
Принципиальная технологическая схема, реализующая случай применения в качестве аппарата для обработки исходного раствора бихромата натрия дымовым газом прямоточного распыливающего скруббера, приведена на фиг.2.
Исходный раствор бихромата натрия подают из бака 1 в прямоточный распыливающий скруббер 2. В скруббер 2 подают одновременно дымовой газ, полученный в ходе сжигания природного газа. Из скруббера 2 поток, включающий в себя газ, жидкость и твердую составляющую, представляющую собой безводные кристаллы бихромата натрия, направляют в бак-расширитель 3. Далее отработанный газ с остающимися брызгами подают в систему брызгоулавливания 4. Уловленные брызги попадают обратно в бак-расширитель 3. Полученная суспензия из бака-расширителя 3 поступает на центрифугу 5. Влажный осадок, снимаемый с центрифуги 5, с жидкой составляющей, содержащей небольшое количество воды, подают в смеситель механического типа 6. Фугат из центрифуги 5 поступает в бак 7 и из него в бак 1. В смеситель механического типа 6 одновременно подают серную кислоту из бака 8. Реакционную смесь из смесителя механического типа направляют в реактор 9. Обычно реактор 9, как указано выше, выполняют в виде вращающегося барабана. Одновременно в реактор 9 подают дымовой газ, полученный при сжигании природного газа, из другого источника. Из реактора 9 бисульфат натрия и хромовый ангидрид в расплавленном виде подают на разделение в отстойник 10.
Влажный осадок, снимаемый с центрифуги 5, с жидкой составляющей, содержащей небольшое количество воды, подают в смеситель механического типа 6. Фугат из центрифуги 5 поступает в бак 7 и из него в бак 1. В смеситель механического типа 6 одновременно подают серную кислоту из бака 8. Реакционную смесь из смесителя механического типа направляют в реактор 9. Обычно реактор 9, как указано выше, выполняют в виде вращающегося барабана. Одновременно в реактор 9 подают дымовой газ, полученный при сжигании природного газа, из другого источника. Из реактора 9 бисульфат натрия и хромовый ангидрид в расплавленном виде подают на разделение в отстойник 10.
Применение безводных кристаллов бихромата натрия в технологии хромового ангидрида позволяет упростить аппаратурное оформление, снизить капитальные затраты и интенсифицировать процесс получения хромового ангидрида. Прежде всего это касается собственно реактора.
В настоящем изобретении предусмотрено изменение конструкции реактора. Реактор целесообразно выполнить в виде барботажного тарельчатого массообменного аппарата, продуваемого дымовым газом от сжигания природного газа (см. , например, В.М.Рамм. «Абсорбция газов». — М.: Химия, 1976 год, с.422-436). При поддержании необходимых температур процесс образования хромового ангидрида проходит в обычном режиме. На тарелках находится жидкий хромовый ангидрид и бисульфат натрия в расплавленном состоянии. Процесс проходит в условиях активного перемешивания реагентов дымовым газом. При этом одновременно возникает известный эффект улучшения качества получаемого продукта, благодаря переходу примесей в бисульфат натрия при продувке реакционной смеси (см. авторское свидетельство СССР №1168511, опубликовано 23.07.1985 года, бюл. №27).
, например, В.М.Рамм. «Абсорбция газов». — М.: Химия, 1976 год, с.422-436). При поддержании необходимых температур процесс образования хромового ангидрида проходит в обычном режиме. На тарелках находится жидкий хромовый ангидрид и бисульфат натрия в расплавленном состоянии. Процесс проходит в условиях активного перемешивания реагентов дымовым газом. При этом одновременно возникает известный эффект улучшения качества получаемого продукта, благодаря переходу примесей в бисульфат натрия при продувке реакционной смеси (см. авторское свидетельство СССР №1168511, опубликовано 23.07.1985 года, бюл. №27).
Замена обычно применяемого в технологии хромового ангидрида барабанного реактора на барботажный тарельчатый массообменный аппарат в значительной мере упрощает аппаратурное оформление технологической схемы и способствует увеличению интенсивности процесса, поскольку вращающийся барабанный реактор имеет значительный объем, сложен по конструкции и по условиям эксплуатации (см., например, авторское свидетельство СССР №1084061, опубликовано 07. 04.1984 года, бюл. №13).
04.1984 года, бюл. №13).
Пример.
Для получения 10000 т/год хромового ангидрида (1320 кг/час с учетом выхода на уровне 97%) потребно ввести в процесс 2580 кг/час раствора бихромата натрия с концентрацией 1000 г/литр по СrO3. Исходный раствор подают в аппарат кипящего слоя, где проходит его обработка дымовым газом от сжигания природного газа. Дымовой газ вводят в аппарат кипящего слоя с температурой 400°С. Температура дымового газа на выходе из аппарата 140°С. При обработке раствора бихромата натрия дымовым газом при непосредственном контакте получают 1785 кг/час безводного бихромата натрия. Безводный бихромат натрия смешивают с серной кислотой, имеющей концентрацию 92,5% H2SO4, в двухвальном шнековом смесителе. В смеситель подают 1440 кг/час серной кислоты. Полученную реакционную массу далее направляют во вращающийся барабанный реактор диаметром 1,2 м и длиной 9 м. В барабанный реактор одновременно подают дымовой газ от сжигания природного газа с температурой 400°С.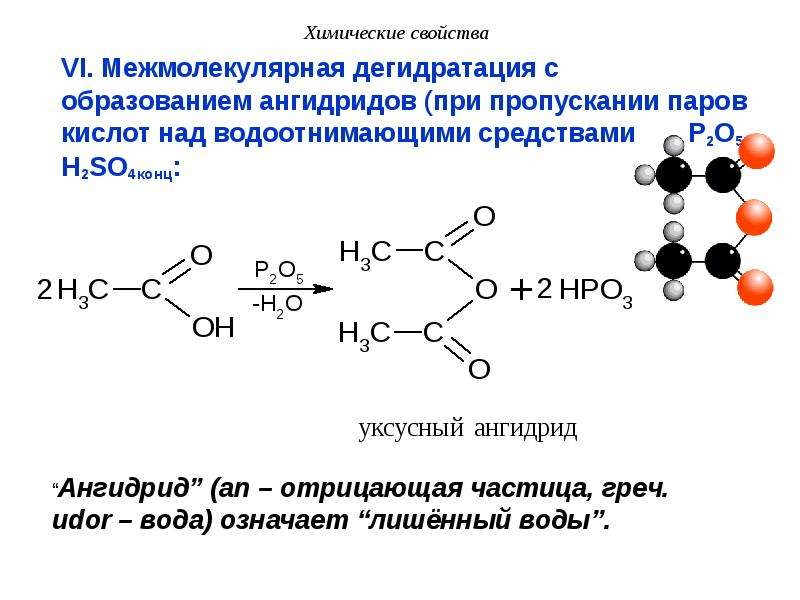 Из барабанного реактора выводят дымовой газ с температурой 250°С. Реакционную массу из барабанного реактора направляют в отстойник, где проходит разделение образовавшегося бисульфата натрия и хромового ангидрида.
Из барабанного реактора выводят дымовой газ с температурой 250°С. Реакционную массу из барабанного реактора направляют в отстойник, где проходит разделение образовавшегося бисульфата натрия и хромового ангидрида.
Барабанный реактор в известном способе непрерывного получения хромового ангидрида имел бы длину, равную 14 м. Следовательно, процесс по настоящему изобретению, в соответствии с приведенными цифрами, более интенсивен по сравнению с известным непрерывным способом получения хромового ангидрида.
Как указано выше, в смеситель механического типа направляют серную кислоту и безводный бихромат натрия. Если безводные кристаллы бихромата натрия получены в аппарате кипящего слоя или в распылительной сушилке, они практически не содержат влаги. Кристаллы безводного бихромата натрия, полученные при проведении обработки концентрированного раствора бихромата натрия дымовым газом в прямоточном распыливающем скруббере с последующим отделением твердой составляющей суспензии на центрифуге, содержат малое количество влаги. Таким образом, в смесителе механического типа не происходит разбавления серной кислоты. При вводе в барабанный реактор реакционной массы, полученной в двухвальном шнековом смесителе, практически не наблюдается значительного коррозионного износа корпуса реактора. С раствором бихромата натрия в известном способе в барабанный реактор вводят 730 кг Н2О, т.е. в начале процесса в реакторе присутствует кислота с концентрацией 61,3% H2SO4, представляющая собой чрезвычайно активный коррозионный агент. В барабанном реакторе при реализации известного способа получения хромового ангидрида для предотвращения выхода из строя реактора и снижения активного коррозионного износа предусмотрен вкладыш из титана. В барабанном реакторе, реализующем настоящее изобретение, подобный прием не используется при одновременном увеличении срока службы корпуса реактора, причем корпус реактора выполняют из обычной стали.
Таким образом, в смесителе механического типа не происходит разбавления серной кислоты. При вводе в барабанный реактор реакционной массы, полученной в двухвальном шнековом смесителе, практически не наблюдается значительного коррозионного износа корпуса реактора. С раствором бихромата натрия в известном способе в барабанный реактор вводят 730 кг Н2О, т.е. в начале процесса в реакторе присутствует кислота с концентрацией 61,3% H2SO4, представляющая собой чрезвычайно активный коррозионный агент. В барабанном реакторе при реализации известного способа получения хромового ангидрида для предотвращения выхода из строя реактора и снижения активного коррозионного износа предусмотрен вкладыш из титана. В барабанном реакторе, реализующем настоящее изобретение, подобный прием не используется при одновременном увеличении срока службы корпуса реактора, причем корпус реактора выполняют из обычной стали.
В известном способе выход готового продукта не превышает 96% из-за имеющего место разложения хромового ангидрида при повышенном времени пребывания реакционной массы в реакторе.
Таким образом, в настоящем изобретении решена поставленная задача и достигнут заявленный технический результат.
1. Способ получения хромового ангидрида из высококонцентрированного раствора бихромата натрия, включающий взаимодействие бихромата натрия с серной кислотой в реакторе при непосредственном контакте реакционной массы с дымовым газом, полученным при сжигании природного газа, сопровождающееся плавлением образующегося хромового ангидрида и бисульфата натрия, и последующее разделение хромового ангидрида и бисульфата натрия в расплавленном состоянии путем отстаивания, отличающийся тем, что высококонцентрированный раствор бихромата натрия обрабатывают дымовым газом от сжигания природного газа при непосредственном контакте дымового газа и раствора с образованием твердой фазы, состоящей из безводных кристаллов бихромата натрия.
2. Способ получения хромового ангидрида по п.1, отличающийся тем, что обработку высококонцентрированного раствора бихромата натрия дымовым газом от сжигания природного газа проводят в распылительной сушилке или в аппарате кипящего слоя, полученные безводные кристаллы бихромата натрия в сухом виде смешивают с серной кислотой в смесителе механического типа, а полученную реакционную массу направляют в реактор.
3. Способ получения хромового ангидрида по п.1, отличающийся тем, что обработку высококонцентрированного раствора бихромата натрия дымовым газом от сжигания природного газа проводят в прямоточном распыливающем скруббере, полученную суспензию, твердой составляющей которой являются безводные кристаллы бихромата натрия, разделяют на центрифуге, снятый с центрифуги осадок смешивают с серной кислотой в смесителе механического типа, полученную реакционную массу направляют в реактор, а маточный раствор возвращают на орошение прямоточного распыливающего скруббера.
4. Способ получения хромового ангидрида по п.1, отличающийся тем, что реактор выполняют в виде тарельчатого барботажного массообменного аппарата.
5. Способ получения хромового ангидрида по п.1, отличающийся тем, что отработанный дымовой газ используют для нагревания воздуха, поступающего на сжигание природного газа, или исходных реагентов.
6. Способ получения хромового ангидрида по п.1 или 2, отличающийся тем, что температуру дымового газа перед подачей на обработку высококонцентрированного раствора поддерживают на уровне не выше 400°С, а после обработки — не ниже 120-150°С.
7. Способ получения хромового ангидрида по п.1 или 3, отличающийся тем, что температуру высококонцентрированного раствора в ходе обработки его дымовым газом поддерживают на уровне не ниже 85°С за счет регулирования температуры дымового газа перед обработкой.
Основное применение технической пигментной окиси хрома
Оксид хрома (III) (химическая формула — Cr2O3) – твёрдый тонкодисперсный порошок оливкового оттенка зелёного цвета. Известен также как хромовая зелень. Его полезными физико-химическими свойствами является высокая укрывистость, устойчивость к свету и действию агрессивных газов, атмосферостойкость. Соединение хрома с кислородом нерастворимо в воде, почти не растворимо в щелочах и разбавленных кислотах. В то же время оно настолько твёрдое, что способно повредить поверхность кварца.
Основное применение хромовой зелени исходит из его свойств и сосредоточено в лакокрасочной промышленности. Выпускаемые несколько марок и сортов окиси хрома обусловлены областями их применения. Выделяется всего три области:
Выделяется всего три области:
- Пигментная;
- Металлургическая;
- Абразивная.
Оксид хрома (III), применяемый в качестве пигмента – это основной компонент для получения оттенков зелёного цвета. Окись хрома как окрашивающий элемент используют в производстве различных стройматериалов. Также с ним, как с пигментом, изготавливаются грунтовки, эмали, художественные и типографские краски, окрашиваются пластмассы и многое другое. Температура нагревания имеет большое влияние как на цвет, так и на технические характеристики пигмента. При прокаливании окиси хрома температурой в 600° цвет будет тёмно-зелёный, укрывистость – низкой, размер частиц – малый. Повышая температуру до 800°, получим более насыщенный цвет, более высокую укрывистость, бОльший размер частиц. При 920° получаем оптимальные технические свойства: цвет – ярко-зелёный, укрывистость – самая высокая. Дальнейшее же прокаливание только ухудшит полезные характеристики пигмента. Большим преимуществом является тот факт, что срок хранения пигментной окиси хрома не ограничен. На сегодняшний день это соединение входит в подавляющее количество сортов и марок краски и лака.
На сегодняшний день это соединение входит в подавляющее количество сортов и марок краски и лака.
В металлургии оксид хрома применяют для создания такого материала, как металлический хром. Он также имеет место быть в производстве огнеупорных изделий и разнообразных абразивных материалов.
Окись хрома применяется при полировке, как главный компонент абразивного материала, в часовой, приборо- и машиностроительных отраслях промышленности.
Оксид хрома (II) является сильным восстановителем и не имеет практического применения, кроме химических опытов в качестве чистого элемента в лаборатории.
В настоящее время науке известно не меньше 9 различных оксидов хрома, у каждого из которых свой «характер»: физические и химические свойства. Чтобы избежать недопонимания, укажем, что в этой статье оксидом хрома мы будем называть его трёхвалентное соединение – оксид хрома (III) (химическая формула – Cr2O3). Данный оксид с точки зрения физических свойств представляет из себя порошок зелёного цвета с высокой степенью твёрдости кристаллов. Известен также как «хромовая охра» и «хромовая зелень». Специализацией нашей компании «Техноимпекс» являются поставки химического сырья для различных отраслей промышленности. У нас вы можете заказать и купить окись хрома по цене опта. В продаже имеется только оригинальная продукция от известных поставщиков. Оставьте заявку, согласуйте с нашим менеджером варианты оплаты и доставки, и вы лично сможете убедиться в высоком качестве поставляемого нами товара. Осуществляем доставку по всей территории Таможенного союза.
Известен также как «хромовая охра» и «хромовая зелень». Специализацией нашей компании «Техноимпекс» являются поставки химического сырья для различных отраслей промышленности. У нас вы можете заказать и купить окись хрома по цене опта. В продаже имеется только оригинальная продукция от известных поставщиков. Оставьте заявку, согласуйте с нашим менеджером варианты оплаты и доставки, и вы лично сможете убедиться в высоком качестве поставляемого нами товара. Осуществляем доставку по всей территории Таможенного союза.
Оксид хрома – это многосторонний продукт с широким кругом применения. Например, это химическое соединение служит основной добавкой к корунду для выращивания искусственных рубинов. Однако, из всего многообразия применений можно выбрать три основных области.
- Пигментирование. «Хромовую зелень» используют в качестве окрашивающего пигмента для строительных материалов (например, бетон, наливные полы, кладочный раствор с помощью неё окрашивают в зелёный цвет), различного рода и назначения пластических масс, производстве стекла, в керамике, а также в изготовлении грунтовок, лаков, эмалей и красок, как промышленных, так и художественных, для придания им зелёного цвета.
 Специфическим считается применение «хромовой охры» при создании денежных знаков. В этой области применения окись хрома должна быть особенно чистой, без растворимых в воде примесей.
Специфическим считается применение «хромовой охры» при создании денежных знаков. В этой области применения окись хрома должна быть особенно чистой, без растворимых в воде примесей. - Абразивный материал. Оксид хрома в мелкоизмельчённом состоянии применяется в устройствах для шлифовки из-за своей высокой твёрдости. Также может быть использован в изготовлении специальных материалов, устойчивых к воздействию высоких температур (огнеупоров).
- Металлургическая промышленность. Трёхвалентное химическое соединение хрома с кислородом для металлургии является исходным материалом в получении чистого металлического хрома или его сплавов.
Триоксид хрома
Триоксид хрома — сильный окислитель, не растворимый в большинстве
органических растворителей и имеет тенденцию взрываться в присутствии органических соединений и
растворители. В воде образует хромовую кислоту и ангидриды, из которых соли такие
в виде дихромата натрия (Na 2 Cr 2 O 7 ) и
дихромат пиридиния являются
в продаже.
Триоксид хрома растворим в трет-бутиловом спирте , пиридине (см. Реагент Саретта, Collins Reagent) и уксусный ангидрид, хотя следует соблюдать осторожность. данные процедуры, потому что эти решения имеют тенденцию к взрыву.Решение триоксид хрома в водной серной кислоте можно безопасно смешивать с ацетоном (Джонс Реагент). Если эту смесь медленно добавить к спирту в ацетоне, продукты окисления, такие как карбонильные соединения и карбоновые кислоты, могут быть изолирован с хорошими урожаями (Джонс Окисление).
Полный обзор реагентов на основе хрома можно найти в книге, написанной Тохо и Фернндес (Окисление Спирты в альдегиды и кетоны, Springer Berlin, 2006 , 1-97.).
Внимание: Соединения хрома (VI) являются токсичен и требует осторожного обращения.
Последняя литература
Бензиловые спирты и бензиловые эфиры TBDMS эффективно окислялись до
соответствующие карбонильные соединения с высоким выходом при катализе периодной кислотой
по CrO 3 при низкой температуре (-78 C). Процедура окисления была
высокофункциональная группа толерантна и очень селективна для группы TBDMS над
группа TBDPS.
Процедура окисления была
высокофункциональная группа толерантна и очень селективна для группы TBDMS над
группа TBDPS.
С. Чжан, Л. Сюй, М. Л. Труделл, Synthesis , 2005 , 1757-1760.
Бензиловые спирты и бензиловые эфиры TBDMS эффективно окислялись до
соответствующие карбонильные соединения с высоким выходом при катализе периодной кислотой
по CrO 3 при низкой температуре (-78 C). Процедура окисления была
высокофункциональная группа толерантна и очень селективна для группы TBDMS над
группа TBDPS.
С. Чжан, Л.Сюй, М. Л. Труделл, Synthesis , 2005 ,
1757-1760 гг.
CrO 3 — эффективный катализатор бензильного окисления с периодическим
кислота как конечный окислитель в ацетонитриле. Замещенные бедные электронами толуолы
и диарилметаны были окислены до соответствующих замещенных бензойных кислот.
и кетоны с отличными выходами. Бензиловые эфиры, такие как изохроман и фталан
были превращены в 3,4-дигидроизокумарин и фталид с количественными выходами.
С. Ямазаки, Орг. Lett. , 1999 , 1 , 2129-2132.
Последовательный процесс Wacker, продвигаемый PdCl 2 / CrO 3 .
посредством кислотно-опосредованной дегидратации делает возможным синтез β-замещенных и
β, β-дизамещенные α, β-ненасыщенные метилкетоны из гомоаллиловых спиртов с
концевую двойную связь, тогда как внутренние гомоаллиловые спирты доставляют
региоселективно несопряженные ненасыщенные карбонильные соединения при тех же
протокол.
В. Бети, Р. А. Фернандес, J. Org. Chem. , 2016 , 81 , 8577-8584.
A CrO 3 -катализируемое окисление первичных спиртов до карбоновых кислот
протекает плавно только с 1-2 мол.% CrO 3 и 2,5 эквивалента
H 5 IO 6 во влажном MeCN для получения карбоновых кислот в
отличный урожай. Для спиртов с
соседние хиральные центры.Вторичные спирты полностью окисляются до кетонов.
М. Чжао, Дж. Ли, З. Сонг, Р. Десмонд, Д. М. Чаен, Э. Дж. Дж. Грабовски, П. Дж.
Reider, Tetrahedron Lett. , 1998 , 39 , 5323-5326.
Ли, З. Сонг, Р. Десмонд, Д. М. Чаен, Э. Дж. Дж. Грабовски, П. Дж.
Reider, Tetrahedron Lett. , 1998 , 39 , 5323-5326.
Тригалогенуксусная кислота может быть хорошо преобразована в трихлорметил и трибромметилкетоны.
выход в результате каталитической реакции с альдегидами с последующим окислением. Сочетание цинкорганических промежуточных соединений с трихлорацетилхлоридом
дает трихлорметилкетоны.
Э. Дж. Кори, Дж. О. Линк, Ю. Шао, Tetrahedron Lett. , 1992 , 33 , 3435-3438.
CrO 3 — эффективный катализатор бензильного окисления с периодическим
кислота как конечный окислитель в ацетонитриле. Замещенные бедные электронами толуолы
и диарилметаны были окислены до соответствующих замещенных бензойных кислот.
и кетоны с отличными выходами. Бензиловые эфиры, такие как изохроман и фталан
были превращены в 3,4-дигидроизокумарин и фталид с количественными выходами.
С. Ямазаки, Орг. Lett. , 1999 , 1 , 2129-2132.
Lett. , 1999 , 1 , 2129-2132.
Реакция между диалкилацетилендикарбоксилатами и β-аминокетонами способствовала
трифенилфосфином позволяет осуществлять эффективный однореакторный синтез полизамещенных
Производные 2,5-дигидропиррола. Приготовленные 2,5-дигидропирролы легко поддаются обработке.
окисляется до соответствующих производных пиррола триоксидом хрома.
М. Анары-Аббасинежад, Э.Пурхассан, А. Хассанабади, Synlett , 2009 ,
1929-1932 гг.
хлопьев триоксида хрома | AMERICAN ELEMENTS ®
РАЗДЕЛ 1. ИДЕНТИФИКАЦИЯ
Наименование продукта: Хлопья триоксида хрома
Номер продукта: Все применимые коды продуктов American Elements, например CR6-OX-02-FK , CR6-OX-03-FK , CR6-OX-04-FK , CR6-OX-05-FK
Номер CAS: 1333-82-0
Соответствующие установленные области применения вещества: Научные исследования и разработки
Информация о поставщике:
American Elements
10884 Weyburn Ave.
Лос-Анджелес, Калифорния
Тел .: +1 310-208-0551
Факс: +1 310-208-0351
Телефон экстренной связи:
Внутренний номер, Северная Америка: +1 800-424-9300
Международный: +1 703-527-3887
РАЗДЕЛ 2. ИДЕНТИФИКАЦИЯ ОПАСНОСТИ
Классификация вещества или смеси в соответствии с 29 CFR 1910 (OSHA HCS)
GHS03 Пламя над кругом
Ox. Sol. 1 h371 Может вызвать пожар или взрыв; сильный окислитель.
GHS06 Череп и скрещенные кости
Acute Tox.3 h401 Токсично при проглатывании.
Acute Tox. 2 h410 Смертельно при контакте с кожей.
Acute Tox. 2 h430 Смертельно при вдыхании.
GHS08 Опасность для здоровья
Респ. Sens. 1 h434 При вдыхании может вызывать симптомы аллергии, астмы или затруднение дыхания.
Muta. 1A h440 Может вызывать генетические дефекты.
Carc. 1A h450 Может вызывать рак.
Репр. 2 h461 Предположительно может нанести ущерб фертильности или нерожденному ребенку.
STOT RE 1 h472 Вызывает повреждение центральной нервной системы, легких и крови в результате длительного или многократного воздействия. Путь воздействия:
Путь воздействия:
Вдыхание.
GHS05 Коррозия
Skin Corr. 1A h414 Вызывает серьезные ожоги кожи и повреждения глаз.
Eye Dam. 1 h418 Вызывает серьезное повреждение глаз.
GHS07
Skin Sens. 1 h417 Может вызывать аллергическую кожную реакцию.
Опасности, не классифицируемые иным образом Данные отсутствуют
Элементы маркировки GHS, включая меры предосторожности
Пиктограммы опасностей
GHS03 GHS05 GHS06 GHS08
Сигнальное слово Опасно
Краткая характеристика опасности
h371 Может вызвать пожар или взрыв; сильный окислитель.
h401 Токсично при проглатывании.
h410 + h430 Смертельно при контакте с кожей или при вдыхании.
h414 Вызывает серьезные ожоги кожи и повреждения глаз.
h434 При вдыхании может вызывать симптомы аллергии, астмы или затруднение дыхания.
h417 Может вызывать аллергическую кожную реакцию.
h440 Может вызывать генетические дефекты.
х450 Может вызывать рак.
h461 Предположительно может нанести вред фертильности или нерожденному ребенку.
h472 Вызывает повреждение центральной нервной системы, легких и крови в результате длительного или многократного воздействия.Путь воздействия: Вдыхание.
Меры предосторожности
P221 Примите все меры, чтобы избежать смешивания с горючими веществами.
P283 Носить огнестойкую / огнестойкую / стойкую к воздействию огня одежду.
P301 + P310 ПРИ ПРОГЛАТЫВАНИИ: Немедленно обратиться в ТОКСИКОЛОГИЧЕСКИЙ ЦЕНТР / к врачу.
P303 + P361 + P353 При попадании на кожу (или волосы): немедленно снять всю загрязненную одежду. Промыть кожу водой / принять душ.
P305 + P351 + P338 ПРИ ПОПАДАНИИ В ГЛАЗА: осторожно промыть глаза водой в течение нескольких минут. Снимите контактные линзы, если они есть и это легко сделать.Продолжайте полоскание. P320 Срочно требуется специальное лечение (см. На этой этикетке).
P361 Немедленно снять всю загрязненную одежду.
P405 Хранить под замком.
P501 Утилизировать содержимое / контейнер в соответствии с местными / региональными / национальными / международными правилами.
Классификация WHMIS
C — Окисляющие материалы
D1A — Очень токсичный материал, вызывающий немедленные и серьезные токсические эффекты
D2A — Очень токсичный материал, вызывающий другие токсические эффекты
E — Коррозийный материал
Система классификации
Рейтинги HMIS (шкала 0-4)
(Опасно Система идентификации материалов)
ЗДОРОВЬЕ
ПОЖАР
РЕАКТИВНОСТЬ
3
0
3
Здоровье (острые эффекты) = 3
Воспламеняемость = 0
Физическая опасность = 3
Другие опасности
Результаты оценки PBT и vPvB
PBT: N / A
vPvB: Н / Д
РАЗДЕЛ 3.СОСТАВ / ИНФОРМАЦИЯ ОБ ИНГРЕДИЕНТАХ
Вещества
Номер CAS / Название вещества:
1333-82-0 Оксид хрома (VI)
Идентификационный номер (а):
Номер ЕС: 215-607-8
Номер индекса: 024-001 -00-0
РАЗДЕЛ 4. МЕРЫ ПЕРВОЙ ПОМОЩИ
Описание мер первой помощи
Общая информация
Немедленно снимите всю одежду, загрязненную продуктом.
Снимать дыхательный аппарат только после полного снятия загрязненной одежды.
При нерегулярном дыхании или остановке дыхания произвести искусственное дыхание.
При вдыхании:
Обеспечить пациента свежим воздухом. Если не дышит, сделайте искусственное дыхание. Держите пациента в тепле.
Немедленно обратитесь за медицинской помощью.
При попадании на кожу:
Немедленно промыть водой с мылом; тщательно промыть.
Немедленно обратитесь за медицинской помощью.
При попадании в глаза:
Промыть открытый глаз под проточной водой в течение нескольких минут. Проконсультируйтесь с врачом.
При проглатывании:
Не вызывать рвоту; немедленно обратитесь за медицинской помощью.
Информация для врача
Наиболее важные симптомы и воздействия, как острые, так и замедленные.
Вызывает серьезные ожоги кожи.
Вызывает серьезное повреждение глаз.
Указание на необходимость немедленной медицинской помощи и специального лечения:
Данные отсутствуют
РАЗДЕЛ 5.
 МЕРЫ ПОЖАРОТУШЕНИЯ
МЕРЫ ПОЖАРОТУШЕНИЯ Средства пожаротушения
Подходящие средства пожаротушения Двуокись углерода, порошковое средство для тушения или водяная струя мелкого разбрызгивания. Для тушения больших пожаров используйте водную струю или спиртоустойчивую пену.
Средства тушения, неподходящие из соображений безопасности Галоуглеродный огнетушитель
Особые опасности, исходящие от вещества или смеси
Это вещество является окислителем, и его теплота реакции с восстановителями или горючими веществами может вызвать возгорание.
При попадании этого продукта в огонь могут образоваться следующие вещества:
Токсичный дым оксида металла
Рекомендации для пожарных
Защитное снаряжение:
Надеть автономный респиратор.
Надеть полностью защитный непромокаемый костюм.
РАЗДЕЛ 6. МЕРЫ ПРИ СЛУЧАЙНОМ ВЫБРОСЕ
Меры личной безопасности, защитное снаряжение и порядок действий в чрезвычайной ситуации
Используйте средства индивидуальной защиты. Не подпускайте незащищенных людей.
Не подпускайте незащищенных людей.
Обеспечьте соответствующую вентиляцию.
Меры по защите окружающей среды: Не допускайте попадания материала в окружающую среду без официального разрешения.
Методы и материалы для локализации и очистки:
Использовать нейтрализующий агент.
Утилизировать зараженный материал как отходы в соответствии с разделом 13.
Обеспечьте соответствующую вентиляцию.
Предотвращение вторичных опасностей:
Действует как окислитель на такие органические материалы, как дерево, бумага и жиры.
Хранить вдали от горючих материалов.
Ссылка на другие разделы.
См. Раздел 7 для получения информации о безопасном обращении.
См. Раздел 8 для получения информации о средствах индивидуальной защиты.
См. Раздел 13 для получения информации об утилизации.
РАЗДЕЛ 7. ОБРАЩЕНИЕ И ХРАНЕНИЕ
Обращение
Меры предосторожности для безопасного обращения
Работать в атмосфере сухого защитного газа.
Хранить контейнер плотно закрытым.
Хранить в сухом прохладном месте в плотно закрытой таре.
Обеспечьте хорошую вентиляцию на рабочем месте.
Осторожно открывайте контейнер и обращайтесь с ним.
Информация о защите от взрывов и пожаров:
Вещество / продукт может снизить температуру воспламенения легковоспламеняющихся веществ.
Это вещество является окислителем, и его теплота реакции с восстановителями или горючими веществами может вызвать возгорание.
Условия безопасного хранения с учетом несовместимости
Требования, предъявляемые к складским помещениям и таре: Особых требований нет.
Информация о хранении в одном общем хранилище:
Хранить вдали от легковоспламеняющихся веществ.
Хранить вдали от восстановителей.
Не хранить вместе с органическими материалами.
Хранить вдали от металлических порошков.
Хранить вдали от воды / влаги.
Дополнительная информация об условиях хранения:
Хранить в сухом инертном газе.
Продукт гигроскопичен.
Хранить контейнер плотно закрытым.
Хранить в прохладном, сухом месте в хорошо закрытой таре.
Беречь от влаги и воды.
Специфическое конечное использование Данные отсутствуют
РАЗДЕЛ 8. КОНТРОЛЬ ВОЗДЕЙСТВИЯ / ЛИЧНАЯ ЗАЩИТА
Дополнительная информация о конструкции технических систем:
Правильно работающий вытяжной шкаф для химических веществ, предназначенный для опасных химикатов и имеющий среднюю скорость потока не менее 100 футов в минуту.
Параметры контроля
Компоненты с предельными значениями, требующие контроля на рабочем месте:
1333-82-0 Оксид хрома (VI) (100,0%)
PEL (США) Долгосрочное значение: 0.005 * мг / м 3
Предельно допустимое значение: 0,1 ** мг / м 3
* как Cr (VI) ** как CrO3; см. 29 CFR 1910.1026
REL (США) Долгосрочное значение: 0,001 мг / м 3
как Cr; См. Приложение Pocket Guide. ПДК A и C
(США) Долгосрочное значение: 0,05 мг / м 3
как Cr; BEI
EL (Канада) Краткосрочное значение: C0,1 мг / м 3
Долгосрочное значение: 0,025 мг / м 3
как Cr; ACIGH A1, IARC 1
Ингредиенты с биологическими предельными значениями:
1333-82-0 Оксид хрома (VI) (100. 0%)
0%)
BEI (США) 25 мкг / л
Среда: моча
Время: конец смены в конце рабочей недели
Параметр: Общий хром (дым)
10 мкг / л
Среда: моча
Время: увеличение во время смены
Параметр: Общий хром (дым)
Дополнительная информация: Нет данных
Средства контроля за опасным воздействием
Средства индивидуальной защиты
Соблюдайте стандартные меры защиты и гигиены при обращении с химическими веществами.
Хранить вдали от продуктов питания, напитков и кормов.
Немедленно снимите всю грязную и загрязненную одежду.
Мыть руки перед перерывами и по окончании работы.
Храните защитную одежду отдельно.
Избегать контакта с глазами и кожей.
Поддерживайте эргономичную рабочую среду.
Дыхательное оборудование: В чрезвычайных ситуациях использовать автономное устройство защиты органов дыхания.
Рекомендуемое фильтрующее устройство для краткосрочного использования:
Используйте респиратор с картриджами типа P100 (США) или P3 (EN 143) в качестве резервного средства технического контроля. Следует провести оценку рисков, чтобы определить, подходят ли респираторы
Следует провести оценку рисков, чтобы определить, подходят ли респираторы
для очистки воздуха.Используйте только оборудование, проверенное и одобренное соответствующими государственными стандартами.
Защита рук:
Непроницаемые перчатки
Осмотрите перчатки перед использованием.
Выбор подходящих перчаток зависит не только от материала, но и от качества. Качество будет варьироваться от производителя к производителю.
Материал перчаток Нитрилкаучук, NBR
Время проницаемости материала перчаток (в минутах) 480
Толщина перчаток 0,11 мм
Защита глаз:
Плотно закрытые очки
Полная защита лица
Защита тела: Защитная рабочая одежда.
РАЗДЕЛ 9. ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА
Информация об основных физико-химических свойствах
Внешний вид:
Форма: Кристаллическая
Цвет: Темно-красный
Запах: Не определено
Порог запаха: Не определено.
pH: нет данных
Точка плавления / интервал плавления: 196 ° C (385 ° F)
Точка кипения / интервал кипения: 250 ° C (482 ° F) (разл. )
)
Температура сублимации / начало: не определено
Воспламеняемость ( твердое вещество, газ) Контакт с горючим материалом может вызвать пожар.
Температура возгорания: Не определено.
Температура разложения: Не определено.
Самовоспламенение: Не определено.
Взрывоопасность: Взрывоопасно при смешивании с горючим материалом.
Пределы взрываемости:
Нижний: Не определено
Верхнее: Не определено
Давление пара: Н / Д
Плотность при 20 ° C (68 ° F): 2,7 г / см 3 (22,532 фунта / галлон)
Относительная плотность Нет определенный.
Плотность пара нет данных
Скорость испарения нет данных
Растворимость в / смешиваемость с водой
при 20 ° C (68 ° F): 630 г / л
Коэффициент распределения (н-октанол / вода): Не определено.
Вязкость:
Динамическая: нет
Кинематическая: нет
Другая информация Нет данных
РАЗДЕЛ 10. СТАБИЛЬНОСТЬ И РЕАКЦИОННАЯ СПОСОБНОСТЬ
Реакционная способность
Может усилить возгорание; окислитель.
Может вызвать пожар или взрыв; сильный окислитель.
Химическая стабильность Стабилен при соблюдении рекомендуемых условий хранения.
Термическое разложение / условия, которых следует избегать: При использовании и хранении в соответствии со спецификациями разложения не происходит.
Возможность опасных реакций
Реагирует с восстановителями
Реагирует с легковоспламеняющимися веществами
Условия, которых следует избегать Данные отсутствуют
Несовместимые материалы:
Восстановители
Горючие вещества
Вода / влага
Органические материалы
Порошки металлов
Опасные продукты разложения: Токсичный оксид металла дым
РАЗДЕЛ 11.ТОКСИКОЛОГИЧЕСКАЯ ИНФОРМАЦИЯ
Информация о токсикологическом воздействии
Острая токсичность:
Смертельно при контакте с кожей.
Смертельно при вдыхании.
Токсично при проглатывании.
Опасность из-за впитывания через кожу.
Проглатывание вызывает сильное разъедание рта и горла и опасность перфорации пищевода и желудка.
Реестр токсических эффектов химических веществ (RTECS) содержит данные об острой токсичности этого вещества.
Значения LD / LC50, относящиеся к классификации:
LD50 при пероральном приеме 80 мг / кг (крыса)
Раздражение или разъедание кожи: Вызывает серьезные ожоги кожи.
Раздражение или коррозия глаз: Вызывает серьезное повреждение глаз.
Сенсибилизация:
При вдыхании может вызвать симптомы аллергии или астмы или затруднение дыхания.
Может вызывать аллергическую кожную реакцию.
Мутагенность зародышевой клетки:
Может вызывать генетические дефекты.
Реестр токсических эффектов химических веществ (RTECS) содержит данные о мутациях этого вещества.
Канцерогенность:
Может вызывать рак.
IARC-1: Канцерогенный для человека: достаточные доказательства канцерогенности.
ACGIH A1: Подтвержденный канцероген для человека: Агент является канцерогенным для человека на основании эпидемиологических исследований или убедительных клинических данных на людях, подвергшихся его воздействию.
ACGIH A5: Не подозревается как канцероген для человека: Не подозревается как канцероген для человека на основании надлежащим образом проведенных эпидемиологических исследований на людях. Исследования
имеют достаточно длительное наблюдение, достоверные истории воздействия, достаточно высокую дозу и адекватную статистическую мощность, чтобы сделать вывод о том, что воздействие агента
не несет значительного риска рака для человека.Доказательства отсутствия канцерогенности у экспериментальных животных будут рассмотрены, если они поддерживаются
другими соответствующими данными.
NTP-K: Известно, что он канцерогенный: достаточно данных исследований на людях.
(вдыхание) EPA-A: канцероген для человека: достаточно данных эпидемиологических исследований, подтверждающих причинную связь между воздействием и раком.
(вдыхание) EPA-K: известные канцерогены для человека.
(оральный) EPA-D: не классифицируется по канцерогенности для человека: неадекватные доказательства канцерогенности для человека и животных или данные отсутствуют.
(перорально) EPA-CBD: канцерогенный потенциал не может быть определен.
Реестр токсических эффектов химических веществ (RTECS) содержит данные о онкогенных, канцерогенных и / или опухолевых заболеваниях для этого вещества.
Репродуктивная токсичность:
Предположительно может нанести вред фертильности или нерожденному ребенку.
Реестр токсических эффектов химических веществ (RTECS) содержит репродуктивные данные для этого вещества.
Специфическая системная токсичность, поражающая отдельные органы-мишени — многократное воздействие:
Вызывает повреждение центральной нервной системы, легких и крови в результате длительного или многократного воздействия.Путь воздействия: Вдыхание.
Специфическая системная токсичность, поражающая отдельные органы-мишени — однократное воздействие: Эффекты неизвестны.
Опасность при вдыхании: Эффекты неизвестны.
От подострой до хронической токсичности: Реестр токсических эффектов химических веществ (RTECS) содержит данные о токсичности при множественных дозах для этого вещества.
Дополнительная токсикологическая информация: Насколько нам известно, острая и хроническая токсичность этого вещества полностью не изучена.
РАЗДЕЛ 12. ЭКОЛОГИЧЕСКАЯ ИНФОРМАЦИЯ
Токсичность
Водная токсичность: данные отсутствуют
Стойкость и разлагаемость Сведения не доступны
Потенциал биоаккумуляции Сведения не доступны
Подвижность в почве Сведения не доступны
Экотоксические эффекты:
Примечание: Очень токсично для водных организмов
Дополнительная экологическая информация:
Не допускать попадания материала в окружающую среду без официального разрешения.
Не допускать попадания продукта в грунтовые воды, водоемы или канализацию, даже в небольших количествах.
Опасность для питьевой воды при попадании в землю даже очень небольшого количества.
Также ядовит для рыб и планктона в водоемах.
Может вызывать длительные вредные последствия для водных организмов.
Избегать попадания в окружающую среду.
Очень токсичен для водных организмов
Результаты оценки PBT и vPvB
PBT: N / A
vPvB: N / A
Другие побочные эффекты Данные отсутствуют
РАЗДЕЛ 13.СООБРАЖЕНИЯ ПО УТИЛИЗАЦИИ
Методы обработки отходов
Рекомендация Для обеспечения надлежащей утилизации обратитесь к официальным предписаниям.
Неочищенная тара:
Рекомендация: Утилизация должна производиться в соответствии с официальными предписаниями.
РАЗДЕЛ 14. ТРАНСПОРТНАЯ ИНФОРМАЦИЯ
Класс 5.1 Окисляющие вещества.
Этикетка 5.1 + 6.1 + 8
Класс 5.1 (OTC) Окисляющие вещества
Этикетка 5.1 + 6.1 + 8
IMDG, IATA
Класс 5.1 Окисляющие вещества.
Наклейка 5.1 + 6.1 + 8
Группа упаковки
DOT, IMDG, IATA II
Опасности для окружающей среды: Твердое вещество, опасное для окружающей среды
Особые меры предосторожности для пользователя Предупреждение: Окисляющие вещества
Транспортировка наливом в соответствии с Приложением II к MARPOL73 / 78 и Кодексом IBC N / A
Транспортировка / Дополнительная информация:
DOT
Морской загрязнитель (DOT): №
Типовой регламент ООН: UN1463, Хром трехокись безводный, 5. 1 (6.1 + 8), II
1 (6.1 + 8), II
РАЗДЕЛ 15. НОРМАТИВНАЯ ИНФОРМАЦИЯ
Нормы безопасности, здоровья и окружающей среды / законодательные акты, относящиеся к веществу или смеси
Элементы маркировки GHS, включая меры предосторожности
Пиктограммы опасностей
GHS03 GHS05 GHS06 GHS08
Сигнальное слово Опасно
Краткая характеристика опасности
h371 Может вызвать пожар или взрыв; сильный окислитель.
h401 Токсично при проглатывании.
h410 + h430 Смертельно при контакте с кожей или при вдыхании.
h414 Вызывает серьезные ожоги кожи и повреждения глаз.
h434 При вдыхании может вызывать симптомы аллергии, астмы или затруднение дыхания.
h417 Может вызывать аллергическую кожную реакцию.
h440 Может вызывать генетические дефекты.
х450 Может вызывать рак.
h461 Предположительно может нанести вред фертильности или нерожденному ребенку.
h472 Вызывает повреждение центральной нервной системы, легких и крови в результате длительного или многократного воздействия.Путь воздействия: Вдыхание.
Меры предосторожности
P221 Примите все меры, чтобы избежать смешивания с горючими веществами.
P283 Носить огнестойкую / огнестойкую / стойкую к воздействию огня одежду.
P301 + P310 ПРИ ПРОГЛАТЫВАНИИ: Немедленно обратиться в ТОКСИКОЛОГИЧЕСКИЙ ЦЕНТР / к врачу.
P303 + P361 + P353 При попадании на кожу (или волосы): немедленно снять всю загрязненную одежду. Промыть кожу водой / принять душ.
P305 + P351 + P338 ПРИ ПОПАДАНИИ В ГЛАЗА: осторожно промыть глаза водой в течение нескольких минут. Снимите контактные линзы, если они есть и это легко сделать.Продолжайте полоскание.
P320 Срочно требуется специальное лечение (см. На этой этикетке).
P361 Немедленно снять всю загрязненную одежду.
P405 Хранить под замком.
P501 Утилизировать содержимое / контейнер в соответствии с местными / региональными / национальными / международными правилами.
Национальные правила
Все компоненты этого продукта перечислены в Реестре химических веществ в соответствии с Законом о контроле за токсичными веществами Агентства по охране окружающей среды США.
Все компоненты этого продукта занесены в Канадский список отечественных веществ (DSL).
SARA Раздел 313 (списки конкретных токсичных химических веществ)
1333-82-0 Оксид хрома (VI)
Предложение штата Калифорния 65
Предложение 65 — Химические вещества, вызывающие рак
1333-82-0 Оксид хрома (VI)
Предложение 65 — Развитие токсичность Вещества не указаны.
Правило 65 — Токсичность для развития, женщины
1333-82-0 Оксид хрома (VI)
Правило 65 — Токсичность для развития, мужчины
1333-82-0 Оксид хрома (VI)
Информация об ограничении использования:
Рабочие не допускаются подвергаться воздействию этого опасного материала.В определенных случаях власти могут делать исключения.
Для использования только технически квалифицированными специалистами.
Это вещество регулируется Правилами значительного нового использования (SNUR), опубликованными в соответствии с разделом 5 (a) (2) Закона о контроле над токсичными веществами (TSCA). См. 40 CFR 721.
Этот продукт продается для исследований и разработок.
Другие постановления, ограничения и запретительные постановления
Вещество, вызывающее особую озабоченность (SVHC) в соответствии с Регламентом REACH (EC) № 1907/2006.
Это вещество включено в Список потенциально опасных веществ (SVHC) в соответствии с Регламентом (ЕС) № 1907/2006 (REACH).
Условия ограничений согласно Статье 67 и Приложению XVII Регламента (ЕС) № 1907/2006 (REACH) для производства, размещения на рынке
и использования должны соблюдаться.
Вещества нет в списке.
Приложение XIV Правил REACH (требуется разрешение на использование) Вещество указано.
Оценка химической безопасности: Оценка химической безопасности не проводилась.
РАЗДЕЛ 16. ПРОЧАЯ ИНФОРМАЦИЯ
Паспорт безопасности в соответствии с Регламентом (ЕС) № 1907/2006 (REACH). Вышеприведенная информация считается правильной, но не претендует на исчерпывающий характер и должна использоваться только в качестве руководства. Информация в этом документе основана на текущем уровне наших знаний и применима к продукту с учетом соответствующих мер безопасности. Это не является гарантией свойств продукта. American Elements не несет ответственности за любой ущерб, возникший в результате обращения или контакта с вышеуказанным продуктом.Дополнительные условия продажи см. На обратной стороне счета-фактуры или упаковочного листа. АВТОРСКИЕ ПРАВА 1997-2021 AMERICAN ELEMENTS. ЛИЦЕНЗИОННЫМ ДАННЫМ РАЗРЕШЕНО ИЗГОТОВЛЕНИЕ НЕОГРАНИЧЕННЫХ КОПИЙ БУМАГИ ТОЛЬКО ДЛЯ ВНУТРЕННЕГО ИСПОЛЬЗОВАНИЯ.
РЕАГЕНТ ДЖОНСА — РЕАГЕНТЫ ANTHONY CRASTO
* Реагент Джонса представляет собой смесь хромового ангидрида и разбавленной серной кислоты (CrO 3 + H 2 SO 4 + H 2 O) в ацетоне. Он используется при окислении вторичных спиртов , не содержащих кислоточувствительных групп, до соответствующих кетонов .
* Первичные спирты сначала окисляются до альдегидов, а затем окисляются до карбоновых кислот.
* Смесь дихромата натрия или дихромата калия в разбавленной серной кислоте и ацетоне также может использоваться в качестве реагента Джонса.
* Это окисление обычно называют окислением Джонса .
Условия реакции и обработка
* Реагент Джонса получают путем добавления хромового ангидрида к разбавленной серной кислоте в ацетоне и добавляют к спирту при 0-25 o ° C.
* Окрашенный в оранжевый или желтый цвет Cr (VI) восстанавливается до сине-зеленых разновидностей Cr (III) во время окисления.
* Избыток Cr (VI), если он остался, разрушается в ходе реакции путем добавления изопропилового спирта.
МЕХАНИЗМ РЕАКЦИИ ДЖОНСА
* Первоначально хромовая кислота (VI) образуется на месте из смеси триоксида хрома и разбавленной серной кислоты.
* Спирт и хромовая кислота образуют моноэфир хрома (VI), который может реагировать внутримолекулярно или межмолекулярно в присутствии основания (H 2 O в данном случае) с образованием соответствующего карбонильного соединения и хрома. (IV) кислота.Внутримолекулярная реакция происходит посредством β-элиминирования через циклическое переходное состояние.
* Альдегиды, которые могут образовывать гидраты в присутствии воды, могут далее подвергаться окислению с образованием карбоновых кислот в реакции Джонса.
* Следовательно, окисление первичных спиртов реактивом Джонса обычно приводит к образованию карбоновых кислот из-за присутствия воды. Однако бензиловый и аллиловый спирты не образуют гидратов в воде и, следовательно, могут избирательно окисляться до альдегидов.
* Если окисление проводится в безводных условиях, можно остановить реакцию на уровне альдегида . См. В конце страницы реагенты, которые могут служить этой цели.
* Последующий химический состав Cr (IV): Кислота хрома (IV) диспропорционирована на оксид Cr (III) и кислоту Cr (VI).
ПРИМЕНЕНИЕ РЕАГЕНТА ДЖОНСА
1) Вторичные спирты окисляются до соответствующих кетонов в реакции Джонса.
2) Первичные спирты окисляются до карбоновых кислот через альдегиды с помощью реактива Джонса.
3) Бензиловый спирт может окисляться до бензальдегида. Дальнейшее окисление до бензойной кислоты невозможно, поскольку бензальдегид не может образовывать стабильные гидраты в воде.
4) В реакции Джонса аллиловые спирты также избирательно окисляются до альдегидов. В этой реакции двойные связи не нарушаются.
Некоторые окисляющие реагенты, содержащие Cr (VI)
1) Реагент Саретта: CrO 3 .2C 5 H 5 N (где C 5 H 5 N = пиридин)
2) Реактив Коллинза : CrO 3 . 2C 5 H 5 N, разбавленный в CH 2 Cl 2
3) Реагент Корнфорта: CrO 3 / Пиридин / H 2 O
4) Реагент Физера: CrO 3 в уксусной кислоте.
5) Реагент Тиле: CrO 3 + уксусный ангидрид + H 2 SO 4
6) Хлорхромат пиридиния (PCC) в CH 2 Cl 2 (Кори-Сагент) : [C 5 H 5 NH] + [CrO 3 Cl] —
7) Дихромат пиридиния (PDC) в CH 2 Cl 2 или DMF (Corey- Реагент Шмидта): (C 5 H 5 NH) 2 Cr 2 O 7
Хромовая кислота — обзор
Неплотно накройте сосуд с хромовой кислотой крышкой без тестовых слайдов или контроля и поставьте в микроволновую печь на 30 секунд при высокой температуре. Поместите слайды в нагретую банку с хромовой кислотой на 1 минуту. Перегрев или кипячение хромовой кислоты может привести к неудовлетворительному окрашиванию. Всегда заменяйте горячую кислоту под вытяжным шкафом сразу после извлечения из духовки.
Удалите предметные стекла из хромовой кислоты и поместите в сосуд Коплина, наполненный дистиллированной водой. Промойте предметные стекла дистиллированной водой, чтобы удалить избыток хромовой кислоты.
Поместите слайды в 1% метабисульфит натрия на 30–60 секунд, чтобы они стали прозрачными.
Поместите предметные стекла обратно в сосуд Коплина и промойте в дистиллированной воде.
Нагрейте рабочий раствор метенамина серебра в микроволновой печи Коплина в течение 33 секунд при высокой температуре. Немедленно поместите слайды в нагретый раствор серебра метенамина. В идеале раствор должен быть прозрачным или слегка серым, когда его вынимают из духовки.Внимательно следите за изменением цвета контрольного образца. Переместите слайды в банку Коплина с дистиллированной водой. Это может варьироваться в зависимости от лаборатории и характеристик воды и растворов. Иногда раствор должен стать темно-черным, прежде чем произойдет адекватное окрашивание. В других случаях темный цвет может указывать на перекрашивание. Поэтому предметные стекла следует удалить до того, как раствор станет непрозрачно-черным, промыть в дистиллированной воде и проверить под микроскопом на предмет окрашивания контрольного предметного стекла.
Промойте контрольное стекло в дистиллированной воде и исследуйте под микроскопом на наличие черного окрашивания (или коричневато-красного перед очисткой в хлориде золота) кисты Pneumocystis .
При необходимости время нахождения в растворе серебра можно продлить, заменив предметные стекла в теплом растворе метенамина. Если образец стал непрозрачно-черным, но окрашивания не произошло, проблема с реагентами, и дополнительное окрашивание не поможет.Обычно проблема заключается в том, что рабочий раствор нитрата серебра в метенамине старый и должен быть свежим, или в том, что образец был перегрет во время микроволновой обработки в хромовой кислоте.
Если окрашивание контроля удовлетворительное, поместите предметные стекла в раствор хлорида золота на 30–60 секунд. Промыть дистиллированной водой.
Поместите предметные стекла в сосуд Коплина, наполненный 2% тиосульфатом натрия, на 2 минуты.
Промыть дистиллированной водой.
Накрыть светло-зеленым рабочим раствором на 2–5 минут. Промыть 95% спиртом и обезвожить до 100% этанола. Очистите с помощью ксилола и покровного стекла.
РЕАГЕНТ ДЖОНСА И РЕАКЦИИ ОКИСЛЕНИЯ
* Реагент Джонса представляет собой смесь хромового ангидрида и разбавленной серной кислоты (CrO 3 + H 2 SO 4 + H 2 O) в ацетоне. Он используется при окислении вторичных спиртов , не содержащих кислоточувствительных групп, до соответствующих кетонов .
* Первичные спирты сначала окисляются до альдегидов, а затем окисляются до карбоновых кислот.
* Смесь дихромата натрия или дихромата калия в разбавленной серной кислоте и ацетоне также может использоваться в качестве реагента Джонса.
* Это окисление обычно обозначается как окисление Джонса .
AdiChemistry
Условия реакции и обработка
* Реагент Джонса получают добавлением хромового ангидрида к разбавленной серной кислоте в ацетоне и добавляют к спирту при 0-25 o ° C.
* Окрашенный в оранжевый или желтый цвет Cr (VI) восстанавливается до сине-зеленых разновидностей Cr (III) во время окисления.
* Избыток Cr (VI), если таковой остался, разрушается в ходе реакции путем добавления изопропилового спирта.
МЕХАНИЗМ РЕАКЦИИ ДЖОНСА
* Первоначально хромовая кислота (VI) образуется из смеси триоксида хрома и разбавленной серной кислоты.
* Спирт и хромовая кислота образуют моноэфир хрома (VI), который может реагировать внутримолекулярно или межмолекулярно в присутствии основания (H 2 O в данном случае) с образованием соответствующего карбонильного соединения и хрома (IV). кислота.Внутримолекулярная реакция происходит посредством β-элиминирования через циклическое переходное состояние.
* Альдегиды, которые могут образовывать гидраты в присутствии воды, могут далее подвергаться окислению с образованием карбоновых кислот в реакции Джонса.
* Следовательно, окисление первичных спиртов реактивом Джонса обычно приводит к образованию карбоновых кислот из-за присутствия воды. Однако бензиловый и аллиловый спирты не образуют гидратов в воде и, следовательно, могут избирательно окисляться до альдегидов.
* Если окисление проводится в безводных условиях, можно остановить реакцию на уровне альдегида . См. В конце страницы реагенты, которые могут служить этой цели.
* Последующий химический состав Cr (IV): Кислота хрома (IV) диспропорционирована на оксид Cr (III) и кислоту Cr (VI).
ПРИМЕНЕНИЕ РЕАГЕНТА ДЖОНСА
1) Вторичные спирты окисляются до соответствующих кетонов по реакции Джонса.
2) Первичные спирты окисляются до карбоновых кислот через альдегиды с помощью реактива Джонса.
3) Бензиловый спирт может окисляться до бензальдегида. Дальнейшее окисление до бензойной кислоты невозможно, поскольку бензальдегид не может образовывать стабильные гидраты в воде.
4) В реакции Джонса аллиловые спирты также избирательно окисляются до альдегидов. В этой реакции двойные связи не нарушаются.
Некоторые окислительные реагенты, содержащие Cr (VI)
1) Реагент Саретта: CrO 3 .2C 5 H 5 N (где C 5 H 5 N = пиридин)
2) Реагент Коллинза: CrO 3 .2C 5 H 5 N, разбавленный в CH 2 Cl 2
3) Реактив Корнфорта: CrO 3 / Пиридин / H 2 O
4) Реагент Физера: CrO 3 в уксусной кислоте.
5) Реагент Тиле: CrO 3 + уксусный ангидрид + H 2 SO 4
6) Хлорхромат пиридини (PCC) в CH 2 Cl 2 (реактив Кори-Саггса): [C 5 H 5 NH] + [CrO 3 Cl] —
7) дихромат пиридиния (PDC) в CH 2 Cl 2 или DMF (реактив Кори-Шмидта): (C 5 H 5 NH) 2 Cr 2 O 7
19.6. Окисление спиртов и альдегидов
Окислители
Окисление спирта с образованием альдегида или кетона очень важно в синтезе. В этом процессе гидрокси-водород спирта заменяется уходящей группой (X на рисунке ниже).
Затем основание может отщеплять протон, связанный с углеродом спирта, что приводит к удалению уходящей группы X и образованию новой двойной связи углерод-кислород. Как вы можете увидеть, внимательно рассмотрев этот общий механизм, третичных спиртов не могут быть окислены таким образом — на последнем этапе нет водорода, который можно было бы выделить!
Окисление хромовой кислотой
В обычном методе окисления вторичных спиртов до кетонов в качестве окислителя используется хромовая кислота ( H 2 CrO 4 ).Хромовая кислота, также известная как реагент Джонса , получается путем добавления триоксида хрома (CrO 3 ) к водной серной кислоте. Окисление Джонса также использует ацетон в качестве сорастворителя в реакции, чтобы предотвратить чрезмерное окисление органического продукта.
Механизм окисления кетона хромовой кислотой показан ниже.
Обратите внимание, что хромовый реагент потерял две связи с кислородом в этой реакции и, таким образом, был восстановлен ( должно быть восстановлено, — это окислитель!).
Кетоны не окисляются хромовой кислотой, поэтому реакция останавливается на стадии кетона. Напротив, первичные спирты окисляются хромовой кислотой сначала до альдегидов, а затем сразу до карбоновых кислот.
На самом деле окисляется гидратная форма альдегида:
Одна из гидроксильных групп гидрата атакует хромовую кислоту, и реакция протекает в основном так, как показано для окисления вторичного спирта.
В некоторых условиях хромовая кислота даже окисляет углерод в бензильном положении до карбоновой кислоты (обратите внимание, что в этом превращении разрывается связь углерод-углерод).Мы наблюдали эту реакцию, используя KMnO 4 в разделе 16.3; подходит либо хромовая кислота, либо KMnO 4 , и они дают ту же самую карбоновую кислоту.
Ряд других распространенных окислителей обсуждается ниже.
Родственное соединение хрома (VI) хлорхромат пиридиния (PCC) также используется для окисления первичных спиртов до альдегидов. Дальнейшего окисления альдегида до стадии карбоновой кислоты не происходит, поскольку реакция проводится в безводных (безводных) органических растворителях, таких как дихлорметан, и поэтому гидратная форма альдегида не может образовываться.
Хлорхромат пиридиния образуется при объединении триоксида хрома, соляной кислоты и пиридина.
Условия окисления PCC также могут использоваться для окисления вторичных спиртов до кетонов.
Окисление по Сверну
Окисление по Сверну использует диметилсульфоксид и оксалилхлорид с последующим добавлением основания, такого как триэтиламин. Фактически окисляющим веществом в этой реакции является ион диметилхлорсульфония, который образуется из диметилсульфоксида и оксалилхлорида.
Механизм приведен ниже, для справки:
Окисление-окисление по Сверну (стадия 1)
Окисление-окисление по Сверну (стадия 2)
На второй стадии спирт реагирует с ионом хлорсульфония с образованием новой соли сульфония и HCl.Окисление-окисление по Сверну (стадия 3)
Окисление серебром (I)
Ион серебра , Ag (I), часто используется для окисления альдегидов до кетонов. Два общих условия реакции:
Набор реагентов в последних условиях реакции обычно известен как «реагент Толленс ».
Видео
Мировой рынок хромового ангидрида в 2021 году по производителям, регионам, типу и применению, прогноз до 2026 года
Список таблиц
Таблица 1.Глобальный доход от хромового ангидрида по типу, (млн долларов США), 2021-2026 гг.
Таблица 2. Глобальный доход от хромового ангидрида по областям применения, (млн долларов США), 2021-2026 гг.
Таблица 3. Основная информация Lanxess, производственная база и конкуренты
Таблица 4. Основной бизнес Lanxess
Таблица 5. Продукция и услуги Lanxess хромового ангидрида
Таблица 6. Продажи хромового ангидрида Lanxess (килотонны), цена (долл. США / тонна), выручка (млн долл. США), валовая прибыль и доля рынка ( 2019-2021д)
Таблица 7.Soda Sanayii Основная информация, производственная база и конкуренты
Таблица 8. Основной бизнес Soda Sanayii
Таблица 9. Продукция и услуги хромового ангидрида Soda Sanayii
Таблица 10. Продажи хромового ангидрида Soda Sanayii (килотонны), цена (долл. США за тонну) ), Выручка (в миллионах долларов США), валовая прибыль и доля рынка (2019-2021e)
Таблица 11. Основная информация Elementis, производственная база и конкуренты
Таблица 12. Elementis Major Business
Таблица 13.Хромовый ангидрид Elementis Продукция и услуги
Таблица 14. Продажи хромового ангидрида Elementis (килотонны), цена (долл. США / тонна), выручка (млн долл. США), валовая прибыль и доля рынка (2019-2021e)
Таблица 15. Hunter Chemical LLC Основная информация, производственная база и конкуренты
Таблица 16. Крупный бизнес Hunter Chemical LLC
Таблица 17. Продукция и услуги компании Hunter Chemical LLC по хромовому ангидриду
Таблица 18. Продажи хромового ангидрида Hunter Chemical LLC (килотонны), цена (долл. За тонну), выручка (млн долларов США), валовая прибыль и доля рынка (2019-2021e)
Таблица 19.Актюбинск Основная информация, производственная база и конкуренты
Таблица 20. Актюбинский основной бизнес
Таблица 21. Актюбинский продукт и услуги хромового ангидрида
Таблица 22. Продажи хромового ангидрида в Актюбинске (килотонны), цена (долл. США / тонна), выручка ( Млн долларов США), валовая прибыль и доля рынка (2019-2021e)
Таблица 23. Основная информация, производственная база и конкуренты MidUral Group
Таблица 24. Основной бизнес MidUral Group
Таблица 25.Продукция и услуги хромового ангидрида MidUral Group
Таблица 26. Продажи хромового ангидрида MidUral Group (килотонны), цена (долл. США / тонна), выручка (млн долл. США), валовая маржа и доля рынка (2019-2021e)
Таблица 27. Основная информация NPCC, производственная база и конкуренты
Таблица 28. Основные направления деятельности NPCC
Таблица 29. Продукция и услуги хромового ангидрида NPCC
Таблица 30. Продажи хромового ангидрида NPCC (килотонны), цена (долл. США / тонна), выручка ( В миллионах долларов США), валовая прибыль и доля рынка (2019-2021e)
Таблица 31.Основная информация Vishnu, производственная база и конкуренты
Таблица 32. Основной бизнес Vishnu
Таблица 33. Продукция и услуги хромового ангидрида Vishnu
Таблица 34. Продажи хромового ангидрида Vishnu (килотонны), цена (долл. США / тонна), выручка ( В миллионах долларов США), валовая прибыль и доля рынка (2019-2021e)
Таблица 35. Основная информация Nippon Chem, производственная база и конкуренты
Таблица 36. Основной бизнес Nippon Chem
Таблица 37.Nippon Chem Chromic Angel Product and Services
Таблица 38. Продажи Nippon Chem Chromic Anghydride (килотонны), цена (долл. США / тонна), выручка (млн долл. США), валовая прибыль и доля рынка (2019-2021e)
Таблица 39. Основная информация Zhenhua Chemical, производственная база и конкуренты
Таблица 40. Основной бизнес Zhenhua Chemical
Таблица 41. Продукция и услуги химического ангидрида Zhenhua
Таблица 42. Продажи химического ангидрида Zhenhua (килотонны), цена (долл. США за тонну) ), Выручка (в миллионах долларов США), валовая прибыль и доля рынка (2019-2021e)
Таблица 43.Yinhe Chemical Основная информация, производственная база и конкуренты
Таблица 44. Основной бизнес Yinhe Chemical
Таблица 45. Продукция и услуги Yinhe Chemical Chromic Angel ), Выручка (в миллионах долларов США), валовая прибыль и доля рынка (2019-2021e)
Таблица 47. Основная информация Chongqing Minfeng Chemical, производственная база и конкуренты
Таблица 48.Chongqing Minfeng Chemical Основной бизнес
Таблица 49. Chongqing Minfeng Химический хромовый ангидрид Продукция и услуги
Таблица 50. Продажи химического хромового ангидрида Chongqing Minfeng (килотонны), цена (долл. США / тонна), выручка (млн. Долл. США), валовая прибыль и Доля рынка (2019-2021e)
Таблица 51. Haining Peace Chemical Основная информация, производственная база и конкуренты
Таблица 52. Haining Peace Chemical Major Business
Таблица 53.Haining Peace Химический хромовый ангидрид Продукт и услуги
Таблица 54. Продажи химического хромового ангидрида Haining Peace (килотонны), цена (долл. США / тонна), доход (млн долл. США), валовая прибыль и доля рынка (2019-2021e)
Таблица 55. Zhonglan Yima Chemical Основная информация, производственная база и конкуренты
Таблица 56. Основной бизнес компании Zhonglan Yima Chemical
Таблица 57. Продукция и услуги Zhonglan Yima Chemical Chromic Anghydride
Таблица 58.Продажи химического хромового ангидрида компании Zhonglan Yima (килотонны), цена (долл. США / тонна), выручка (млн долл. США), валовая маржа и доля рынка (2019-2021e)
Таблица 59. Мировые продажи хромового ангидрида по производителям (2019-2021e) & (Килотон)
Таблица 60. Мировая выручка от хромового ангидрида по производителям (2019-2021e) и (млн долларов США)
Таблица 61. Положение производителей хромового ангидрида (уровень 1, уровень 2 и уровень 3), По выручке в 2020 г.
Таблица 62.Глобальные производственные мощности хромового ангидрида по компаниям (килотонн): 2020 VS 2021
Таблица 63. Головной офис и производственная площадка основного производителя хромового ангидрида
Таблица 64. Новые участники и планы по расширению производственных мощностей
Таблица 65. Хромовый ангидрид Слияния и поглощения за последние пять лет
Таблица 66. Мировые продажи хромового ангидрида по регионам (2016-2021e) и (килотонны)
Таблица 67. Мировые продажи хромового ангидрида по регионам (2021-2026) и (килотонны)
Таблица 68.Глобальный доход от хромового ангидрида по регионам (2016-2021e) и (млн долларов США)
Таблица 69. Глобальный доход от хромового ангидрида по регионам (2021-2026) и (млн долларов США)
Таблица 70. Мировые продажи хромового ангидрида по типам (2016 год) -2021e) и (килотонн)
Таблица 71. Мировые продажи хромового ангидрида по типам (2021-2026) и (килотонны)
Таблица 72. Мировые продажи хромового ангидрида по типам (2016-2021e) и (в миллионах долларов США)
Таблица 73. Мировая выручка от хромового ангидрида по типу (2021-2026) и (в миллионах долларов США)
Таблица 74.Глобальная цена хромового ангидрида по типу (2016-2021e) и (долл. США / тонна)
Таблица 75. Мировая цена хромового ангидрида по типу (2021-2026 гг.) И (долл. США / тонна)
Таблица 76. Мировые продажи хромового ангидрида по приложениям (2016-2021e) и (килотонн)
Таблица 77. Мировые продажи хромового ангидрида по приложениям (2021-2026) и (килотонны)
Таблица 78. Мировые доходы от хромового ангидрида по приложениям (2016-2021e) и (долл. США Миллион)
Таблица 79. Мировая выручка от хромового ангидрида по приложениям (2021-2026) и (в миллионах долларов США)
Таблица 80.Глобальная цена хромового ангидрида по областям применения (2016-2021e) и (долл. США / тонна)
Таблица 81. Мировая цена хромового ангидрида по областям применения (2021-2026 гг.) И (долл. США / тонна)
Таблица 82. Хромовый ангидрид в Северной Америке Продажи по странам (2016-2021e) и (килотонн)
Таблица 83. Продажи хромового ангидрида в Северной Америке по странам (2021-2026) и (килотонн)
Таблица 84. Выручка от хромового ангидрида в Северной Америке по странам (2016-2021e) & (Млн долларов США)
Таблица 85.Выручка от хромового ангидрида в Северной Америке по странам (2021-2026) и (млн долларов США)
Таблица 86. Продажи хромового ангидрида в Северной Америке по типам (2016-2021e) и (килотонны)
Таблица 87. Продажи хромового ангидрида в Северной Америке по типам (2021-2026) и (килотонн)
Таблица 88. Продажи хромового ангидрида в Северной Америке по приложениям (2016-2021e) и (килотонны)
Таблица 89. Продажи хромового ангидрида в Северной Америке по приложениям (2021-2026) и (килотонны) )
Таблица 90.Продажи хромового ангидрида в Европе по странам (2016-2021e) и (килотонны)
Таблица 91. Продажи хромового ангидрида в Европе по странам (2021-2026) и (килотонны)
Таблица 92. Выручка хромового ангидрида в Европе по странам (2016-2021e) ) & (Миллион долларов США)
Таблица 93. Выручка от хромового ангидрида в Европе по странам (2021-2026) и (в миллионах долларов США)
Таблица 94. Продажи хромового ангидрида в Европе по типу (2016-2021e) и (килотонны)
Таблица 95. Продажи хромового ангидрида в Европе по типу (2021-2026) и (килотонн)
Таблица 96.Продажи хромового ангидрида в Европе по приложениям (2016-2021e) и (килотонны)
Таблица 97. Продажи хромового ангидрида в Европе по приложениям (2021-2026) и (килотонны)
Таблица 98. Продажи хромового ангидрида в Азиатско-Тихоокеанском регионе по регионам (2016 -2021e) и (килотонн)
Таблица 99. Продажи хромового ангидрида в Азиатско-Тихоокеанском регионе по регионам (2021-2026) и (килотонны)
Таблица 100. Выручка от хромового ангидрида в Азиатско-Тихоокеанском регионе по регионам (2016-2021e) и (долл. США Миллион)
Таблица 101.Выручка хромового ангидрида в Азиатско-Тихоокеанском регионе по регионам (2021-2026 гг.) И (млн долларов США)
Таблица 102. Продажи хромового ангидрида в Азиатско-Тихоокеанском регионе по типам (2016-2021e) и (килотонны)
Таблица 103. Хромовый ангидрид в Азиатско-Тихоокеанском регионе Продажи по типу (2021-2026) и (килотонн)
Таблица 104. Продажи хромового ангидрида в Азиатско-Тихоокеанском регионе по приложениям (2016-2021e) и (килотонны)
Таблица 105. Продажи в Азиатско-Тихоокеанском регионе по приложениям (2021- 2026) & (Килотон)
Таблица 106.Продажи хромового ангидрида в Южной Америке по странам (2016-2021e) и (килотонны)
Таблица 107. Продажи хромового ангидрида в Южной Америке по странам (2021-2026) и (килотонны)
Таблица 108. Выручка от хромового ангидрида в Южной Америке по странам ( 2016-2021e) и (в миллионах долларов США)
Таблица 109. Выручка от хромового ангидрида в Южной Америке по странам (2021-2026) и (в миллионах долларов США)
Таблица 110. Продажи хромового ангидрида в Южной Америке по типам (2016-2021e) и ( Килотонн)
Таблица 111.Продажи хромового ангидрида в Южной Америке по типу (2021-2026) и (килотонн)
Таблица 112. Продажи хромового ангидрида в Южной Америке по приложениям (2016-2021e) и (килотонны)
Таблица 113. Продажи хромового ангидрида в Южной Америке по приложениям ( 2021-2026) и (килотонн)
Таблица 114. Продажи хромового ангидрида на Ближнем Востоке и в Африке по странам (2016-2021e) и (килотонны)
Таблица 115. Продажи хромового ангидрида на Ближнем Востоке и в Африке по странам (2021-2026) & (Килотон)
Таблица 116.Ближний Восток и Африка Выручка от хромового ангидрида по странам (2016-2021e) и (млн долларов США)
Таблица 117. Выручка от хромового ангидрида на Ближнем Востоке и в Африке по странам (2021-2026 годы) и (млн долларов США)
Таблица 118. Ближний Восток И продажи хромового ангидрида в Африке по типам (2016-2021e) и (килотонн)
Таблица 119. Продажи хромового ангидрида на Ближнем Востоке и в Африке по типам (2021-2026) и (килотонны)
Таблица 120. Ближний Восток и Африка Продажи по приложениям (2016-2021e) и (килотонн)
Таблица 121.Продажи хромового ангидрида на Ближнем Востоке и в Африке по областям применения (2021-2026) и (килотонн)
Таблица 122. Плюсы и минусы прямого канала
Таблица 123. Плюсы и минусы непрямого канала
Таблица 124. Типичные дистрибьюторы хромового ангидрида
Таблица 125. Типичные покупатели хромового ангидрида
Список рисунков
Рисунок 1. Хромовый ангидрид Рисунок
Рисунок 2. Доля мирового рынка продаж хромового ангидрида по типам в 2020 году
Рисунок 3.Чистота 99,7%
Рисунок 4. Чистота 99,8%
Рисунок 5. Чистота 99,9%
Рисунок 6. Доля мирового рынка продаж хромового ангидрида по областям применения в 2020 году
Рисунок 7. Полиграфическая промышленность и красящая промышленность
Рисунок 8. Гальваническая промышленность
Рисунок 9. Консервация древесины
Рисунок 10. Прочее
Рисунок 11. Размер мирового рынка хромового ангидрида, (млн долларов США) и (килотонн): 2020 VS 2021 VS 2026
Рисунок 12.Объем и прогноз мирового рынка хромового ангидрида (2016-2026) и (млн долларов США)
Рисунок 13. Мировые продажи хромового ангидрида (2016-2026) и (килотонн)
Рисунок 14. Мировые цены на хромовый ангидрид по типу (2016-2026 годы) ) & (Долл. США / тонна)
Рисунок 15. Мировые производственные мощности хромового ангидрида (2016-2026) и (килотонны)
Рисунок 16. Глобальные производственные мощности хромового ангидрида по географическим регионам: 2020 VS 2021
Рисунок 17.Движущие силы рынка хромового ангидрида
Рисунок 18. Ограничения рынка хромового ангидрида
Рисунок 19. Тенденции на рынке хромового ангидрида
Рисунок 20. Доля мирового рынка продаж хромового ангидрида по производителям в 2020 году
Рисунок 21. Доля мирового рынка выручки от хромового ангидрида по производителям в 2020 году
Рисунок 22. Доля рынка хромового ангидрида по типу компании (уровень 1, уровень 2 и уровень 3)
Рисунок 23. Доля рынка трех крупнейших производителей хромового ангидрида (выручка) в 2020 году
Рисунок 24.Доля рынка шести ведущих производителей хромового ангидрида (выручка) в 2020 г.
Рисунок 25. Доля мирового рынка продаж хромового ангидрида по регионам (2016-2026 гг.)
Рисунок 26. Доля мирового рынка выручки от хромового ангидрида по регионам (2016-2026 гг.)
Рисунок 27. Выручка от хромового ангидрида в Северной Америке (2016-2026) и (млн долларов США)
Рисунок 28. Выручка от хромового ангидрида в Европе (2016-2026 годы) и (млн долларов США)
Рисунок 29. Выручка от хромового ангидрида в Азиатско-Тихоокеанском регионе (2016 год) -2026) & (Миллионы долларов США)
Рисунок 30.Выручка от хромового ангидрида в Южной Америке (2016-2026 гг.) И (млн долларов США)
Рисунок 31. Выручка от хромового ангидрида на Ближнем Востоке и в Африке (2016-2026 годы) и (млн долларов США)
Рисунок 32. Доля мирового рынка продаж хромового ангидрида по типам (2016-2026)
Рисунок 33. Доля мирового рынка хромового ангидрида по типу (2016-2026)
Рисунок 34. Мировая цена хромового ангидрида по типу (2016-2026) и (долл. США / тонна)
Рисунок 35 . Доля мирового рынка продаж хромового ангидрида по приложениям (2016-2026)
Рисунок 36.Доля мирового рынка хромового ангидрида в выручке по приложениям (2016-2026)
Рисунок 37. Мировая цена хромового ангидрида по приложениям (2016-2026) и (долл. США за тонну)
Рисунок 38. Доля рынка продаж хромового ангидрида в Северной Америке по типу (2016-2026)
Рисунок 39. Доля рынка продаж хромового ангидрида в Северной Америке по приложениям (2016-2026)
Рисунок 40. Доля рынка продаж хромового ангидрида в Северной Америке по странам (2016-2026)
Рисунок 41.Доля рынка выручки от хромового ангидрида в Северной Америке по странам (2016-2026)
Рис. 42. Выручка от хромового ангидрида в США и темпы роста (2016-2026) и (в миллионах долларов США)
Рис. 43. Выручка от хромового ангидрида в Канаде и темпы роста ( 2016-2026) & (млн долларов США)
Рисунок 44. Мексика: выручка и темпы роста хромового ангидрида (2016-2026) и (млн долларов США)
Рисунок 45. Доля рынка продаж хромового ангидрида в Европе по типам (2016-2026)
Рисунок 46.Доля рынка продаж хромового ангидрида в Европе по приложениям (2016-2026 гг.)
Рисунок 47. Доля рынка продаж хромового ангидрида в Европе по странам (2016-2026 гг.)
Рисунок 48. Доля рынка выручки от хромового ангидрида в Европе по странам (2016-2026 гг.)
Рисунок 49. Выручка и темпы роста в Германии (2016-2026 гг.) И (в миллионах долларов США)
Рисунок 50. Выручка и темпы роста во Франции в отношении хромового ангидрида (2016-2026 годы) и (в миллионах долларов США)
Рисунок 51.Выручка от хромового ангидрида и темпы роста Соединенного Королевства (2016-2026) и (млн долларов США)
Рисунок 52. Выручка и темпы роста хромового ангидрида в России (2016-2026) и (млн долларов США)
Рисунок 53. Выручка от хромового ангидрида в Италии и Темпы роста (2016-2026) и (в миллионах долларов США)
Рисунок 54. Доля рынка продаж хромового ангидрида в Азиатско-Тихоокеанском регионе по регионам (2016-2026)
Рисунок 55. Доля рынка продаж хромового ангидрида в Азиатско-Тихоокеанском регионе по приложениям (2016- 2026)
Рисунок 56.Доля рынка продаж хромового ангидрида в Азиатско-Тихоокеанском регионе по регионам (2016-2026)
Рисунок 57. Доля рынка выручки от хромового ангидрида в Азиатско-Тихоокеанском регионе по регионам (2016-2026)
Рисунок 58. Выручка от хромового ангидрида в Китае и темпы роста (2016- 2026) & (Миллион долларов США)
Рисунок 59. Выручка от хромового ангидрида в Японии и темпы роста (2016-2026) & (Миллион долларов США)
Рисунок 60. Выручка и скорость роста хромового ангидрида в Корее (2016-2026) & (Миллион долларов США) )
Рисунок 61.Выручка от хромового ангидрида и темпы роста в Индии (2016-2026) и (млн долларов США)
Рисунок 62. Выручка от хромового ангидрида в Юго-Восточной Азии и темпы роста (2016-2026) и (млн долларов США)
Рисунок 63. Выручка от хромового ангидрида в Австралии и темпы роста Темпы роста (2016-2026) и (в миллионах долларов США)
Рисунок 64. Доля рынка продаж хромового ангидрида в Южной Америке по типу (2016-2026)
Рисунок 65. Доля рынка продаж хромового ангидрида в Южной Америке по приложениям (2016-2026)
Рисунок 66.Доля рынка продаж хромового ангидрида в Южной Америке по странам (2016-2026 гг.)
Рисунок 67. Доля рынка выручки от хромового ангидрида в Южной Америке по странам (2016-2026 гг.)
Рисунок 68. Выручка от хромового ангидрида в Бразилии и темпы роста (2016-2026 гг.) & (Млн. Долл. США)
Рисунок 69. Выручка и темпы роста Аргентины (2016-2026 гг.) & (Млн. Долл. США)
Рисунок 70. Доля рынка продаж хромового ангидрида на Ближнем Востоке и в Африке по типам (2016-2026 гг.)
Рисунок 71.Доля рынка продаж хромового ангидрида на Ближнем Востоке и в Африке по приложениям (2016-2026)
Рисунок 72. Доля рынка продаж хромового ангидрида Ближнего Востока и Африки по странам (2016-2026)
Рисунок 73. Рынок доходов от хромового ангидрида Ближнего Востока и Африки Доля по странам (2016-2026)
Рисунок 74. Выручка от хромового ангидрида в Турции и темпы роста (2016-2026) и (в миллионах долларов США)
Рисунок 75. Египетские доходы и темпы роста хромового ангидрида (2016-2026) и (в долларах США) Миллион)
Рисунок 76.Выручка от хромового ангидрида и темпы роста в Саудовской Аравии (2016-2026 гг.) И (млн долларов США)
Рисунок 77. Выручка и скорость роста хромового ангидрида в Южной Африке (2016-2026 годы) и (млн долларов США)
Рисунок 78. Канал продаж: прямой Канал и косвенный канал
Рисунок 79.

 7%
7% Специфическим считается применение «хромовой охры» при создании денежных знаков. В этой области применения окись хрома должна быть особенно чистой, без растворимых в воде примесей.
Специфическим считается применение «хромовой охры» при создании денежных знаков. В этой области применения окись хрома должна быть особенно чистой, без растворимых в воде примесей.