Амфотерные свойства веществ
1
H
ВодородВодород
1,008
1s1
2,2
Бесцветный газ
t°пл=-259°C
t°кип=-253°C
2
He
ГелийГелий
4,0026
1s2
Бесцветный газ
t°кип=-269°C
3
Li
ЛитийЛитий
6,941
2s1
0,99
Мягкий серебристо-белый металл
t°пл=180°C
t°кип=1317°C
4
Be
БериллийБериллий
9,0122
2s2
1,57
Светло-серый металл
t°пл=1278°C
t°кип=2970°C
5
B
БорБор
10,811
2s2 2p1
2,04
Темно-коричневое аморфное вещество
t°пл=2300°C
t°кип=2550°C
6
C
УглеродУглерод
12,011
2s2 2p2
2,55
Прозрачный (алмаз) / черный (графит) минерал
t°пл=3550°C
7
N
АзотАзот
14,007
2s2 2p3
3,04
Бесцветный газ
t°пл=-210°C
t°кип=-196°C
8
O
КислородКислород
15,999
2s2 2p4
3,44
Бесцветный газ
t°пл=-218°C
t°кип=-183°C
9
F
ФторФтор
18,998
2s2 2p5
4,0
Бледно-желтый газ
t°пл=-220°C
t°кип=-188°C
10
Ne
НеонНеон
20,180
2s2 2p6
Бесцветный газ
t°пл=-249°C
t°кип=-246°C
11
Na
НатрийНатрий
22,990
3s1
0,93
Мягкий серебристо-белый металл
t°пл=98°C
t°кип=892°C
12
Mg
МагнийМагний
24,305
3s2
1,31
Серебристо-белый металл
t°пл=649°C
t°кип=1107°C
13
Al
АлюминийАлюминий
26,982
3s2 3p1
1,61
Серебристо-белый металл
t°пл=660°C
t°кип=2467°C
14
Si
КремнийКремний
28,086
3s2 3p2
1,9
Коричневый порошок / минерал
t°пл=1410°C
t°кип=2355°C
15
P
ФосфорФосфор
30,974
3s2 3p3
2,2
Белый минерал / красный порошок
t°пл=44°C
t°кип=280°C
16
S
СераСера
32,065
3s2 3p4
2,58
Светло-желтый порошок
t°пл=113°C
t°кип=445°C
17
Cl
ХлорХлор
35,453
3s2 3p5
3,16
Желтовато-зеленый газ
t°пл=-101°C
t°кип=-35°C
18
Ar
АргонАргон
39,948
3s2 3p6
Бесцветный газ
t°пл=-189°C
t°кип=-186°C
19
K
КалийКалий
39,098
4s1
0,82
Мягкий серебристо-белый металл
t°пл=64°C
t°кип=774°C
20
Ca
КальцийКальций
40,078
4s2
1,0
Серебристо-белый металл
t°пл=839°C
t°кип=1487°C
21
Sc
СкандийСкандий
44,956
3d1 4s2
1,36
Серебристый металл с желтым отливом
t°пл=1539°C
t°кип=2832°C
22
Ti
ТитанТитан
47,867
3d2 4s2
1,54
Серебристо-белый металл
t°пл=1660°C
t°кип=3260°C
23
V
ВанадийВанадий
50,942
3d3 4s2
1,63
Серебристо-белый металл
t°пл=1890°C
t°кип=3380°C
24
Cr
ХромХром
51,996
3d5 4s1
1,66
Голубовато-белый металл
t°пл=1857°C
t°кип=2482°C
25
Mn
МарганецМарганец
54,938
3d5 4s2
1,55
Хрупкий серебристо-белый металл
t°пл=1244°C
t°кип=2097°C
26
Fe
ЖелезоЖелезо
55,845
3d6 4s2
1,83
Серебристо-белый металл
t°пл=1535°C
t°кип=2750°C
27
Co
КобальтКобальт
58,933
3d7 4s2
1,88
Серебристо-белый металл
t°пл=1495°C
t°кип=2870°C
28
Ni
НикельНикель
58,693
3d8 4s2
1,91
Серебристо-белый металл
t°пл=1453°C
t°кип=2732°C
29
Cu
МедьМедь
63,546
3d10 4s1
1,9
Золотисто-розовый металл
t°пл=1084°C
t°кип=2595°C
30
Zn
ЦинкЦинк
65,409
3d10 4s2
1,65
Голубовато-белый металл
t°пл=420°C
t°кип=907°C
31
Ga
ГаллийГаллий
69,723
4s2 4p1
1,81
Белый металл с голубоватым оттенком
t°пл=30°C
t°кип=2403°C
32
Ge
ГерманийГерманий
72,64
4s2 4p2
2,0
Светло-серый полуметалл
t°пл=937°C
t°кип=2830°C
33
As
МышьякМышьяк
74,922
4s2 4p3
2,18
Зеленоватый полуметалл
t°субл=613°C
(сублимация)
34
Se
СеленСелен
78,96
4s2 4p4
2,55
Хрупкий черный минерал
t°пл=217°C
t°кип=685°C
35
Br
БромБром
79,904
4s2 4p5
2,96
Красно-бурая едкая жидкость
t°пл=-7°C
t°кип=59°C
36
Kr
КриптонКриптон
83,798
4s2 4p6
3,0
Бесцветный газ
t°пл=-157°C
t°кип=-152°C
37
Rb
РубидийРубидий
85,468
5s1
0,82
Серебристо-белый металл
t°пл=39°C
t°кип=688°C
38
Sr
СтронцийСтронций
87,62
5s2
0,95
Серебристо-белый металл
t°пл=769°C
t°кип=1384°C
39
Y
ИттрийИттрий
88,906
4d1 5s2
1,22
Серебристо-белый металл
t°пл=1523°C
t°кип=3337°C
40
Zr
ЦирконийЦирконий
91,224
4d2 5s2
1,33
Серебристо-белый металл
t°пл=1852°C
t°кип=4377°C
41
Nb
НиобийНиобий
92,906
4d4 5s1
1,6
Блестящий серебристый металл
t°пл=2468°C
t°кип=4927°C
42
Mo
МолибденМолибден
95,94
4d5 5s1
2,16
Блестящий серебристый металл
t°пл=2617°C
t°кип=5560°C
43
Tc
ТехнецийТехнеций
98,906
4d6 5s1
1,9
Синтетический радиоактивный металл
t°пл=2172°C
t°кип=5030°C
44
Ru
РутенийРутений
101,07
4d7 5s1
2,2
Серебристо-белый металл
t°пл=2310°C
t°кип=3900°C
45
Rh
РодийРодий
102,91
4d8 5s1
2,28
Серебристо-белый металл
t°пл=1966°C
t°кип=3727°C
46
Pd
ПалладийПалладий
106,42
4d10
2,2
Мягкий серебристо-белый металл
t°пл=1552°C
t°кип=3140°C
47
Ag
СереброСеребро
107,87
4d10 5s1
1,93
Серебристо-белый металл
t°пл=962°C
t°кип=2212°C
48
Cd
КадмийКадмий
112,41
4d10 5s2
1,69
Серебристо-серый металл
t°пл=321°C
t°кип=765°C
49
In
ИндийИндий
114,82
5s2 5p1
1,78
Мягкий серебристо-белый металл
t°пл=156°C
t°кип=2080°C
50
Sn
ОловоОлово
118,71
5s2 5p2
1,96
Мягкий серебристо-белый металл
t°пл=232°C
t°кип=2270°C
51
Sb
СурьмаСурьма
121,76
5s2 5p3
2,05
Серебристо-белый полуметалл
t°пл=631°C
t°кип=1750°C
52
Te
ТеллурТеллур
127,60
5s2 5p4
2,1
Серебристый блестящий полуметалл
t°пл=450°C
t°кип=990°C
53
I
ИодИод
126,90
5s2 5p5
2,66
Черно-серые кристаллы
t°пл=114°C
t°кип=184°C
54
Xe
КсенонКсенон
131,29
5s2 5p6
2,6
Бесцветный газ
t°пл=-112°C
t°кип=-107°C
55
Cs
ЦезийЦезий
132,91
6s1
0,79
Мягкий серебристо-желтый металл
t°пл=28°C
t°кип=690°C
56
Ba
БарийБарий
137,33
6s2
0,89
Серебристо-белый металл
t°пл=725°C
t°кип=1640°C
57
La
ЛантанЛантан
138,91
5d1 6s2
1,1
Серебристый металл
t°пл=920°C
t°кип=3454°C
58
Ce
ЦерийЦерий
140,12
f-элемент
Серебристый металл
t°пл=798°C
t°кип=3257°C
59
Pr
ПразеодимПразеодим
140,91
f-элемент
Серебристый металл
t°пл=931°C
t°кип=3212°C
60
Nd
НеодимНеодим
144,24
f-элемент
Серебристый металл
t°пл=1010°C
t°кип=3127°C
61
Pm
ПрометийПрометий
146,92
f-элемент
Светло-серый радиоактивный металл
t°пл=1080°C
t°кип=2730°C
62
Sm
СамарийСамарий
150,36
Серебристый металл
t°пл=1072°C
t°кип=1778°C
63
Eu
ЕвропийЕвропий
151,96
f-элемент
Серебристый металл
t°пл=822°C
t°кип=1597°C
64
Gd
ГадолинийГадолиний
157,25
f-элемент
Серебристый металл
t°пл=1311°C
t°кип=3233°C
65
Tb
ТербийТербий
158,93
f-элемент
Серебристый металл
t°пл=1360°C
t°кип=3041°C
66
Dy
ДиспрозийДиспрозий
162,50
f-элемент
Серебристый металл
t°пл=1409°C
t°кип=2335°C
67
Ho
ГольмийГольмий
164,93
f-элемент
Серебристый металл
t°пл=1470°C
t°кип=2720°C
68
Er
ЭрбийЭрбий
167,26
f-элемент
Серебристый металл
t°пл=1522°C
t°кип=2510°C
69
Tm
ТулийТулий
168,93
f-элемент
Серебристый металл
t°пл=1545°C
t°кип=1727°C
70
Yb
ИттербийИттербий
173,04
f-элемент
Серебристый металл
t°пл=824°C
t°кип=1193°C
71
Lu
ЛютецийЛютеций
174,96
f-элемент
Серебристый металл
t°пл=1656°C
t°кип=3315°C
72
Hf
ГафнийГафний
178,49
5d2 6s2
Серебристый металл
t°пл=2150°C
t°кип=5400°C
73
Ta
ТанталТантал
180,95
5d3 6s2
Серый металл
t°пл=2996°C
t°кип=5425°C
74
W
ВольфрамВольфрам
183,84
5d4 6s2
2,36
Серый металл
t°пл=3407°C
t°кип=5927°C
75
Re
РенийРений
186,21
5d5 6s2
Серебристо-белый металл
t°пл=3180°C
t°кип=5873°C
76
Os
ОсмийОсмий
190,23
5d6 6s2
Серебристый металл с голубоватым оттенком
t°пл=3045°C
t°кип=5027°C
77
Ir
ИридийИридий
192,22
5d7 6s2
Серебристый металл
t°пл=2410°C
t°кип=4130°C
78
Pt
ПлатинаПлатина
195,08
5d9 6s1
2,28
Мягкий серебристо-белый металл
t°пл=1772°C
t°кип=3827°C
79
Au
ЗолотоЗолото
196,97
5d10 6s1
2,54
Мягкий блестящий желтый металл
t°пл=1064°C
t°кип=2940°C
80
Hg
РтутьРтуть
200,59
5d10 6s2
2,0
Жидкий серебристо-белый металл
t°пл=-39°C
t°кип=357°C
81
Tl
ТаллийТаллий
204,38
6s2 6p1
Серебристый металл
t°пл=304°C
t°кип=1457°C
82
Pb
СвинецСвинец
207,2
6s2 6p2
2,33
Серый металл с синеватым оттенком
t°пл=328°C
t°кип=1740°C
83
Bi
ВисмутВисмут
208,98
6s2 6p3
Блестящий серебристый металл
t°пл=271°C
t°кип=1560°C
84
Po
ПолонийПолоний
208,98
6s2 6p4
Мягкий серебристо-белый металл
t°пл=254°C
t°кип=962°C
85
At
АстатАстат
209,98
6s2 6p5
2,2
Нестабильный элемент, отсутствует в природе
t°пл=302°C
t°кип=337°C
86
Rn
РадонРадон
222,02
6s2 6p6
2,2
Радиоактивный газ
t°пл=-71°C
t°кип=-62°C
87
Fr
ФранцийФранций
223,02
7s1
0,7
Нестабильный элемент, отсутствует в природе
t°пл=27°C
t°кип=677°C
88
Ra
РадийРадий
226,03
7s2
0,9
Серебристо-белый радиоактивный металл
t°пл=700°C
t°кип=1140°C
89
Ac
АктинийАктиний
227,03
6d1 7s2
1,1
Серебристо-белый радиоактивный металл
t°пл=1047°C
t°кип=3197°C
90
Th
ТорийТорий
232,04
f-элемент
Серый мягкий металл
91
Pa
ПротактинийПротактиний
231,04
f-элемент
Серебристо-белый радиоактивный металл
92
U
УранУран
238,03
f-элемент
1,38
Серебристо-белый металл
t°пл=1132°C
t°кип=3818°C
93
Np
НептунийНептуний
237,05
f-элемент
Серебристо-белый радиоактивный металл
94
Pu
ПлутонийПлутоний
244,06
f-элемент
Серебристо-белый радиоактивный металл
95
Am
АмерицийАмериций
243,06
f-элемент
Серебристо-белый радиоактивный металл
96
Cm
КюрийКюрий
247,07
f-элемент
Серебристо-белый радиоактивный металл
97
Bk
БерклийБерклий
247,07
f-элемент
Серебристо-белый радиоактивный металл
98
Cf
КалифорнийКалифорний
251,08
f-элемент
Нестабильный элемент, отсутствует в природе
99
Es
ЭйнштейнийЭйнштейний
252,08
f-элемент
Нестабильный элемент, отсутствует в природе
100
Fm
ФермийФермий
257,10
f-элемент
Нестабильный элемент, отсутствует в природе
101
Md
МенделевийМенделевий
258,10
f-элемент
Нестабильный элемент, отсутствует в природе
102
No
НобелийНобелий
259,10
f-элемент
Нестабильный элемент, отсутствует в природе
103
Lr
ЛоуренсийЛоуренсий
266
f-элемент
Нестабильный элемент, отсутствует в природе
104
Rf
РезерфордийРезерфордий
267
6d2 7s2
Нестабильный элемент, отсутствует в природе
105
Db
ДубнийДубний
268
6d3 7s2
Нестабильный элемент, отсутствует в природе
106
Sg
СиборгийСиборгий
269
6d4 7s2
Нестабильный элемент, отсутствует в природе
107
Bh
БорийБорий
270
6d5 7s2
Нестабильный элемент, отсутствует в природе
108
Hs
ХассийХассий
277
6d6 7s2
Нестабильный элемент, отсутствует в природе
109
Mt
МейтнерийМейтнерий
278
6d7 7s2
Нестабильный элемент, отсутствует в природе
110
Ds
ДармштадтийДармштадтий
281
6d9 7s1
Нестабильный элемент, отсутствует в природе
Металлы
Неметаллы
Щелочные
Щелоч-зем
Благородные
Галогены
Халькогены
Полуметаллы
s-элементы
p-элементы
d-элементы
f-элементы
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
Оксиды — что это такое? Химические свойства и классификация
Поможем понять и полюбить химию
Начать учиться
133.6K
Знакомство с оксидами обычно начинается на уроках химии в 8 классе. Из этой статьи вы узнаете, что такое оксиды в химии, их классификацию и свойства, а также способы получения.
Определение оксидов
Оксиды — это сложные вещества, состоящие из двух химических элементов (т. е. бинарные соединения), один из которых — кислород в степени окисления −2.
Общая формула оксидов: ЭxOy, где Э – химический элемент, а x и y — индексы, определяемые степенью окисления химических элементов.
Узнай, какие профессии будущего тебе подойдут
Пройди тест — и мы покажем, кем ты можешь стать, а ещё пришлём подробный гайд, как реализовать себя уже сейчас
Виды оксидов
Все оксиды делятся на солеобразующие и несолеобразующие.
Несолеобразующие оксиды — это оксиды, которые не взаимодействуют с кислотами и щелочами, то есть не способны образовать соли.
К несолеобразующим оксидам относят: CO, SiO, N2O, NO.
Солеобразующие оксиды — это оксиды, которые взаимодействуют с кислотами и щелочами с образованием солей.
Солеобразующие оксиды делятся на три группы:
Основные оксиды — это оксиды, образованные металлами со степенью окисления +1 или +2.
Примеры основных оксидов: Na+12O, Ca+2O, Ba+2O.

Амфотерные оксиды — оксиды, образованные металлами со степенью окисления +3 или +4.
К амфотерным оксидам относят также: ZnO, BeO, PbO, SnO.
Несмотря на то, что эти металлы проявляют степень окисления +2 в данных соединениях, их оксиды проявляют амфотерные свойства.
Примеры амфотерных оксидов: Al+32O3, Fe2+3O3.
Кислотные оксиды — оксиды, образованные металлами с валентностью V и более или неметаллами с любой валентностью (за исключением несолеобразующих оксидов, то есть CO, SiO, N2O, NO).
Примеры кислотных оксидов: S+6O3, N2+5O5, Mn2+7O7.
Если один и тот же химический элемент образовывает несколько оксидов, то с увеличением степени окисления основные свойства оксидов ослабевают и усиливаются кислотные.
Например:
CrO (оксид хрома (II)) — проявляет основные свойства;
Cr2O3 (оксид хрома (III)) — проявляет амфотерные свойства;
CrO3 (оксид хрома (VI)) — проявляет кислотные свойства.
Закрепим знания о типах оксидов, изучив схему:
Номенклатура оксидов
Названия оксидов строятся по систематической номенклатуре следующим образом:
Пишем слово «оксид».
Указываем название второго химического элемента в родительном падеже.
Если этот элемент имеет переменную валентность, то указываем валентность элемента в этом соединении в скобках римской цифрой.
Примеры названий оксидов:
Fe2O3 — оксид железа (III).
 Читается: феррум два о три.
Читается: феррум два о три.Na2O — оксид натрия. Читается: натрия два о.
SO3 — оксид серы (VI). Читается: эс о три.
До появления систематической номенклатуры вещества называли по присущим им специфическим свойства (цвету, запаху и т. д.). Такой способ названия веществ — тривиальная номенклатура. Некоторые названия используются и сейчас.
Названия некоторых оксидов: таблица
Химическая формула оксида | Бытовое (тривиальное название) | Возможное научное название |
|---|---|---|
| H2O | Вода | Оксид водорода |
| CO2 | Углекислый газ | Оксид углерода (IV), диоксид углерода |
| CO | Угарный газ | Оксид углерода (II), монооксид углерода |
| SO3 | Серный газ | Оксид серы (VI), триоксид серы |
| SO2 | Сернистый газ | Оксиды серы (IV), диоксид серы |
| SiO2 | Кварц, горный хрусталь, песок кварцевый, речной и морской | Оксид кремния |
| Al2O3 | Глинозем | Оксид алюминия |
| Fe2O3 | Гематит (крокус) | Оксид железа (III) |
| CaO | Негашеная известь | Оксид кальция |
Химические свойства основных оксидов
1.
 Взаимодействие с водой
Взаимодействие с водойС водой способны реагировать оксиды тех металлов, которым соответствуют растворимые гидроксиды. То есть с водой реагируют только оксиды щелочных и щелочноземельных металлов.
Основный оксид + вода = основание Например: Na2O + H2O = 2NaOH |
|---|
Оксид магния взаимодействует с водой только при нагревании.
2. Взаимодействие с кислотными оксидами и кислотами
Основные оксиды, соответствующие щелочам, взаимодействуют со всеми кислотными оксидами и кислотами. Оксиды неактивных металлов взаимодействуют только с кислотными оксидами, соответствующими сильным кислотам, или с сильными кислотами.
Основный оксид + кислотный оксид = соль Например: BaO + SO3 = BaSO4 Основный оксид + кислота = соль + вода Например: Mg(OH)2 + 2HNO3 = Mg(NO3)2 + 2H2O |
|---|
3.
 Взаимодействие с амфотерными оксидами
Взаимодействие с амфотерными оксидамиВ эту реакцию могут вступать только основные оксиды щелочных или щелочноземельных металлов. При сплавлении двух оксидов образуется соль.
Основный оксид + амфотерный оксид = соль Например: Na2O + Al2O3 = NaAlO2 |
|---|
Как составлять такие соли: металл в этой соли берем из основного оксида, а кислотный остаток из амфотерного оксида (они проявляют более кислотные свойства).
Химические свойства кислотных оксидов
1. Взаимодействие с водой
Кислотные оксиды взаимодействуют с водой с образованием соответствующих кислот. За исключением SiO2, которому соответствует нерастворимая кремниевая кислота.
Кислотный оксид + вода = кислота Например: SO3 + H2O = H2SO4 |
|---|
2.
 Взаимодействие с основными оксидами и щелочами
Взаимодействие с основными оксидами и щелочамиКислотные оксиды сильных кислот способны взаимодействовать с любыми основными оксидами или основаниями.
Кислотный оксид + основный оксид = соль Например: SO3 + CuO = CuSO4 Кислотный оксид + основание = соль + вода Например: N2O5 + 2NaOH = 2NaNO3 + H2O |
|---|
Кислотные оксиды, соответствующие слабым кислотам (такие как CO2, SO2), способны взаимодействовать с основными оксидами, соответствующим щелочам, а также с щелочами.
3. Взаимодействие с амфотерными оксидами и гидроксидами
С амфотерными оксидами в реакцию вступают кислотные оксиды — как правило, сильных кислот.
Кислотный оксид + амфотерный оксид = соль Например: SO3 + Al2O3 = Al2(SO4)3 Кислотный оксид + амфотерный оксид = соль + вода Например: SO3 + Al(OH)3 = Al2(SO4)3 + H2O |
|---|
Химические свойства амфотерных оксидов
1. Взаимодействие с водой
Амфотерные оксиды не взаимодействуют с водой — даже при нагревании!
Амфотерный оксид + вода ≠ |
|---|
2. Взаимодействие с кислотными оксидами и кислотой
Амфотерные оксиды взаимодействуют только с сильными и средними кислотами и их оксидами.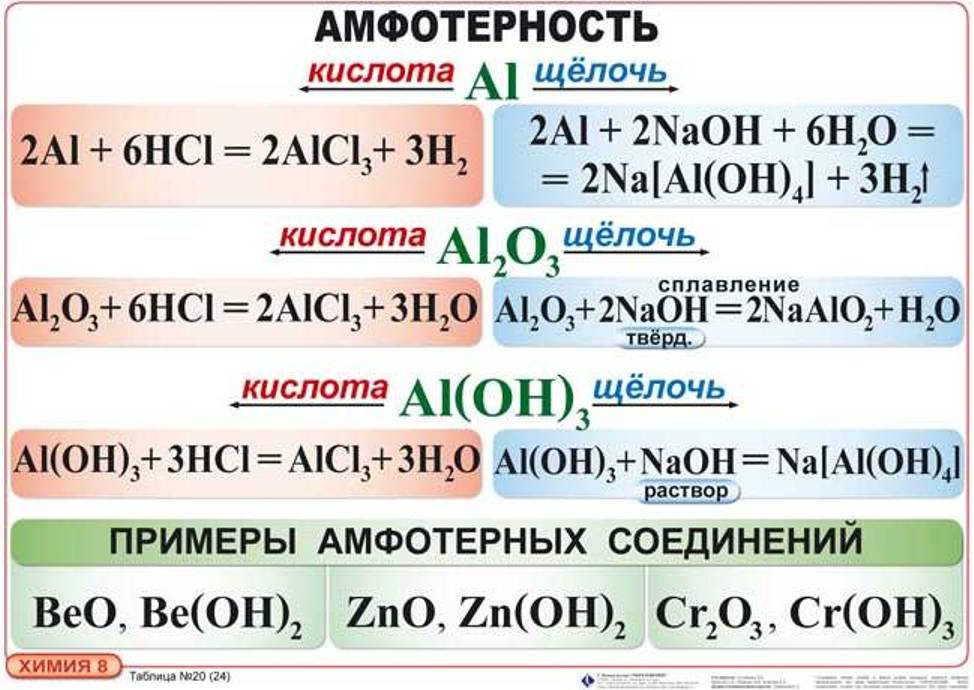
Амфотерный оксид + кислотный оксид = соль Например: Al2O3 + N2O5 = 2Al(NO3)3 Амфотерный оксид + кислота = соль + вода Например: Al2O3 + 6HCl = 2AlCl3 + 3H2O |
|---|
3. Взаимодействие с основными оксидами
Амфотерные оксиды взаимодействуют только с теми оксидами, которые соответствуют щелочам. Реакция протекает только в расплаве, так как в растворе такие оксиды взаимодействуют преимущественно с водой с образованием щелочей.
Амфотерный оксид + основный оксид (расплав) = соль Например: Al2O3 + Na2O = 2NaAlO2 |
|---|
4.
 Взаимодействие со щелочами
Взаимодействие со щелочамиПродукты взаимодействия амфотерных оксидов со щелочами зависят от условий проведения реакции. В растворе образуются комплексные соли, а при сплавлении – средние соли.
Амфотерный оксид + щелочь (раствор) + вода = комплексная соль Например: Al2O3 + 2NaOH + 3H2O = 2Na[Al(OH)4] Амфотерный оксид + щелочь (расплав) = средняя соль + вода Например: ZnO + 2KOH = K2ZnO2 + H2O |
|---|
Получение оксидов
1. Окисление металлов
Почти все металлы окисляются кислородом до устойчивых степеней окисления.
Например: 4Al + 3O2 = 2Al2O3
Исключение
Не взаимодействуют с кислородом: платина, золото и палладий.
Металлы с переменной степенью окисления, как правило, образуют соединения в степени окисления +3:
4Cr + 3O2 = 2Cr2O3
При взаимодействии щелочных металлов (элемента IA группы) образуются пероксиды Me2O2 или надпероксиды MeO2, где Ме — щелочной металл.
2. Окисление простых веществ — неметаллов
При окислении неметаллов в избытке кислорода, как правило, образуются высшие оксиды (это оксиды, в которых неметалл проявляют высшую степень окисления):
4P + 5O2 (избыток) = 2P2O5
При недостаточном количестве кислорода образуются оксиды неметаллов в промежуточной степени окисления:
4P + 3O2 (недостаток) = 2P2O3
Существуют и исключения. Например, сера окисляется лишь до оксида серы (IV) даже в избытке кислорода:
S + O2 = SO2
Или азот, который взаимодействует с кислородом только при температуре 2 000̊С или под действием электрического разряда с образованием оксида азота (II):
N2 + O2 = 2NO
Запомнить
Галогены (элементы VIIA группы) вовсе не взаимодействуют с кислородом, так же как и инертные газы (элементы VIIIA группы).
3. Разложение гидроксидов
Некоторые кислоты и гидроксиды неустойчивы и самопроизвольно разлагаются по схеме:
Гидроксид (кислота) = оксид + вода
Например:
H2SO3 = SO2↑ + H2O
H2CO3 = CO2↑ + H2O
Ag(OH) = Ag2O + H2O
NH4OH = NH3↑ + H2O
Оксиды тяжелых металлов (нерастворимые гидроксиды) и кремниевая кислота разлагаются при нагревании по той же самой схеме.
Например:
4. Окисление сложных веществ
Сложные бинарные (состоящие из двух химических элементов) соединения окисляются с образованием двух оксидов этих элементов в устойчивых степенях окисления.
Например:
2H2S + 3O2 = 2SO2 + 2H2O
4NH3 + 5O2 = 4NO + 6H2O
Также оксиды получают разложением солей, например, карбонатов, нитратов сульфатов и т. д.
д.
Например, Li2CO3 = Li2O + CO2↑
Мы узнали, какие вещества в химии называют оксидами, какие бывают оксиды, а также разобрали свойства каждого вида. Осталось подкрепить теорию практикой — а сделать это можно на курсах по химии в онлайн-школе Skysmart!
Татьяна Сосновцева
К предыдущей статье
107.3K
Ковалентные неполярные и полярные связи
К следующей статье
130.7K
Химические свойства металлов
Получите план обучения, который поможет понять и полюбить химию
На вводном уроке с методистом
Выявим пробелы в знаниях и дадим советы по обучению
Расскажем, как проходят занятия
Подберём курс
Амфотерные соединения, элементы, металлы характеристики
Амфотерных элементов (металлов) в таблице Менделеева пять Be, Al, Zn, Sn, Pb. Также эти оксиды и гидроксиды элементов являются амфотерными соединениями.
Амфотерные элементы и соединения реагируют как с кислотами, так и с основаниями и дают соответствующие продукты.
Также эти оксиды и гидроксиды элементов являются амфотерными соединениями.
Амфотерные элементы и соединения реагируют как с кислотами, так и с основаниями и дают соответствующие продукты.
Что такое амфотеризм?
Способность реагировать как кислота или основание известна как амфотеризм .
В этом уроке,
Сначала мы обсудим амфотерное поведение различных амфотерных элементов. Затем мы изучаем другие амфотерные соединения переходные металлы. Затем объясните некоторые вопросы амфотерных свойств и соединений.
Амфотерные металлы и их положение в таблице Менделеева
Все амфотерные элементы являются металлами и располагаются в блоках s, p, d.
- Be: s-блок (группа IIA)
- Al: p-блок (IIIA группа)
- Zn: d-блок (IIB группа)
- Sn: p-блок (IVA группа)
- Pb: p-блок (IVA группа) )
Амфотерное поведение Be, Al, Zn, Sn, Pb
Теперь поговорим об амфотерном поведении металлов Be, Al, Zn, Sn, Pb и их оксидов.
Амфотерное поведение бериллия
Бериллий является металлом щелочноземельных металлов. Бериллий реагирует с HCl с образованием хлорида бериллия (BeCl 2 ) и газа H 2 . Также бериллий реагирует с NaOH и дает берилат натрия. (NaBeO 2 .2H 2 O или Na 2 [Be(OH) 4 ]) и газообразный водород (H 2 ).
Бериллий и гидроксид натрия
Бериллий и HCl
Амфотерное поведение алюминия
Алюминий реагирует как с кислотами, так и с основаниями, проявляя амфотерные свойства.
Алюминий реагирует с кислотой HCl с образованием хлорида алюминия (AlCl 3 ) и газообразного водорода (H 2 ). Алюминий реагирует с NaOH и дает NaAlO 2 или Na + [Al(OH) 4 ] — , которые представляют собой водные растворы.
Реакция алюминия и гидроксида натрия
Алюминий и HCl
Гидроксид алюминия ( Al(OH) 3 ) также является амфотерным соединением.
Амфотерное поведение цинка
Цинк реагирует как с кислотами, так и с основаниями с образованием продуктов.
Реакция Zn и HCl
Реакция Zn и NaOH
Амфотерное поведение оксида цинка (ZnO)
ZnO может реагировать как кислотный, так и основной оксид, поэтому он известен как амфотерный оксид. ZnO реагирует с HCl (водн.) , NaOH (водн.) , Na 2 O (водн.) .
Реакция оксида цинка и соляной кислоты
Оксид цинка (ZnO) реагирует с соляной кислотой (HCl) с образованием хлорида цинка (ZnCl 2 ).
Реакция оксида цинка и гидроксида натрия
Оксид цинка (ZnO) реагирует с гидроксидом натрия (NaOH) с образованием цинката натрия (Na 2 ZnO 2 ).
Реакция оксида цинка и оксида натрия
Оксид цинка (ZnO) реагирует как кислота с оксидом натрия (Na 2 O ) и образует комплексный ион цинката [Zn(OH) 4 ] 2- . Формально эта реакция эквивалентна
реакция без воды.
Формально эта реакция эквивалентна
реакция без воды.
Амфотерное поведение гидроксида цинка
Гидроксид цинка ( Zn(OH) 2 ) представляет собой амфотерное соединение и белый осадок. Он реагирует с кислотой HCl (водн.) и дает водный раствор хлорида цинка ( ZnCl 2 ). Также Zn(OH) 2 реагирует с избытком NaOH и образует Na 2 [Zn(OH) 4 ].
Амфотерное поведение свинца
Свинец(Pb) реагирует с HCl с образованием хлорида свинца ( PbCl 2(s) ) и газообразного водорода ( H 2(g) ). Но Pb не растворяется в концентрированной HCl. потому что поверхностное покрытие PbCl 2 . Pb медленно реагирует с холодной щелочью и быстро горячей щелочью, образующей плюмбаты.
Реакция Pb и HCl
Реакция Pb и NaOH
Амфотерное поведение олова
Реакция олова(Sn) с разбавленной HNO 3 кислоты с образованием Sn(NO 3 ) 2 , NH 4 NO 3 и
вода. Sn медленно реагирует с холодной щелочью, но с горячей щелочью Sn реагирует быстро, образуя станнаты.
Sn медленно реагирует с холодной щелочью, но с горячей щелочью Sn реагирует быстро, образуя станнаты.
Реакция олова и азотной кислоты нитрат (NH
4 № 3 ) и вода как продуктыРеакция олова и гидроксида натрия
Олово реагирует с гидроксидом натрия с образованием станната натрия ( Na 2 [Sn(OH) 6 ] )
Амфотерное поведение иона бериллия
Оксид бериллия, гидроксид бериллия оксид проявляет амфотерное поведение.
Be(OH)
2 и OH —Be(OH)
2 и H +Амфотерные соединения d-блочных металлов 9 0016
Амфотерные характеристики соединений хрома
Некоторые соединения металлов 3d такие как гидроксид хрома, оксид хрома (III), оксид железа имеет амфотерные характеристики.
Амфотерные свойства гидроксида хрома (Cr(OH)
3 ) Хром
гидроксид (Cr(OH) 3 ) представляет собой амфотерное соединение и зеленый осадок. При добавлении NaOH (водн.) осадок растворяется и превращается в раствор [Cr(OH) 4 ] — (водн.) . Cr(OH) 3 реагирует с кислотами.
При добавлении NaOH (водн.) осадок растворяется и превращается в раствор [Cr(OH) 4 ] — (водн.) . Cr(OH) 3 реагирует с кислотами.
Амфотерные свойства оксида хрома(III)
Оксид хрома(III) (Cr 2 O 3 ) представляет собой амфотерное соединение. Он зеленого цвета и реагирует с как кислоты, так и основания.
Оксид хрома (III) и реакция NaOH
Оксид хрома (III) и реакция HCl
Амфотерное поведение оксида железа (Fe
2 O 3 )Оксид железа(Fe 2 O 3 ) реагирует как с кислотами, так и с основными оксидами
Fe
2 O 3 и кислотамиFe
2 O 3 и CaO или Na 2 CO 3Больше точек амфотерных соединений
- Ga 2 O 3 проявляет амфотерные характеристики.

Обзор амфотерных соединений, элементов, металлов
Ниже на рисунке показана сводка амфотерных соединений, таких как оксиды, гидроксиды и амфотерные металлы.
Вопросы учащихся
Все ли амфотерные элементы являются металлами?
Да. Все амфотерные элементы являются металлами.
Является ли NaOH амфотерным?
Нет. Гидроксиды, оксиды щелочных металлов не проявляют амфотерных свойств. Следовательно, NaOH не является амфотерным соединением.
Почему амфотерные оксиды образуют комплексные соединения?
Амфотерные соединения образуют комплексы с водой или щелочами. Также вы должны знать, что не только амфотерные соединения образуют комплексы. Если ион металла способен образовывать комплексы , нет необходимости в комплексном соединении для образования координационных комплексов. Все переходные металлы образуют комплексные соединения.
Щелочные металлы обладают меньшей способностью образовывать сложные соединения из-за их меньшего заряда (+1).
>Все блочные элементы 3d являются амфотерными по своей природе
НЕТ. Цинк — единственный амфотерный трехмерный блочный элемент.
расположение амфотерных гидроксидов в периодической таблице
Как существующие местоположения амфотерных металлов, амфотерные гидроксиды металлов расположены в местах расположения амфотерных металлов, поскольку все гидроксиды амфотерных металлов являются амфотерными. Вместо этого 3d металлический хром образует амфотерный гидроксид Cr(OH) 3 .
Связанные учебники по амфотерным соединениям
Амфотерная природа воды
Характеристики металлов в периодической таблице
Химия щелочных металлов
Идентифицировать катионы путем осаждения
Осаждает составные цвета
Характеристики металлов в периодической таблице
Узнать, идентификация, свойства и применение
Амфотерное вещество в химии — это молекула или ион, которые реагируют как с кислотой, так и с основанием. Амфотерные оксиды — это соединения, которые реагируют как с кислотами, так и с основаниями с образованием солей и воды. Многие металлы, в том числе бериллий, цинк, олово, свинец и алюминий, могут образовывать амфотерные оксиды или гидроксиды. Примером амфотерного оксида является \(Al_2O_3\). Степени окисления оксида сильно определяют амфотеризм.
Многие металлы, в том числе бериллий, цинк, олово, свинец и алюминий, могут образовывать амфотерные оксиды или гидроксиды. Примером амфотерного оксида является \(Al_2O_3\). Степени окисления оксида сильно определяют амфотеризм.
В этой статье мы узнаем об амфотерных оксидах, их определении, примерах, идентификации, свойствах и применении, а также часто задаваемых вопросах.
Амфотерные оксиды
Амфотерность, также известная как амфотерность, представляет собой способность химического вещества действовать как кислота и как основание. Молекула проявляет кислотное или основное поведение в зависимости от реагентов и других параметров реакции. Как правило, оксиды металлов являются основными, тогда как оксиды неметаллов являются кислотными.
В то время как некоторые металлические или полуметаллические оксиды являются амфотерными, некоторые неметаллические оксиды являются нейтральными. Эти обобщения имеют ряд исключений. Когда амфотерный оксид металла реагирует с кислотой, он образует соль и воду, что указывает на основное поведение амфотерного оксида. С другой стороны, когда амфотерный оксид реагирует с основанием, он снова образует соль и воду, что указывает на кислое поведение оксида.
С другой стороны, когда амфотерный оксид реагирует с основанием, он снова образует соль и воду, что указывает на кислое поведение оксида.
В этом состоянии рН амфотерного оксида варьируется в зависимости от реагентов. Если он реагирует с кислотой, pH амфотерного оксида будет больше 7, а при реакции с основанием pH будет меньше 7.9{-})\) также являются примерами амфотерных или амфипротонных соединений.
Амфотерные оксиды образуются из различных металлов, включая оксид алюминия \((Al_{2}O_{3})\), оксид свинца (PbO), цинк (ZnO) и оксид олова (SnO), а также такие металлы, как ванадий, хром, олово, железо, кобальт, медь, серебро, золото, галлий, индий, скандий, титан, цирконий, германий, сурьма, висмут, бериллий и теллур.
Идентификация амфотерных оксидов
Кислота и основание могут быть нейтрализованы амфотерным оксидом. Следовательно, необходимо изучить реакции соединения с кислотой, такой как HCl, и основанием, таким как NaOH, чтобы определить, является ли оно амфотерным. Данный материал должен быть определен, является ли он оксидом или нет, после подтверждения того, что он амфотерный. Существуют тесты на различные анионы, такие как сульфаты, нитраты, нитриты, хлориды и т. д. Если каждый тест дает отрицательный результат, сообщаемое вещество является оксидом.
Данный материал должен быть определен, является ли он оксидом или нет, после подтверждения того, что он амфотерный. Существуют тесты на различные анионы, такие как сульфаты, нитраты, нитриты, хлориды и т. д. Если каждый тест дает отрицательный результат, сообщаемое вещество является оксидом.
Элемент можно нагревать в кислороде для получения любого из оксидов. Гидратированные оксиды образуются при взаимодействии водных растворов тригалогенидов металлов с гидроксидом. По мере продвижения вниз по группе металлический характер вовлеченных элементов вызывает изменение кислотных оксидов на амфотерные и основные.
Природа оксидов элементов группы 13:
| Оксиды | Свойства |
| Слабокислая | |
| \(Al_{2}O_{3}\) | Амфотерная |
| \(Ga_{2}O_{3}\) | Амфотерная терик |
| \(In_{ 2}O_{3}\) | Слабоосновное |
| \(Tl_{2}O_{3}\) | Высокоосновное. окисляющий окисляющий |
Амфотерные оксиды в периодической таблице
В периодической таблице различные тенденции следуют слева направо в периоде и сверху вниз в группе. Кислотное, основное и амфотерное поведение различных оксидов металлов и неметаллов также можно объяснить изменяющейся тенденцией степени окисления, размера оксида и природы центрального элемента.
- Кислотность оксидов увеличивается в данный период таблицы Менделеева по мере увеличения неметаллического характера центрального элемента. Тенденция поведения оксидов в 3-м периоде таблицы Менделеева следующая:
| 2}О_{ 3}\) | \(SiO_{2}\) | \(P_{4}O_{18}\) | \(SO_{2}\) | \(Cl_{2}O_{7} \) | |||
| Поведение | Сильноосновные | Основные | Амфотерные | Слабокислые | Кислые | Кислые | Сильнокислые |
- Основная природа оксида металла увеличивается с увеличением атомного номера и размера центрального атома металла спустившись в группе.

\(NO_{2}\) и \(P_{2}O_{3}\) — кислотные, \(As_{2}O_{3}\) и \(Sb_{2}O_{3} \) являются амфотерными, а \(Bi_{2}O_{3}\) являются основными.
- Кислотная природа оксидов металлов увеличивается с увеличением степени окисления центрального атома металла.
\(MnO < Mn_{2}O_{3} < Mn_{2}O_{7}\)
Свойства амфотерных оксидов
Физические и химические свойства амфотерных оксидов обсуждаются следующим образом:
Физические Свойства
Амфотерные оксиды обычно имеют чрезвычайно высокие температуры плавления и кипения. Они имеют большие ковалентные структуры, для растворения которых требуется много энергии. Амфотерные оксиды обычно нерастворимы в воде.
Химические свойства
Наиболее важным свойством амфотерных оксидов является реакция как с кислотой, так и с основанием.
- Оксид свинца (PbO)
- Реакция с кислотой- \( PbO + 2HCl \rightarrow PbCl_{2} + H_{2}O\)
- Реакция с основание- \( PbO + 2NaOH + H_{2}O \rightarrow Na_{2}[Pb(OH)_{4}]\)
- Оксид алюминия \((Al_{2}O_{3 })\)
- Реакция с кислотой: \( Al_{2}O_{3} + 6HCl\rightarrow 2AlCl_{3} + 3 H_{2}O\)
- Реакция с основанием: \ (Al_{2}O_{3} + 2NaOH + 3H_{2}O \rightarrow 2Na[Al(OH)_{4}]\)
- Оксид цинка (ZnO)
- Реакция с кислота: \(ZnO + H_{2}SO_{4} \rightarrow ZnSO_{4} + H_{2}O\)
- Реакция с основанием: \(ZnO + 2NaOH + H_{2 }O \rightarrow Na_{2}[Zn(OH)_{4}]\)
- Оксид олова (SnO)
- Реакция с кислотой: \(SnO + 2HCl \rightleftharpoons SnCl_{2} + H_{2}O\) 9 0021
- Реакция с основанием : \(SnO + 4NaOH + H_{2}O \rightleftharpoons Na_{4}[Sn(OH)_{6}]\)
Применение амфотерных оксидов
Применение амфотерных оксидов довольно широко благодаря их способность реагировать как с кислотами, так и с основаниями. Вот некоторые из наиболее распространенных применений амфотерных оксидов:
Вот некоторые из наиболее распространенных применений амфотерных оксидов:
- Электрическое сопротивление, показатель преломления и поглощение рентгеновских лучей стеклом увеличиваются при добавлении PbO. Это также уменьшает вязкость стекла в то же время. Поэтому PbO имеет решающее значение для стекольной промышленности. PbO также используется в керамической промышленности для создания магнитно- и электрически инертных керамических изделий.
- Оксид цинка (ZnO) может использоваться для улучшения характеристик многих различных товаров и материалов, включая пластмассы, резину, стекло, керамику, смазочные материалы (включая цемент), мази (включая мази и кремы), краски (включая герметики), клеи (включая пищевые), пигменты (включая антипирены), батареи (включая батареи) и ленты для оказания первой помощи. Кроме того, он используется в производстве постоянных элементов, включая сухие элементы.
- Амфолиты представляют собой амфотерные соединения, включающие как кислотные, так и основные группы.
 В определенном диапазоне pH они обычно обнаруживаются в виде цвиттер-ионов. При изоэлектрическом фокусировании можно использовать аминолиты для поддержания стабильного градиента pH.
В определенном диапазоне pH они обычно обнаруживаются в виде цвиттер-ионов. При изоэлектрическом фокусировании можно использовать аминолиты для поддержания стабильного градиента pH. - В процессе производства алюминия дополнительно используется оксид алюминия \(Al_{2}O_{3}\). Этот оксид также является популярным наполнителем в полимерах, поскольку он химически белый и инертный. Помимо того, что он является обычным ингредиентом солнцезащитного крема, его также можно обнаружить в косметике, включая румяна, губную помаду и лак для ногтей. Иногда различные типы стекла изготавливаются с оксидом алюминия в качестве компонента. Он используется в качестве катализатора как в процессе Клауса, так и в дегидратации спирта до алкенов.
Нужна бесплатная помощь в подготовке к экзамену? Testbook содержит тщательно подобранные учебные материалы, практические наборы для экзаменов и полезные советы от профессионалов. Загрузите бесплатное приложение Testbook прямо сейчас и улучшите свою подготовку к экзамену благодаря специальным предложениям, которые ждут вас!
Часто задаваемые вопросы об амфотерных оксидах
Q. 1 Что такое амфотерные оксиды в двух примерах?
1 Что такое амфотерные оксиды в двух примерах?
Ans.1 Амфотерные оксиды представляют собой соединения, которые реагируют как с кислотами, так и с основаниями с образованием солей и воды. Например, ZnO, \(Al_{2}O_{3}\), PbO и др.
Q.2 Называется ли оксид алюминия также амфотерным оксидом?
Ответ 2 Да, \(Al_{2}O_{3}\) также называют амфотерным оксидом, так как он способен реагировать с кислотой и основанием.
Q.3 Какой элемент образует амфотерные оксиды?
Ans.3 Наиболее распространенными элементами, образующими амфотерные оксиды, являются Zn, Al, Pb, Sn, Cu, Be, As, Sb и т. д.
Q.4 Какой оксид является амфотерным?
Ans.4 Оксиды металлов, которые могут действовать как кислота или основание в химической реакции, называются амфотерными по своей природе.
Q.5 Является ли оксид цинка амфотерным или нейтральным?
Ans.


 Читается: феррум два о три.
Читается: феррум два о три.

 В определенном диапазоне pH они обычно обнаруживаются в виде цвиттер-ионов. При изоэлектрическом фокусировании можно использовать аминолиты для поддержания стабильного градиента pH.
В определенном диапазоне pH они обычно обнаруживаются в виде цвиттер-ионов. При изоэлектрическом фокусировании можно использовать аминолиты для поддержания стабильного градиента pH.