Сплав железа с алюминием: история открытия, свойства, преимущества
Сплавы железа с алюминием обладают уникальными свойствами, позволяющими применять их для изготовления деталей, подверженных термическим воздействиям, окислению или коррозии. Их использование имеет узкую направленность — они ориентированы на промышленные сферы эксплуатации.

Сплав железа с алюминием
История открытия
Первые попытки применения сплавов алюминия и железа были предприняты Фарадеем в 1820 году. Были попытки использовать сплав алюминия в качестве легирующего элемента для получения высокопрочной стали, но они оказались неэффективными.
Тщательные исследования были возобновлены после 1918 года в СССР, Германии, Англии. Было показано, что при добавлении Al возрастают жаропрочные свойства чугуна. Образцы обладают повышенной прочностью, хрупкостью, стойко переносят контакт с кислыми средами, не склонны к образованию окалин.
Было обнаружено, что появление окалин зависит от толщины оксидной плёнки на образцах: чем она толще, однороднее, тем выше защита поверхности. Важно, чтобы окислы не формировали эвтектическую фазу и не подвергались возгонке, а их ионная проводимость была минимальной.
Условием жаростойкости образца являются потери с окалиной в пределах 2-10-3–4-10-3 г/см2/ч.
Множество проведённых исследований сплавов Fe и Al закончились определением их химических и физических свойств. Это связано с проблемами газового насыщения образцов, угаром алюминия, формированием внутренних оксидных плёнок, разрушением образцов при нормальных условиях.
Наиболее перспективными оказались сплавы с содержанием от 16 до 20% Al и 3% углерода, получившие название «чугаль». Именно их начали выплавлять в СССР.
Позже группа изобретателей во главе с З. Эмингером разработала технологию производства качественных отливок железоалюминиевых образцов. Благодаря этому были получены новые данные.
Состав и структура
Структура сплава алюминия с железом представляет собой пересыщенный раствор Al в α-Fe с упорядочением структуры FeAl (тип В2), наличием включений Fe3AlCx. Свойства определяются упорядочением альфа-фазы и пересыщением. Чтобы сформировать однородный состав, необходим отжиг при температуре выше упорядочения состава с последующим регулируемым охлаждением.
При количестве Al 8–14% формируется столбчатая матричная структура. В процессе отжига структура немного упорядочивается: включения длиной до 150 мкм находятся вдоль границы зёрен. Выделение включений происходит при охлаждении из твёрдой фазы.
Метастабильное состояние фазы определяется количеством включений. Отжиг позволяет их сократить до 2%. Чем больше в составе алюминия, тем больше создаётся негомогенных областей, в результате чего понижается микротвёрдость матрицы до 0,4 ГПа и износостойкость образца.
С увеличением скорости отжига при водяном или воздушном охлаждении количество карбидных включений снижается.
14-20% сплав алюминия с железом имеет также матричную структуру, но карбидная фаза обеднена по Al и структура FeAl не упорядочена. При отжиге на воздухе количество карбидных включений возрастает, за счёт чего повышаются свойства износостойкости и прочности. Если проводить охлаждение в воде, то такого эффекта не наблюдается и образец получается хрупким.
При повышенном содержания в сплаве Al от 20 до 30% карбидной фазы становится меньше, при охлаждении образцов данная фаза отсутствует в структуре или не более 3%. За счёт большого количества алюминия образец приобретает высокую прочность и пластичность. Воздушное охлаждение после отжига стимулирует образование твёрдых износостойких фаз.
Увеличение содержания алюминия в расплаве становится причиной формирования интерметаллида Fe4Al13, который не устраняется после отжига, а образец становится непригодным для какого-либо практического применения.
Для улучшения свойств расплава в состав вводятся следующие легирующие элементы:
- 0,1–10% Cr;
- 0,1–0,2% Nb;
- 0,1–2,0% Si;
- 0,1–5% B;
- от 50 до 200 мг/кг Zr.
Содержание углерода — от 100 до 500 мг/кг.

Температура плавления
Характеристики и свойства
Сплавы железа и алюминия имеют следующие характеристики:
- количество циклов термического нагрева до 240, в зависимости от химического состава;
- предел прочности на растяжение 100 МПа;
- отличные литейные свойства сплава;
- допустимо применение легирующих элементов: Cr, Ni, Ti, Mo, Cu, B, Si, Nb, Zr.
Свойства сплава:
- хорошая свариваемость при условии термообработки выше +7000С;
- высокая химическая стойкость;
- необходимость формирования стабильной фазы расплава при температуре до 9000С;
- коррозионная стойкость.
Изготовление
Сплав создаётся из отходов дюрали, алюминия и железа путём алитирования. В жаростойкую ёмкость (электродуговую печь) засыпают, очищенные от окалин и грязи, куски стали (степень очистки 99%), 49% смесь Al или алюминиевого сплава, содержащего 2% хлористого аммония, а затем спекают в атмосфере аргона. Температура термообработки может составлять от +9000С до +15000С.
Нагрев ёмкости осуществляют подачей тока на нагревательные элементы или через саму конструкцию, при условии её высокого омического сопротивления.
После нагрева выбирают оптимальный способ отжига, в зависимости от состава компонент, с последующим естественным охлаждением.
Где применяют?
Железоалюминиевые расплавы применяются при производстве деталей и агрегатов, которые подвержены следующим воздействиям:
- термическому;
- механическому;
- окислительному.
Также сплавы заменяют никелевые сверхпрочные сплавы и специальные стали.

Изделия из сплава
Достоинства и недостатки
Преимущество сплава железа с алюминием — механические характеристики, которые сравнимы с некоторыми титановыми и никелевыми суперсплавами. Предел прочности при растяжении составляет до 100 МПа.
Другим достоинством является стойкость к окислению и коррозии при температурах до +7000С. При более высоких температурах допустимо применение таких конструкций, но без значительных механических нагрузок.
К недостаткам относят:
- хрупкость, проявляемую при определённых условиях эксплуатации и зависящую от температуры и нагрузок;
- при концентрации алюминия менее 12% сплав подвержен окислению, коррозии снижению пластичности;
- сложность получения стабильной фазы с заданными характеристиками;
- низкая прочность на растяжение.
Сплав легко расплавляется, что позволяет снизить расходы на его производство. Допустимо использование вторсырья, которое прошло соответствующие этапы очистки от примесей.
metalloy.ru
Железо и алюминий 2019
Железо против алюминияЖелезо и алюминий — это разные металлы, которые обладают различными свойствами. Оба металла «железо и алюминий» имеют разную молекулярную массу, атомный вес и атомные числа. Они также имеют разницу в химических и физических свойствах.
Одно из первых различий между двумя металлами заключается в том, что железо тяжелее алюминия. Алюминий имеет удельный вес 2,7 г / см3, что намного ниже, чем у железа. Этот малый вес делает алюминий лучшим металлом для использования на различных машинах.
С доисторических времен железо использовалось. В то время как алюминий был обнаружен Хансом Христианом в 1825 году. Хотя алюминий имеет атомное число 13 и атомный вес 26,981539 г моля, железо имеет атомное число 26 и атомный вес 55,845 г моля. Железо представлено в Периодической таблице как Fe (полученное из железа на латыни). Алюминий представлен символом Al (полученным из латинского Alumen).
При сравнении температуры плавления железо поставляется с более высокой температурой плавления 1535 градусов Цельсия. С другой стороны, алюминий имеет точку плавления 660,37 градуса Цельсия. Когда речь идет о точках кипения, у железа есть небольшое преимущество над Алюминием. Когда температура кипения железа составляет 2750 ° C, точка кипения Al составляет 2467 градусов Цельсия.
Ну, еще одно отличие, которое можно увидеть в том, что железо является магнитным, а алюминий немагнитным. Сравнивая цены, алюминий дороже железа. Это связано с тем, что извлечение алюминия из его руды довольно дорого, чем добыча железа из его руды. Однако алюминий является самым распространенным металлом в мире.
Алюминий — лучший проводник электричества, чем железо. Al также более пластичный, чем железо. Что касается ковкости, то алюминий занимает второе место среди металлов. Он также занимает шестое место по пластичности.
Резюме
1. Алюминий легче, чем железо.
2. Алюминий — самый распространенный металл, доступный в земле.
3. Железо магнитное и Алюминий немагнитный
4. Алюминий имеет атомный номер 13 и атомный вес 26,981539 г моля, железо имеет атомное число 26 и атомный вес 55,845 г моля.
5. Утюг имеет более высокую температуру кипения и плавления, чем алюминий.
6. Алюминий дороже железа.
7. Алюминий — лучший проводник электричества и более пластичный, чем железо.
ru.esdifferent.com
Железо в алюминии: источники и роль
Самая вредная примесь
Железо по праву считается одной из самых вредных примесей в алюминии. Особенно это заметно при производстве изделий из литейных алюминиевых сплавов при литье в кокиль и песчаные формы. Железо вместе с алюминием и другими легирующими элементами, такими как марганец, медь, магний и кремний образует промежуточные железосодержащие фазы, которые существенно снижают механическим свойства конечного изделия.
Железо из алюминиевого лома
Основное загрязнение алюминия железом происходит при переплавке алюминиевого лома, который смешан с железным ломом. Кроме того, алюминиевый лом сам может содержать высокую концентрацию железа. Это относится, например, к отходам литья алюминиевых сплавов под давлением. Чтобы свести к минимуму проблемы с загрязнением алюминия железным ломом, алюминиевая промышленность применяет тщательную сортировку лома перед загрузкой его в плавильную печь. Это включает ручную сортировку, магнитную сортировку, электромагнитную сортировку и так называемый «воздушный нож» для сортировки частиц измельченного лома по плотности.
Разбавлять вторичный алюминий первичным?
Простым путем снижения содержания железа в алюминии является разбавление его первичным алюминием. Однако часто это невыгодно.
Железосодержащие частицы в жидком и твердом алюминии
При затвердевании обычных алюминиево-кремниевых литейных сплавов первой обычно начинает затвердевать алюминиевая фаза. Другие составляющие сплава скапливаются в оставшихся жидкими областях между зернами первичной фазы. Загрязнение железом может приводить к изменениям в порядке затвердевания фаз: первыми появляются частицы железосодержащей промежуточной фазы, а уж затем происходит кристаллизации зерен алюминия. Когда эти частицы образуются раньше алюминия, то они имеют возможность свободного роста и поэтому вырастают в грубые кристаллы, окруженные жидкой фазой.
Влияние марганца на эффективность удаления железа
В литейных алюминиевых сплавах обычно применяют кремний для снижения вязкости алюминиевого расплава. Сплавы системы алюминий-железо-кремний имеют относительно высокую растворимость железа в жидкой фазе даже после удаления первичных кристаллов, содержащих железо. Поэтому, для снижения содержания железа в жидкой фазе в сплав добавляют марганец, который трансформирует систему алюминий-железо-креминий в систему алюминий-железо-марганец-кремний.
Добавление марганца дает изменение механизмов затвердевания, способствуя выделению промежуточных фаз, содержащих железо, а также снижению остаточной концентрации железа в жидкой фазе до приемлемым для литейных сплавов пределов. Расплавленный алюминий поддерживается при промежуточной температуре между образованием промежуточной фазы и появлением алюминия. Отделение твердой фазы от жидкой происходит путем фильтрования расплава при этой температуре.
Процесс удаления железа из алюминия
Эффективность добавок марганца на кинетику образования первичных фаз при затвердевании алюминиевых литейных сплавов дает способ удаления железа путем осаждения промежуточных фаз с последующим фильтрованием через керамический фильтр. Однако легким и дешевым его не назовешь. Тем не менее, он дает возможность применять алюминиевый лом из любого источника, независимо от первоначального содержания в нем железа, для применений, которые требуют низкого содержания железа, таких как литье алюминия в кокили или в песчаные формы.
Каждый состав вторичного алюминиевого расплава требует определенного количества добавок марганца и кремния (до состава литейных сплавов) для достижения высокой эффективности удаления железа. Количество добавленного марганца зависит от содержания в расплаве железа.
Удаление железа из алюминия производят в четыре этапа (рисунок):
1) добавление в расплав марганца и, при необходимости, кремния;
2) контролируемое охлаждение расплава для выделения в расплаве частиц промежуточной фазы Al(FeMn)Si;
3) отстаивание расплава для осаждения железосодержащих частиц на дно печи;
4) фильтрование расплава через керамический фильтр.
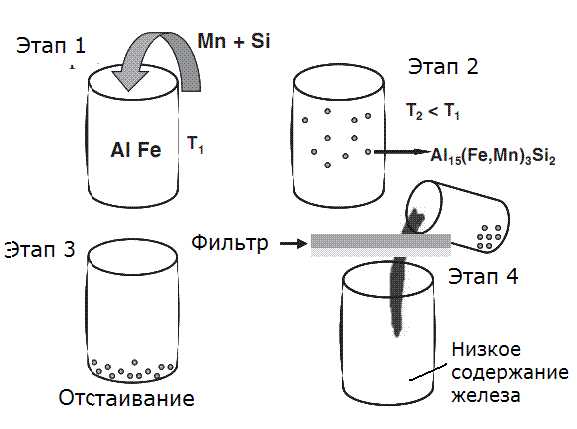
Рисунок — Схема процесса удаления железа из алюминия
Materials Transactions, Vol. 47, No. 7 (2006)
aluminium-guide.ru
Сплавы алюминия и железа — Справочник химика 21
Из сплавов алюминия наиболее распространен дюралюминий, сокращенно дюраль ( дюр означает твердый ). Большую твердость дюралю по сравнению с чистым А1 придают добавки меди ( 4%), марганца (—0,57о), магния (- 1,5%), кремния и железа (доли %). Применение нашли также сплав А1 с Si — силумин (16% Si) — и алюминиевая бронза (89% Си).СПЛАВЫ ХРОМ—АЛЮМИНИЙ —ЖЕЛЕЗО [c.207]
Сплав алюминий-железо [c.19]
Заслуживает интерес применение напыленного алюминиевого покрытия для повышения стойкости стали к высокотемпературному окислению при температурах до 900° С. Деталь подвергают обдуву металлической крошкой, после чего напыляют слой алюминия толщиной около 0,2 мм. Затем наносят слой битума или жидкого стекла и подвергают деталь диффузионному отжигу в печи при 850° С в течение 30 мин. Окончательное покрытие состоит пз последовательности сплавов алюминий — железо и наружной пленки алюминиевого окисла (рис. 6.29). Такое покрытие будет сопротивляться окислению в течение очень длительного времени при температурах до 900 С. При более высоких температурах диффузия железа в алюминий становится настолько быстрой, что слой сплава обогащается железом, и верхний слой содержит уже недостаточное количество алюминия для того, чтобы обеспечивать дальнейшую защиту. Усовершенствование этого процесса заключается в использовании алюминия, содержащего 0,75% d. Для этого сплава отпадает необходимость в операции покрытия деталей слоем битума или жидкого стекла. Деталь после нанесения на нее покрытия сразу же помещают в печь. Использование этого метода позволяет получать более толстый диффузионный слой. Этот процесс может быть использован и для некоторых марок чугуна. Но если в последнем слишком высоко содержание свободного графита, то алюминиевый слой не будет защищать от высокотемпературного окисления. [c.383]
Большая часть алюминия применяется в виде его сплавов с магнием, медью, кремнием, цинком, никелем, железом и другими металлами. Наиболее важные — сплавы типа дюралюминия (я 94% А1, 4% Си, 5% Mg и 0,5% Мп), литейные сплавы — силумины ( — 12% 51) и сплавы с магнием ( 10% Mg). По своим ценным свойствам сплавы алюминия занимают второе место после сплавов железа, причем области применения их неуклонно расширяются. Особенно возросло их применение в транспорте и строительном деле. Благодаря таким свойствам, как малая плотность,
В настоящее время алюминий получают электролитическим методом, так как попытка восстановления глинозема углем при высокой температуре ведет к образованию карбида. Восстановлением руд в мощных электропечах получают не чистый алюминий, а сплавы алюминия с медью и железом, кремнием, марганцем и другими металлами. [c.477]
Высокая вторичная электронная эмиссия сплава алюминия, железа, кремния и германия обусловливает возможность применения его в качестве катодного материала электронных ламп. [c.386]
Диаграмма состояния сплава алюминий-железо представлена на фиг. 16. [c.19]
Сплав алюминия с кремнием, так же как и сплав алюминий-железо, в нейтральных растворах вследствие наличия устойчивой пленки на алюминии корродирует медленно, и обнаружить разность потенциалов структурных составляющих не представляется возможным. В 0,Ш растворе МаОН пленка на алюминии разрушается, поэтому удалось [c.21]
В цехах, где соблюдается искробезопасность, применяется инструмент, изготовленный из сплавов алюминия, бронзы, бериллиевой бронзы. Взрывобезопасные гаечные ключи, молотки, кувалды изготовляются из сплава меди (70%), марганца, алюминия, железа и цинка. [c.380]
При получении покрытия из расплава в ванну с расплавленным алюминием обычно добавляют кремний, чтобы затруднить образование слоя хрупкого сплава. Полученные из расплава покрытия используют для повышения устойчивости к окислению при умеренных температурах таких изделий, как отопительные устройства и выхлопные трубы автомобилей. Они стойки к действию температуры до 480 °С. При еще более высоких температурах покрытия становятся огнеупорными, но сохраняют защитные свойства вплоть до 680 °С [21]. Использование алюминиевых покрытий для защиты от атмосферной коррозии ограничено вследствие более высокой стоимости по сравнению с цинковыми, а также из-за непостоянства эксплуатационных характеристик. В мягкой воде потенциал алюминия положителен по отношению к стали, поэтому покрытие является коррозионностойким, В морской и некоторых видах пресной воды, особенно содержащих С1″ и SO4″, потенциал алюминия становится более отрицательным и может произойти перемена полярности пары алюминий—железо. В этих условиях алюминиевое покрытие является протекторным и катодно защищает сталь. Показано, что покрытие из сплава А1—Zn, состоящего из 44 % Zn, 1,5 % Si, остальное — Al, имеет очень высокую стойкость в морской и промышленной атмосферах. Оно защищает также от окисления при повышенных температурах.
Металлический церий в смеси с другими элементами (А1, Са, М , V, Т1 и 51) используется в металлургии при изготовлении качественных сталей. Церий очищает металлическую ванну от азота, кислорода, серы и фосфора и делает шлак легкоплавким. Применяемый флюс в виде сплава содержит 5—15% церитовых металлов, 25—60% Л1 или 5—15%Са, Mg или 51 и 5—3% Т1, остальное — железо. Введение Се в металлический алюминий позволяет резко уменьшить в последнем содержание 51, нарушающего его структуру и снижающего прочность. В то время как нечистый металлический алюминий издает почти деревянный звук, металл, рафинированный церием, издает чистый колокольный звон. Церий в виде сплава с железом применяется для изготовления камней для зажигалок. [c.280]
При определении в бронзах алюминия, железа, никеля и цинка мед
www.chem21.info
Сплав железа с алюминием
Сплав на основе железа и алюминия содержит следующие компоненты, ат.%: алюминий 12-18; хром 0,1-10; ниобий 0,1-2,0; кремний 0,1-2,0; бор 0,1-5; титан 0,01-2,0, а также мг/кг: углерод 100-500; цирконий 50-200; железо — остальное. Техническим эффектом изобретения является повышение механических свойств при температурах свыше 700oС и значительное улучшение свариваемости. 1 з.п.ф-лы, 3 табл.,1 ил.
Сплавы железа с алюминием могут применяться в термически сильно нагруженных и подверженных окисляющим и/или корродирующим воздействиям деталях термических машин. Там во все возрастающей мере они должны заменить специальные стали, а также суперсплавы на основе никеля.
В литературной статье «Acceptable Aluminium Additions for Minimal Environmental Effect in Iron — Aluminium Alloys», Mat. Res. Soc. Symp. Proc. Vol. 288, s. 971-976, В.К. Сикка и другие описывают сплав железа с алюминием с содержанием около 16 вес.% алюминия и около 5 вес.% хрома, который при необходимости содержит около 0,1 вес.% углерода, и/или циркония, и/или 1 вес.% молибдена. Известный сплав имеет при комнатной температуре по сравнению со сплавами железа с алюминием с содержанием алюминия от 22 до 28 вес.% значительно более высокую пластичность. При температуре 700oC предел прочности при растяжении этого сплава с механическим напряжением около 100 МПа относительно невелик. Поэтому изготовленные из сплава детали не следовало бы применять при температурах выше 700oC. В основе изобретения, как это указано в пункте 1 формулы изобретения, лежит задача разработки сплава железа с алюминием, который отличается хорошими механическими свойствами при температурах свыше 700oC. Задачей изобретения является также надлежащее применение этого сплава. Сплав в соответствии с изобретением даже при температурах от 700 до 800oC еще обладает механическими свойствами, которые позволяют использовать его в механически незначительно нагруженных деталях. Наряду с этим сплав в соответствии с изобретением отличается отличной стойкостью при тепловых ударах и поэтому с особым преимуществом может использоваться в подверженных нагрузкам с изменением температуры деталях тепловых установок, как, в частности, в качестве корпуса или части корпуса газовой турбины или турбонагнетателя или в качестве соплового кольца, в частности, для турбонагнетателя. Помимо этого сплав можно получать с очень небольшими затратами с помощью литья или литья и прокатки. Другое преимущество сплава в соответствии с изобретением заключается в том, что его компоненты содержат исключительно металлы, которые можно приобрести сравнительно недорого и независимо от стратегического и политического влияния. На чертеже представлена диаграмма, на которой показан предел прочности при растяжении UTS (МПа) сплава I в соответствии с изобретением и сплава II в соответствии с уровнем техники в зависимости от температуры T (oC). В табл. 1 приведен состав сплава I (в соответствии с предпочтительным примером выполнения изобретения). В табл. 2 приведен состав сплава II (в соответствии с уровнем техники). Сплав I выплавляется в электродуговой печи в присутствии аргона в качестве защитного газа. В качестве исходных материалов служили отельные элементы со степенью чистоты выше 99%. Расплав отливался в виде отливки диаметром около 100 мм и высотой около 100 мм. Отливка вновь расплавлялась в вакууме и также в вакууме отливалась в форме цилиндрических стержней диаметром около 12 мм и длиной около 70 мм, в форме каротелей с минимальным диаметром около 10 мм, с максимальным диаметром около 16 мм и длиной около 65 мм или в форме дискообразных пластин диаметром 80 мм, толщиной до 14 мм и радиусом у кромки пластины около 1 мм. В ходе последующей технологической операции в дискообразных пластинах вдоль их оси выполнялось соответственно отверстие диаметром 19,5 мм. Из цилиндрических стержней и каротелей были изготовлены испытуемые образцы для испытаний на растяжение. Пластины предназначены для определения стойкости при тепловых ударах. В соответствии с выбранными размерами испытуемые образцы для определения механической прочности и стойкости при тепловых ударах были изготовлены из имеющегося в продаже и используемого в большом объеме в качестве материала для корпуса газовых турбин сплава II и родственного сплава с меньшим содержанием на 25% кремния и с меньшим содержанием на 40% молибдена. Испытания на растяжение проводились в зависимости от температуры. В результате для сплава I в соответствии с изобретением был получен предел прочности при растяжении, который при температуре 800oC с механическим напряжением около 100 МПа был значительно выше, чем предел прочности при растяжении сплава II в соответствии с уровнем техники. Соответствующее относится также и к не показанному на диаграмме сплаву в соответствии с уровнем техники с уменьшенным содержанием кремния и молибдена. С помощью дискообразных пластин определялась стойкость от тепловых ударов по Гленни. По две пластины каждого сплава циклически нагревались соответственно в псевдоожиженном слое до температуры 650oC и затем охлаждались с помощью сжатого воздуха до температуры 200oC. После определенного количества таких циклов нагревания и охлаждения затем было подсчитано количество возможно образующихся на кромке пластин трещин длиной более 2 мм. В табл. 3 указано суммированное количество появившихся на обеих пластинах трещин в зависимости от количества циклов для сплава I в соответствии с изобретением, а также для обоих сплавов в соответствии с уровнем техники. Из этого видно, что при использовании в качестве материала для корпусов газовых турбин сплавов в соответствии с уровнем техники уже после 240 циклов появляются нежелательные трещины, в то время как сплав в соответствии с изобретением даже после 740 циклов еще не имеет трещин. Сплав в соответствии с изобретением превосходит используемые сплавы в соответствии с уровнем техники не только относительно механической прочности при температурах выше 700oC, но и с точки зрения стойкости при тепловых ударах. Поэтому сплав в соответствии с изобретением может использоваться с большим преимуществом в качестве материала для деталей тепловых установок, которые при температурах от 700 до 800oC обладают еще сравнительно высокой механической прочностью и которые, как корпус газовых турбин, подвержены воздействию нагрузок при изменении температур. Изготовленный в соответствии с изобретением сплав имеет хорошие прочностные свойства при температурах от 700 до 800oC и большую стойкость при тепловых ударах тогда, когда содержание алюминия составляет минимум 12 и максимум 18 вес. %. Если содержание алюминия уменьшается ниже 12 вес.%, то ухудшается неокисляемость, коррозинностойкость и стойкость при тепловых ударах сплава в соответствии с изобретением. Если содержание алюминия более 18 вес.%, то сплав приобретает все более хрупкие свойства. Благодаря добавлению легирующей присадки хрома от 0,1 до 10 вес.% хрома повышается стойкость при тепловых ударах, улучшается неокисляемость и коррозинностойкость. Одновременно с помощью хрома улучшается пластичность. Однако добавление хрома более 10 вес.% вновь ухудшает механические свойства. Путем добавления легирующей присадки ниобия от 0,1 до 2 вес.% повышается твердость и прочность сплава в соответствии с изобретением. Наряду с ниобием или вместо него в качестве легирующей присадки можно добавлять также от 0,1 до 2 вес.% вольфрама и/или тантала. Содержание кремния от 0,1 до 2 вес.% кремния улучшает литейные свойства сплава в соответствии с изобретением и благоприятно сказывается на неокисляемости и коррозионностойкости. Кроме того, кремний повышает твердость. Благодаря добавлению легирующих присадок бора от 0,1 до 5 вес.% и титана от 0,01 до 2 вес.% значительно повышается стойкость при тепловых ударах, неокисляемость и коррозионностойкость сплава в соответствии с изобретением. Это обусловлено прежде всего тем, что в этом случае в сплаве образуется тонкодисперсный диборид титана TiB2. При высоких температурах и при вызывающих окисление и/или коррозию условиях на поверхности сплава в соответствии с изобретением образуется содержащий в основном окислы алюминия защитный слой. Фаза диборида титана способствует значительной стабилизации этого защитного слоя, так как фаза диборида титана в виде игольчатых кристаллитов проникает из сплава в защитный слой и в результате этого способствует особенно хорошему сцеплению защитного слоя с находящимся под ним сплавом. Содержание бора не должно составлять более 5 вес.%, а содержание титана должно быть не более 2 вес. %, так как в ином случае образуется слишком много диборида титана и сплав приобретает хрупкие свойства. Если содержание бора менее 0,1 вес.% и титана менее 0,01 вес.%, то значительно ухудшаются стойкость при тепловых ударах, неокисляемость и коррозионностойкость сплава в соответствии с изобретением. Незначительное повышение механической прочности и одновременно значительное улучшение свариваемости достигается благодаря добавлению легирующих присадок: от 100 до 500 мг/кг углерода и от 50 до 200 мг/кг циркония. Особенно хорошие показатели механической прочности и стойкости при тепловых ударах имеют сплавы следующего состава: от 14 до 16 вес.% алюминия, от 0,5 до 1,5 вес.% ниобия, от 4 до 6 вес.% хрома, от 0,5 до 1,5 вес.% кремния, от 3 до 4 вес.% бора, от 1 до 2 вес.% титана, около 300 мг/кг углерода, около 100 мг/кг циркония, остальное — железо.Формула изобретения
1. Сплав на основе железа и алюминия, содержащий хром, ниобий, кремний и бор, отличающийся тем, что он дополнительно содержит титан, углерод и цирконий при следующем соотношении компонентов, ат.%: Алюминий — 12 — 18 Хром — 0,1 — 10,0 Ниобий — 0,1 — 2,0 Кремний — 0,1 — 2,0 Бор — 0,1 — 5,0 Титан — 0,01 — 2,0 а также, мг/кг: Углерод — 100 — 500Цирконий — 50 — 200
Железо — Остальное
2. Сплав по п.1, отличающийся тем, что он содержит компоненты при следующем соотношении, ат.%:
Алюминий — 14 — 16
Хром — 4 — 6
Ниобий — 0,5 — 1,5
Кремний — 0,5 — 1,5
Бор — 3 — 4
Титан — 1 — 2
а также, мг/кг:
Углерод — Около 300
Цирконий — Около 100
Железо — Остальноел
РИСУНКИ
Рисунок 1, Рисунок 2findpatent.ru
Роль железа в литейных алюминиевых сплавах
Железо является обычной примесью всех алюминиевых сплавах — литейных и деформируемых. Оно попадает в него из нескольких источников и, по крайней мере, для сплавов Al—Si считается по разным причинам вредным. Необходимо отметить, что железо вредно не всегда.
В некоторых деформируемых алюминиевых сплавах, то есть сплавах, предназначенных для ковки, прессования или прокатки, железо может быть намеренным легирующим элементом для улучшения технологических свойств сплава и/или повышения прочности конечного изделия. Однако при изготовлении отливок не применяют эти деформируемые сплавы, а работают с литейными сплавами, которые имеют намного большее содержание легирующих элементов по сравнению с деформируемыми сплавами, а также почти всегда — то или иное количество кремния. Именное кремний делает эти сплавы литейными.
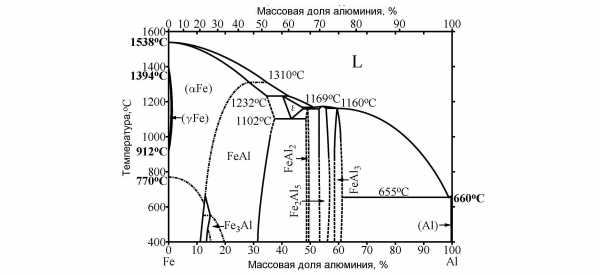 Фазовая диаграмма железо-алюминий
Фазовая диаграмма железо-алюминий
Железо — естественная примесь
Железо является естественной примесью, которая возникает в ходе производства первичного алюминия – превращения бокситов в глинозем и глинозема в расплавленный алюминий. В зависимости от качества исходной руды, степени контроля технологии и качества других исходных материалов жидкий первичный алюминий обычно содержит от 0,03 до 0,15 % железа, в среднем — от 0,07 до 0,10 %.
Экономичного способа удаления железа из алюминия не существует (см. также Железо в алюминии), поэтому эти «первичные» величины являются типичным нижним уровнем содержания железа в литейных и деформируемых алюминиевых сплавах, а все последующие обработки расплава могут только увеличивать его. Железо может попадать в расплав при его обработке по следующим двум основным механизмам.
Как железо попадает в алюминий
1. Жидкий алюминий способен растворять железо не защищенного от расплава стального плавильного инструмента, а также стального печного оборудования. При длительном контакте алюминия со сталью уровень железа в расплаве может достигать 2 % при температуре расплава 700 °С (эвтектика Al—Feвозникает при содержании железа 1,7 % и температуре 655 °С). Если расплав держать при температуре 800 °С, то уровень железа может достигнуть 5 %.
2. Железо может попадать в алюминиевый расплав через добавки не слишком чистых легирующих элементов, например, кремния, а также при добавлении лома, который обычно содержит значительно большее содержание железа, чем первичный металл.
По этим причинам уровень железа в алюминиевых сплавах продолжает увеличиваться с каждым переплавом. Поэтому вторичные алюминиевые сплавы, особенно те сплавы Al—Si, которые предназначены для литья под высоким давлением, ограничивают содержание железа величиной 1,5 %. В случае литья под высоким давлением высокое содержание железа как раз не так уж и плохо, так как оно помогает минимизировать дорогостоящую проблему налипания металла на матрицу. Однако типичные вторичные сплавы Al—Si для литья не под давлением обычно содержат железа намного меньше, в интервале от 0,25 до 0,8 %, а чаще всего – от 0,4 до 0,7 %.
Причина такого низкого содержания железа в сплавах происходит от коммерческого баланса между выгодами от пониженной стоимости металла и приемлемых технологических проблем с его литьем и/или уровнем конечных механических свойств.
Уровень железа в литейных алюминиевых сплавах
1. Насколько это возможно уровень железа в литейных алюминиевых сплавах Al—Si должен быть как можно более низким, чтобы избежать его отрицательного влияния на механические свойства, особенно на пластичность и вязкость разрушения. Это означает, что нужно свести до минимума загрязнения алюминиевых сплавов железом путем тщательного выбора шихты и применения огнеупорных защитных покрытий на всем стальном инструменте, который применяется при приготовлении и обработке расплавов.
2. Необходимо избегать содержания железа выше критического уровня для данного содержания кремния, так как это может привести к серьезной потере пластичности конечного литого изделия и снизить производительность разливки из-за увеличения брака из-за усадочной пористости и, в частности, по герметичности.
3. Предельное содержание железа (в %) для сплава Al—Si приближенно вычисляют по следующей формуле: Fe≈0,075 x [%Si] – 0,05.
4. Если скорость затвердевания/охлаждения очень высокая (например, при литье под высоким давлением), высокое содержание железа может быть полезным, но со снижением скорости охлаждения (литье в кокиль -> литье в песчаные формы) вероятность возникновения проблем при высоком содержании железа резко возрастает.
5. Традиционные режимы термической обработки для алюминиевых сплавов Al—Si, например Т6, не меняют природы железосодержащих фаз. В структуре остаются те же интерметаллические соединения и хотя в результате термической обработки общий уровень механических свойств сплава может улучшиться, он будет выше при изначально более низком содержании железа.
6. Часто применяют добавление марганца для «нейтрализации» вредного влияния железа в соотношении содержания марганца к содержанию железа около 0,5. Однако выгоды от этого не всегда очевидны. Избыток марганца может понизить долю β-фазы и способствовать образованию α-фазы железосодержащих соединений. Это может улучшить пластичность, но может привести к образованию так называемых твердых пятен и трудностям при механической обработке. При высоком содержании железа добавки марганца не всегда улучшают жидкотекучесть литейного алюминиевого сплава и снижают его пористость. Кроме того, добавление марганца в расплав с высоким содержанием железа может способствовать чрезмерному образованию шлака.
Источник: www.aomevents.com/conferences/…/Taylor
aluminium-guide.ru
Соединения алюминия и железа
Количество просмотров публикации Соединения алюминия и железа — 985
— характеристика элемента алюминия: электронное строение, возможные степени окисления, основные соединения: оксид, гидроксид, соли.
Алюминий — элемент 13-й группы периодической таблицы химических элементов (элемент главной подгруппы III группы), третьего периода, с атомным номером 13. Обозначается символом Al (лат. Aluminium). Относится к группе лёгких металлов. Электронная конфигурация нейтрального атома 1s22s22p63s23p1 = [10Ne]3s23p1, согласно которой алюминий в соединениях может иметь степень окисления +3 и 0.
Наиболее распространённый металл и третий по распространённости химический элемент в земной коре (после кислорода и кремния).
Простое вещество алюминий — лёгкий, парамагнитный металл серебристо-белого цвета͵ легко поддающийся формовке, литью, механической обработке. Алюминий обладает высокой тепло- и электропроводностью, стойкостью к коррозии за счёт быстрого образования прочных оксидных плёнок, защищающих поверхность от дальнейшего взаимодействия.
Основные соединения:
Оксид алюминия Al2O3– Амфотерный оксид, кислотные и основные свойства равно выражены. Белый, имеет ионное строение (Al 3+) 2(O 2-) 3. Тугоплавкий, термически устойчивый. Аморфный порошок гигроскопичен и химически активен, кристаллический – очень тверд и химически пассивен. Не реагирует с водой, разбавленными кислотами и щелочами. Переводится в раствор концентрированными кислотами и щелочами, реагирует со щелочами и карбонатом натрия при сплавлении. Применяется как сырье в производстве алюминия, для изготовления огнеупорных, химически стойких и абразивных материалов, особо чистый Al 2O 3– для изготовления рубиновых лазеров и синтетических драгоценных камней (рубины, сапфиры и др.), окрашенных примесями оксидов других металлов – Cr 2O 3(красный цвет), Ti 2O 3и Fe 2O 3(голубой цвет).
Уравнения важнейших реакций:
(эта реакция используется для ʼʼвскрытияʼʼ бокситов)
В природе входит в состав глиныи бокситов,образует минерал корунд.
Гидроксид алюминияAl(ОН)3 –Амфотерный гидроксид, кислотные и основные свойства равно выражены. Белый, аморфный (гелеобразный) или кристаллический. Связи Al–ОН преимущественно ковалентные. Разлагается при нагревании без плавления. Практически не растворяется в воде. Реагирует с кислотами, щелочами в растворе и при сплавлении. Не реагирует с NH 3Н 2O, NH 4Cl, СO 2, SO 2и H2S.
МетагидроксидАlO(ОН) химически менее активен, чем Al(ОН) 3. Промежуточный продукт в производстве алюминия. Применяется для синтеза других соединений алюминия (в том числекриолита),органических красителей, как лекарственный препарат при повышенной кислотности желудочного сока.
Уравнения важнейших реакций:
— термическое разложение
— основная и кислотная диссоциация в растворе
(реакции характеризуют очень малую растворимость в воде и амфотерность гидроксида, поставляющего в раствор одновременно ионы ОН и Н +примерно в равной концентрации; гидроксид диссоциирует слабее, чем сама вода)
— амфотерные свойства
Al(ОН)3+ ЗНСlразб.) = AlCl 3+ ЗН 2O
Al(ОН)3+ NaOH (т)= NaAlO 2+ 2Н 2O (1000 °C)
Al(ОН)3+ NaOH(конц.) = Na[Al(OH) 4] (p)
Для получения осадка Al(ОН) 3щелочь обычно не используют из-за легкости перехода осадка в раствор, а действуют на соли алюминия гидратом аммиака. При комнатной температуре образуется Al(ОН) 3, а при кипячении – менее активный АlO(ОН):
Удобный способ получения Al(ОН) 3– пропускание СO 2через раствор гидроксокомплекса:
[Al(ОН) 4] —+ СO 2= Al(ОН) 3↓ +HCO 3—
Соли алюминия
Тетрагидроксоалюминат(III) натрияNa[Al(OH) 4] – Комплексная соль. С таким составом существует при комнатной температуре в концентрированном растворе NaOH. Для твердого состояния состав условный, так как при кристаллизации из раствора он усложняется (выделены Na 4[Al(OH) 7], Na 4[Al4O3(OH)10] и др.). При прокаливании твердые соли разлагаются до диоксоалюмината(III) натрия NaAlO2, при разбавлении их растворов – до Al(ОН) 3. По-разному реагируют с сильными и слабыми кислотами, с хлоридом алюминия и карбонатом аммония.
Уравнения важнейших реакций:
Получение: взаимодействие Al(ОН) 3и солей алюминия с NaOH в концентрированном растворе:
Al(OH) 3+ NaOH(конц.) = Na[Al(OH) 4]
AlCl 3+ 4NaOH(конц.) = Na[Al(OH) 4]+ 3NaCl
Образуется из оксида алюминия как промежуточный продукт при промышленном ʼʼвскрытииʼʼ бокситов.
Хлорид алюминияAlCl 3–Бескислородная соль. Белый, легкоплавкий, сильнолетучий. В паре состоит из ковалентных мономеров AlCl 3(треугольное строение, sр 2-гибридизация, преобладают при 440–800 °C) и димеров Al 2Cl 6(точнее, Cl 2AlCl 2AlCl 2, строение – два тетраэдра с общим ребром, sр 3-гибридизация, преобладают при 183–440 °C). Гигроскопичен, на воздухе ʼʼдымитʼʼ. Образует кристаллогидрат, разлагающийся при нагревании. Хорошо растворим в воде (с сильным экзо-эффектом), полностью диссоциирует на ионы, создает в растворе сильнокислотную среду вследствие гидролиза. Реагирует со щелочами, гидратом аммиака. Восстанавливается при электролизе расплава. Вступает в реакции ионного обмена.
Качественная реакцияна ион Al 3+– образование осадка AlРO 4, который переводится в раствор концентрированной серной кислотой.
Применяется как сырье в производстве алюминия, катализатор в органическом синтезе и при крекинге нефти, переносчик хлора в органических реакциях. Уравнения важнейших реакций:
ПолучениеAlCl3в промышленности– хлорирование каолина, глинозёма или боксита в присутствии кокса:
Al 2O 3+ ЗС (кокс) + ЗCl 2= 2AlCl 3+ ЗСО (900 °C)
Сульфид алюминияAl 2S 3–Бескислородная соль. Белый, связь Al – S преимущественно ковалентная. Плавится без разложения под избыточным давлением N 2, легко возгоняется. Окисляется на воздухе при прокаливании. Полностью гидролизуется водой, не осаждается из раствора. Разлагается сильными кислотами. Применяется как твердый источник чистого сероводорода. Уравнения важнейших реакций:
Al 2S 3+ 6Н 2O = 2Al(ОН) 3↓ + 3H 2S↑ (чистый)
Al 2S 3+ 6НCl (разб.) = 2AlCl 3+ 3H 2S↑
Al 2S 3+ 24HNO 3(конц.) = Al 2(SO 4) 3+ 24NO 2↑ + 12H 2O (100 °C)
2Al 2S 3+ 9O 2(воздух) = 2Al 2O 3+ 6SO 2 (700–800 °C)
Получение: взаимодействие алюминия с расплавленной серой в отсутствие кислорода и влаги:
2Al + 3S = Al2S3(150–200 °C)
Cульфат алюминия-калияKAl(SO 4)2–Двойная оксосоль. Белый, гигроскопичный. При сильном нагревании разлагается. Образует кристаллогидрат — алюжокалиевые квасцы.Умеренно растворим в воде, гидролизуется по катиону алюминия. Реагирует со щелочами, гидратом аммиака.
Применяется как протрава при крашении тканей, дубитель кож, коагулянт при очистке пресной воды, компонент составов для проклеивания бумаги, наружное кровоостанавливающее средство в медицине и косметологии. Образуется при совместной кристаллизации сульфатов алюминия и калия.
Уравнения важнейших реакций:
— характеристика элемента железа: электронное строение, возможные степени окисления, основные соединения: оксид, гидроксид, соли.
Железо– элемент 4-го периода и VIIIБ-группы Периодической системы, порядковый номер 26. Электронная формула атома 1s22s22p63s23p63d64s2=[18Ar]3d 64s 2, характерные степени окисления 0, +II и +III (последняя наиболее устойчива).
Шкала степеней окисления железа:
Железо Fe простое вещество. Серый мягкий, ковкий, тугоплавкий металл. Обычное железо медленно окисляется во влажном воздухе (ржавеет), чистое железо коррозии не подвергается. Не реагирует с водой, пассивируется в концентрированных серной и азотной кислотах.
Компактный металл покрывается при нагревании на воздухе оксидной пленкой (окалиной),а порошок сгорает; реагирует с хлором и серой:
Восстанавливает водяной пар (старый способ получения водорода в промышленности):
3Fe + 4Н 2O (пар) = (Fe IIFe 2III)O 4+ 4Н 2(800 °C)
В ряду напряжений стоит левее водорода, реагирует с разбавленными кислотами НCl и H 2SO 4, при этом образуются соли железа(II) и выделяется водород:
Fe + 2Н += Fe 2++ Н 2↑
(реакции проводятся без доступа воздуха, иначе Fe IIпостепенно переводится кислородом в Fe III).
При действии на железо более сильного окислителя (здесь – азотная кислота) оно сразу переходит в катион Fe 3+:
Fe + 4HNO 3(разб.) = Fe(NO 3) 3+ NO↑ + 2H 2O
Амфотерность железа проявляется только в концентрированных щелочах при кипячении:
Fe + 2NaOH (50 %) + 2Н 2O = Na 2[Fe(OH) 4]↓ + Н 2↑
и образуется осадок тетрагидроксоферрата(II) натрия.
Железо вытесняет (по ряду напряжений) менее активные металлы из растворов их солей:
Fe + CuSO 4= FeSO 4+ Cu↓
Железо медленно окисляется во влажном воздухе (ржавеет), из-за рыхлости коричневой ржавчины(Fe IIFe 2III)O 4защитный слой не создается. Процесс ржавления:
Техническое железо– сплавы железа с углеродом: чугунсодержит 2,06—6,67 % С, сталь0,02—2,06 % С, часто присутствуют другие естественные примеси (S, Р, Si) и вводимые искусственно специальные добавки (Mn, Ni, Cr), что придает сплавам железа технически полезные свойства – твердость, термическую и коррозионную стойкость, ковкость и др.
Оксид железа(II)FeO – Амфотерный оксид с большим преобладанием базовых свойств. Черный, имеет ионное строение Fe 2+O 2-. При нагревании вначале разлагается, затем образуется вновь. Не образуется при сгорании железа на воздухе. Не реагирует с водой. Разлагается кислотами, сплавляется со щелочами. Медленно окисляется во влажном воздухе. Восстанавливается водородом, коксом. Участвует в доменном процессе выплавки чугуна. Применяется как компонент керамики и минеральных красок. Уравнения важнейших реакций:
Получение в лаборатории: термическое разложение соединений железа (II) без доступа воздуха:
Fe(OH) 2= FeO+ H 2O (150–200 °C)
FeCO 3= FeO+ СO 2(490–550 °C)
Оксид дижелеза (III) – железа(II) (Fe IIFe 2III)O4 – двойной оксид. Черный, имеет ионное строение Fe 2+(Fe 3+) 2(O 2-) 4. Термически устойчив до высоких температур.
Размещено на реф.рф
Не реагирует с водой. Разлагается кислотами. Восстанавливается водородом, раскаленным железом. Участвует в доменном процессе производства чугуна. Применяется как компонент минеральных красок ( железный сурик),керамики, цветного цемента. Продукт специального окисления поверхности стальных изделий ( чернение, воронение).По составу отвечает коричневой ржавчине и темной окалине на железе. Применение брутто-формулы Fe 3O 4не рекомендуется. Уравнения важнейших реакций:
Получение: сгорание железа (см.) на воздухе.
В природе – оксидная руда железа магнетит.
Оксид железа(III)Fe 2O 3–Амфотерный оксид с преобладанием базовых свойств. Красно-коричневый, имеет ионное строение (Fe 3+) 2(O 2-) 3. Термически устойчив до высоких температур.
Размещено на реф.рф
Не образуется при сгорании железа на воздухе. Не реагирует с водой, из раствора выпадает бурый аморфный гидрат Fe 2O 3nН 2O. Медленно реагирует с кислотами и щелочами. Восстанавливается монооксидом углерода, расплавленным железом. Сплавляется с оксидами других металлов и образует двойные оксиды — шпинели(технические продукты называются ферритами). Применяется как сырье при выплавке чугуна в доменном процессе, катализатор в производстве аммиака, компонент керамики, цветных цементов и минеральных красок, при термитной сварке стальных конструкций, как носитель звука и изображения на магнитных лентах, как полирующее средство для стали и стекла.
Уравнения важнейших реакций:
Получениев лаборатории– термическое разложение солей железа(III) на воздухе:
Fe 2(SO 4) 3= Fe 2O 3+ 3SO 3(500–700 °C)
4{Fe(NO 3) 39 H 2O} = 2Fe aO 3+ 12NO 2+ 3O 2+ 36H 2O (600–700 °C)
В природе – оксидные руды железа гематит Fe 2O 3и лимонит Fe 2O 3nН 2O.
Гидроксид железа (II)Fe(OH) 2–Амфотерный гидроксид с преобладанием базовых свойств. Белый (иногда с зеленоватым оттенком), связи Fe – ОН преимущественно ковалентные. Термически неустойчив. Легко окисляется на воздухе, особенно во влажном состоянии (темнеет). Нерастворим в воде. Реагирует с разбавленными кислотами, концентрированными щелочами. Типичный восстановитель. Промежуточный продукт при ржавлении железа. Применяется в изготовлении активной массы железоникелевых аккумуляторов.
Уравнения важнейших реакций:
Получение: осаждение из раствора щелочами или гидратом аммиака в инертной атмосфере:
Fe 2++ 2OН(разб.) = Fe(OH) 2↓
Fe 2++ 2(NH 3H 2O) = Fe(OH) 2↓ + 2NH 4+
Метагидроксид железаFeO(OH)–Амфотерный гидроксид с преобладанием базовых свойств. Светло-коричневый, связи Fe–О и Fe – ОН преимущественно ковалентные.
При нагревании разлагается без плавления. Нерастворим в воде. Осаждается из раствора в виде бурого аморфного полигидрата Fe 2O 3nН 2O, который при выдерживании под разбавленным щелочным раствором или при высушивании переходит в FeO(OH). Реагирует с кислотами, твердыми щелочами. Слабый окислитель и восстановитель. Спекается с Fe(OH) 2. Промежуточный продукт при ржавлении железа. Применяется как основа желтых минеральных красок и эмалей, поглотитель отходящих газов, катализатор в органическом синтезе.
Соединение состава Fe(OH) 3не известно (не получено).
Уравнения важнейших реакций:
Получение: осаждение из раствора солей железа(III) гидрата Fe 2O 3nН 2O и его частичное обезвоживание (см. выше).
В природе – оксидная руда железа лимонитFe 2O 3nН 2O и минерал гётитFeO(OH).
Соли железа:
Феррат калияK 2FeO 4–Оксосоль. Красно-фиолетовый, разлагается при сильном нагревании. Хорошо растворим в концентрированном растворе КОН, реагирует с кипящей водой, неустойчив в кислотной среде. Сильный окислитель. Качественная реакция– образование красного осадка феррата бария. Применяется в синтезе ферритов – промышленно важных двойных оксидов железа (III) и других металлов.
Уравнения важнейших реакций:
Получение: образуется при окислении соединений железа, к примеру метагидроксида FeO(OH), бромной водой, а также при действии сильных окислителей (при спекании) на железо
Fe + 2KOH + 2KNO 3= K 2FeO 4+ 3KNO 2+ H 2O (420 °C)
и электролизе в растворе:
(феррат калия образуется на аноде).
Качественные реакции на ионыFe 2+и Fe 3+.Обнаружение ионов Fe 2+и Fe 3+в водном растворе проводят с помощью реактивов K 3[Fe(CN) 6] и K 4[Fe(CN) 6] соответственно; в обоих случаях выпадает синий продукт одинакового состава и строения, KFe III[Fe II(CN) 6]. В лаборатории данный осадок называют берлинская лазурь,или турнбуллева синь:
Fe 2++ К ++ [Fe(CN) 6] 3-= KFe III[Fe II(CN) 6]↓
Fe 3++ K ++ [Fe(CN) 6] 4-= KFe III[Fe II(CN) 6]↓
Химические названия исходных реактивов и продукта реакций:
K 3[Fe(CN) 6] – гексацианоферрат (III) калия
K 4[Fe(CN) 6] – гексацианоферрат (II) калия
KFe III[Fe II(CN) 6] – гексацианоферрат (II) железа(III) калия
Вместе с тем, хорошим реактивом на ионы Fe 3+является тиоцианат-ион NCS —, железо (III) соединяется с ним, и появляется ярко-красная (ʼʼкроваваяʼʼ) окраска:
Fe 3++ 6NCS– = [Fe(NCS) 6] 3-
Этим реактивом (к примеру, в виде соли KNCS) можно обнаружить даже следы железа (III) в водопроводной воде, в случае если она проходит через железные трубы, покрытые изнутри ржавчиной.
Хлорид железа(Н)FeCl 2–Бескислородная соль. Белый (гидрат голубовато-зеленый), гигроскопичный. Плавится и кипит без разложения. При сильном нагревании летуч в потоке HCl. Связи Fe – Cl преимущественно ковалентные, пар состоит из мономеров FeCl 2(линейное строение, sp-гибридизация) и димеров Fe 2Cl 4. Чувствителен к кислороду воздуха (темнеет). Хорошо растворим в воде (с сильным экзо-эффектом), полностью диссоциирует на ионы, слабо гидролизуется по катиону. При кипячении раствора разлагается. Реагирует с кислотами, щелочами, гидратом аммиака. Типичный восстановитель. Вступает в реакции ионного обмена и комплексообразования.
Применяется для синтеза FeCl 3и Fe 2O 3, как катализатор в органическом синтезе, компонент лекарственных средств против анемии.
Уравнения важнейших реакций
Получение:взаимодействие Fe с соляной кислотой:
Fe + 2НCl = FeCl 2+Н 2↑
(в промышленностииспользуют хлороводород и ведут процесс при 500 °C).
Хлорид железа(III)FeCl 3–Бескислородная соль. Черно-коричневый (темно-красный в проходящем свете, зеленый в отраженном), гидрат темно-желтый. При плавлении переходит в красную жидкость. Весьма летуч, при сильном нагревании разлагается. Связи Fe – Cl преимущественно ковалентные. Пар состоит из мономеров FeCl 3(треугольное строение, sр 2-гибридизация, преобладают выше 750 °C) и димеров Fe 2Cl 6(точнее, Cl 2FeCl 2FeCl 2, строение – два тетраэдра с общим ребром, sр 3-гибридизация, преобладают при 316–750 °C). Кристаллогидрат FeCl 36Н 2O имеет строение [Fe(H 2O) 4Cl2]Cl ‣‣‣ 2Н 2O. Хорошо растворим в воде, раствор окрашен в желтый цвет; сильно гидролизован по катиону. Разлагается в горячей воде, реагирует со щелочами. Слабый окислитель и восстановитель.
Применяется как хлорагент, катализатор в органическом синтезе, протрава при крашении тканей, коагулянт при очистке питьевой воды, травитель медных пластин в гальванопластике, компонент кровоостанавливающих препаратов.
Уравнения важнейших реакций:
Сульфид железа (II)FeS – Бескислородная соль. Черно-серый с зеленым оттенком, тугоплавкий, разлагается при нагревании в вакууме. Во влажном состоянии чувствителен к кислороду воздуха. Нерастворим в воде. Не выпадает в осадок при насыщении растворов солей железа(II) сероводородом. Разлагается кислотами. Применяется как сырье в производстве чугуна, твердый источник сероводорода.
Соединение железа(III) состава Fe 2S 3не известно (не получено).
Уравнения важнейших реакций:
Получение:
Fe + S = FeS (600 °C)
Fe 2O 3+ H 2 + 2H 2S = 9 FeS+ 3H 2O (700-1000 °C)
FeCl 2+ 2NH 4HS (изб.) = FeS↓ + 2NH 4Cl + H 2S↑
Дисульфид железаFeS 2–Бинарное соединение. Имеет ионное строение Fe 2+(—S – S—) 2-. Темно-желтый, термически устойчивый, при прокаливании разлагается. Нерастворим в воде, не реагирует с разбавленными кислотами, щелочами. Разлагается кислотами-окислителями, подвергается обжигу на воздухе. Применяется как сырье в производстве чугуна, серы и серной кислоты, катализатор в органическом синтезе. В природе – рудные минералы пирити марказит.
Уравнения важнейших реакций:
FeS 2= FeS + S (выше 1170 °C, вакуум)
2FeS 2+ 14H 2SO 4(конц., гор.) = Fe 2(SO 4) 3+ 15SO 2↑ + 14Н 2O
FeS 2+ 18HNO 3(конц.) = Fe(NO 3) 3+ 2H 2SO 4+ 15NO 2↑ + 7H 2O
4FeS 2+ 11O 2(воздух) = 8SO 2+ 2Fe 2O 3(800 °C, обжиг)
Сульфат железа (II)FeSO 4–Оксосоль. Белый (гидрат светло-зеленый, техническое название железный купорос),гигроскопичный. Разлагается при нагревании. Хорошо растворим в воде, в малой степени гидролизуется по катиону. Быстро окисляется в растворе кислородом воздуха (раствор желтеет и мутнеет). Реагирует с кислотами-окислителями, щелочами, гидратом аммиака. Типичный восстановитель.
Применяется как компонент минеральных красок, электролитов в гальванотехнике, консервант древесины, фунгицид, лекарственное средство против анемии. В лаборатории чаще берется в виде двойной соли Fe(NH 4) 2(SO 4) 26Н 2O ( соль Мора),более устойчивой к действию воздуха.
Уравнения важнейших реакций:
Получение:
Fe + H 2SO 4(разб.) = FeSO 4+ H 2↑
FeCO 3+ H 2SO 4(разб.) = FeSO 4+ CO 2↑ + H 2O
— применение соединений алюминия и железа.
Железо — один из самых используемых металлов, на него приходится до 95 % мирового металлургического производства.
Железо является основным компонентом сталей и чугунов — важнейших конструкционных материалов.
Железо может входить в состав сплавов на базе других металлов — к примеру, никелевых.
Магнитная окись железа (магнетит) — важный материал в производстве устройств долговременной компьютерной памяти: жёстких дисков, дискет и т. п.
Ультрадисперсный порошок магнетита используется во многих чёрно-белых лазерных принтерах в смеси с полимерными гранулами в качестве тонера. Здесь одновременно используется чёрный цвет магнетита и его способность прилипать к намагниченному валику переноса.
Уникальные ферромагнитные свойства ряда сплавов на базе железа способствуют их широкому применению в электротехнике для магнитопроводов трансформаторов и электродвигателей.
Хлорид железа(III) (хлорное железо) используется в радиолюбительской практике для травления печатных плат.
Семиводный сульфат железа (железный купорос) в смеси с медным купоросом используется для борьбы с вредными грибками в садоводстве и строительстве.
Железо применяется в качестве анода в железо-никелевых аккумуляторах, железо-воздушных аккумуляторах.
Водные растворы хлоридов двухвалентного и трёхвалентного железа, а также его сульфатов используются в качестве коагулянтов в процессах очистки природных и сточных вод на водоподготовке промышленных предприятий.
Алюминий широко применяется как конструкционный материал. Основные достоинства алюминия в данном качестве — лёгкость, податливость штамповке, коррозионная стойкость (на воздухе алюминий мгновенно покрывается прочной плёнкой Al2O3, которая препятствует его дальнейшему окислению), высокая теплопроводность, неядовитость его соединений. В частности, эти свойства сделали алюминий чрезвычайно популярным при производстве кухонной посуды, алюминиевой фольги в пищевой промышленности и для упаковки. Первые же три свойства сделали алюминий основным сырьем в авиационной и авиакосмической промышленности (в последнее время медленно вытесняется композитными материалами, в первую очередь, углеволокном).
Основной недостаток алюминия как конструкционного материала — малая прочность, в связи с этим для упрочнения его обычно сплавляют с небольшим количеством меди и магния (сплав принято называть дюралюминий).
Электропроводность алюминия всего в 1,7 раза меньше, чем у меди, при этом алюминий приблизительно в 4 раза дешевле за килограмм, но, за счёт в 3,3 раза меньшей плотности, для получения равного сопротивления его нужно приблизительно в 2 раза меньше по весу. По этой причине он широко применяется в электротехнике для изготовления проводов, их экранирования и даже в микроэлектронике при изготовлении проводников в чипах. Меньшую электропроводность алюминия (37 ом−1) по сравнению с медью (63 ом−1) компенсируют увеличением сечения алюминиевых проводников. Недостатком алюминия как электротехнического материала является наличие прочной оксидной плёнки, затрудняющей пайку и за счёт большего сопротивления вызывающей повышенное нагревание в местах электрических соединений — что, в свою очередь, отрицательно сказывается на надежности контакта и состоянии изоляции.
Благодаря комплексу свойств широко распространён в тепловом оборудовании.
Алюминий и его сплавы сохраняют прочность при сверхнизких температурах. Благодаря этому он широко используется в криогенной технике.
Высокий коэффициент отражения в сочетании с дешевизной и лёгкостью напыления делает алюминий идеальным материалом для изготовления зеркал.
В производстве строительных материалов как газообразующий агент.
Алитированием придают коррозионную и окалиностойкость стальным и другим сплавам, к примеру клапанам поршневых ДВС, лопаткам турбин, нефтяным платформам, теплообменной аппаратуре, а также заменяют цинкование.
Сульфид алюминия используется для производства сероводорода.
Идут исследования по разработке пенистого алюминия как особо прочного и лёгкого материала.
Как компонент термита͵ смесей для алюмотермии
В пиротехнике.
Алюминий применяют для восстановления редких металлов из их оксидов или галогенидов.
Ограничено применяется как протектор при анодной защите.
Сплавы на базе алюминия.
В качестве конструкционного материала обычно используют не чистый алюминий, а разные сплавы на его основе.
Алюминий и его соединения используются в качестве высокоэффективного ракетного горючего в двухкомпонентных ракетных топливах и в качестве горючего компонента в твёрдых ракетных топливах. Следующие соединения алюминия представляют наибольший практический интерес как ракетное горючее:
referatwork.ru
